右美托咪啶复合臂丛神经阻滞在30例断指再植术中的应用
江 恬,黄红芳
(南通大学附属医院麻醉科,江苏南通 226000)
断指再植术是一种精细手术,手术时间长,要求患者绝对安静。臂丛神经阻滞起效快、镇痛完善、操作简便,对循环、呼吸功能影响小,临床上此类手术常选用这种麻醉方法[1]。但是由于患者意识清醒,许多人会感到紧张、恐惧,造成严重的应激反应,而应激反应可引起儿茶酚胺的释放,导致血管挛缩和血液高凝,影响断指再植成活率。故对此类患者术中辅助镇静、镇痛药物,可提高麻醉质量,改善预后[2]。右美托咪啶(dexmedetomidine,Dex)是一种新型高选择性α2肾上腺受体激动药,具有镇静、镇痛、抗交感而无呼吸抑制作用,能在增加围术期血流动力学稳定的同时,减少麻醉及镇静用药[3]。本研究对断指再植术患者分别使用Dex和丙泊酚镇静,观察患者生命体征的变化和镇静情况,旨在为临床药物的选择提供依据。
1 资料与方法
1.1 一般资料 选择2009年6月至2010年3月,美国麻醉医师学会(american society of anesthesiologists,ASA)根据病情分级为Ⅰ~Ⅱ级,在本院急诊手术室行断指再植术患者60例,年龄18~56岁,体质量45~73kg。无严重的呼吸或循环系统疾病,无麻醉镇痛药成瘾史,术前1周无镇静药物使用史。随机分为Dex组和丙泊酚组各30例。两组患者年龄、体质量、性别比、手术时间和ASA分级比较差异无统计学意义(P>0.05)。Dex组给予Dex负荷量1.0μg/kg微量泵15min注入,后给予维持量0.5μg/(kg·h);丙泊酚组按血浆靶浓度1~2μg/mL靶控输注丙泊酚。记录神经阻滞前(T0)、阻滞后(T1)、用药后10min(T2)、用药后30min(T3)、用药后1h(T4)、用药后2h(T5)的循环呼吸和镇静(Ramsay评分)效果。
1.2 麻醉方法 所有患者麻醉前30min肌内注射阿托品0.5 mg、苯巴比妥钠0.1g。入室后常规开放静脉,面罩吸氧,监测血压(blood pressure,BP)、心电图(electrocardiogram,ECG)、心率(heart rate,HR)、脉搏血氧饱和度(saturation of peripheral oxygen,SpO2)和呼吸频率(respiratory rate,RR)。选择肌间沟入路行臂丛神经阻滞,寻找异感后注入0.5%罗哌卡因20~25mL,10~15min确定麻醉效果。若麻醉效果满意,且无血流动力学紊乱,则开始施行镇静。Dex组给予Dex(江苏恒瑞医药股份有限公司,批号:09112443)负荷量1.0μg/kg微量泵15min注入,后给予维持量0.5μg/(kg·h);丙泊酚组给予丙泊酚(北京费森尤斯卡比医药有限公司,批号:0908006)按血浆靶浓度1~2μg/mL靶控输注。术毕送入麻醉后恢复室。
1.3 统计学处理 应用SPSS13.0软件进行数据处理,计量资料以±s表示,组间比较采用单因素方差分析,组内不同时点的比较采用重复测量资料的方差分析,以P<0.05为差异有统计学意义。
表1 两组患者不同时间点循环、呼吸指标和Ramsay镇静评分情况比较(±s)
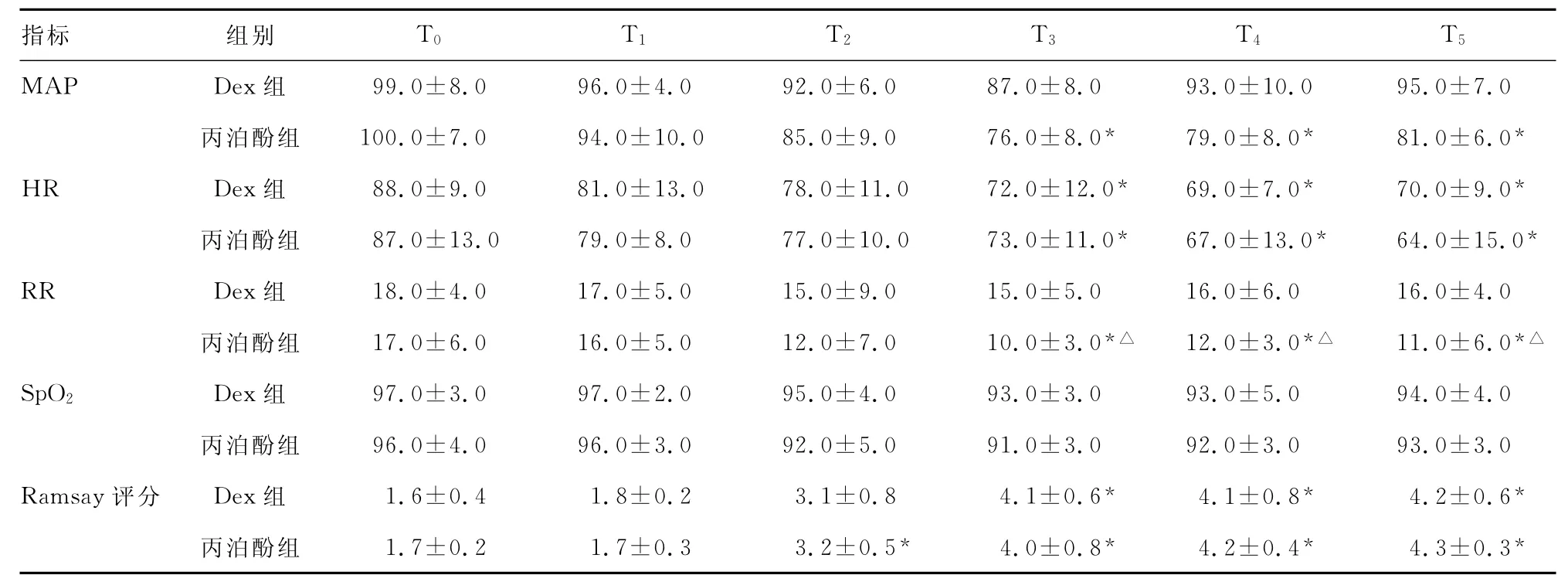
表1 两组患者不同时间点循环、呼吸指标和Ramsay镇静评分情况比较(±s)
*:P<0.05,与T0时点比较;△:P<0.05,Dex组比较。
指标 组别 T0 T1 T2 T3 T4 T5.0 95.0±7.0丙泊酚组 100.0±7.0 94.0±10.0 85.0±9.0 76.0±8.0* 79.0±8.0* 81.0±6.0*HR Dex组 88.0±9.0 81.0±13.0 78.0±11.0 72.0±12.0* 69.0±7.0* 70.0±9.0*丙泊酚组 87.0±13.0 79.0±8.0 77.0±10.0 73.0±11.0* 67.0±13.0* 64.0±15.0*RR Dex组 18.0±4.0 17.0±5.0 15.0±9.0 15.0±5.0 16.0±6.0 16.0±4.0丙泊酚组 17.0±6.0 16.0±5.0 12.0±7.0 10.0±3.0*△ 12.0±3.0*△ 11.0±6.0*△SpO2 Dex组 97.0±3.0 97.0±2.0 95.0±4.0 93.0±3.0 93.0±5.0 94.0±4.0丙泊酚组 96.0±4.0 96.0±3.0 92.0±5.0 91.0±3.0 92.0±3.0 93.0±3.0 Ramsay评分 Dex组 1.6±0.4 1.8±0.2 3.1±0.8 4.1±0.6* 4.1±0.8* 4.2±0.6*丙泊酚组 1.7±0.2 1.7±0.3 3.2±0.5* 4.0±0.8* 4.2±0.4* 4.3±0.3 MAP Dex组 99.0±8.0 96.0±4.0 92.0±6.0 87.0±8.0 93.0±10*
2 结 果
2.1 T3~T5时丙泊酚组平均动脉压(mean arterial pressure,MAP)显著低于T0时(P<0.05)。T3~T5时Dex组和丙泊酚组HR显著慢于T0时(P<0.05)。T3~T5时丙泊酚组RR比T0时明显减慢(P<0.05),且显著低于同时点Dex组(P<0.05),见表1。
2.2 T2~T5时Dex组和丙泊酚组Ramsay评分显著高于T0时(P<0.05)。两组患者SpO2虽下降,但差异无统计学意义(P>0.05),见表1。
3 讨 论
臂丛神经阻滞后,应激反应很大程度与心理应激相关。过强的应激反应会对循环、神经、内分泌、凝血和免疫系统产生影响,干扰手术的顺利进行,引起术后并发症,影响手术的预后[4]。适度的镇静、镇痛可消除其心理压力,抑制应激反应,对改善断指再植的预后很重要。过去传统的镇静药物很多,如丙泊酚,但是容易引起呼吸和循环系统的抑制,不利于术中安全。
Dex是一种强效、高选择性α2肾上腺素受体激动药,与α2受体的结合力比α1受体强1 600余倍,与α2肾上腺素受体的亲和力是可乐定的8倍[5-6];对α2受体具有更强的内在活性,更短的分布半衰期(约6min)和清除半衰期(约2h)[7]。由于其有独特的镇静、镇痛作用而逐渐应用于临床麻醉中。1999年美国食品药品管理局(food and drug administration,FDA)批准其应用于重症监护病房镇静,2008年FDA批准用于非插管患者在手术和其他操作中的镇静。Dex与传统的镇静药物(如咪达唑仑、丙泊酚等)的作用机制有明显的不同。Dex产生镇静、催眠作用的关键部位是篮斑核,而不是大脑皮层。脊髓是Dex的主要镇痛部位,其通过激动突触前膜α2受体,抑制了去甲肾上腺素等血浆儿茶酚胺的释放,并终止疼痛信号的传导,从而产生镇静、镇痛,抑制交感神经活动等效应[8]。
Dex对血压呈双向作用,有剂量依赖性,也受给药速度的影响[9]。快速输注Dex可引起短暂的高血压,反射性降低心率,这主要是直接激活血管平滑肌突触后α2肾上腺素能受体产生的血管收缩作用[10]。接着持续输注引起的低血压是因作用于心血管调节中枢,产生抗交感和增加迷走神经活性的作用[11]。根据FDA推荐剂量[12],结合临床经验,本研究采用负荷量1.0μg/kg,微量泵15min内缓慢注入,后给予维持量0.5 μg/(kg·h)。选择持续缓慢静脉输注方法有效地避免了心血管系统发生不良反应。结果显示Dex组在用药后各时点的MAP仅有轻度下降,均维持在正常范围内。有研究证实[13],Dex有轻微呼吸抑制作用,其表现为轻微降低静息每分钟通气量,潮气量降低,而呼吸频率几乎无变化,其抑制程度比丙泊酚及咪达唑仑明显减轻,且与其他镇静镇痛药无协同作用[14]。在本研究中,Dex组的SpO2和RR在用药后出现了轻微的下降,并未引起明显的呼吸抑制,无需特别处理。
丙泊酚是一种速效静脉全身麻醉药,具有起效快而平稳,苏醒快且脑功能恢复完善,术后恶心、呕吐发生率低等优点。有研究发现,在以Ramsay和脑电双频指数评价镇静深度时,Dex与丙泊酚的镇静效果相似[15]。本研究中,两组同时点的Ramsay评分证明,两种药物均能提供满意的镇静效果。但丙泊酚在提供满意镇静的同时常常会引起循环和呼吸抑制。本研究中丙泊酚组在用药后的多个时点出现了MAP、HR和RR的明显下降。此缺点明显增加了麻醉的风险性,限制了其在临床上的应用。
综上所述,Dex是一种新型、高选择性的α2肾上腺受体激动剂,其在提供满意的镇静效果的同时还具有以下优点:作用时间相对较短,可控性好;具有抗焦虑作用;血流动力学稳定;对呼吸抑制作用小;在维持镇静同时保持一定的可唤醒能力。因Dex的抗交感作用可引起心动过缓、血压下降,在临床应用中应注意控制注药速度及药物的浓度,密切注意循环系统的变化,随时调整剂量,防止发生不良反应。
[1] 梁华,陶国才.经肌间沟连续臂丛阻滞用于断指(肢)回植麻醉和术后镇痛[J].重庆医学,2003,32(12):118-120.
[2] 刘萍,杨钰香,姚尚龙,等.臂丛神经阻滞时咪唑安定清醒镇静的研究[J].中华麻醉学杂志,2004,24(4):31-33.
[3] Dere K,Sucullu I,Budak ET,et al.A comparison of dexmedetomidine versus midazolam for sedation,pain and hemodynamic control,during colonoscopy under conscious sedation[J].Eur J Anaesthesiol,2010,27(7):648-652.
[4] 徐华.手术应激反应研究进展[J].国外医学麻醉与复苏分册,2003,24(5):23-26.
[5] Mantz J.Alpha2-adrenoceptoragonists:analgesia,sedation,anxiolysis,haemodynamics,respiratory function and weaning[J].Baillere Anaesthesiol,2000,14(2):443-448.
[6] 吴新民,许幸,王俊科,等.静脉注射右美托咪啶辅助全身麻醉的有效性和安全性[J].中华麻醉学杂志,2007,27(9):773-776.
[7] 李民,张利萍,吴新民.右美托咪啶在临床麻醉中应用的研究进展[J].中国临床药理学杂志,2007,23(6):466-470.
[8] Scholz J,Tonner PH.Alpha2-adrenoceptor in anesthesia:a new paradigm[J].Curt Opin Anaesthesiol,2000,13(4):437-442.
[9] Bloor BC,Ward DS,Belleville JP,et al.Effects of intravenous dexmedetomidine in humans [J].Anesthesiology,l992,77(6):1134-1142.
[10]徐永明,杜冬琴,江伟.围术期α2-肾上腺素受体激动剂应用进展[J].国际麻醉与复苏分册,2006,27(3):176-178.
[11]Particalf M,Kenneth P,Erik K,et al.Dexmedetomodine and neuro-cognitive testing in awake cmniotomy[J].Neuresurg Anesthesiol,2004,16(1):20-25.
[12]Donnelly AB,Gonzales J,Tomsik F.Anesthesiology and critical care drug handbook[M].6th ed.Hudson:Lexi-Comp,2005.
[13]Ebert TJ,Hall JE,Barney JA,et al.The effects of increasing plasma concentrations of dexmedetomidine in humans[J].Anesthesiology,2000,93(2):382-394.
[14]Tobias JD.Dexmedetomidine:applications in pediatric critical care and pediatric anesthesiology[J].Pediatr Crit Care Med,2007,8(2):115-131.
[15]Dutta S,Karol MD,Cohen T,et al.Effect of dexmedetomidine on propofol requirements in healthy subjects[J].Pharm Sci,2001,90(2):172-181.

