流动注射化学发光分析法实验条件的控制*
嵇正平 郁金丹 胡效亚
(扬州大学化学化工学院 江苏扬州 225002)
化学发光是指化学反应致使反应产物处于激发态,在退激时以光辐射形式释放能量的现象。以此为基础的化学发光分析法不需要外源性激发源,因此设备简单,误差来源少。其内源性激发源为化学能,对被检光信号无背景干扰,因此有较高的信噪比。
化学发光分析法是一种在非平衡状态下进行的检测方法,属于动力学分析法。反应物的加入速度、混和状态、体系温度及反应时间等都会对检测结果产生较大影响。所以,化学发光分析法常与流动注射技术相结合,建立流动注射化学发光分析法。图1是其典型的流程。
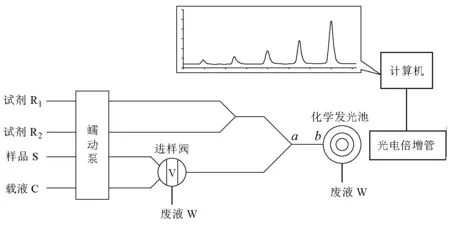
图1 流动注射化学发光分析流程图
目前,流动注射化学发光分析法已得到了广泛的应用[1-5],其内容也被编入了教材[6]。在诸多文献和笔者教学过程中,发现一个非常普遍的现象:条件优化及检测时,随着某种反应物浓度的增大,化学发光信号出现先上升再下降的情况(图2)。对于这种“随着试剂浓度增大,信号不升反降”的情况,许多文献未作解释。也有一些文献认为这是由于过量的试剂对光产生了吸收,导致发光信号减弱。
为了讨论这一现象的成因,本文以间苯二酚-KMnO4发光体系为研究对象,采用流动注射及静态注射法,研究了反应物KMnO4浓度对化学发光强度的影响。
1 仪器与试剂
IFFM-E流动注射化学发光分析仪(西安瑞迈电子科技有限公司)。
间苯二酚(0.20mmol·L-1),KMnO4(0.20mmol·L-1),H2SO4(0.2mol·L-1),HAc(0.2mol·L-1)。
2 实验内容
2.1 流动注射化学发光
0.20mmol·L-1间苯二酚作为R1,0.2mol·L-1H2SO4溶液作为R2,蒸馏水作为载液C,将不同浓度KMnO4作为样品S(图1),做流动注射化学发光试验。管径2mm,流速1.0mL·min-1。
2.2 静态注射化学发光
取0.10mmol·L-1间苯二酚-0.1mol·L-1HAc溶液1.00mL加入到小烧杯中,置于暗盒内,开启化学发光检测仪,用注射器注入1.00mL不同浓度的KMnO4溶液,记录化学发光-时间图谱。
3 结果与讨论
3.1 试剂浓度的影响
根据流动注射化学发光-时间谱图,求出发光峰值并作出I-c(KMnO4)浓度关系图(图2)。
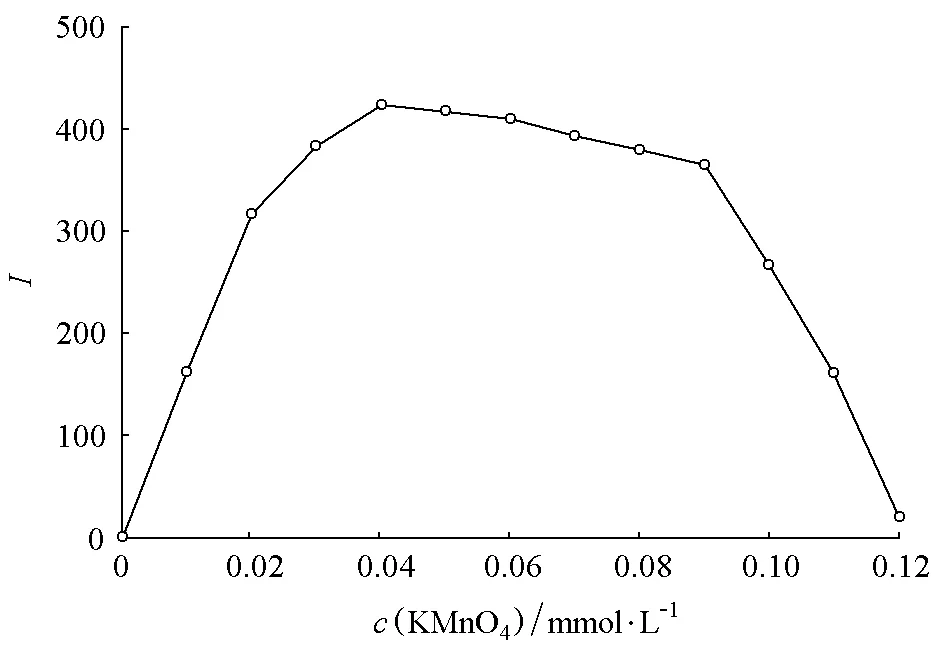
图2 发光强度与KMnO4浓度的关系
由图2可知,发光强度峰值(I)随KMnO4浓度(c)呈非单调函数关系:当c在0.00~0.04mmol·L-1范围内,I与c呈正相关性(其中c在0.00~0.02mmol·L-1范围内,有较好线性关系);而当c高于0.04mmol·L-1时,I与c呈负相关性。
笔者认为图2的非线性(乃至非单调性)并不是由于过量的反应物KMnO4对光吸收所造成的,原因如下:
如果是由于过量的KMnO4对光的吸收所导致,根据朗比定律:
(1)
式中I0为反应发出光强,ε为摩尔吸光系数,b为光程长度。对式(1)进行转换,得:
I=I0×10-εbc
(2)
式(2)虽表明I与c有负相关性,但I减小的斜率应随c增加呈渐缓趋势;而在图2中,c在高浓度时下降速度很快。这表明过量KMnO4浓度产生的光吸收不是其负相关性的主要原因。
根据KMnO4的最大吸收波长(525nm)的摩尔吸光系数,可计算0.12mmol·L-1相对于0.04mmol·L-1的吸光度:
其中0.1cm为发光池螺旋管半径,可近似作为平均光程长度。

3.2 静态注射反应时间的影响
为了讨论上述现象产生的主要原因,我们进行了静态注射实验。考虑到强酸性条件下的反应速度相对于静态注射的操作速度过快,静态注射实验采用HAc溶液作为介质。结果如图3。
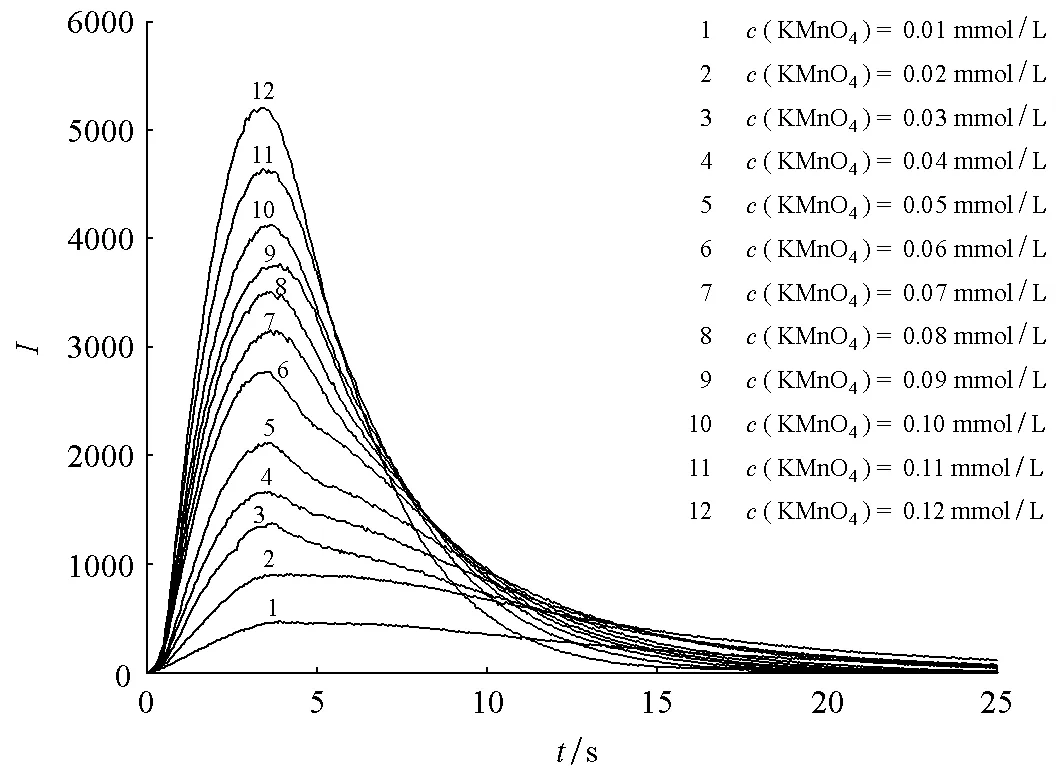
图3 静态注射发光强度与浓度及时间的关系
① 在静态注射中,I-t的总趋势为:KMnO4注入后,发光强度开始增大,在3s时,发光强度达最大;随后发光强度逐渐下降。
合理的解释是:开始时两种溶液相互混合,随着混合均匀性增强,发光强度增加;在3s后随着反应的进行,两反应物的浓度下降,反应速度下降,曲线呈现一般动力学曲线的特征。
② 在反应的最初5s,KMnO4在0.00~0.12mmol·L-1浓度范围内,I-c呈正相关性,其中在反应的最初3s呈良好的线性关系。说明在本文研究的浓度范围内,KMnO4对光的吸收几乎不影响发光强度。
③ 反应至7s时,呈正相关性的浓度范围为0.00~0.11mmol·L-1,浓度大于0.11mmol·L-1时,发光强度反而下降。
④ 反应7s之后,随时间延长,正相关性及线性范围逐渐变窄。
3.3 流动注射化学发光线性范围的主要影响因素
虽然本文的流动注射、静态注射实验分别在强酸性、弱酸性条件下进行,反应速度相差较大,但流动注射中液体的流动速度快、体积小、混匀时间也短,所以两者反应的趋势是相似的。据此可以认为:在流动注射化学发光分析中,造成I-c“非线性”乃至“非单调性”关系的主要原因是检测过程中反应时间过长。对此可用速度方程进行分析:
对于一个化学发光反应:

化学发光强度与反应速度成正比:
其中v为反应速度,x、y分别为A、B两物质的反应级数,kCL、kv及k均为常数。
若两物质的反应级数均为1,则为:
I=kcAcB
若将不同浓度A物质注入固定浓度B中,反应时间为0s时刻,则有:
式中cA0、cB0分别为A、B的起始浓度。
可以看出发光强度与A浓度呈正比关系。
反应至t时刻,由于A、B浓度降低,发光强度It为:

可以看出t越大,It-cA0线性关系越差。而t较大时,It-cA0还有可能呈负相关性。
反应时间还与所连接管路有关。如图1所示,化学发光池前有一段管路ab,反应物在此相互混合并反应。如果ab太长,则反应物将在此段管路发生了较大程度的反应(这部分发光信号未被检测),当溶液进入化学发光池时,所检测的是反应时间为t时刻的发光强度。显然,若ab段越长,t就越大,I-c线性范围也就越小。
4 结论
对于一般的流动注射化学发光分析,反应物相互混匀后,反应时间越长,发光强度与反应物浓度的线性关系越差,甚至造成两者之间为非单调性函数关系。
如果被研究反应物是被测组分,此现象对检测线性范围及灵敏度均会产生不良影响。作者在科研和教学实践中,采取了如下改善措施:
① 调整连接管路ab长度,使反应物能尽快在化学发光池中混匀,尽可能减小反应时间。
② 若因技术原因,无法缩短ab,可以适当提高蠕动泵速度。
③ 调节介质条件,适当降低反应速度常数,以降低ab段内反应的程度。
④ 适当增大另一个反应物的浓度,使其在反应过程中近似为常量。
当然,上述条件的改变可能会引起其他不良影响。故具体实验参数需要通过条件实验进行优化。
[1] 陈效兰,杨娟,徐淑静,等.分析化学,2009,37(11):1622
[2] 李银环,吕九如.分析化学,2007,35(5):743
[3] 何树华,何德勇,章竹君.分析化学,2006,34(11):1622
[4] Zheng J,Springston S R,Lioyd J W.AnalChem,2003,75:4696
[5] Fletcher P J,Andrew K N,Forbes S,etal.AnalChem,2003,75:2618
[6] 扬州大学,徐州师范大学,盐城师范学院,等.新编大学化学实验(三).北京:化学工业出版社,2010

