磷酸铁锂磁性杂质对电池自放电的影响
杨续来,刘成士,谢 佳,徐小明
(安徽省动力锂离子电池工程技术研究中心,合肥国轩高科动力能源有限公司,安徽合肥 230011)
在磷酸铁锂(LiFePO4)的合成过程中,会伴随生成少量的γ-Fe2O3、FeP、Fe2P 及 Fe2P2O7等杂质[1],单质铁也会在还原性气氛,如CO、H2等气氛下,在500~700℃经Fe3+的还原而生成[2]。这些杂质的存在,会降低材料的比容量和能量密度,杂质铁在电解液中溶解等副反应,会影响电池的使用寿命和安全性能。
磁性实验可用来研究样品基本性质和检测样品纯度,可以检测到样品中XRD等仪器检测不到的、低于1 mg/kg的铁磁和亚铁磁纳米粒子[3]。使用超导量子干涉仪(SQUID)可检测LiFePO4的磁性杂质含量,并判断材料的性能,低磁性杂质含量的LiFePO4,高温下不会发生明显的铁溶解[3]。
本文作者通过对商业化LiFePO4材料的磁性分析,考察磁性杂质对电池性能的影响,以期提高LiFePO4正极锂离子电池的性能。
1 实验
选取3种不同工艺生产的商业化LiFePO4正极材料,记为 LFP-A(山东产,草酸亚铁合成路线)、LFP-B(台湾省产,氧化铁合成路线)和 LFP-C(加拿大产,水热合成路线)。
1.1 电池的制作
以1 mol/L LiPF6/EC+EMC+DEC(体积比1∶1∶1,张家港产,电池级)为电解液,25 μ m厚的Entek聚烯烃隔膜(美国产)为隔膜,SAG-20型石墨(深圳产,电池级)为负极活性物质,按本公司的设计工艺,制作容量为10 Ah的1865140型铝壳电池。
1.2 样品的分析
用X'Pert PRO型X射线衍射仪(荷兰产)进行粉末样品的微观结构的测定,CuKα(λ=0.154 056 nm),管压40 kV,管流50 mA,扫描速率为4(°)/min;用 MPMS XL-7型精密SQUID磁学测量系统(美国产),测定 LiFePO4的磁性;用Sirion-200型场发射扫描电子显微镜(美国产)对拆解后电池的隔膜进行表面形貌观察和微区成分分析。
1.3 电池自放电率的测定
用BTS1002型电池内阻测试仪(广州产),在328 K和298 K下分别记录满电态电池的电压变化,电池的自放电率(SDR)按式(1)计算。

式(1)中:U1为电池在某温度下储存前的初始电压,U2为储存后的电压,t为储存时间。
2 结果与讨论
2.1 XRD结果分析
图1是3种LiFePO4材料的XRD图。

图1 3种 LiFePO4材料的 XRD图Fig.1 XRD pattern of 3 kinds of LiFePO4materials
从图1可知,3种LiFePO4材料均具有橄榄石型晶体的特征。碳源热解后为无定型碳,不会影响材料的晶体结构。LFP-A较LFP-B和LFP-C存在明显的Fe2P杂质峰,通过对峰面积积分,得到LFP-A材料中Fe2P的含量约为3%。除LFP-A检测到Fe2P外,LiFePO4材料均未发现其他杂质。
2.2 SQUID磁性分析
N.A.Chernova等[4]提出了LiFePO4及可能存在的铁元素杂质的磁性转变温度点:Li3Fe2(PO4)3、LiFeP2O7、Fe2P2O7和 LiFePO4的尼尔温度分别为26 K、27 K、12.5 K和52 K;Fe(0)、Fe2P和Fe2O3的居里温度分别为 215 K、215 K和>850 K。由此,可以区分LiFePO4所含铁元素杂质的种类。
3种材料的摩尔磁化率倒数与温度的关系见图2。

图2 3种LiFePO4材料摩尔磁化率的倒数与温度的关系Fig.2 Relation between temperature and the reciprocal magnetic susceptibility for 3 kinds of LiFePO4materials
从图2可知,3种LiFePO4材料中,均没有居里温度低于200 K的铁磁簇杂质。由于晶体结构中Fe-O-Li-O-Fe的长程有序相互作用,LiFePO4在尼尔温度(52 K)以下表现为反铁磁性,在尼尔温度以上表现为顺磁性,服从居里-外斯定律。LFP-A由于明显杂相的存在,摩尔磁化率的倒数与温度关系的曲线偏离居里-外斯定律,呈现典型含Fe2P材料的特征[5],与XRD分析的结果吻合。LiFePO4材料烧结过程在惰性气氛中进行,同时材料中含有碳,铁磁簇或亚铁磁簇成分为Fe3O4的可能性较小,因此LFP-A中的杂质很可能是Fe2P和Fe(0)或γ-Fe2O3,而 LFP-B和 LFP-C中的杂质很可能是 Fe(0)或γ-Fe2O3。
LFP-A存在明显的Fe2P杂质,与合成条件有密切的关系。一般而言,在碳热还原的过程中,Fe2P杂质会伴随着LiFePO4生成,温度越高,Fe2P的含量越高[6]。LFP-A为草酸亚铁路线合成的产品,合成温度一般在700℃以上。与此相比,水热法能够在较低的温度下得到高度结晶的产品[7],且反应时间短、能耗少,而氧化铁合成路线的合成温度也在600℃左右[8]。LFP-B和LFP-C的合成温度低于LFP-A,导致LFP-A较其他两个产品存在明显的Fe2P杂质。
根据居里-外斯定律,对实验数据的顺磁区进行拟合,得到 1 mol LiFePO4的居里常数C,由式(2)计算有效磁矩ueff。

式(2)中:NA是阿佛加德罗常数,kB是波尔兹曼常数,μB是波尔磁子。计算可知:LFP-A、LFP-B和LFP-C的ueff分别为 12.7uB、6.70uB和 5.18uB。 不含任何锂空缺的 μeff值与高自旋态Fe2+的理论值4.9uB一致,但大部分LiFePO4粒子中存在有<1%的低浓度锂空位[9],导致LiFePO4的ueff一般会高于4.9uB。LFP-C材料的有效磁矩与4.9uB接近,表明LFP-C在3种材料中的磁性杂质最少。
3种材料的杂质居里温度均高于200 K,材料的磁化曲线只在一个温度,即2 K的条件下获得,如图3所示。

图3 3种LiFePO4材料磁化强度与磁场强度的关系Fig.3 Relation between magnetization and magnetic field intensity for 3 kinds of LiFePO4materials
材料的磁化强度是由材料自身和外加的磁化强度叠加而来。材料自身的磁化强度与外加磁场强度呈线性关系,外加的磁化强度在外加磁场下易饱和。从图3可知,LFP-A在高磁场强度(>5 000 Oe)下的磁化曲线呈线性,在低磁场下的磁化曲线出现了一个弯曲,说明存在一些铁磁或亚铁磁成分;LFP-B在低磁场强度下的磁化曲线出现了一个小的弯曲,说明存在少量的铁磁或亚铁磁成分;LFP-C在低磁场强度范围内呈线性,为出现明显的铁磁或亚铁磁成分的饱和磁化引起的弯曲现象,磁化强度随磁场强度成正比,说明LFPC未发现外加磁化强度,无明显的铁磁或亚铁磁杂相存在。
材料的磁化曲线可采用超顺磁模型来分析,在此模型中,磁化强度M可由式(3)来计算。



表1 以γ-Fe2O3为代表的杂质在 3种 LiFePO4材料中的物质的量含量Table 1 Molar content of impurities(represented as γ-Fe2O3)in 3 kinds of LiFePO4materials
2.3 全电池自放电分析
将电池在328 K下储存7 d,或在298 K下储存21 d,满电态电池的电压变化情况见图4。

图4 不同温度下满电态电池的电压随储存时间的变化Fig.4 Changes of voltage of full-charged battery with storage time under different temperatures
以第2 d后较稳定的电压为基础,分析图4中的数据,结果表明:在298 K下,LFP-A、LFP-B和LFP-C制成的电池的自放电率分别为 0.57 mV/d、0.38 mV/d和 0.23 mV/d,差别不明显;在328 K下,电池的自放电率分别为4.86 mV/d、0.86 mV/d和0.85 mV/d,体现了低磁性杂质材料的优势。
为了进一步分析可能引起自放电的因素,对在328 K下储存的电池进行拆解分析,发现自放电较大的LFP-A制备的电池,部分隔膜上存在明显的黑点,而LFP-B和LFP-C制备的电池,隔膜上没有明显的黑点。对黑点进行SEM观察和 X射线微区(EDS)分析,结果见图5、图6。

图5 LFP-A制备的电池隔膜上黑点的SEM图Fig.5 SEM photograph of the black spots on the separator of battery prepared with LFP-A
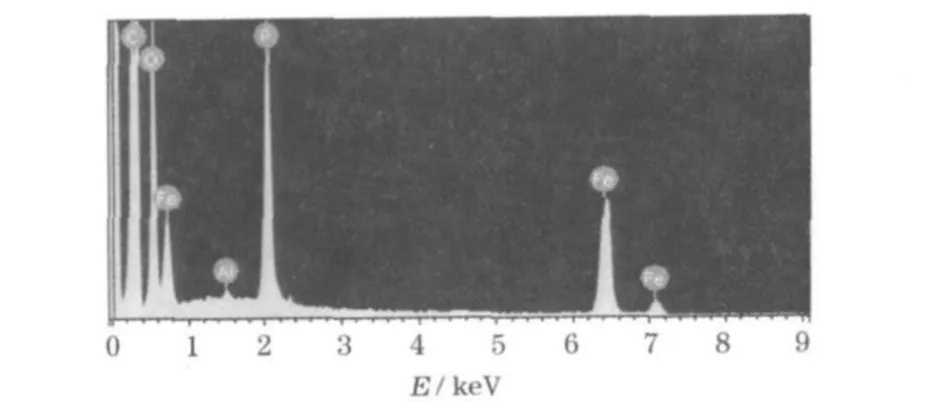
图6 LFP-A制备的电池隔膜上黑点的EDS图Fig.6 EDS spectrum of the black spots on the separator of battery prepared with LFP-A
从图 5、图6可知:隔膜的黑点中,C、O、Al、P 及Fe元素的物质的量含量分别为78.26%、19.45%、0.04%、1.17%和1.08%,主要金属元素为Fe。这部分铁,可能来源于正极材料中杂质铁元素(特别是单质铁[10])在电解液中的溶解,继而在负极处于较低电位时的沉积。这种铁溶解反应在高温下更为明显[11]。研究证明,3价铁杂质的存在,会导致隔膜黑点的产生[12]。这也是 328 K高温下,LFP-A、LFP-B和LFP-C等材料制成的电池自放电率出现明显差别的原因。
3 结论
用SQUID对3种商品化LiFePO4中磁性杂质的种类及含量进行分析,发现因生产工艺的不同,LFP-B和LFP-C中的磁性杂质含量较LFP-A低,其中LFP-C几乎无磁性杂质,而LFP-A中Fe2P含量较高。
全电池自放电研究结果表明,LiFePO4材料中磁性杂质对电池自放电有直接的影响,LiFePO4材料中磁性杂质含量与电池自放电率成正比,即磁性杂质含量越高的材料,制成的电池的自放电率越大。
致谢:感谢本公司刘大军、李华、王晨旭、韦佳兵和宫璐博士在本文实验数据分析和论文撰写过程中所提供的帮助。
[1]Yu D Y W,Donoue K,Kadohata T,et al.Impurities in LiFePO4and their influence on material characteristics[J].J Electrochem Soc,2008,155(7):A526-A530.
[2]Salah A A,Mauger A,Zaghib K,et al.Reduction Fe3+of impurities in LiFePO4from pyrolysis of organic precursor used for carbon deposition[J].J Electrochem Soc,2006,153(9):A1 692-A1 701.
[3]Zaghib K,Ravet N,Gauthier M,et al.Optimized electrochemical performance of LiFePO4at 60℃with purity controlled by SQUID magnetometry[J].J Power Sources,2006,163(1):560-566.
[4]Chernova N A,Nolis G M,Omenya F O,et al.What can we learn about battery materials from their magnetic properties?[J].J Mater Chem,2011,21(27):9 865-9 875.
[5]Omenya F,Chernova N A,Upreti S,et al.Can vanadium be substituted into LiFePO4?[J].Chem Mater,2011,23(21):4 733-4 740.
[6]Rho Y H,Nazar L F,Perry L,et al.Surface chemistry of LiFePO4studied by Mossbauer and X-ray photoelectron spectroscopy and its effect on electrochemical properties[J].J Electrochem Soc,2007,154(4):A283-A289.
[7]ZHANG Shu-ping(张淑萍),NI Jiang-feng(倪江锋),ZHOU Heng-hui(周恒辉),et al.溶剂热法控制合成规则的LiFePO4颗粒[J].Acta Physico-Chimica Sinica(物理化学学报),2007,23(6):830-834.
[8]Chang C.Cathode material for Li-ion battery application[P].US:7585593B2,2009-09-08.
[9]Rhee C H,Lee I K,Moon S J,et al.Neutron diffraction and Mö ssbauer studies of LiFePO4[J].J Korean Phy Soc,2011,58(3):472-475.
[10]Xu F,He H,Liu Y D,et al.Failure investigation of LiFePO4cells under overcharge conditions[J].J Electrochem Soc,2012,159(5):A678-A687.
[11]Aurbach D,Boris M,Gregory S,et al.Review on electrode-electrolyte solution interactions,related to cathode materials for Li-ion batteries[J].J Power Sources,2007,165(2):491-499.
[12]DING Dong(丁冬),WU Guo-liang(吴国良),PANG Jing(庞静),et al.正极材料 LiFePO4的研究与产业化的进展[J].Battery Bimonthly(电池),2010,40(5):282-284.

