苏打盐碱土对氮转化的影响
张先富,李 卉,洪 梅,宋博宇,张福全,梁 爽
吉林大学地下水资源与环境教育部重点实验室,长春 130021
苏打盐碱土对氮转化的影响
张先富,李 卉,洪 梅,宋博宇,张福全,梁 爽
吉林大学地下水资源与环境教育部重点实验室,长春 130021
以苏打盐碱土中的主要成分NaHCO3作为主要影响因素,通过室内培养方法,研究不同苏打盐碱化条件对氮的吸附、矿化、硝化及反硝化作用的影响。结果表明,在不同NaHCO3质量浓度影响下:NH+4-N吸附符合Langmuir吸附等温式;矿化模型符合一阶动力学方程,随着NaHCO3质量浓度的增大,潜在矿化势(M0)和矿化速率常数(km)分别由358.48mg/kg和0.088d-1降低到337.08mg/kg和0.059d-1;硝化作用符合“S”形曲线模型,随着NaHCO3质量浓度的增大,最大速率(kmax)由22.56mg/(kg·d)降低到16.68mg/(kg·d);反硝化作用符合零阶动力学方程,但NaHCO3与Na2CO3混合质量浓度变化对反硝化速率常数(kd)影响不显著。随着NaHCO3质量浓度的增大,苏打盐碱土中NH+4-N吸附、有机氮矿化和硝化作用均受到抑制。
苏打盐碱土;氮;吸附作用;硝化作用;反硝化作用;动力学
0 前言
盐碱化是指土壤中含有大量可溶性盐,对农业和环境带来有害影响。可溶盐分的积累可促进土壤养分的失衡,降低土壤的渗透性,影响微生物生长、氮转化和有机物分解,甚至会减少农作物产量。在盐碱地施肥过程中,发现氮肥利用率偏低,有时甚至肥效不明显。大量施肥易引起土壤表层氮素累积,氮素随渗流不断向深层迁移转化,易使地下水水质恶化。研究表明,地下水中“三氮”的增加是土壤和地表水中污染源的增加与补给地下水的渗流共同作用的结果[1]。土壤盐碱化已成为一个世界性的资源问题和生态问题。研究盐碱化条件对氮素转化的影响显得十分重要,为氮素污染地下水的定量评价与预测和科学合理施肥以及提高氮肥利用率提供科学依据。目前,国外学者对不同盐碱化条件下氮的矿化、硝化、氨挥发及N2O释放都有过研究报道,常见影响因素有盐分、盐碱度、电导率、pH等[2-4];国内学者依据不同盐碱化土壤特性,研究了不同盐碱化条件对氮素矿化、硝化及氨挥发的影响[5-8]。笔者以苏打盐碱土中的主要成分NaHCO3作为主要影响因子,研究苏打盐碱土对氮的吸附、矿化、硝化及反硝化作用的影响。
1 材料与方法
1.1 供试土壤
供试土壤取自吉林省前郭灌区重点试验站内地表下20~40cm深土层,质地为黏土。根据基本理化性质分析显示,土壤碱化度为13.76%,属于中等碱化土。为便于研究不同盐碱化程度的土壤对于氮转化的影响,采取在供试土壤中填加NaHCO3的方法,以模拟不同盐碱化程度的土壤。
1.2 实验方法
1.2.1 吸附实验
称取20g风干后过2mm筛的供试土壤,与0.06g NaHCO3混匀后分别装入6个250mL具塞锥形瓶中。另用蒸馏水配制质量浓度分别为20、40、60、80、100和150mg/L的NH4Cl溶液,分别向锥形瓶中加入200mL上述不同质量浓度的NH4Cl溶液(水土比为10∶1),加塞密封放在恒温振荡器上在10℃时以120r/min振荡24h,以100r/min转速离心分离8min。取上清液测铵态氮(NH+4-N)平衡浓度,将初始浓度与平衡浓度作差,计算NH+4-N吸附量。再分别取0.10和0.16g NaHCO3,重复上述实验步骤。加入不同质量的NaHCO3分别对应质量浓度为300、500和800 mg/L。NH+4-N采用纳氏试剂比色法测定。
1.2.2 矿化实验
分别称取50g风干后过2mm筛的供试土壤,装入21个150mL锥形瓶中。每个锥形瓶加入0.1g尿素(CO(NH2)2)。用蒸馏水配制质量浓度分别为300和800mg/L的NaHCO3溶液。取10mL上述不同质量浓度的NaHCO3溶液加入装有土壤的锥形瓶中,使土壤均匀湿润。另设1个只加10mL蒸馏水的对照处理。共设置3个处理。采用室内恒温密闭培养法,每个锥形瓶均用薄膜封口,并放置于20℃的恒温培养箱中,于培养后5、10、15、20、30、40和50d分7次取样,分别测定土壤中NH+4-N和硝态氮(NO-3-N)质量分数。NH+4-N测定采用纳氏试剂比色法,NO-3-N测定采用酚二磺酸比色法。
1.2.3 硝化实验
分别称取50g风干后过2mm筛的供试土壤,与0.1g(NH4)2SO4混匀后,装入24个150mL锥形瓶中。配制的NaHCO3溶液与处理方法同矿化实验。在30℃恒温培养,于培养后3、6、9、12、15、18、21和24d分8次取样,分别测定土壤中NH+4-N和NO-3-N质量分数。
1.2.4 反硝化实验
称取与硝化作用相同的土样20g,与0.2g KNO3混匀,配制的NaHCO3溶液与硝化实验相同,采用恒温密闭法测定反硝化情况。实验结果表明,反硝化作用不明显,故对实验方案进行调整。
称取20g风干土,与0.05g KNO3混匀后分别装入28个250mL锥形瓶中。用蒸馏水配制不同质量浓度的NaHCO3和Na2CO3混合溶液,二者质量比为5∶1,混合溶液质量浓度分别为600和120、1 600和320、5 000和1 000mg/L。取200mL上述不同质量浓度的混合溶液加入装有土壤的锥形瓶中,并充分混匀。另设1个只加200mL蒸馏水的对照处理。共设置4个处理。采用恒温密闭培养法,在30℃恒温培养,于培养后2、4、6、8、12、16和20d分7次取样,测定NO-3-N质量分数。
2 结果分析与讨论
2.1 NaHCO3对NH+4-N吸附的影响
图1是10℃时NH+4-N吸附等温线。从图1可以看出,随着NaHCO3质量浓度增大,NH+4-N吸附量呈下降趋势。这是由于土壤中吸附的Na+含量较高,占据了较多的吸附位,使得NH+4的吸附相对受到抑制,从而使NH+4-N吸附量降低。这说明,NaHCO3质量浓度的增大,不利于NH+4-N吸附。采用Langmuir吸附等温线方程进行拟合:
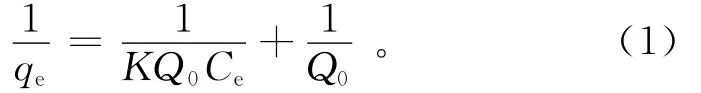
式中:qe为NH+4-N平衡吸附量,mg/g;K为与温度、吸附过程焓变有关的常数,L/mg;Q0为NH+4-N最大吸附量,mg/g;Ce为吸附达到平衡时溶液中NH+4-N的质量浓度,mg/L。拟合结果(图2)表明,在不同NaHCO3质量浓度影响下,NH+4-N吸附均符合Langmuir吸附等温式。随着NaHCO3质量浓度增大,NH+4-N吸附受到抑制。
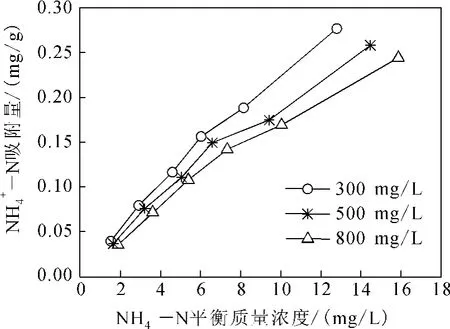
图1 NH+4-N吸附等温线(10℃)Fig.1 NH+4-N adsorption isotherm(10℃)
2.2 NaHCO3对有机氮矿化作用的影响
图3为不同NaHCO3质量浓度土壤中NH+4-N随时间的变化。从图3可见,从培养开始到20d,不同土壤中NH+4-N均逐渐增大,这是由于尿素水解产生NH+4,使NH+4-N逐渐累积,且同一时刻的NH+4-N质量分数随NaHCO3质量浓度的增大而呈降低的趋势,说明随着NaHCO3质量浓度的增大,氨化作用受到抑制。从20d到30d,曲线斜率变小并趋向负值,说明同时存在氨化和硝化作用,且硝化逐渐占优势。从40d到培养结束,随NaHCO3质量浓度的增大,相同时刻的NH+4-N质量分数升高,说明硝化作用受到抑制,NH+4转化速率变慢。
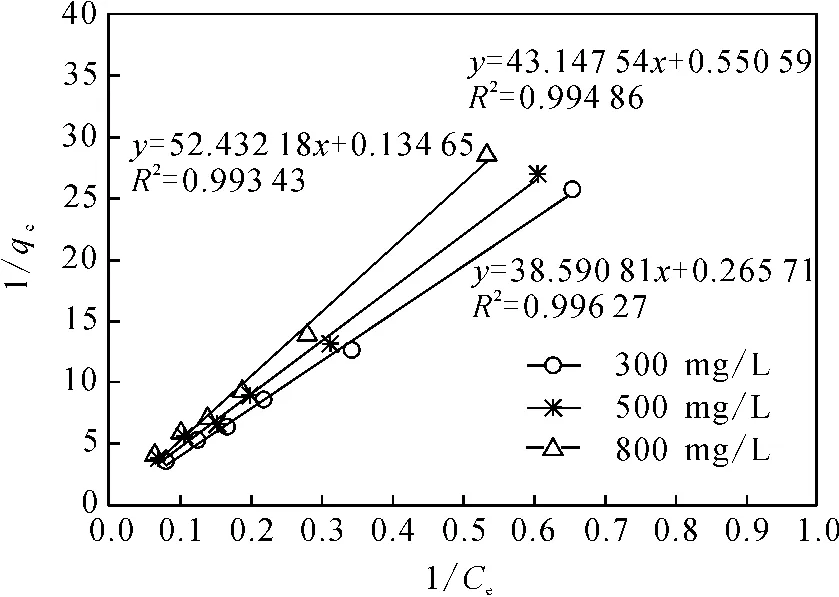
图2 Langmuir吸附等温线Fig.2 Langmuir’s adsorption isothermal line
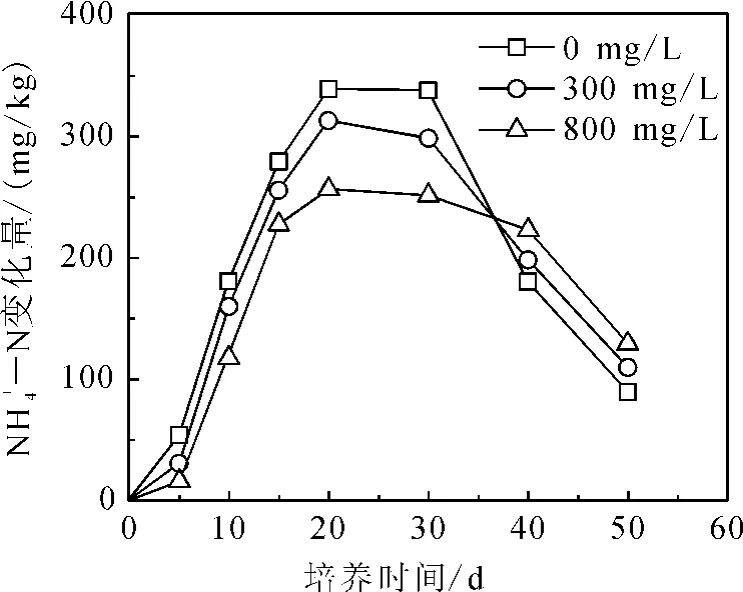
图3 不同土壤NH+4-N随时间的变化Fig.3 NH+4-N in soils versus time
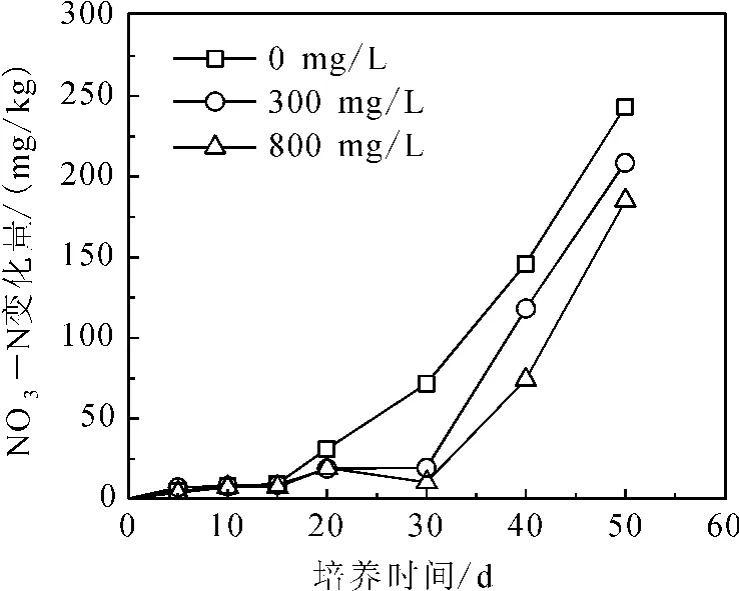
图4 不同土壤NO-3-N随时间的变化Fig.4 NO-3-N in soils versus time
图4 为不同NaHCO3质量浓度土壤中NO-3-N随时间的变化。从培养开始到15d,不同土壤中NO-3-N增加缓慢,表明硝化作用微弱。从20d以后,硝化作用逐渐增强,在30d时尤以0mg/L NaHCO3土壤中NO-3-N变化明显。随着NaHCO3质量浓度增大,相同时刻的NO-3-N质量分数有逐渐降低的趋势,表明随着NaHCO3质量浓度的增大,硝化作用受到抑制。
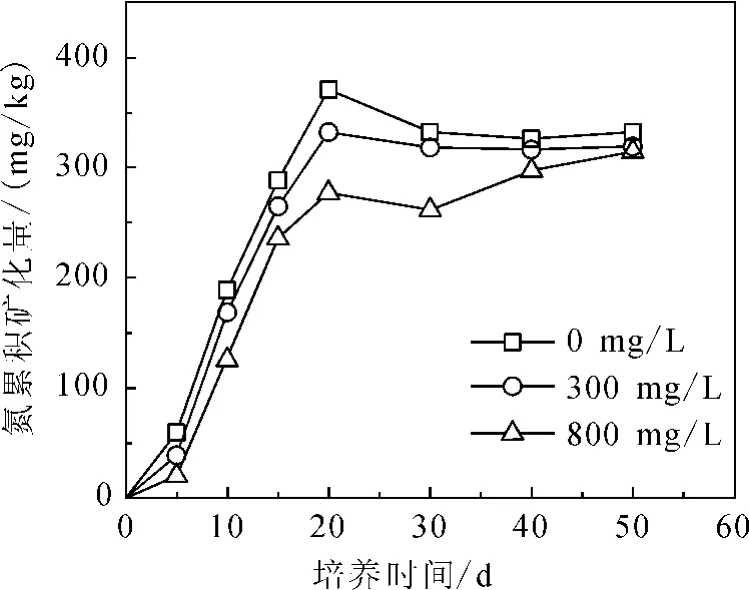
图5 不同土壤氮累积矿化量随时间的变化Fig.5 Cumulative N mineralization in soils versus time
图5 为不同NaHCO3质量浓度土壤中氮累积矿化量(以NH+4-N与NO-3-N质量分数之和(mg/kg)计)随时间的变化。从图5可以看出,不同土壤的氮累积矿化量随时间延长而增大,20d以前曲线较陡是由于尿素水解使NH+4-N量迅速升高,20d以后曲线趋于平缓是由于可转化为无机氮的有机氮逐渐消耗殆尽。培养结束时,NaHCO3质量浓度为300和800mg/L的累积矿化量(318.87和314.46mg/kg)分别是对照处理(332.88mg/kg)的95.8%和94.5%。培养过程中,相同时刻的氮累积矿化量随着NaHCO3质量浓度的递增有逐渐降低的趋势,说明随着土壤中NaHCO3质量浓度的增大,土壤有机氮矿化作用受到抑制。由于累积矿化量百分数相对接近,表明土壤本底盐分含量较高对氮矿化有影响,使得不同NaHCO3质量浓度梯度对氮矿化影响不显著。
2.3 NaHCO3对硝化作用的影响
图6为不同NaHCO3质量浓度土壤中NH+4-N随时间的变化。从培养开始到6d,NH+4-N质量分数随时间迅速增大,这可能与土壤对NH+4-N吸附和解吸有关;从6d开始,NH+4-N质量分数随时间逐渐降低,说明硝化作用逐渐增强,且相同时刻随NaHCO3质量浓度增大,NH+4-N质量分数也增大,表明NaHCO3质量浓度越大,硝化作用愈受抑制。
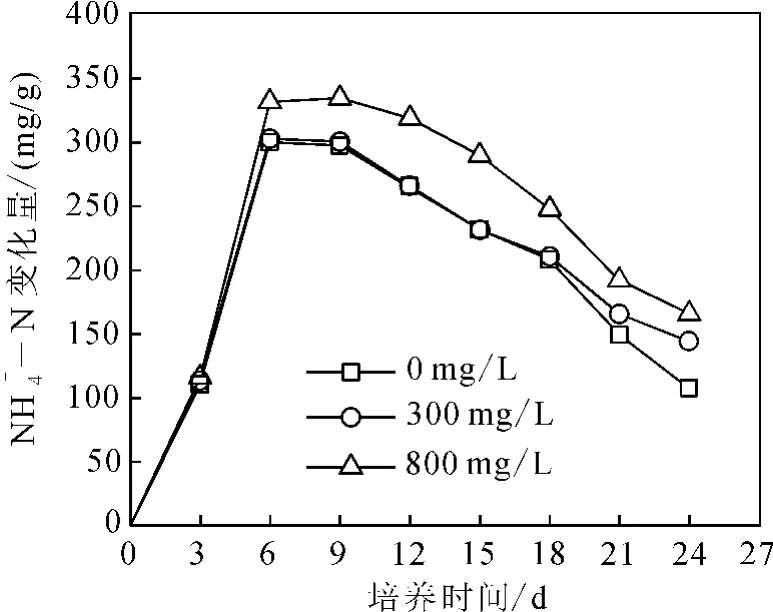
图6 不同土壤NH+4-N随时间的变化Fig.6 NH+4-N in soils versus time
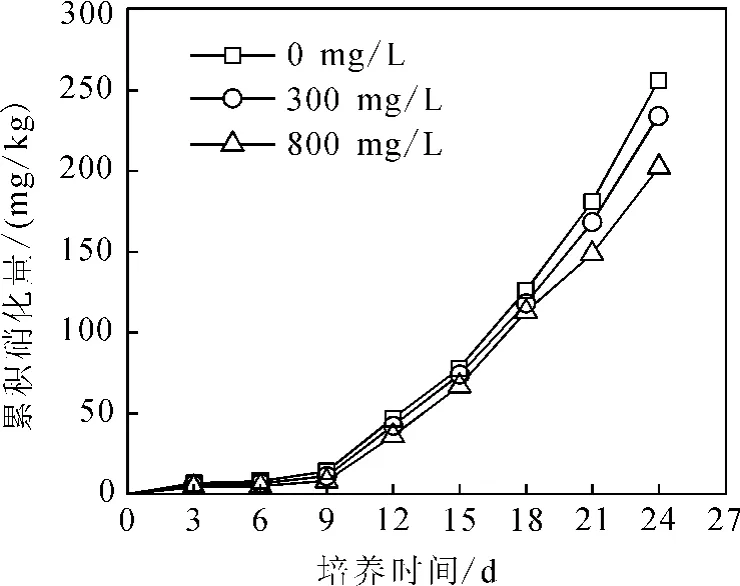
图7 不同土壤累积硝化量随时间的变化Fig.7 Cumulative nitrification in soils versus time
图7 为不同NaHCO3质量浓度土壤中累积硝化量(以NO-3-N质量分数(mg/kg)计)随时间的变化。从图7可以看出,各处理累积硝化量随时间延长而增大。培养结束时,NaHCO3质量浓度为300和800mg/L处理的累积硝化量(234.08和202.40mg/kg)分别是对照处理(255.96mg/kg)的91.5%和79.1%。培养过程中,相同时刻累积硝化量随着NaHCO3质量浓度的增大呈现降低的趋势,说明随着土壤中NaHCO3质量浓度的增大,硝化作用受到抑制。这是由于随着NaHCO3质量浓度的增大,硝化细菌的生物活性受到抑制。
2.4 NaHCO3和Na2CO3混合物对反硝化作用的影响
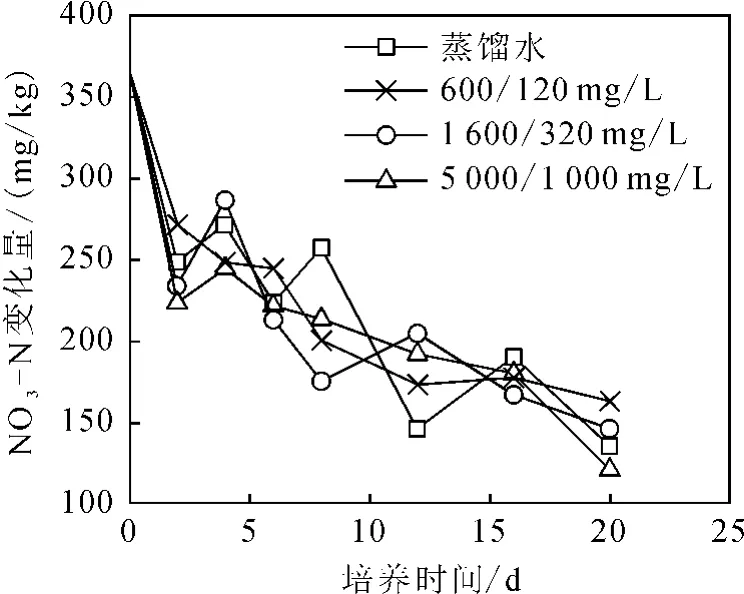
图8 NO-3-N随时间的变化Fig.8 NO-3-N in treatments versus time
图8为NO-3-N随时间的变化曲线。从图8中可以看出,不同处理的NO-3-N质量分数在整体上随时间延长呈降低的趋势,但是相同时刻不同盐碱化条件对-N质量分数影响不显著。图8表明,NaHCO3和Na2CO3混合质量浓度变化对反硝化作用影响不显著。培养过程中,体系pH变化基本保持稳定,表明反硝化细菌具有较强的耐碱耐盐性(pH为6.4~9.3)。
2.5 动力学分析
2.5.1 矿化动力学
采用Stanford等[9]的一阶反应动力学模型来模拟矿化随时间变化的过程:
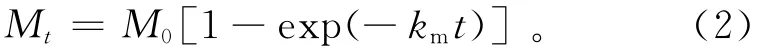
式中:M0为潜在矿化势,mg/kg;km为一阶矿化速率常数,d-1;Mt为累积矿化量,mg/kg;t为培养时间,d。对矿化参数拟合结果见表1。从表1可以看出,潜在矿化势和矿化速率常数随着土壤中NaHCO3质量浓度(ρ(NaHCO3))的增大而降低,说明NaHCO3对矿化的抑制作用部分是通过抑制土壤的潜在矿化势所致。
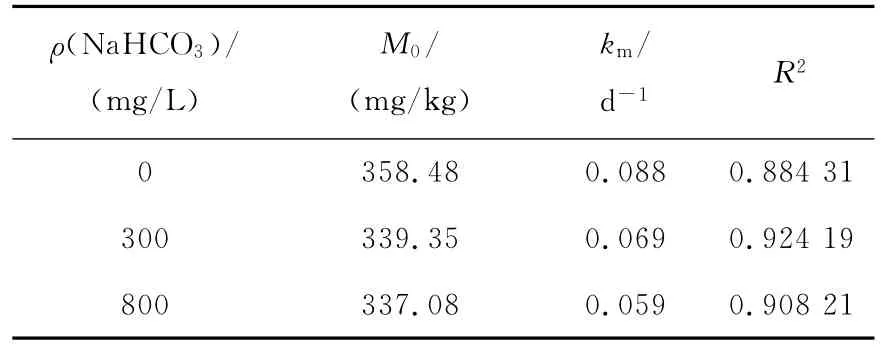
表1 矿化作用拟合参数Table 1 Fitted parameters for mineralization
2.5.2 硝化动力学
硝化作用速率呈“S”形曲线,分为迟缓阶段(硝化细菌数量生长时期)、最大速率阶段和停滞阶段[10]。从图7可以看出,培养过程明显分为迟缓阶段和最大速率阶段,可能由于培养时间较短,停滞阶段并未出现。选用dN/dt=bN(B-N)/B方程,其积分表示“S”形曲线[11-12]:
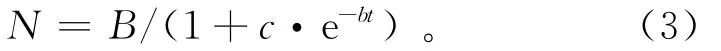
式中:N为累积硝化量,mg/kg;B为累积硝化量的渐进值,依赖于实验所加入土壤中NH+4-N的量;b,c为常数;t为培养时间,d。此硝化作用模型能够描述硝化作用曲线的3个阶段,由此导出2个函数最大速率(kmax)和迟缓期(td),能表征土壤的硝化特征。计算公式分别为
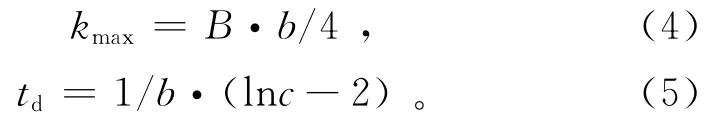
式中:kmax为最大硝化速率,mg/(kg·d);td为迟缓期,是最大斜率直线的外推与横坐标相交的时间,d。对硝化拟合计算结果见表2。从表2可以看出,最大速率kmax随着土壤中NaHCO3质量浓度的增大而减小,说明苏打盐碱土中NaHCO3对硝化作用产生抑制作用。
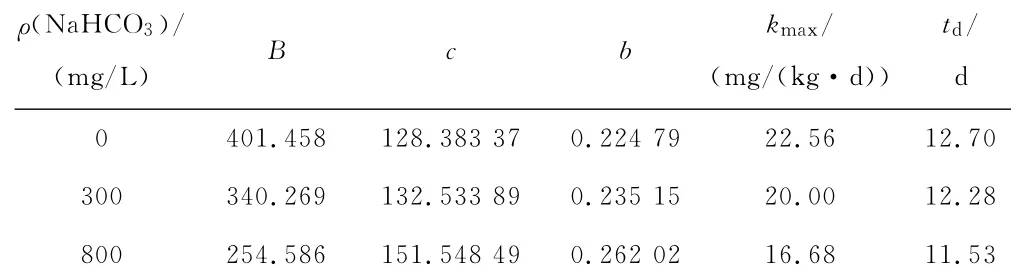
表2 硝化作用拟合参数Table 2 Fitted parameters for nitrification
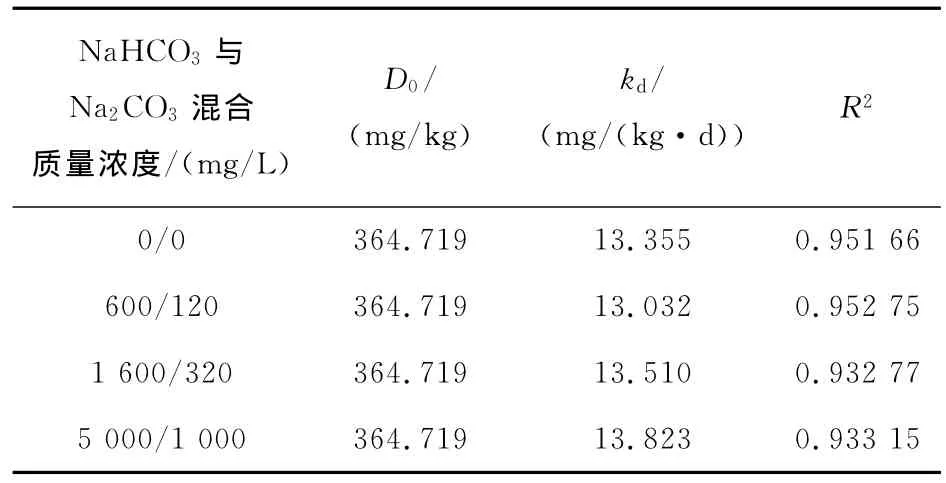
表3 反硝化作用拟合参数Table 3 Fitted parameters for denitrification
2.5.3 反硝化动力学
反硝化作用可用零阶动力学方程进行拟合:
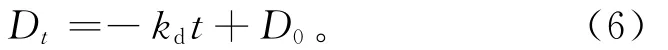
式中:D0为初始硝氮质量分数,mg/kg;kd为零阶反硝化速率常数,mg/(kg·d);Dt为t时刻硝氮质量分数,mg/kg。反硝化拟合参数见表3。从表3可以看出,NaHCO3与Na2CO3混合质量浓度变化对反硝化速率常数影响不显著。
3 结论
1)苏打盐碱土中随着NaHCO3质量浓度的增加,不利于NH+4-N的吸附。NH+4-N吸附符合Langmuir吸附等温式。
2)随着土壤中NaHCO3质量浓度的增大,有机氮矿化作用受到抑制;矿化模型符合一阶反应动力学方程;潜在矿化势和矿化速率常数随着土壤中NaHCO3质量浓度的增大而降低。
3)随着土壤中NaHCO3质量浓度的增大,硝化作用受到抑制,硝化作用可用“S”形曲线拟合;最大速率随着土壤中NaHCO3质量浓度的增大而减小。
4)土壤中NaHCO3和Na2CO3混合质量浓度变化对反硝化作用影响不显著。反硝化细菌具有较强的耐碱耐盐性。反硝化符合零阶反应动力学方程。
(References):
[1] 梁秀娟,肖长来,盛洪勋,等.吉林市地下水中“三氮”迁移转化规律[J].吉林大学学报:地球科学版,2007,37(2):335-340.
Liang Xiu-juan,Xiao Chang-lai,Sheng Hong-xun,et al.Migration and Transformation of Ammonia-Nitrite-Nitrates in Groundwater in the City of Jilin[J].Journal of Jilin University:Earth Science Edition,2007,37(2):335-340.
[2] Pathak H,Rao D L N.Carbon and Nitrogen Mineralization from Added Organic Matter in Saline and Alkali Soils[J].Soil Biology Biochemistry,1998,30(6):695-702.
[3] Inubushi K,Barahona M A,Yamakawa K.Effects of Salts and Moisture Content on N2O Emission and Nitrogen Dynamics in Yellow Soil and Andosol in Model Experiments[J].Biology and Fertility of Soils,1999,29(4):401-407.
[4] Badía D.Potential Nitrification Rates of Semiarid Cropland Soils from the Central Ebro Valley,Spain[J].Arid Soil Research and Rehabilitation,2000,14(3):281-291.
[5] 王龙昌,玉井理,永田雅辉,等.水分和盐分对土壤微生物活性的影响[J].垦殖与稻作,1998(3):40-42.
Wang Long-chang,Tamai Ri,Nagata Masaki,et al.Effects of Moisture and Salinity on Microbial Activity in Soil[J].Reclaiming and Rice,1998(3):40-42.
[6] 李建兵,黄冠华.NaCl对粉壤土氨挥发及硝化、反硝化的影响[J].农业环境科学学报,2006,25(4):945-948.
Li Jian-bing,Huang Guan-hua.Effect of NaCl on Ammonia Volatilization,Nitrification and Denitrification in Silt Loam Soil[J].Journal of Agro-Emvironment Science,2006,25(4):945-948.
[7] 李建兵,黄冠华.盐分对粉壤土氮转化的影响[J].环境科学研究,2008,21(5):98-103.
Li Jian-bing,Huang Guan-hua.Pilot Study of Salinity(NaCl)Affecting Nitrogen Transformation in Silt Loam Soil[J].Research of Environmental Sciences,2008,21(5):98-103.
[8] 徐万里,刘骅,张云舒.新疆盐渍化土壤氮素矿化和硝化作用特征[J].西北农林科技大学学报:自然科学版,2007,35(11):141-145.
Xu Wan-li,Liu Hua,Zhang Yun-shu.Characteristics of Nitrogen Mineralization and Nitrification in Salinized Soils of Xinjiang[J].Journal of Northwest Sci-Tech University of Agriculture and Forestry:Natural Science Edition,2007,35(11):141-145.
[9] Stanford G,Smith S J.Nitrogen Mineralization Potentials of Soils[J].Soil Science Society of America Journal,1972,36(3):465-472.
[10] Sabey B R,Frederick L R,Bartholomew W V.The Formation of Nitrate from Ammonium Nitrogen in Soils:III:Influence of Temperature and Initial Population of Nitrifying Organisms on the Maximum Rate and Delay Period[J].Soil Science Society of America Journal,1959,23(6):462-465.
[11] Hadas A,Sala F,Feigin A,et al.Nitrification Rates in Profiles of Differently Managed Soil Types[J].Soil Science Society of America Journal,1986,50(3):633-639.
[12] 张树兰,杨学云,吕殿青,等.几种土壤剖面的硝化作用及其动力学特征[J].土壤学报,2000,37(3):372-379.
Zhang Shu-lan,Yang Xue-yun,LüDian-qing,et al.Nitrification and Dynamics in Profiles of Differently Managed Soil Types[J].Acta Pedologica Sinica,2000,37(3):372-379.
Effects of Saline-Alkali Soil on Nitrogen Transformations
Zhang Xian-fu,Li Hui,Hong Mei,Song Bo-yu,Zhang Fu-quan,Liang Shuang
Key Laboratory of Groundwater Resources and Environment,Ministry of Education,Jilin University,Changchun 130021,China
The main component NaHCO3was considered as the main factor in Soda saline-alkali soil in order to study the effects of different soda salinization levels on nitrogen adsorption,mineralization,nitrification and denitrification by using laboratory incubation.The results showed that in the experimental conditions with the different NaHCO3concentrations,the NH+4-N adsorptions obeyed Langmuir linear adsorption isotherm,while,the N mineralization could be described by the first-order kinetic equation.With the increasing of NaHCO3concentration,the N mineralization potential(M0)and mineralization rate constant(km)decreased from 358.48mg/kg and 0.088d-1to 337.08mg/kg and 0.059d-1,respectively,and the nitrification could be described by“S”curve model,the maximal rate of nitrification(kmax)decreased from 22.56to 16.68mg/(kg·d);the denitrification obeyed zero-order kinetic equation,and there was no significant effect of mixed concentrations variation of NaHCO3and Na2CO3on the denitrification rate constant(kd).NH+4-N adsorption,organic nitrogen mineralization and nitrification were inhibited with NaHCO3concentrations increasing in soda saline-alkali soil.
soda saline-alkali soil;nitrogen;adsorption;nitrification;denitrification;kinetics
book=2012,ebook=535
X53
A
1671-5888(2012) 04-1145-06
2011-10-08
国家自然科学基金项目(41102146);国家水体污染控制与治理科技重大专项课题(2008ZXD7207-006-02)
张先富(1982-),男,博士研究生,主要从事地下水资源评价、模拟与管理,水土污染控制与治理方面的研究,E-mail:xuanfeng0528@163.com
洪梅(1972-),女,教授,主要从事污染场地控制与修复、土壤地下水环境污染模拟方面的研究,E-mail:hongmeizhangbo@163.com。

