蛋白酶体功能障碍通过激活P53抑制人骨髓间充质干细胞增殖*
刘雪芹, 宋慧芳, 陆 利
(山西医科大学人体解剖学教研室,山西 太原 030001)
人骨髓间充质干细胞(human bone marrow mesenchymal stem cells,hBMSCs)是存在于骨髓中的成体干细胞,因具有易获得、低免疫原性等特点成为医学组织工程理想的种子细胞[1-2]。然而,与体细胞相似hBMSCs也存在复制性衰老,因而限制了hBMSCs的临床应用。我们近期研究[3]显示蛋白酶体功能障碍与hBMSCs老化进程密切相关,应用蛋白酶体抑制剂MG132能够诱导早期hBMSCs细胞增殖能力下降,出现早衰现象,其潜在的调控机制亟待阐明。p53属于抑癌基因家族,位于染色体17p13.1,全长16~20 kb,编码分子量为53 kD的核内磷酸化蛋白。P53具有转录因子作用,在调控凋亡、发育、分化以及DNA修复等过程中扮演重要角色。有报道证实[4-5],P53作为细胞周期调节蛋白在细胞衰老进程发挥重要作用,抑制P53激活能够延缓成纤维细胞老化。那么,蛋白酶体功能障碍是否可能通过激活P53,进而导致晚期hBMSCs细胞增殖能力降低?为验证这一推测,我们进行了以下研究。
材料和方法
1 体外培养hBMSCs
hBMSCs购自 ScienCell Research Laboratory,含10%胎牛血清(HyClone)的DMEM(Gibco)培养基培养,待细胞生长至90%融合时进行传代。依据体外传代次数将hBMSCs分为早期组(第3~4代)与晚期组(≥14代)。
2 干预实验分组
早期hBMSCs依据干预条件不同分为:(1)DMSO(二甲基亚砜)对照组;(2)MG132组:10 μmol/L蛋白酶体抑制剂MG132作用4 h;(3)P53抑制剂pifithrin-α(PFT-α)+MG132组:20 μmol/L P53抑制剂PFT-α作用1 h随后加入终浓度为10 μmol/L MG132作用4 h。
晚期hBMSCs分为:(1)DMSO对照组;(2)PFT-α 组:20 μmol/L PFT -α 作用48 h。
3 蛋白酶体活性检测实验
收集早、晚期hBMSCs,用RIPA buffer提取蛋白质,BCA蛋白浓度测定试剂盒测定蛋白浓度,依照蛋白酶体活性分析试剂盒(Millipore)说明书进行操作,荧光酶标仪(Bio-Rad)检测分析。
4 Western blotting
收集早、晚期hBMSCs,用RIPA buffer提取蛋白质,BCA法测定蛋白浓度。取20μg总蛋白上样,10%聚丙烯酰胺凝胶电泳,将蛋白转印于PVDF膜,5%脱脂奶粉液封闭后加入Ⅰ抗:兔抗P53(1∶400,Santa Cruz),兔抗 β -actin(1∶2000,康为世纪生物科技有限公司)4℃孵育过夜。辣根过氧化物酶偶联抗兔Ⅱ抗室温杂交2 h(1∶5000,中杉金桥),按照化学发光检测试剂盒(GE Healthcare Life Science)说明书曝光显影于胶片。
5 BrdU掺入实验检测hBMSCs增殖能力
含 BrdU(终浓度 10 μmol/L)10%FBS-DMEM培养基培养细胞72 h,4%多聚甲醛室温20 min固定细胞,加入2 mol/L HCl 37℃水浴10 min使DNA变性,鼠抗 BrdU(1∶100,Abtech Biotechnology)4 ℃孵育过夜,山羊抗鼠Cy3(1∶100,Invitrogen)37℃孵育2 h,DAP封片液封片,Olympus荧光显微镜计数、拍片。
6 流式细胞术检测细胞周期
收集细胞,70%冷乙醇4℃固定4 h,1000 r/min室温离心5 min弃上清,PBS重悬细胞团,300目网过滤,加入50 mg/L碘化丙啶(PI)染液,室温避光20 min后流式细胞仪进行检测。
7 统计学处理
采用SPSS 16.0软件进行统计分析,数据以均数±标准差()表示,多组间的比较采用Oneway ANOVA方差分析,两组间比较采用t检验,以P<0.05为差异有统计学意义。
结 果
1 早、晚期hBMSCs蛋白酶体活性及P53表达变化
传代晚期hBMSCs蛋白酶体活性较早期细胞降低31.06% ±3.67%(P <0.01),见图 1A。Western blotting结果显示,晚期hBMSCs P53表达水平为早期细胞的 1.2倍(P <0.05),见图 1B、C,提示晚期hBMSCs伴随蛋白酶体活性降低,P53表达上调、活性增强。
2 阻断P53对蛋白酶体功能障碍hBMSCs增殖能力的影响
BrdU掺入实验结果显示,MG132组BrdU阳性率(33.36% ±2.24%)较 DMSO 对照组(72.80% ±7.46%)显著降低(P<0.01),提示抑制蛋白酶体活性可抑制hBMSCs增殖潜能。PFT-α +MG132组BrdU阳性率(49.23% ±2.67%)显著高于MG132组(33.36% ±2.24%;P <0.05),提示阻断 P53 活化能够削弱蛋白酶体功能障碍对hBMSCs增殖能力的影响,见图2。
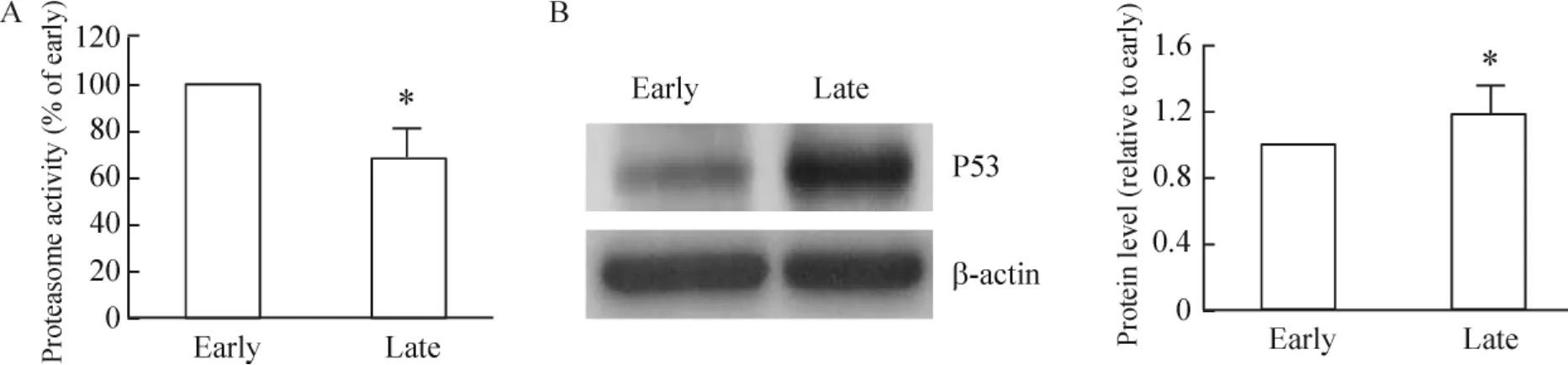
Figure1.The decreased proteasomal activity(A)and elevated P53 expression(B)in late-passage hBMSCs..n=4.*P<0.05 vs early.图1 晚期hBMSCs蛋白酶体活性和P53的表达

Figure2.The influence of inhibition of P53 on proliferation of hBMSCs with proteasome dysfunction assayed by BrdU incorporation.BrdU-positive cells were shown in red and nuclei were counterstained with DAPI(blue).Scale bar=100 μm..n=15.**P <0.01 vs DMSO control group;#P <0.05 vs MG132 group.图2 BrdU掺入法检测阻断P53对蛋白酶体功能障碍hBMSCs增殖的影响
3 阻断P53对蛋白酶体功能障碍hBMSCs细胞周期的影响
流式细胞术分析结果显示,MG132组G1期细胞较DMSO对照组显著增加,S期和G2/M期细胞减少,增殖指数显著低于DMSO组(P<0.01)。PFT-α+MG132组各期细胞分布与DMSO对照组相似,增殖指数显著高于MG132组(P<0.05)。结果提示蛋白酶体活性下调可使hBMSCs阻滞于G1期,抑制P53激活则能够促使细胞越过G1/S转换点,进而恢复hBMSCs增殖能力,见表1。
4 P53抑制剂对晚期hBMSCs增殖能力的影响
BrdU掺入实验结果显示,PFT-α组BrdU阳性率34.42% ±8.35%显著高于DMSO对照组9.68%±5.23%(P <0.01),提示抑制 P53 活性有助于维持晚期hBMSCs增殖潜能,见图3。
表1 流F式细胞术检测hBMSCs细胞周期分布Table1.Cell cycle distribution of hBMSCs measured by flow cytometry(%..n=4)
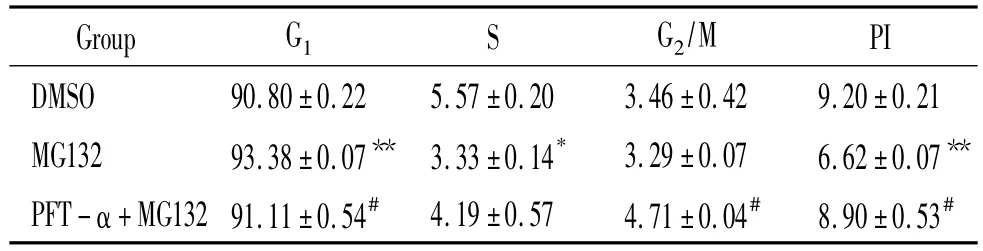
表1 流F式细胞术检测hBMSCs细胞周期分布Table1.Cell cycle distribution of hBMSCs measured by flow cytometry(%..n=4)
*P <0.05,**P <0.01 vs DMSO control group;#P <0.05 vs MG132 group.
Group G1 S G2/M PI DMSO 90.80±0.22 5.57±0.20 3.46±0.42 9.20±0.21 MG132 93.38±0.07** 3.33±0.14* 3.29±0.07 6.62±0.07**PFT-α +MG13291.11±0.54# 4.19±0.57 4.71±0.04# 8.90±0.53#

Figure3.The effect of PFT-α on late-passage hBMSCs assayed by BrdU incorporation.BrdU -positive cells were shown in red and nuclei were counterstained with DAPI(blue).Scale bar=100 μm..n=15.**P<0.01 vs DMSO control group.图3 BrdU掺入法检测PFT-α对晚期hBMSCs增殖的影响
讨 论
间充质干细胞是来源于中胚层的具有高度自我更新能力和多向分化潜能的成体干细胞,广泛存在于全身结缔组织和器官间质中,以骨髓组织中含量最为丰富。hBMSCs不仅能够向多种组织和细胞分化,而且易于外源基因的导入和表达,遗传背景稳定,已经成为组织工程、细胞治疗、基因治疗等方面的研究热点。然而,组织工程需要高浓度细胞进行移植接种,源自体内的hBMSCs存在数量上的局限性,需经体外扩增后用于移植治疗。新近的研究与我们的报道证实[6-7],伴随传代次数增多 hBMSCs出现老化现象,表现为胞体变大、胞浆内颗粒物聚集,细胞增殖和分化潜能下降,hBMSCs的老化现象直接限制了其临床应用。
蛋白酶体是体内除溶酶体之外的另一重要蛋白水解体系,它通过降解泛素化的底物蛋白参与维持细胞内环境稳态。我们的前期研究结果表明[3],蛋白酶体与hBMSCs功能的维持密切相关,抑制蛋白酶体活性能够诱导早期hBMSCs出现早衰表型;相反,若激活蛋白酶体活性则能维持hBMSCs增殖潜能和分化潜能。本研究结果也证实晚期hBMSCs蛋白酶体活性较早期细胞降低31.06% ±3.67%,应用蛋白酶体抑制剂MG132能够诱导早期hBMSCs细胞出现衰老细胞的特征,表现为G1期细胞增多,S期和G2/M期细胞减少,细胞生长阻滞于G1期,进一步表明蛋白酶体是维持hBMSCs细胞活力的重要因素。Arslan 等[8]和 Chondrogianni等[9]研究也证明,抑制蛋白酶体活性能够使细胞内错误折叠蛋白和氧化蛋白堆积,造成细胞周期停滞,增殖能力降低,细胞抵御氧化应激和热应激的能力下降。
P53是一种短半衰期转录因子,其稳定性主要由泛素-蛋白酶体水解途径调节,P53在细胞周期调节、凋亡、衰老、分化等多种生物过程中发挥重要作用[10]。本研究结果显示晚期hBMSCs伴随蛋白酶体活性降低,P53表达水平增高,提示P53激活可能是蛋白酶体功能障碍导致晚期hBMSCs增殖能力降低的重要下游事件。应用P53抑制剂PFT-α能够削弱蛋白酶体功能障碍对hBMSCs增殖能力的影响,PFT-α +MG132组 BrdU阳性率(49.23% ±2.67%)显著高于 MG132 组(33.36% ±2.24%)。此外,PFT-α +MG132组细胞周期分布与DMSO对照组相似,G1期细胞较MG132组减少,S期和G2/M期细胞增多,提示抑制P53激活能够促使细胞越过G1/S转换点,进而恢复hBMSCs增殖能力。Liu等[11]应用p53-shRNA慢病毒表达载体转染hBMSCs,他们发现沉默p53基因能够推迟hBMSCs衰老进程,p53-shRNA组细胞于第21代出现胞体增大、衰老标志物β-Gal活性上调、细胞增殖能力下降等老化征象,但是单纯抑制p53基因并不能使hBMSCs永生化逃离老化命运。我们在研究中发现P53抑制剂介导的保护作用仅限于蛋白酶体功能障碍的晚期hBMSCs,抑制P53激活并不能影响早期hBMSCs的增殖能力,说明晚期细胞增殖活力下降可能是由于蛋白酶体活性下调,造成P53积聚、激活等综合作用的结果。今后仍需在蛋白质、基因水平深入研究泛素-蛋白酶体通路及其下游事件在hBMSCs增殖过程中的调控机制,建立高效、科学的扩增方式,推动hBMSCs在组织工程学中的应用。
[1]Bianco P,Riminucci M,Gronthos S,et al.Bone marrow stromal stem cells:nature,biology and potential applications[J].Stem Cells,2001,19(3):180 -192.
[2]Lu L,Chen X,Zhang CW,et al.Morphological and functional characterization of predifferentiation of myelinating glia-like cells from human bone marrow stromal cells through activation of F3/Notch signaling in mouse retina[J].Stem Cells,2008,26(2):580 -590.
[3]Lu L,Song HF,Zhang WG,et al.Potential role of 20S proteasome in maintaining stem cell integrity of human bone marrow stromal cells in prolonged culture expansion[J].Biochem Biophys Res Commun,2012,422(1):121-127.
[4]Ben-Porath I,Weinberg RA.The signals and pathways activating cellular senescence[J].Int J Biochem Cell Biol,2005,37(5):961 -976.
[5]Shay JW,Wright WE.Senescence and immortalization:role of telomeres and telomerase [J].Carcinogenesis,2005,26(5):867-874.
[6]Mareschi K,Ferrero I,Rustichelli D,et al.Expansion of mesenchymal stem cells isolated from pediatric and adult donor bone marrow[J].J Cell Biochem,2006,97(4):744-754.
[7]Yew TL,Chiu FY, TsaiCC, etal. Knockdown of p21Cip1/Waf1enhances proliferation,the expression of stemness markers,and osteogenic potential in human mesenchymal stem cells[J].Aging Cell,2011,10(2):349 -361.
[8]Arslan MA,Chikina M,Csermely P,et al.Misfolded proteins inhibit proliferation and promote stress-induced death in SV40-transformed mammalian cells[J].FASEB J,2012,26(2):766-777.
[9]Chondrogianni N,Stratford FL,Trougakos IP,et al.Central role of the proteasome in senescence and survival of human fibroblasts:induction of a senescence-like phenotype upon its inhibition and resistance to stress upon its activation[J].J Biol Chem,2003,278(30):28026-28037.
[10]Pittenger MF,Mackay AM,Beck SC,et al.Multilineage potential of adult human mesenchymal stem cells[J].Science,1999,284(5411):143-147.
[11]Liu TM,Ng WM,Tan HS,et al.Molecular basis of immortalization of human mesenchymal stem cells by combination of p53 knockdown and hTERT overexpression [J].Stem Cells Dev,2012 Aug 21.[Epub ahead of print].

