电解液中添加LiBOB改善LiMn2O4的高温性能
宋晓娜,王锦富
(1.浙江天虹能源科技有限公司,浙江湖州 313100;2.杭州金色能源科技有限公司,浙江杭州 311400)
尖晶石LiMn2O4存在比容量低,容量衰减较快,尤其是高温循环性能差等缺点[1]。容量衰减的主要原因是Jahn-Teller畸变和 Mn在电解液中的溶解。离子掺杂可抑制Jahn-Teller畸变,但Mn在电解液中溶解的问题,还未得到有效解决[2]。在高温条件下,Mn容易溶解并沉积在阳极上。
双草酸硼酸锂(LiBOB)可抑制M n的溶解。LiBOB的热稳定好,分解温度达300℃,成膜性能好;但导电性能较差,会降低电池的低温性能,LiBOB形成的固体电解质相界面(SEI)膜较厚,会导致负极阻抗急剧上升[3]。LiPF6导电性能优异,但热稳定性不好,遇到微量水分或其他杂质,易分解为LiF、HF,限制了电池的工作温度、高温性能及动力性能。
为了综合LiPF6和 LiBOB的优点,本文作者把LiBOB作为电解液添加剂加入到以LiPF6为锂盐的电解液中,试图改善LiMn2O4的性能,尤其是高温性能。
1 实验
正极极片的制备:将活性物质[LiMn2O4(河北产,AR)+LiCoO2(北京产,AR)质量比4∶1]、导电炭黑(上海产,AR)和聚偏氟乙烯(PVDF,法国产,AR)按照质量比 95.0∶2.5∶2.5配制成浆料,再按照面密度1.82 g/dm2进行涂覆,集流体为14μ m厚的铝箔(上海产,99.8%);涂覆后辊压(压实密度为3.0 g/cm3),然后进行分切,极片宽度为64 mm。
负极极片的制备:将石墨(宁波产,AR)、羧甲基纤维素钠(CMC,荷兰产,AR)和丁苯橡胶(SBR,广州产,AR)按照质量比94∶3∶3配成浆料,再按照面密度0.78 g/dm2进行涂覆,集流体为8μ m厚的铜箔(长春产,99.8%);涂覆后辊压(压实密度为1.5 g/cm3);然后进行分切,极片宽度为66 mm。
电解液为 1 mol/L LiPF6/EC+PC+DEC(体积比 1∶1∶1,广州产,AR),电解液中添加1%的LiBOB(德国产,AR);隔膜为Celgard聚丙烯多孔膜(ED16,美国产)。按照生产线流程制作506971型锂离子电池。化成、容量及恒流充放电测试在 RF2T3005型电池测试系统(深圳产)上进行,电压为3.0~4.2 V,电流为 0.50 C。化成步骤为:静置 5 min,以0.02 C恒流充电至3.4 V;再以0.10 C恒流充电至3.9 V,静置5 min。在CHI660B型电化学工作站(上海产)上进行电化学阻抗测试,频率为10 Hz~100 kHz,振幅为5 mV。
2 结果与讨论
2.1 电化学阻抗谱的分析
电解液中添加LiBOB前后,电池的电化阻抗谱及相关数据见图1、表1,样品均为2只。
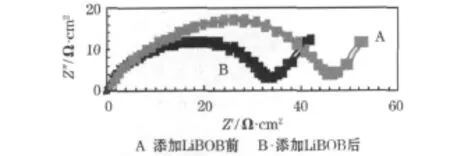
图1 电解液中添加LiBOB前后电池的电化阻抗谱Fig.1 Electrochemical impedance spectroscopy(EIS)plots of battery with electrolyte before and after adding LiBOB

表1 电解液中添加LiBOB前后电池的电化学阻抗数据Table 1 EIS data of battery with electrolyte before and after adding LiBOB
从图1及表1可知,电解液中添加LiBOB后,SEI膜的阻抗增大,表明SEI膜变得更致密。K.Xu等[4-5]用X射线光电子能谱及红外光谱分析LiBOB形成的SEI膜,发现膜中含原硼酸根(BO33-)、草酸根(C2O42-)及羧酸根(CO3COO-)等官能团,认为SEI膜的稳定性与它们的存在有关。
2.2 化成曲线的分析
添加 LiBOB前后电池的化成曲线见图2,样品均为2只。

图2 电解液中添加LiBOB前后电池的化成曲线Fig.2 Formation curves of battery with electrolyte before and after adding LiBOB
从图2可知,电解液中添加LiBOB前后,电池的化成曲线发生了明显的变化。在2.0~2.5 V,加入LiBOB后电池的曲线明显低于未加入LiBOB时,表明LiBOB在2.0 V左右开始形成SEI膜,在形成SEI膜的过程中,消耗了一部分Li+,导致电压偏低;在2.6~3.2 V,未加入 LiBOB的电池的曲线比加入LiBOB的电池低,应该是PC成膜所致。
2.3 充放电性能的分析
电解液中添加LiBOB前后,电池的循环性能及数据见图3、表 2。45℃时的样品均为3只,60℃时的样品均为5只。

图3 添加LiBOB前后电池的循环性能Fig.3 Cycle performance of battery with electrolyte before and after adding LiBOB

表2 添加LiBOB前后电池的循环数据Table 2 Cycle performance data of battery with electrolyte before and after adding LiBOB
从表 2和图3可知,电解液中添加 LiBOB前后,电池的首次放电比容量差别不大,添加LiBOB后略低一些,是由于LiBOB在形成SEI膜时消耗了较多的Li+。添加LiBOB改善了电池的循环性能,是由于添加LiBOB后,极片表面形成的 SEI膜较致密,且热稳定性较好,抑制了Mn的溶解[2]。
3 结论
LiBOB作为添加剂加入到电解液后,电池的电化学阻抗有所增大;化成曲线的结果表明,添加LiBOB后SEI膜形成的电位降低。从高温循环性能及放电容量数据可知,LiBOB可改善正极材料LiMn2O4的高温循环性能。
[1]CAI Zhen-ping(蔡振平),LI Ming-xun(李明勋),LU Shi-gang(卢世刚),et al.LiCoO2改性 LiMn2O4的结构及性能[J].Battery Bimonthly(电池),2005,35(2):89-91.
[2]Amine K,Liu J,Kang S,et al.Improved lithium manganese oxide spin/graphite Li-ion cells for high power application[J].J Power Sources,2004,19(1):14-21.
[3]Zinigrad E,Larush-Asraf L,Salitra G,et al.On the thermal behavior of Li bis(oxalate)borate LiBOB[J].Thermochim Acta,2007,457(3):64-69.
[4]Xu K,Lee U,Zhang S M,et al.Chemical analysis of graphite/electrolyte interface formed in LiBOB-based electrolytes[J].Electrochem Solid-State Lett,2003,6(7):A144-A148.
[5]Zhuang G V,Xu K,Jow T R,et al.Study of SEI layer formed on graphite anodes in PC/LiBOB electrolyte using IR spectroscopy[J].Electrochem Solid-State Lett,2004,8(7):A224-A230.

