碳材料在锂空气电池中的应用及研究进展
武 巍,田艳艳,高 军,杨 勇
(厦门大学化学化工学院固体表面物理化学国家重点实验室,福建 厦门 361005)
1 前言
1.1 锂空气电池简介
锂空气电池的概念最早是由Lockheed的研究人员在1976年提出[1],它是将金属锂作为负极,空气(或氧气)作为正极,以及碱性水溶液作为电解液组成的一种金属-空气电池。这种锂空气电池放电时,来自大气中的氧气在空气电极(正极)表面还原,形成氧化物或氢氧化物,电池电压为2.21 V。电池反应为:
正极 O2+2 H2O+4 e→4 OH-
负极 Li-e→Li+
电池总反应4 Li+O2+2 H2O→4 LiOH
这种电池存在锂负极在水性电解液中发生反应的问题。而后在1996年,由Abraham和Jiang提出了一种基于聚合物电解质/有机电解液体系的锂空气电池[2],由于聚合物电解质可延缓水在电解质的传输,可部分解决负极锂腐蚀的问题。它是以锂作为负极,多孔碳电极作为正极,聚合物电解质膜作为隔膜和离子传输中介(即电解质)。电池开路电压在3 V左右,其放电电压在2.0~2.8 V。该电池反应为:
正极 1/2 O2+2 e→ O2-或 O2+2 e→O22-
负极 Li-e→Li+
电池总反应4 Li+O2→2 Li2O或2 Li+O2→Li2O2
从那以后,应用聚合物电解质或有机电解液的锂空气电池才受到较多的重视。
在所有金属中,锂的原子量最小,密度最低并且电负性最大,它非常容易失去电子形成阳离子,因此以锂及其化合物为负极材料的化学电源具有较高的比容量和电压[3]。在锂空气电池中,氧气不需要储存在电池体系中而是由空气中扩散到空气电极(正极)表面并发生还原,因此它在所有的化学电源中就具有最高的理论比能量。如果仅以负极锂的质量计算,它的理论比能量是11140 Wh/kg(比容量是3862 mAh/g Li[4]);如果将正极活性物质氧气的质量也计算在内,它的比能量为5200 Wh/kg[2]。Zheng等人[5]将锂负极、空气电极(碳材料)和电解液的质量之和作为电池质量,分别计算了锂空电池在水性电解液和有机电解液的理论比容量和比能量,计算结果表明:水性电解液中分别为378~435 mAh/g和1300~1400 Wh/kg,有机电解液中分别为940 mAh/g和2790 Wh/kg。正因为锂空气电池具有很高的比容量与比能量,近年来受到人们广泛关注。
近些年关于锂空气电池的文献报道中多应用液态有机电解液或固态聚合物电解质,这种电池虽解决了锂负极与水反应的问题,但又带来了新的问题:由于放电产物Li2O2或Li2O不溶于有机电解液,在电池放电的过程中,将逐渐堵塞气体扩散电极的孔道,从而导致氧气传输的路径和发生氧还原的活性表面越来越少,从而导致正极失效,电池放电终止[6]。因此人们意识到要提高有机电解液体系的锂空气电池的放电容量,空气电极是关键因素。Wang和Zhou提出了一种新型锂空气电池[7],它是在正极和负极端分别应用水性电解液和有机电解液,两种电解液以一种无机锂离子导体膜(例如LISICON)隔开。这种电池实现了50000 mAh/g的放电容量,成功解决了正极孔堵塞和负极锂与水反应的问题,但它的LISICON膜的导电性及其在碱性水溶液中的稳定性成为了制约电池性能的关键因素。本文拟重点讨论空气电极及其碳材料对锂空气电池的影响,鉴于水性电解液中空气电极的碳材料应用研究已有较多的文献报道及其总结,因此本文主要讨论关于有机电解液或固态聚合物电解质相关的空气电极及其相关碳材料。
1.2 空气电极的结构与性能
锂空气电池中所用的空气电极,即气体扩散电极与其它金属空气电池中的空气电极结构类似,其基本构成主要有透气层、集流体和催化层[8],如图1所示。这种结构的空气电极的优势在于很容易形成气-液-固三相反应界面。透气层一般是以PTFE为主要材料制成,它是多孔、电解液非浸润,能够为氧气进入催化层提供通道。在它的催化层一面接触电解液时,有一指向电解液内部的表面张力,正是由于这种表面张力的作用,不仅使得空气能通过多孔的空气电极进入电解液,而且能防止电解液堵塞空气电极的气体扩散通道或者渗漏出来。催化层是实际发生电化学反应的界面,它的载体通常选用碳材料。因为碳材料不仅具有较好的导电性、较强的氧吸附性以及氧还原催化活性,而且它的微观多孔结构还能为不可溶的放电产物提供储存空间。对于空气电极,碳材料并没有显著参与电化学反应,而只是作为氧电化学还原的反应介质。
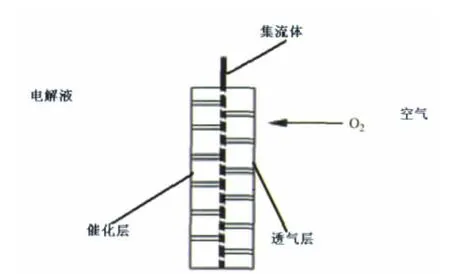
图1 锂空气电池中空气电极结构示意图[8]
空气电极是影响锂空气电池性能的关键因素。经过研究发现,锂空气电池正极内部的形貌、孔径、孔体积、比表面积、电极的厚度以及导电性等因素对电池的放电容量有很大的影响[9]。而上述这些因素除了与电极制作工艺有关外,还与碳材料的种类有着最直接的关系,因为碳材料在空气电极中既充当电化学反应界面又为放电产物提供储存空间,因此碳材料的选择与优化成为提高有机电解液锂空气电池电化学性能的关键。在近几年所报道的文献中,很多种类的碳材料都被尝试用于制作锂空气电池的空气电极。尽管不同的研究者所采用的空气电极制作方法、催化剂的使用、电池组装方式、电解液成分以及放电条件等实验方法略有不同,但仍能为碳材料的选择提供一个参考。
2 空气电极中常用碳材料及其性能
在有关锂空气电池的文献报道中,应用于其空气电极的碳材料种类很多,主要有Super P(比利时M.M.M.碳材料公司)、Norit碳黑 (SX,Norit公司生产)、Ketjin black(EC600JD,Akzo Nobel公司)、Darco G-60 活性碳(美国 Notir公司)等等。对于不同碳材料,其导电性、颗粒尺寸、孔径、孔体积以及比表面积等物理性质有很大差异,它们应用在锂空气电池空气电极中的性能差别也非常大。
2.1 Super P
Super P是应用于锂空气电池正极最多的一种碳材料。与很多碳材料相比,Super P的比表面积相对较低,只有62 m2/g。但是许多文献[6,9-20]报道使用Super P碳材料的空气电极放电比容量却较高,达到1300~2300 mAh/g(0.1 mA/cm2的电流密度放电),如果在其上负载纳米尺度的MnO2催化剂,放电比容量可达到3400 mAh/g(70 mA/g碳)[12]。由此说明,尽管碳材料的比表面积是一个重要的参数,却不是唯一的参数。

图2 三种碳材料(a)Super P;(b)BP2000;(c)VGCF的SEM图[21]
至于为何Super P具有较小的比表面积却能达到较高的放电容量的原因,我们的研究结果认为[21]:碳材料分为基面和边缘面两个部分,基面上的碳原子一般具有饱和的结构,因此活性较低;而边缘面上的碳原子由于结构不饱和,因此具有较高的活性。从图2(a)的Super P碳材料的扫描电子显微镜(SEM)图中可以看出,Super P呈现颗粒状,因此其边缘面所占的面积相应的比较大;而有些碳材料,如图2(b)中所示的BP2000,其微观结构呈现条状,其表面积主要是由基面的面积构成,而基面几乎是没有活性的,因此其表面积虽然大,但是由于真正起作用的边缘面的面积不大,因此其电化学性能明显不如Super P。图2(c)中所示的VGCF呈棒状,其比表面积很小,而且其具有活性的边缘面所占比例更小,因此其电化性性能更差。也就是说尽管Super P的比表面积不大,但是它的有活性的表面积比较大,因此放电容量较大。
有一种类似的观点[22]认为,很多碳材料的比表面积主要来自于微孔,如果这些微孔中充满了电解液,而使氧无法在其中扩散,对放电容量没有贡献;即便有些较大的孔可以接触到电解液中的溶解氧,但这些孔的表面只有极少一部分面积有氧还原活性。因此也可以解释为这些具有较高比表面积的碳材料实际活性表面积没有Super P大,因此放电容量也比Super P要差。还有一种观点[11]认为,Super P的粒子尺度约为40 nm,放电产物主要堆积在由其纳米粒子间隙形成的约50 nm的孔中。这种孔的体积越大,能存放的放电产物越大,其放电容量也会越大。有文献报道[20],Super P的孔体积是0.32 cm3/g。可能具有几十纳米的粒子的碳材料对于锂空气电池是比较好的。Super P粒子间隙能存放大量的放电产物,这可能就是它尽管没有很大的比表面积,却有比许多碳材料放电容量大得多的原因。
以上几种解释都不约而同的说明了碳材料微观形貌的重要性。可以认为:Super P较为优异的性能正是缘于其优越的微观形貌,使其比表积、孔体积、孔径等因素适合锂空气电池。
2.2 介孔碳
介孔碳[Mesocellular carbon foams(MCF-C)]材料在锂空气电池中应用较少,它是应用蔗糖和介孔硅材料合成的。夏永姚等人[11]报道了介孔碳在锂空气电池中的应用,并取得了较高的放电容量。
介孔碳具有大小一致的球型胞状孔,碳胞的内径是28 nm,外径是35 nm,孔径30 nm左右;其BET比表面积是824 m2/g,孔体积为1.45 cm3/g。它具有高的比表面积和大的孔体积。
他们的研究结果表明,在0.1 mA/cm2的放电电流密度下,放电比容量达到了2500 mAh/g。相对于Super P,介孔碳具有更大的比表面积,碳胞内部表面也具有氧还原活性。如图3所示,它微观上的窗口结构为电解液和氧气进入碳壳内部的空腔提供了通道;而且它的直径约30 nm的内孔也能容纳放电产物,放电产物不仅沉积在碳粒之间,还沉积在碳粒内部。而普通的碳黑材料仅能在粒子的外表面发生氧还原,并且放电产物也仅能储存在粒子外部的孔中。这也就是说,介孔碳具有比Super P更高的活性表面积和更大的可容纳放电产物的空间[11]。
2.3 Norit碳黑

K.Scott等人将负载纳米MnO2催化剂的Norit碳黑(SX,Norit公司生产)应用于锂空气电池的空气电极中,在70 mA/g(碳)的放电电流(放电至2 V)下,达到了4400 mAh/g的放电比容量[12]。Norit碳黑具有比较大的比表面积,为800 m2/g。K.Scott等人发现相比于其它具有较低比表面积的碳材料,纳米MnO2催化剂在Norit碳黑表面分散得更好,催化剂与它的接触面积更大,因此催化剂活性更高,放电容量也更高[12]。这表明了碳材料的比表面积(不一定是活性比表面积)在某种程度对空气电极的放电容量具有影响,尤其是应用催化剂负载于碳材料上时,这方面的影响更加明显。
2.4 M-30碳
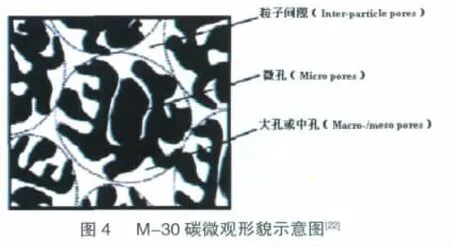
M-30碳由Osaka气体化学公司生产。它比表面为2500~3200 m2/g,粒径为 25~30 μm[18,22]。以 LiSO3CF3/PC∶DME(1∶3)为电解液,以0.05 mA/cm2的电流密度放电至2.0 V,放电容量约为1500 mAh/g,以0.1 mA/cm2的电流密度放电至2.0 V,放电容量约为800 mAh/g[18]。M-30碳材料虽然具有很高的比表面积,但其主要来源于微孔的贡献。若这些微孔中充满了电解液,而使氧无法在其中扩散,则其对放电容量没有贡献。而其大孔可以接触到电解液中的溶解氧,但这些孔的表面只有极少一部分面积有氧还原活性[22]。其微观形貌示意图如图4所示。因此,粒子间隙对锂空气电池放电容量起到重要作用。理想状态是所有粒子间隙都对氧是开放的,即气态氧能自由地通过这些孔隙,否则氧在电解液中的低扩散速率导致低的放电容量。
2.5 Ketjin black碳
Ketjin black,由Akzo Nobel公司生产,应用于锂空气电池的较常用的有两种型号:Ketjin black(EC600JD)和Ketjin black(EC300JD),前者应用较多。
Ketjin black(EC600JD)的比表面积是2672 m2/g[23](也有报道称是1400 m2/g[12])。它的孔体积是7.6510 cm3/g(也有报道称是1.2 cm3/g[24]或2.47 cm3/g[20]),孔尺寸为2.217~15 nm,其孔隙率为39%,粒子尺度约40 nm[25]。Ji-Guang Zhang等人[18]将Ketjin black(EC600JD)应用于扣式锂空气电池中,以0.05 mA/cm2的电流密度恒流放电至2.0 V,再在2.0 V以恒压放电至I/5=0.01 mA/cm2,放电容量为851 mAh/g。他们还将Ketjin black(EC600JD)进行球磨,得到的材料的比表面积和孔体积反而大大降低,分别为342 m2/g和0.43 cm3/g,而其电池比容量仅有47 mAh/g。
Ketjin black(EC300JD)的比面积是 890 m2/g,孔体积是1.98 cm3/g[20],粒子尺度约 30 nm[24]。韩国的 C.K.Park 等[20]人将些种碳材料应用于扣式电池中,以0.1 mA/cm2的电流密度恒流放电至1.5 V,得到约2200 mAh/g的放电比容量。
2.6 Darco G-60活性碳
Darco G-60活性碳也是一种在锂空气电池中较常应用的碳材料,在多篇文献中有报道[26-29]。它是由美国Notir公司生产。Ji-Guang Zhang等人将Darco G-60、二氧化锰催化剂和PTFE溶液混合后制成电极,以0.05 mA/cm2的电流密度恒流放电至2.0 V,得到了20~180 mAh/g的容量[28]。Jian Zhang等人以0.05 mA/cm2的电流密度恒流放电至2.0 V得到了约280 mAh/g 的容量[26]。
2.7 其它碳材料
还有另外一些碳材料在锂空气电池中的应用也有文献报道,包括Shawinigan Black乙炔黑(SAB,Chevron Phillips化学公司生产,比表面积 70 m2/g)[9,24]、Vulcan XC-72(比表面积2500 m2/g)[11,30]、Black Pearls 2000(Cabot公司生产,比表面积1567 m2/g,孔体积 0.835 cm3/g)[9,16]、Super S(比利时 M.M.M.碳材料公司)[31-32]、Calgon活性碳(Calgon碳材料公司,比表面积 1006 m2/g,孔体积 0.546 cm3/g,孔隙率 69%)[16,23]、Denka(日本Denka公司,比表面积102 m2/g,孔体积0.535 cm3/g)[16,20]、Ensaco 250G(比表面积62 m2/g,孔体积0.18 cm3/g)[20]、YEC8(福州Yihuan碳材料公司,比表面积1550 m2/g)[33]、Chevron乙炔黑(休斯顿Chevron化工集团,比表面积40 m2/g)[2]以及碳纳米管(比表面积40 m2/g,孔径10 nm)[11]和石墨(比表面积5~6 m2/g)[2,11]等。由这些碳材料制作的锂空气电池在不同的放电电流下,所得的放电比容量在50~3900 mAh/g,因其研究应用较少,本文不再赘述。
另外,锂空气电池的反应机理研究中常采用玻璃碳材料。玻碳材料是将聚丙烯腈树脂或酚醛树脂等在惰性气氛中缓慢加热至高温(达1800℃)处理成外形似玻璃状的非晶形碳,玻璃碳具有导电性好,化学稳定性高,热胀系数小,硬度高,光洁度高,气密性好等优点。将其做成玻碳电极,其氢过电位高,极化范围宽,是一种较好的惰性电极,常应用于电化学实验或电分析化学中。更为关键的是,其表面状态稳定、结构简单、其真实表面积较为固定,因此利用它作为锂空气电池中氧还原机理的研究是一个很好的选择。在最近的研究中,我们通过采用玻碳电极的循环伏安实验证明了,空气电极上的氧气首先发生的是一电子还原生成O2-的过程。并且当非水电解液中的电解质盐阳离子及有机溶剂不同时,氧的电化学还原过程表现出很大的差异[34],即在碳酸酯的溶剂中,超氧根阴离子会与溶剂反应,使得氧电极的可逆性受到很大的影响。
2.8 碳材料的修饰改性
对碳材料进行处理,可改变其表面性质,进而影响或改善其在锂空气电池中的性能。对碳材料进行球磨是一种简单的碳材料改性处理的方式。例如将石墨球磨后,其比表面积大大增加,可以由5 m2/g变为480 m2/g。由处理前后的石墨材料所制得的锂空气电池在0.1 mA/cm2的放电电流密度下,放电容量由560 mAh/g提高到了1136 mAh/g[11]。然而并非所有碳材料都能够利用球磨的方法改善其性能。将Ketjin black(EC600JD)进行球磨后,其比表面积反而降为342 m2/g,孔体积降为0.43 cm3/g,其所制得的锂空气电池在0.05 mA/cm2的放电电流密度下,放电比容量仅有47 mAh/g[18]。
Qu等人[35]将商品化的碳材料在二氧化碳气氛保护下的高温炉进行热处理,将处理后的碳材料制成空气电极。然后将空气电极放在含有5%浓度的氟代聚乙二醇溶液中并且真空的条件下浸泡30 min,然后仍在真空条件下100℃下进行干燥。研究认为,处理后的碳电极电压衰减相比未处理的碳电极要缓慢的多,放电时间更长。作者认为处理后的碳材料,由于材料表面附着了疏水性的氟碳键,能够部分阻止氧化锂或过氧化锂碳表面的形成,类似起到提高材料活性表面积的功效,从而提高其电极的放电容量。
Kichambare 等人[23]将 Ketjin black(EC600JD)和 Calgon 活性碳以及这两种碳的混合进行氮掺杂。具体方法是先将碳材料在6 mol/L HCl中洗去金属杂质,再用去离子水反复漂洗;然后将其放在70%的HNO3溶液中过液浸泡,用去离子水洗涤后,在100℃下烘干;最后在不同温度下进行热处理氮掺杂。经过氮掺杂处理后,这两种碳材料的比表面积、孔体积、孔尺寸以及孔隙率均有所提高,放电容量也有所提高。
3 碳材料的物理化学性质对氧电极性能的影响规律
3.1 材料导电性及比表面积
对于应用于锂空气电池正极的碳材料来说,由于氧的电化学还原发生在碳表面,因此碳材料的导电性与比表面积对锂电池性能有重要的影响。通常的规律是碳材料的导电性与活性比表面积越大,电极的极化与单位电流密度就越小,导致其放电容量越高。尤其是当碳材料负载催化剂时,若催化剂能更好地分散于碳表面,催化活性更高。但并不是所有的高比表面积的碳材料都能具有良好的放电性能。前文已提到,有些碳材料的比表面积很高,可是具有氧还原活性的表面积比例很低;或是有些表面积为微孔的表面,微孔被电解液浸满,无法进行氧还原,因此它的放电性能较差。而Super P这种碳材料虽然具有较低的比表面积,但由于其真正能参与氧还原的表面比例较高,所以它在锂空气电池应用中的性能优于很多其它碳材料。
3.2 孔体积和孔尺寸
有机电解液的锂空气电池由于其放电产物不溶于电解液,会堵塞在空气电极的孔隙中,因此应用于空气电极的碳材料的孔体积对锂空气电极放电性能也有重要的影响。很显然,碳材料的孔体积越大,其能容纳的放电产物越多,放电容量也会越大。比如前文提到的Ketjin black(EC600JD),正因为它具有较大的孔体积,才具有远远高于同篇文献报道中的其它碳材料所达到的放电容量。另外介孔碳由于其颗粒间和颗粒内部均可以容纳放电产物,因此它在锂空气电池中所达到的放电容量也很高。
碳材料的孔包括粒子间隙、大孔、中孔和微孔。通常认为,碳材料的微孔会被电解液浸没,它既不能在其表面发生氧还原,也不能容纳放电产物,因此对放电容量没有贡献。但如果孔径过大,也会使孔体积利用率降低[18]。
3.3 碳电极中粒子间隙和粒子尺度
粒子间隙是气态氧从大气中扩散到活性碳材料表面的通道,只有其合适大小的粒子间隙才能保证气态氧能自由通过;否则氧在电解液中的低扩散速率将对电池放电性能产生消极影响。粒子间隙的大小决定于粒子的尺度。因此适合的孔径大小和粒子尺度不仅能保证碳材料的孔体积有较高的利用效率,而且可以为气态氧提供自由通过的通道。
4 结论及展望
对于应用于锂空气电池的碳材料基本要求是必须具备使氧能够在其表面顺利、连续发生还原反应的特性,一般需要具备如下物性特征:①较高的比表面积,并且具有氧还原活性的比表面积;②较大的可以容纳放电产物的孔体积有利于氧还原反应的发生;③合适的孔径大小和粒子尺度能够使气态氧自由通过,从而使反应可以连续不断地进行;④较好的材料电导性是电极反应的必备条件。可以说,能够应用于锂空气电池中性能优异的碳材料,均应具有合适的微观结构、形貌及其表面特性。比表面积、孔体积和孔隙率等碳材料的物理参数在某种程度上是其微观结构与形貌的反映,也就决定了它们对电池性能的影响方式和程度。因此,在锂空气电池碳材料选择和优化研究上,应首先根据电池放电机理和产物性质,并兼顾碳材料的必备特征,设计出一种最优化的碳材料微观形貌。在此基础上,选择或者改性优化碳材料,使其构成这种理想的微观结构,使其具备最优化的性能,以达到改善锂空气电池性能的目的。另外,关于碳纳米管及其石墨烯做为锂空电池空气电极的研究还很少,由于这两种材料均提供体相微观结构及表面结构的可调控性,因此具有很好的发展潜力。
当然,碳材料的优选和改性是锂空气电池研究的重要工作。但是这未能改变锂空气电池极高的理论比容量几乎完全受制于空气电极一端的情况。因此,锂空气电池的研究不应局限于空气电极的改进,而应着眼于锂空气电池整个体系,包括电解液、透气膜、防水膜,甚至负极锂,以改变这种由于空气电极内部阻塞而造成的电极失效和放电结束。只有这样,才能真正使锂空气电池能够达到它的理论比容量,才能更好地发挥它相比于其它化学电源的优势。幸运的是,现在人们对锂空气电池的研究兴趣迅速增长,锂空气电池的发展也将会迅速提高。相信在将来,随着锂空气电池实用技术的不断完善,必将在多个领域发挥其极高比能量的巨大优势 (碳材料物理参数及其在锂空气电池中电化学性能见下页表1)。

[1]LITTAUER E L,TSAI K C.Anodic behavior of lithium in aqueous electrolytes[J].J Electrochem Soc,1976,123(6):771-776.
[2]ABRAHAM K M,JIANG Z.A polymer electrolyte-based rechargeable lithium/oxygen battery[J].J Electrochem Soc,1996,143(1):1-5.
[3]ENDO M,KIM C,NISHIMURA K,et al.Recent development of carbon materials for Li ion batteries[J].Carbon,2000,38(2):183-197.
[4]LINDEN D,REDDY T B.Handbook of batteries[M].3rd edit.NewYork:McGraw-Hill,1995:1-1446.
[5]ZHENG J P,LIANG R Y,HENDRICKSON M,et al.Theoretical energy density of Li-air batteries[J].Journal of the Electrochemical Society,2008,155(6):A432-A437.
[6]READ J,MUTOLO K,ERVIN M,et al.Oxygen transport properties of organic electrolytes and performance of lithium/oxygen battery[J].Journal of the Electrochemical Society,2003,150(10):A1351-A1356.
[7]ZHOU H S,WANG Y G.A lithium-air battery with a potential to continuously reduce O(2)from air for delivering energy[J].Journal of Power Sources,2010,195(1):358-361.
[8]FANG Z Q,HU M,LIU W X,et al.Preparation and electrochemical property of three-phase gas-diffusion oxygen electrodes for metal air battery[J].Electrochimica Acta,2006,51(26):5654-5659.
[9]READ J.Characterization of the lithium/oxygen organic electrolyte battery[J].Journal of the Electrochemical Society,2002,149(9):A1190-A1195.
[10]YANG X H,XIA Y Y.The effect of oxygen pressures on the electrochemical profile of lithium/oxygen battery[J].Journal of Solid State Electrochemistry,2010,14(1):109-114.
[11]YANG X H,HE P,XIA Y Y.Preparation of mesocellular carbon foam and its application for lithium/oxygen battery[J].Electrochemistry Communications,2009,11(6):1127-1130.
[12]CHENG H,SCOTT K.Carbon-supported manganese oxide nanocatalysts for rechargeable lithium-air batteries[J].Journal of Power Sources,2010,195(5):1370-1374.
[13]ZHANG D,FU Z H,WEI Z,et al.Polarization of oxygen electrode in rechargeable lithium oxygen batteries[J].Journal of the Electrochemical Society,2010,157(3):A362-A365.
[14]ZHANG S S,READ J.Partially fluorinated solvent as a co-solvent for the non-aqueous electrolyte of Li/air battery[J].Journal of Power Sources,2011,196(5):2867-2870.
[15]READ J.Ether-based electrolytes for the lithium/oxygen organic electrolyte battery[J].Journal of the Electrochemical Society,2006,153(1):A96-A100.
[16]ZHANG D,LI R S,HUANG T,et al.Novel composite polymer electrolyte for lithium air batteries[J].Journal of Power Sources,2010,195(4):1202-1206.
[17]ZHANG S S,XU K,READ J.A non-aqueous electrolyte for the operation of Li/air battery in ambient environment[J].Journal of Power Sources,2011,196:3906-3910.
[18]ZHANG S S,FOSTER D,READ J.A high energy density lithium/sulfur-oxygen hybrid battery[J].Journal of Power Sources,2010,195(11):3684-3688.
[19]REN X M,ZHANG S S,TRANAND D T,et al.Oxygen reduction reaction catalyst on lithium/air battery discharge performance[J].J Mater Chem,2011,21:10118-10125.
[20]PARK C K,PARK S B,LEE S Y,et al.Electrochemical performances of lithium-air cell with carbon materials[J].Bulletin of the Korean Chemical Society,2010,31(11):3221-3224.
[21]路密.碳材料在锂(离子、空气)电池中的性能[D].厦门:厦门大学,2008:1-47.
[22]ZHANG S S,FOSTER D,READ J.Discharge characteristic of a non-aqueous electrolyte Li/O(2)battery[J].Journal of Power Sources,2010,195(4):1235-1240.
[23]XIAO J,WANG D H,XU W,et al.Optimization of air Electrode for Li/air batteries[J].Journal of the Electrochemical Society,2010,157(4):A487-A492.
[24]KICHAMBAREA P,KUMARB J,RODRIGUESA S,et al.Electrochemical performance of highly mesoporous nitrogen doped carbon cathode in lithium-oxygen batteries[J].Journal of Power Sources,2011,196:3310-3316.
[25]CROWTHER O,MEYER B,SALOMON M.Primary Li-air cell development[J].Journal of Power Sources,2011,196:1498-1502.
[26]XU W,XIAO J,WANG D Y,et al.Crown ethers in nonaqueous electrolytes for lithium/air batteries[J].Electrochemical and Solid State Letters,2010,13(4):A48-A51.
[27]ZHANG J,XU W,LIU W.Oxygen-selective immobilized liquid membranes for operation of lithium-air batteries in ambient air[J].Journal of Power Sources,2010,195(21):7438-7444.
[28]ZHANG J,XU W,LI X H,et al.Air dehydration membranes for nonaqueous lithium-air batteries[J].Journal of the Electrochemical Society,2010,157(8):A940-A946.
[29]XU W,XIAO J,ZHANG J,et al.Optimization of nonaqueous electrolytes for primary lithium/air batteries operated in ambient environment[J].Journal of the Electrochemical Society,2009,156(10):A773-A779.
[30]LU Y C,XU Z C,GASTEIGER H A,et al.Platinum-gold nanoparticles:A highly active bifunctional electrocatalyst for rechargeable lithium-air batteries[J].Journal of the American Chemical Society,2010,132(35):12170-12171.
[31]OGASAWARA T,DEBART A,HOLZAPFEL M,et al.Rechargeable Li2O2electrode for lithium batteries[J].Journal of the Ameri-can Chemical Society,2006,128(4):1390-1393.
[32]DEBART A,BAO J,ARMSTRONG G,et al.An O-2 cathode for rechargeable lithium batteries:The effect of a catalyst[J].Journal of Power Sources,2007,174(2):1177-1182.
[33]ESWARAN M,MUNICHANDRAIAH N,SCANLON L G.High capacity Li-O(2)cell and electrochemical impedance spectroscopy study[J].Electrochemical and Solid State Letters,2010,13(9):A121-A124.
[34]田艳艳,武巍,杨勇,等.溶剂及电解质盐对氧在有机电解液体系中电化学还原的影响[J].电化学,2010,16(4):420-424.
[35]TRAN C,KAFLE J,YANG X Q,et al.Increased discharge capacity of a Li-air activated carbon cathode produced by preventing carbon surface passivation[J].Carbon,2011,49(4):1266-1271.
[36]BEATTIE S D,MANOLESCU D M,BLAIR S L.High-capacity lithium-air cathodes[J].Journal of the Electrochemical Society,2009,156(1):A44-A47.
[37]XIAO J,XU W,WANG D Y,et al.Hybrid air-electrode for li/air batteries[J].Journal of the Electrochemical Society,2010,157(3):A294-A297.

