毛竹催化热解动力学研究
欧阳赣,单胜道,罗锡平,杨 亮,宋成芳,2
(1.浙江农林大学 环境与资源学院,浙江 临安 311300;2.浙江工业大学 化学与材料学院 生物质能研究中心,浙江 杭州 310014)
生物质热解转化是目前国内外学者研究的热点[1-4]。热解是指在隔绝空气或通入少量空气的条件下,利用热能切断生物质大分子中的化学键,使之转变为低分子物质的热化学反应。生物质热解后可有气、液和固多种状态产物,对热解的分析有助于热化学转化过程控制及高效转化工艺的开发[5]。热解动力学是表征热解过程参数对原料转化率影响的重要手段[6],动力学分析可为生物质热化学转化工艺的研究提供重要的基础数据。很多研究者对中国农林废弃物热解做了大量研究,包括秸秆、稻壳等。中国是世界上竹类资源最丰富的国家,其中毛竹Phyllostachys edulis产量占中国竹材产量的三分之二以上。毛竹林采伐周期短,产量高,能较好地维持竹林生态系统的稳定,是营造能源林的理想树种,而且毛竹的成分以纤维素和半纤维素为主,是一种很好的进一步转化的原料。若能充分利用生物质的各种热化学转化技术,将毛竹高效地转化为可利用的洁净的燃料,能够在一定程度上缓解能源危机。目前,尚未发现有关于毛竹催化热解的详细报道。本研究是针对氯化亚铜存在的条件下,研究毛竹的热解动力学特性,可为毛竹高效热解转化提供基础数据。
1 实验部分
1.1 原料与仪器
本实验所用的毛竹来自浙江临安的一家竹木粉加工厂,粒度为60~80目;氯化亚铜为分析纯。应用德国VARIOEL-3元素自动分析仪对毛竹原料进行元素分析,采用文献[7]中的方法对毛竹进行了工业分析和元素分析,其结果见表1。热重实验在TG209F3Tarsus型热重分析仪(TGA)上进行,仪器精度为1 μg。

表1 毛竹的工业分析和元素分析Table1 Industrial and elemental analysis of Phyllostachys edulis samples
1.2 实验方法
热重实验前,将毛竹粉和氯化亚铜的按照质量4∶1配比混合,在漩涡混合器上混合均匀。取10 mg左右在热重分析仪上,于100 mL·min-1氮气气氛中分别以10,20,40℃·min-1加热速率进行程序升温热重实验。温度由室温升至700℃,系统自动采集数据。
2 实验结果
2.1 毛竹的工业分析和元素分析
生物质裂解反应过程中,生物气和生物油主要来自可挥发组分的裂解。由表1可见:毛竹粉中挥发分相当高,为81.64%,表明理论上可挥发组分较高,有利于毛竹的能源化。原料的元素分析结果表明:毛竹粉成分主要由碳(C),氢(H)和氧(O)3种元素组成,氮(N)和硫(S)的都比较低,采用毛竹制备的生物气和油氮、硫低,将它们作为燃料使用,燃烧后NOx,SOx等酸性气体的排放量很少,将是一种环境友好型的能源。
2.2 毛竹催化热裂解特性
毛竹和氯化亚铜及其混合物的热质量分析(TG)和微商热质量(DTG)曲线如图1和图2所示,热解曲线的特征值列于表2。
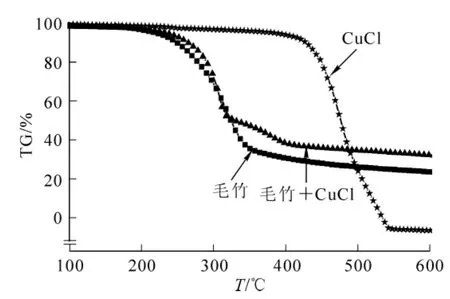
图1 氯化亚铜催化毛竹热解热质量分析(TG)曲线Figure1 TG curves of Ph.edulis and Ph.edulis-CuCl

图2 氯化亚铜催化毛竹热解微商热质量曲线(DTG)Figure2 DTG curves of Ph.edulis and Ph.edulis-CuCl
如图2所示:根据DTG曲线的拐点可知,毛竹的热解可分3个阶段。第1阶段,140℃之前的原料失水过程;第2阶段,为200~380℃,是毛竹热解的主要阶段,失重明显,失重率占整个温度区间的60%~70%;第3阶段,是400℃以后残留物的缓慢分解。
由图2还可见:氯化亚铜的添加使毛竹热裂解TG曲线向左移动,DTG曲线中失重峰发生了提前现象且失重峰也变得更加尖锐,说明添加氯化亚铜后热裂解的温度降低,最大热裂解速率对应的温度降低了10℃,为318.5℃;主要失重温度范围明显变窄,最大失重速率显著变大,这与文献[8~11]中无机盐的加入可以促进生物质的热裂解的结果相同。同时通过图1中的纯毛竹失重曲线1和添加氯化亚铜失重曲线2的对比可见,曲线2的残留物量大于曲线1的残留物量,即表明添加氯化亚铜能促使残留炭产量增加。
由图1和图2还可知:氯化亚铜催化热裂解时,毛竹在478℃时再次出现失重现象,对应DTG曲线也出现一个失重峰,这说明氯化亚铜的加入改变了毛竹的热解机制,出现了第2个热解峰。

表2 毛竹热裂解微商热质量曲线(TDG)特征值Table2 Eigenvalues of Phyllostachys edulis pyrolysis DTG curves
从表2中可见:由于氯化亚铜的作用,毛竹的最大热解速率由原来的17.18%提高到26.14%。热解速度的增大暗示热解所需要的时间将缩短,通过热解峰的终点和起点温度差值与加热速率的比值确定热解时间,实验中纯毛竹的热解时间是7.5 min,而添加氯化亚铜后,热解时间为6.0 min。
2.3 不同升温速率下毛竹热解曲线
毛竹在3种升温速率下热裂解的TG和DTG曲线如图3所示。升温速率影响毛竹热裂解的起始温度、失重峰对应温度和热裂解终止温度。升温速率越小,试样有足够的时间吸收热量,起始分解温度和终止温度相对降低;升温速率增大,由于试样内反应存在传热温差和温度梯度,导致热滞后现象加重,TG曲线向高温侧轻微移动,失重峰对应温度和失重峰起止对应温度均略有增高。由TG曲线可见,升温速率的不同,热裂解最终炭生成量没有明显变化。添加氯化亚铜后毛竹的热裂解TG和DTG曲线如图4所示,可见加热速率对热裂解的影响与是否添加氯化亚铜无关,但多了氯化亚铜的挥发峰。

图3 不同升温速率下毛竹热解TG和DTG曲线Figure3 TG and DTG curves of Ph.edulis in different heating rates
2.4 不同升温速率下毛竹热裂解的动力学分析
2.4.1 Flynn-wall-Ozawa动力学模型推导[12]假设生物质在热重分析仪中的热裂解反应是一步热裂解,其热裂解方程可以描述为方程,A(s)→B(s)+C(g),反应动力学可以简化为方程(1):

根据阿累乌斯(Arrhenius)方程,式(1)可以转化为:

图4 不同升温速率下氯化亚铜催化毛竹热解TG和DTG曲线Figure4 TG and DTG curves of Phylloslachys edulis and Ph.edulis-CuCl in different heating rates

式(1)和(2)中:α 是生物质的转化率,可以写为 α=(w0-w)/(w0-w∞),w 是 t时刻生物质样品的量,w0和w∞是样品的最初的量和最终剩余量。f(α)是反应机制函数,E和A分别是热裂解反应的活化能和指前因子,R指理想气体常数[R=8.314 J·(mol·K)-1]。对非等温反应,反应的升温速率为β,则:

其中:G(α)为动力学模型f(α)的积分函数,也代表反应机制。为了得到生物质热裂解动力学参数E,lg β对1/T作图,结果如图7和图8所示。得到一条直线,便可从直线的斜率计算出样品热裂解的活化能E;假设反应为一级反应,则通过直线的截距可计算出指前因子A值。
2.4.2 动力学参数的求取 一般情况下研究者比较关心生物质热裂解反应主要阶段的特性,因此,本研究在求解动力学参数时也主要考察这一阶段。由于毛竹的热解主要集中在200~379℃温度段,活化能的求解也采用了这段系统采集的数据,结果如图5和图6所示。不同的转化率α对应的活化能值如表3所示。表3可见:纯毛竹热解活化能为199.88~252.07 kJ·mol-1,添加氯化亚铜后毛竹热解活化能在204.16~54.72 kJ·mol-1范围,说明添加氯化亚铜没有显著改变毛竹的热解的平均活化能。在转化率α小于0.3之前,由于氯化亚铜的作用,热解的活化能明显大于纯毛竹的热解活化能;而转化率α大于0.8之前活化能又小于纯毛竹的热解活化能。指前因子也呈现类似规律。从表3还可见:指前因子A值增大了10倍,指前因子表达的是分子参加化学反应的速率,说明氯化亚铜的加入增加了反应活性位,提高了反应分子之间的反应机会,从而导致了热解速率的增大。
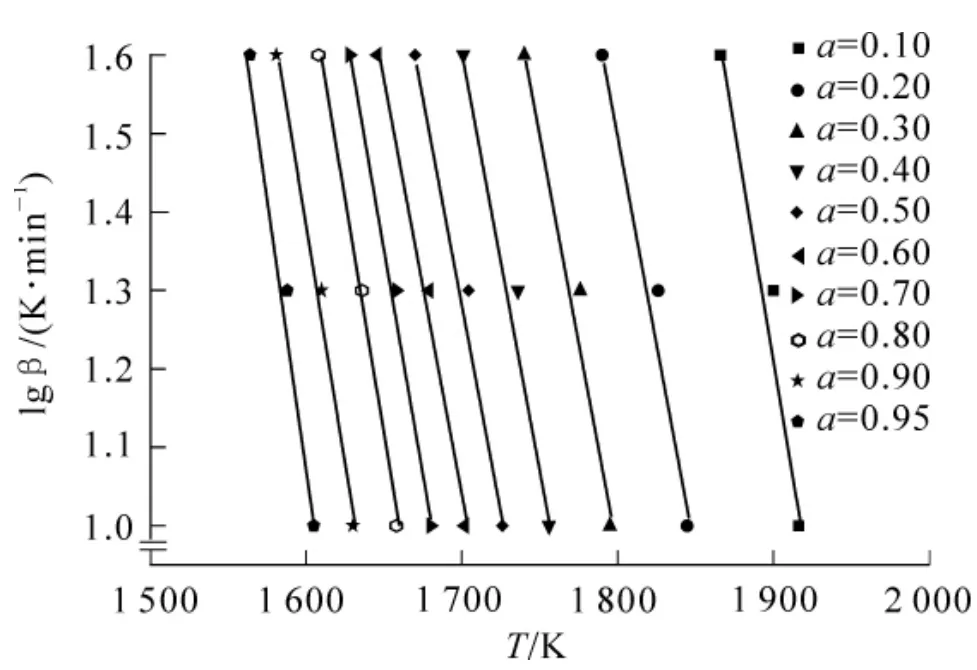
图5 纯毛竹热解的阿累乌斯图Figure5 Arrhenius plots lg β vs 1/T at selected T values for Phllostachys edulis
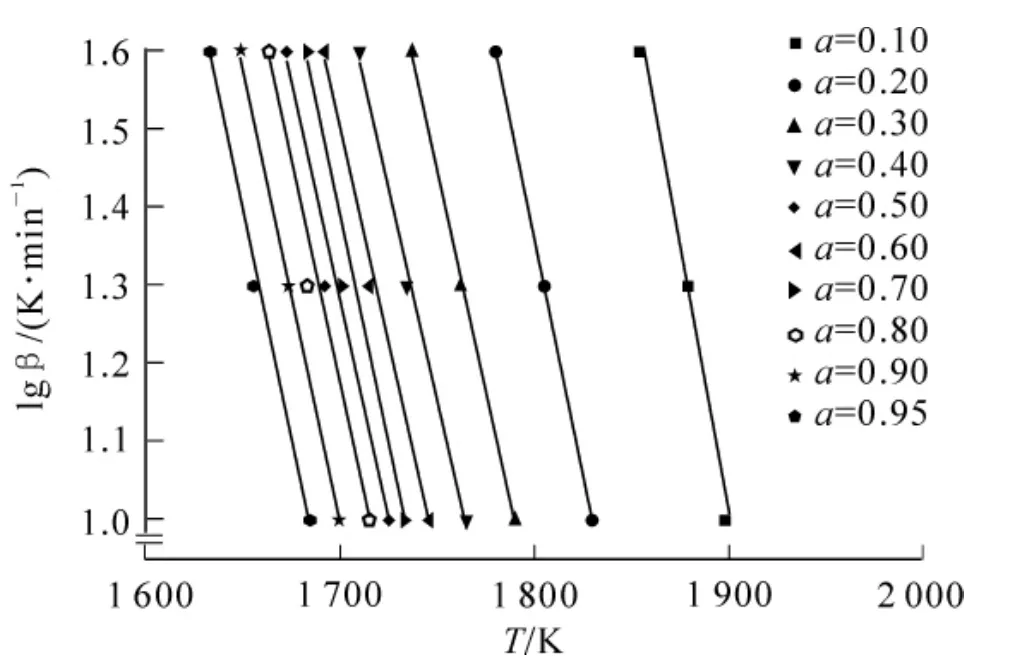
图6 毛竹+氯化亚铜热解的阿累乌斯图Figure6 Arrhenius plots lg β vs 1/T at selected T values for Ph.edulis+CuCl

表3 毛竹热解活化能和指前因子Table3 Activation energy and Preexponential factor of Ph.edulis catalytic pyrolysis
3 结论
通过在纯毛竹中添加氯化亚铜的方法,本研究对氯化亚铜对毛竹热裂解的催化影响进行研究。
氯化亚铜对毛竹的热解有催化效果,氯化亚铜加入使毛竹的热解温度提前10℃左右,热解速率显著增大,热解所需时间缩短,残余碳量增大。
毛竹热解动力学分析结果显示,纯毛竹热解的活化能为213.21 kJ·mol-1,指前因子为17.25;加入氯化亚铜后,毛竹热解的平均活化能变化不明显,但热解起始阶段活化能显著增大,结束阶段又显著减小,同时使得指前因子增加了约10倍,反应速度得到显著提高。
[1]SADHUKHAN A K,GUPTA P,GOYAL T,et al.Modelling of pyrolysis of coal-biomass blends using thermogravimetric analysis [J].Bioresour Technol,2008,99 (17):8022-8026.
[2]SONOBE T,WORASUWANNARAK N.Kinetic analyses of biomass pyrolysis using the distributed activation energy model[J].Fuel,2008,87 (3):414-421.
[3]SUTCU H.Pyrolysis by thermogravimetric analysis of blends of peat with coals of different characteristics and biomass[J].J Chin Inst Chem Eng,2007,38 (3):245-249.
[4]di BLASI C.Modeling chemical and physical processes of wood and biomass pyrolysis [J].Progr Energy Comb Sci,2008,34 (1):47-90.
[5]曹青,鲍卫,吕永康,等.玉米芯热解及过程分析[J].燃料化学学报,2004,33(5):557-562.CAO Qing,BAO Wei,LÜ Yongkang,et al.Pyrolysis and reaction mechanism analysis of corncob [J].J Fuel Chem Technol,2004,33 (5):557-562.
[6]傅旭峰,仲兆平,肖刚,等.几种生物质热解特性及动力学的对比[J].农业工程学报,2009,25(1):199-202.FU Xufeng,ZHONG Zhaoping,XIAO Gang,et al.Comparative study on pyrolysis characteristics and dynamics of grass biomass [J].Trans CSAE,2009,25 (1):199-202.
[7]朱锡锋.生物质热解原理与技术[M].合肥:中国科学技术大学出版社,2006:36-41.
[8]BAO Li,ZHANG Ting’an,LIU Yan,et al.The most probable mechanism function and kinetic parameters of gibbsite dissolution in NaOH [J].Chin J Chem Eng,2010,18 (4):630-634.
[9]VARHEGYI G,ANTAL M J Jr,JAKAB E,et al.Kinetic modeling of biomass pyrolysis [J].J Anal Appl Pyrolysis,1997,42 (1):73-87.
[10]AGBLEVOR F A,BESLER S.Inorganic compounds in biomass feedstocks(1) effect on the quality of fast pyrolysis oils [J].Energy Fuels,1996,10 (2):293-298.
[11]RAVEENDRAN K,GANESH A K,KHILAR C.Influence of mineral matter on biomass pyrolysis characteristics[J].Fuel,1995,74 (12):1812-1822.
[12]HU Rongzu.Thermal Analysis Kinetics[M].Beijing:Science Press,2008.

