[BMIM]HSO4离子液体的热力学性质研究*
王晓丹,范洪涛,崔天放
(沈阳化工大学应用化学学院,辽宁 沈阳 110142)
由有机阳离子和无机或有机阴离子组成的低熔点盐称为室温离子液体,或简称为离子液体、室温熔盐[1]。 作为新型的绿色溶剂和环保电解质,其具有低蒸气压,高热稳定性、强溶解能力,高电导率及更宽电化学窗口宽等一系列突出优点[2]。 因此,离子液体的合成、开发与应用越来越受到化学工作者的重视。 近年来,关于离子液体的研究主要集中在相对稳定的非AlCl3型离子液体,并以二烷基咪唑阳离子形成的离子液体最具代表性[3-7]。
根据一些易测得的离子液体性质数据对相关的一些未知物化性能进行估算,已成为当前离子液体研究的热点之一[8-10],最近,Zhu等[9]还针对离子液体形成过程中的热力学进行了研究。 在前期工作中,我们合成了[BMIM]HSO4离子液体,发现该离子液体具备作为低温电解液的基本性质[11],并且有文献报道该离子液体表现出良好的酸催化性能和溶剂性质[12-13]。 本文作为前期工作的继续,在273.15~353.15 K范围内精确测定了该离子液体的表面张力和密度,估算了离子液体的热力学参数,并探讨了Glasser方程及空隙模型对该离子液体的适用性。
1 实验部分
1.1 离子液体的合成及表征
离子液体[BMIM]HSO4的合成及表征参见文献[11],样品进行测试前在80 ℃下经真空干燥24 h。
1.2 离子液体的密度和表面张力测定
干燥后的离子液体用ZSD/2型测水仪根据卡尔·费休法测定其水的质量分数均小于0.1%。 使用DF-101S型恒温浴槽控制温度;用SYS-1861A型附温比重瓶和FC-104型分析天平得到273.15~353.15 K范围内离子液体[BMIM]HSO4的密度(每间隔5 K一个值)。 利用DZ3318型最大气泡法表面张力仪测定了纯离子液体的表面张力。 事先在测量温度范围内测定了水的表面张力,与文献值[14]基本相同。
2 结果与讨论
将测定的离子液体[BMIM]HSO4的密度ρ和表面张力γ的数据列入表1中,其中每个数据为3次测量的平均值,其数据与文献[11]基本一致。
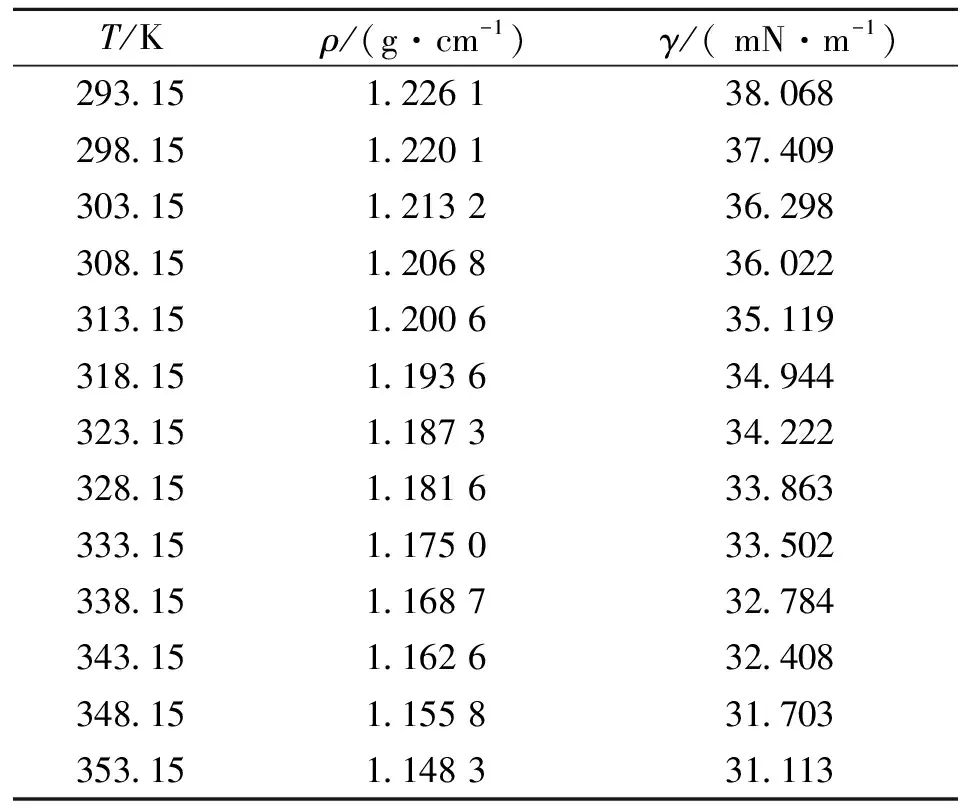
表1 离子液体[BMIM]HSO4的密度和表面张力
2.1 [BMIM]HSO4的体积性质
将测得的[BMIM]HSO4的lnρ对T作线性拟合,得到一条很好的直线(见图1),其经验方程为
lnρ=0.1988-1.08×10-3(T-298.15)
(1)
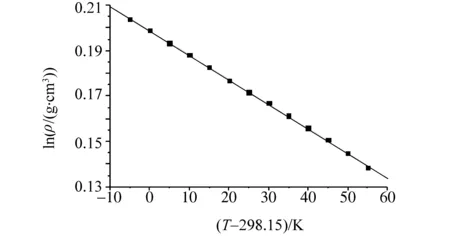
图1 离子液体lnρ对(T-298.15)的线性拟合
拟合的相关系数r=0.999 8,标准偏差s=4.4×10-4。根据恒压热膨胀系数定义α≡-(∂lnρ/∂T)P可知,方程(1)的斜率负值即是离子液体的热膨胀系数α=10.8×10-4K-1。而离子液体正负离子的体积和Vm为
Vm=(M/Nρ)
(2)
式中M是离子液体的摩尔质量(236.29 g/mol),N是Avogadro常数。在298.15 K下计算得到Vm=0.321 7×10-21cm3。将其它几种阳离子相同,阴离子不同的离子液体的Vm和M-(阴离子摩尔质量)列于表2中。

表 2 几种[BMIM]+阳离子离子液体的体积性质参数值
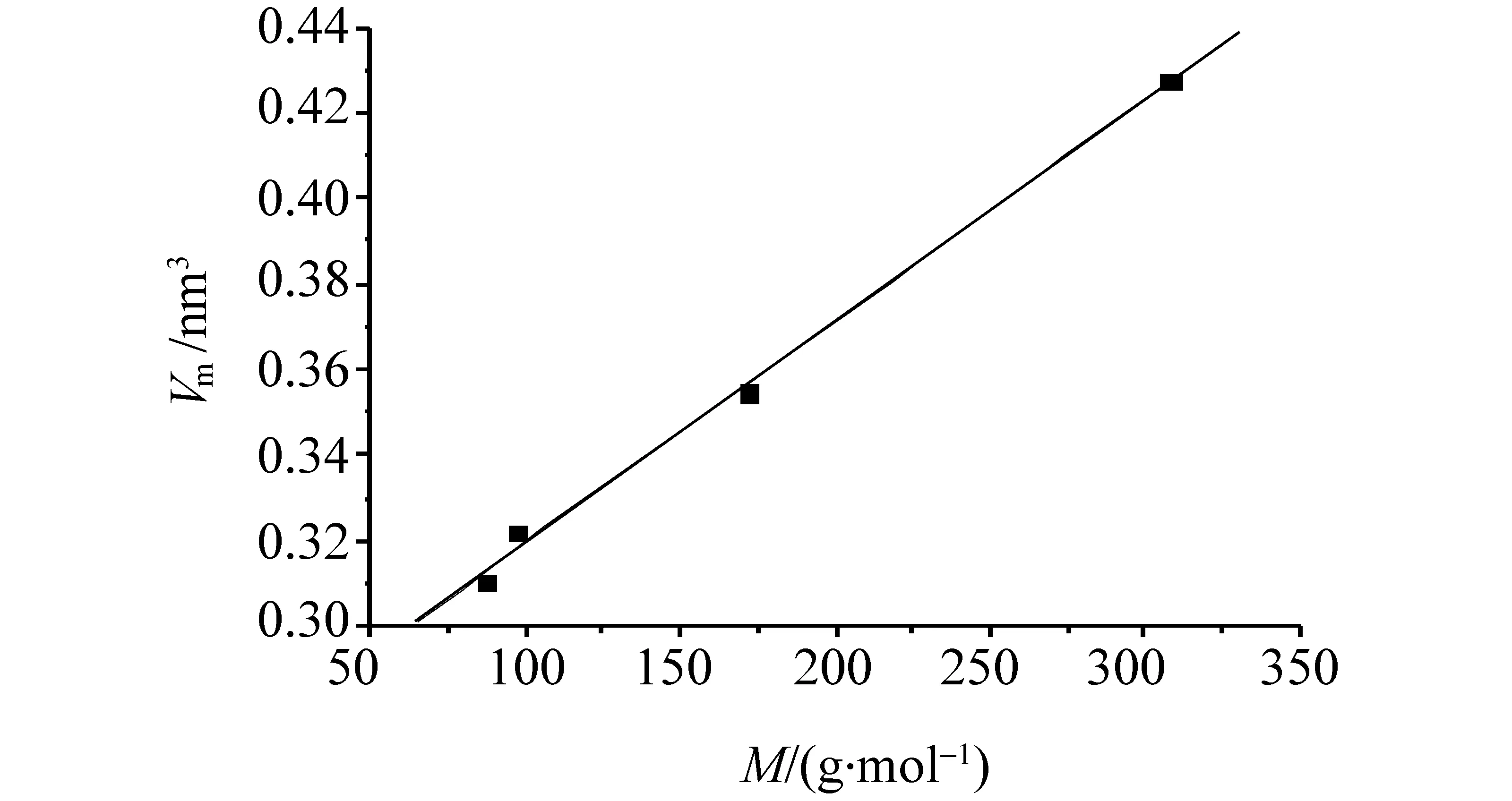
图2 Vm对M-作图
从表2中数据可以得出,Vm和负离子的摩尔质量M-呈很好的线性关系(见图2)。 将表中离子液体Vm对M-作线性拟合,相关系数为0.998 6,其截距为0.267 9 nm3,可将截距看作阳离子[BMIM]+的体积,进而得到阳离子[BMIM]的半径r([BMIM]+)=0.400 nm。 这一半径与文献[18]报道值0.403 nm十分接近。 利用[BMIM]+的体积,可以得到表2中所有阴离子的体积及阴离子半径,将这些数据也同时列入表2。
根据Glasser理论[19],在温度298 K下,1-1价型离子液体的摩尔标准熵可用下面方程计算
S0=1246.5Vm+29.5
(3)
由上述方程计算得到[BMIM]HSO4离子液体的摩尔标准熵S0=430.5 J·K-1·mol-1。该值与多数[BMIM]+型离子液体的摩尔标准熵相近,但略高于[EMIM]+型离子液体的值[10]。 离子液体的体积性质对热力学计算和过程设计是非常重要的,可以获得液体的结构和分子间相互作用的信息。
2.2 [BMIM]HSO4的表面性质
测得[BMIM]HSO4在不同温度下的表面张力γ结果如图3所示。 从图上可以看到,该离子液体表面张力γ随温度线性下降,相关系数0.995 0。
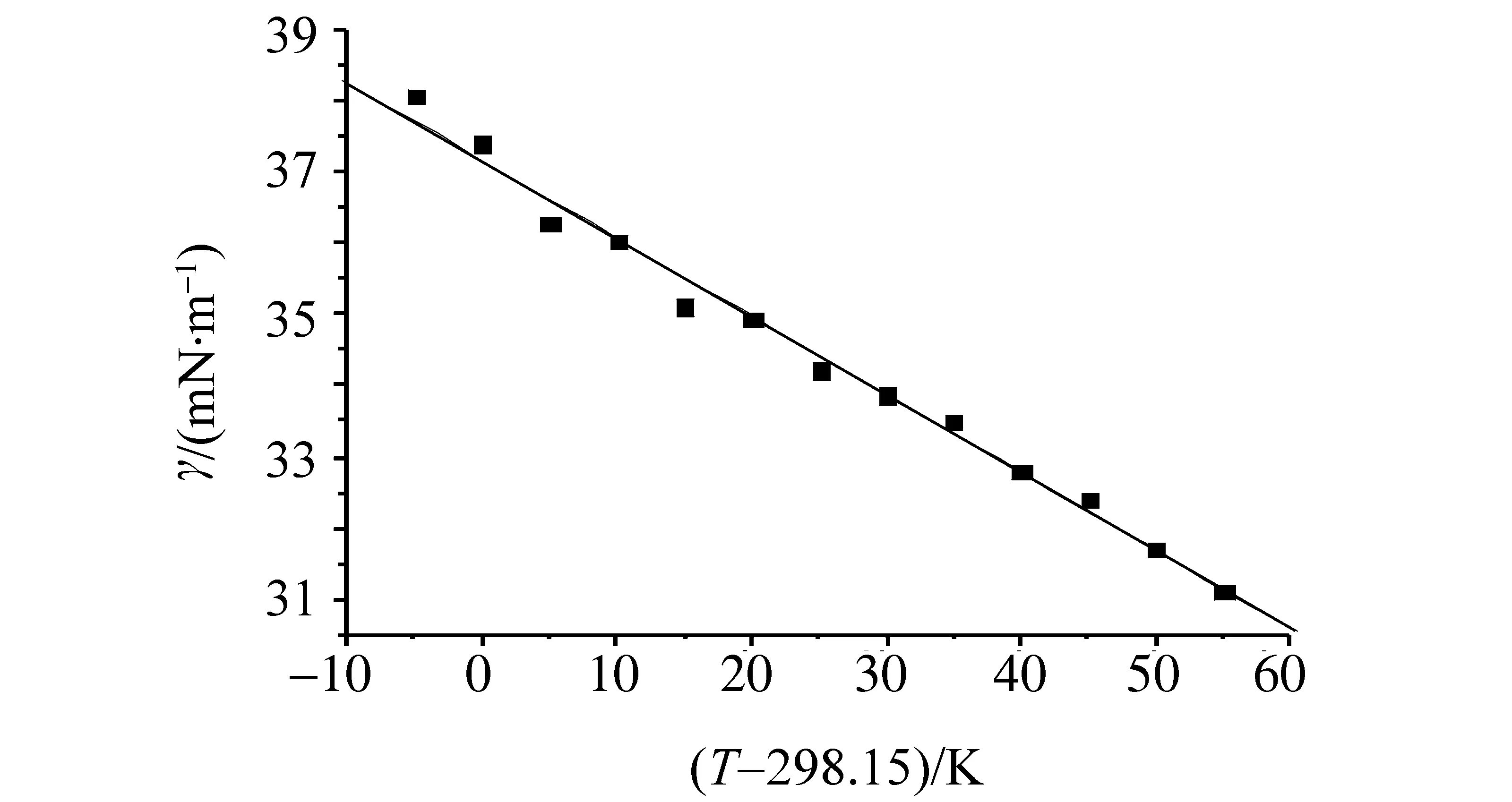
图3 离子液体表面张力γ与温度的关系
拟合式中斜率的负值即为在298.15 K下离子液体的表面熵Sa=-(∂σ/∂T)P=109.7×10-6J·K-1·m-2,进而得到离子液体的表面能Ea=γ-T(∂σ/∂T)P=70.12×10-3J·m-2。与通常的熔盐相比(如,硝酸钠熔盐表面能为Ea= 146×10-3J·m-2),该离子液体的表面能要小很多,与有机溶剂的表面能差不多(如正辛烷表面能为Ea= 51.1×10-3J·m-2[20])。而且阳离子同为[BMIM]+的离子液体表面能相近([BMIM]AlCl4的表面能为Ea= 62.56×10-3J·m-2[18],[BMIM]BF4的表面能为Ea= 59.3×10-3J·m-2[17])。液态物质表面能的大小取决于其固态的晶格能UPOT,离子液体的晶格能可利用Glasser经验方程计算
UPOT=1981.2(ρ/M)1/3+103.8
(4)
利用该方程计算得到离子液体的晶格能UPOT=446.2 kJ·mol-1。与晶格能最小的碱金属卤化物CsI的UPOT=613 kJ·mol-1相比[21],[BMIM]HSO4的晶格能也还是小了很多,而且比同为咪唑类阳离子[EMIM]NO3及[EMIM][MetSO4]的晶格能(分别为480.9及457.7 kJ·mol-1)小一些[10],具有较小的晶格能是离子液体在室温下能以液态形式存在的一个重要原因。
通常离子液体表面张力与温度的关系可由Eötvös方程表示[20]
γV2/3=k(TC-T)
(5)
式中,V是离子液体的摩尔体积,TC是临界温度,k经验常数。将[BMIM]HSO4离子液体的γ和V2/3的乘积对温度(T-298.15)做线性拟合,基本得到直线(图4)。
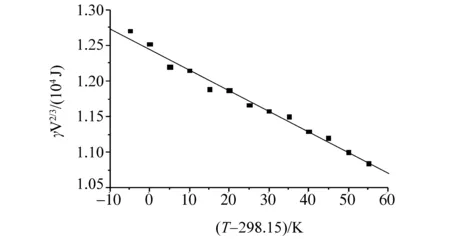
图4 离子液体γV2/3对(T-298.15)的线性拟合
其斜率的负值,常数k=2.9×10-7J·K-1,大多数有机液体的k值在2.1×10-7J·K-1[22],而极性很大的熔盐的k值都比较小,例如NaCl的k=0.4×10-7J·K-1[18]。常数k可以代表离子液体的极性大小的量度[15],值越大,离子液体的极性越小,可见[BMIM]HSO4离子液体的极性与同类的离子液体相似,更接近有机液体。因此,该离子液体有望作为反应介质代替挥发性的毒性有机溶液。
2.3 离子液体的空隙模型
Yang等[17]根据离子液体固有的特点提出了空隙模型,应用统计热力学推导出了离子液体的平均空隙体积ν的计算公式
v=0.6791(kbT/γ)3/2
(6)
式中,kb是Boltzmann常数,γ是表面张力。按照方程计算得到离子液体[BMIM]HSO4的ν=24.8×10-24cm3,体系中的总空隙体积Σν=2Nν=29.9 cm3,空隙率Σν/V为15%。离子固体融化时体积增大10 %~15 %,[BMIM]HSO4的空隙率落在这个区间。
离子液体的摩尔体积V可看作由其固有体积Vi和空隙总体积Σν=2Nν组成
V=Vi+2Nν
(7)
假设当温度升高体积膨胀时,离子液体的固有体积Vi不变,只有空隙膨胀,根据空隙模型可以推导出离子液体热膨胀系数α的计算公式
α=(1/V)(∂V/∂T)p=3Nν/VT
(8)
在298.15 K下利用以上方程计算可得到α=7.8×10-4K-1,与实验值α= 10.8×10-4K-1偏差并不是大,这说明该模型具有一定的合理性。这也为今后其它类似离子液体的热力学推算提供了一些基础数据。
3 结 论
估算得到[BMIM]HSO4离子液体的诸多物化性能,如摩尔体积、空隙体积、空隙率、热膨胀系数、标准摩尔熵和活化能等。其中计算得到的热膨胀系数值与实验值很接近,说明空隙模型具有一定的合理性。
参考文献:
[1]FU C P,ZHAO H H,WU H M,et al.Research on electrochemical properties of nonaqueous ionic liquid microemulsions[J].Colloid Polym Sci,2008,286: 1499.
[2]GALIALIńSKI M,LEWANDOWSKI A,STEPNIAK I.Ionic liquids as electrolytes[J].Electrochimica Acta,2006,51(26): 5567.
[3]GAO H Y,ZHANG Y,WANG H J,et al.Theoretical study on the structure and Cation-Anion interaction of amino acid Cation based amino acid ionic liquid [Pro]+[NO3]-[J].J Phys Chem:A,2010,114(37): 10243.
[4]刘青山,杨淼,谭志诚,等.咪唑基离子液体的物理化学性质估算及预测[J].物理化学学报,2010,26(6): 1463.
[5]BANDRÉS I,PERA G,MARTN S,et al.Thermophysical study of 1-butyl-2-methylpyridinium tetrafluoroborate ionic liquid[J].J Phys Chem:B,2009,113(35):11936.
[6]TONG J,LIU Q S,GUAN W,et al.Studies on volumetric properties of concentrated aqueous amino acid ionic liquid [C3mim][Glu][J].J Chem Eng Data,2009,54(3):1110.
[7]ZHANG Q G,CAI K D,JIN Z X,et al.Enthalpy of solution of the amino acid ionic liquid 1-butyl-3-methylimidazolium glutamine[J].J Chem Eng Data,2010,55:4044.
[8]KROSSING I,SLATTERY J M ZEIT.Semi-empirical methods to predict the physical properties of ionic liquids: An overview of recent developments[J].Phys Chem,2006,220(10/11): 1343.
[9]ZHU J F,HE L,ZHANG L,et al.Experimental and theoretical enthalpies of glycine-based sulfate/bisulfate amino acid ionic liquids[J].J Phys Chem:B,2012,116(1): 113.
[10]王晓玲,王建英,李小云,等.离子液体[C2mim]NO3与[C2mim][MetSO4]的热力学性能研究[J].河北科技大学学报,2011,32(2):103.
[11]王晓丹,吴文远,涂赣峰,等.酸性离子液体[BMIM]HSO4的合成及其物化性能[J].中山大学学报:自然科学版,2009,48(6): 69.
[12]蒋栋,李伟,许成娣,等.Brnsted 酸性离子液体催化合成阿司匹林[J].应用化学,2007,24(9): 1080.
[13]黄勇,魏作君,刘迎新,等.离子液体催化大豆异黄酮醇解反应工艺研究[J].高校化学工程学报,2008,22(4): 720.
[14]LIDE D R.Handbook of chemistry and physics[M].82nd ed.Boca Raton: CRC Press,2001.
[15]魏颖,张国庆.锌基离子液体BMIZn2Cl5的性质研究[J].化学学报,2008,66(16): 1879.
[16]ZHANG Q G,WEI Y.Study on properties of ionic liquid based on ZnCl2with 1-butyl-3-methylimidazolium chloride[J].J Chem Thermodyn,2008,40(4): 640.
[17]杨家振,桂劲松,吕兴梅,等.离子液体BMIBF4性质的研究[J].化学学报,2005,63(7): 577.
[18]佟静,张国庆,洪梅,等.铝基离子液体BMIAlCl4的热力学性质[J].物理化学学报,2006,22(1): 71.
[19]GLASSER L.Lattice and phase transition thermodynamics of ionic liquids[J].Thermochim Acta,2004,421(1/2): 87.
[20]ADAMSON A W.Physical Chemistry of Surfaces[M].3rd Ed.New York: John-Wiley,1976: 57.
[21]黄子卿.电解质溶液理论导论[M].北京:科学出版社,1983:40.
[22]REBELO L P N,CANONGIA L,ESPERANCA J,et al.On the critical temperature,normal boiling point,and vapor pressure of ionic liquids[J].J Phys Chem:B,2005,109(13): 6040.

