开窗支架型血管治疗近肾腹主动脉瘤的初步临床结果
左尚维, 贾 鑫, 杜 昕, 刘小平, 熊 江, 马晓辉, 张宏鹏, 张敏宏,许永乐, 张 佳, 郭 伟
开窗支架型血管治疗近肾腹主动脉瘤的初步临床结果
左尚维, 贾 鑫, 杜 昕, 刘小平, 熊 江, 马晓辉, 张宏鹏, 张敏宏,许永乐, 张 佳, 郭 伟
(解放军总医院血管外科, 北京 100853)
回顾性分析开窗支架型血管治疗近肾腹主动脉瘤(AAA)的初步结果。4例合并严重疾病无法行开放手术的近肾AAA患者, 根据术前CT数据定制个体化开窗支架型血管。于全身麻醉下置入此支架型血管并置入肾动脉支架。术后即时造影示各分支血管血流通畅, 支架形态良好, 两例有少量近端Ⅰ型内漏。术后3个月复查4例患者支架形态正常, 两例Ⅰ型内漏均消失, 但另一名患者出现Ⅱ型内漏。应用个体化开窗支架型血管治疗近肾AAA近期效果良好。
开窗支架型血管; 腔内修复术; 主动脉瘤, 腹
自1991年Parodi等[1]开始使用腔内修复术(en- dovascular repair, EVAR)治疗腹主动脉瘤(abdo- minal aortic aneurysm, AAA)以来, 随着技术的进步和移植物的改进, 已成为AAA治疗的首选方法。但对于距肾动脉较近或累及肾动脉甚至内脏动脉的AAA, 腔内治疗的局限性仍较大。近日, 我们在国内首次采用开窗腔内修复术应用ZenithTM(Cook公司, 美国)开窗支架型血管治疗了4例近肾AAA患者, 现汇报初步临床结果。
1 对象与方法
1.1 对象
2011年2月以来采用个体定制开窗支架型血管实施了EVAR的近肾AAA患者4例, 患者基本资料见表1。4例患者均为男性, 瘤体形态不宜使用常规支架行EVAR, 且患者年龄较大, 基础情况差, 无法耐受开放手术, 故根据其薄层CT定制个体化开窗支架型血管, 制作周期为2个月。

表1 患者基本情况
1.2 支架设计
1.2.1 近段主体 为前段带有裸支架的直筒型开窗支架血管, 根据患者的CT数据定制, 肠系膜上动脉为支架上缘扇型开窗, 双侧肾动脉为圆型开窗设计。支架的腹侧有不透X线的五点十字标记, 用以确定支架的方位角, 保证各开窗处对准分支。
1.2.2 远段主体 其形态类似于普通支架主体, 但主体缩短; 远端为分叉髂支。
1.2.3 髂支 支架其余部分使用ZenithTM(Cook公司, 美国)不同规格的分支。
1.3 治疗经过
患者入院后, 完善各项检查, 评估脏器功能, 对于肾功能不全的3例患者给予术前水化, 水化方案为1.5 ml/(kg·h), 于术前12 h开始。手术于复合手术间进行, 患者全身麻醉, 静脉使用抗生素预防感染, 平卧于导管床, 双侧腹股沟斜切口暴露股动脉, 游离双股动脉并以8F尿管控制其近远端。穿刺股动脉, 置入6F短鞘及导丝, 静脉注射肝素以达到全身肝素化, 防止操作过程中形成血栓。置入5F黄金标记猪尾导管, 退出导丝并经猪尾导管造影, 显示腹主动脉瘤与肾动脉关系。对侧穿刺置入6F短鞘、Terumo超滑导丝及椎动脉导管, 交换导丝为Amplatz超硬导丝, 退出椎动脉导管和6F短鞘, 置入开窗支架第一段主体, 造影确认肠系膜上动脉及双侧肾动脉通畅, 释放第一节支架, 并确认支架十字标记位于正前方。此后释放远端支架(此时支架头端仍未展开), 从支架主体鞘中置入两支8F Arrow鞘管, 并使用BMW 300 cm 0.014英寸(1英寸= 2.54cm)导丝及眼镜蛇导管或椎动脉导管引导配合鞘管进入肾动脉。最后释放第一段主体支架的头端, 支架全部展开。造影确认支架未移位, 肠系膜上动脉及双肾动脉血流通畅, 选择合适直径的GraftmasterTM(Abbott公司, 美国)球囊扩张支架通过SupercoreTM(Cook公司, 美国)导丝置入肾动脉, 使其2/3位于肾动脉内, 1/3位于支架内, 撤出Arrow长鞘, 球囊扩张释放肾动脉支架, 此后使用稍大口径球囊扩张肾动脉支架近端, 使其成喇叭口状。造影双肾血流通畅。撤出双肾鞘管及导丝, 撤出支架第一段主体输送器, 送入第二段支架主体输送器, 重叠一节支架释放。撤出第二段主体输送器, 同侧送入与患者髂动脉直径相符的髂支, 对侧采用眼镜蛇或Simon导管与超滑导丝配合进入支架主体另一髂支内, 造影检查无误后, 置换导丝为Amplatz 超硬导丝, 撤出导管及短鞘, 置入对侧髂支。球囊扩张各连接段, 造影显示各分支血管血流通畅, 如有内漏则以橡皮球囊持续扩张3 min。造影检查支架位置及形态, 其后撤出导管导丝系统, 以Prolene线缝合血管, 清点器械纱布无误后, 逐层缝合切口。部分患者术前及术后主动脉CT重建见图1。
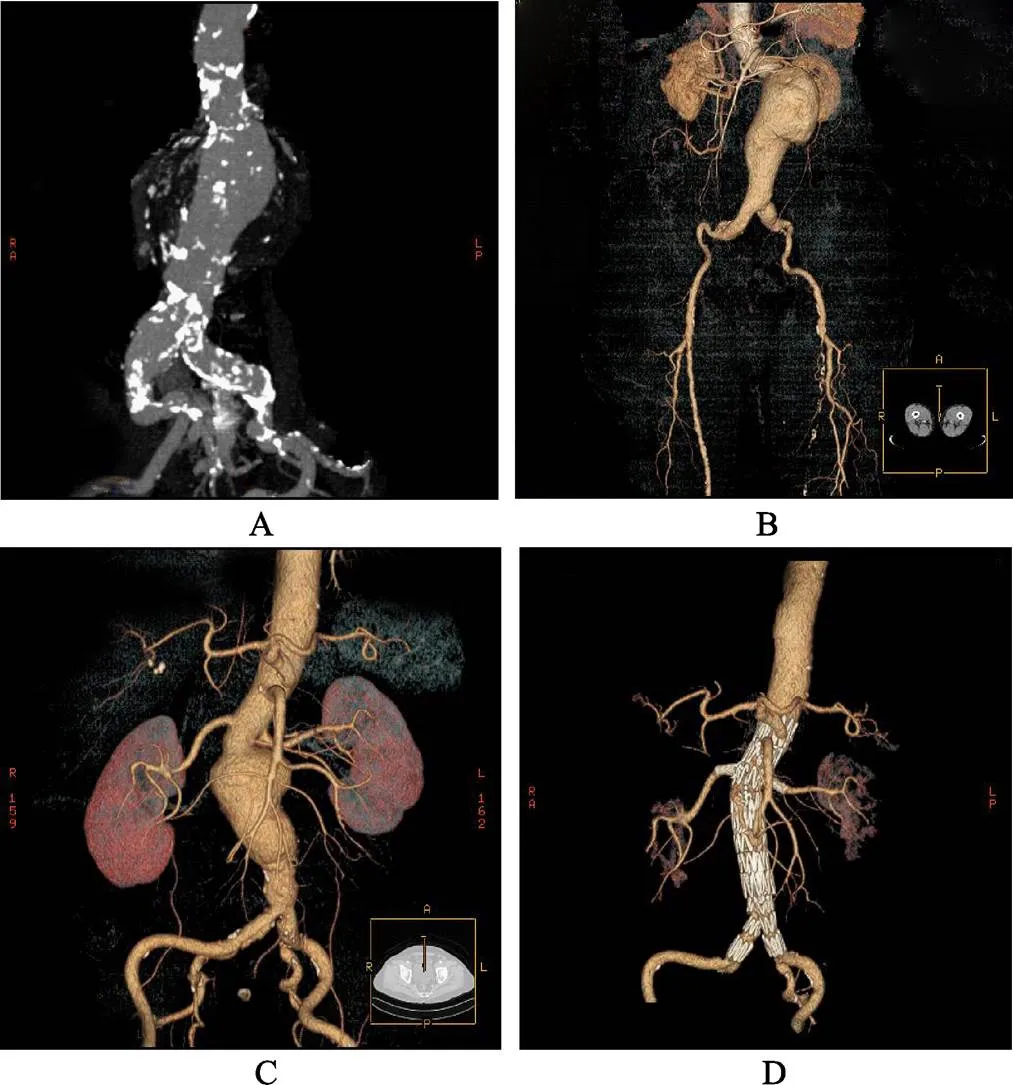
图1 腹主动脉CT重建图像
Figure 1 CT reconstructed image of aorta abdominalis
A, B, C: 患者术前腹主动脉CT重建图像, 可见瘤体近肾, 近端锚定区过短, 无法置入传统支架型血管; C: 左副肾动脉供血范围较小, 故术中未予特殊处理; D: 患者术后腹主动脉CT重建图像。术后复查血流信号消失, 患者肌酐无明显改变
2 结 果
2.1 围手术期情况
本研究共有4例患者应用开窗分支型支架血管。4例患者均患近肾AAA, 其中有3例患者合并肾功能不全。4例患者均成功进行手术, 围手术期无死亡, 具体情况见表2。术后4例患者均出现不同程度的血红蛋白下降, 经输血及其他支持治疗后好转。

表2 患者围术期情况
注: 1, 2号患者已于手术当日于重症监护病房行血液透析1次。
2.2 术后3个月随访情况
术后3个月进行随访, 与患者或家属谈话了解患者术后身体情况及有无不良主诉; 所有患者均行腹部大血管超声检查, 并检测血常规及生化指标; 1例肾功能正常者行腹部动脉CT血管造影检查。随访结果显示, 4例患者支架均未移位, 但1例发生Ⅱ型内漏, 根据CT判断为肠系膜下动脉来源, 待下次随访时观察其发展情况再行处理。2号患者肌酐较高, 达290 μmol/L。术后3个月随访结果见表3。

表3 术后3个月随访情况
3 讨 论
1999年, Faruqi等[2]第一次采用开窗支架行肾周腹主动脉瘤EVAR, 此后国外逐渐有人使用开窗支架型血管治疗肾周甚至累及内脏动脉的动脉瘤[3-5]。国内亦开始尝试使用开窗技术治疗主动脉疾病[6]。我们于2011年2月成功使用开窗支架实施了4例肾周腹主动脉EVAR。现将经验、教训总结如下。
开窗支架主要适用于治疗AAA累及肾动脉或内脏动脉, 且因身体状况或患者意愿不适宜行开放手术治疗的患者。开窗支架具有传统腔内技术所具有的各种优势, 同时可以克服传统支架型血管的一些既有问题, 如分支动脉的供血问题、迂曲瘤颈的处理等。但开窗支架仍具有EVAR的一些缺点, 如对入路血管的要求较高, 且主要为国外设计, 其设计的支架直径偏大, 输送鞘较粗, 对于我国女性患者有时无法通过入路血管; 另外, 开窗支架目前需要定制, 定制周期较长, 不适用于急诊手术, 价格也相对较高, 限制了此类手术的广泛开展。
开窗支架EVAR的围手术期死亡率明显低于开放手术, 甚至较传统EVAR更低[7]。这可能是因为开展开窗支架EVAR的中心技术更为娴熟, 经验更加丰富。主要的围手术期并发症为内漏、移植物移位导致分支动脉狭窄或闭塞、操作相关的血管损伤等。开窗支架EVAR围手术期(术后30d)内漏的发生率在国外各中心报道不一, 从2.6%到25.2%不等[7,8], 其中Ⅰ型、Ⅱ型最常见, Ⅲ型仅见个案报道[9]。在我们本次治疗的4例患者中, 有2例术中发现近端Ⅰ型内漏, 球囊扩张后好转, 术后3个月随访时内漏均消失。肾动脉狭窄或闭塞的原因则可能是支架内急性血栓形成或移植物移位。本次手术的患者置入的肾动脉支架直径分别为5, 6, 6 mm, 术后第2天超声示肾动脉血流均通畅, 此后每日口服氯吡格雷75 mg,术后3个月随访过程中未发现有肾动脉狭窄。但在术后第4天发现2例患者腹股沟切口出现淤血, 且淤血逐渐扩大, 减少氯吡格雷药量为每日25 mg后, 淤血范围停止扩大。4例患者均未出现操作相关性假性动脉瘤。术后3个月随访, 肾动脉血流均通畅, 未发生支架移位导致的肾动脉狭窄或闭塞等问题。
开窗支架EVAR的中远期并发症同样包括内漏、肾动脉狭窄或闭塞、移植物移位等。术后中远期内漏的类型同样包括Ⅰ型、Ⅱ型和Ⅲ型, 其中Ⅱ型发生最多, 但预后相对较好。如动脉瘤体未继续扩大则无需处理; 但Ⅰ型及Ⅲ型内漏通常不会自行愈合, 需行二次手术予以处理。有报道称在平均25个月的随访中, 需行二次手术的Ⅰ型内漏和Ⅲ型内漏的发生率分别为7.5%和9.3%[10]。在分支动脉通畅性方面, 有报道称开窗支架EVAR后1年肾动脉血流通畅率为92%[11]; 也有报道称在平均15个月的随访期中, 肾动脉狭窄及闭塞的发生率为3%[8], 其原因主要为支架断裂和术前存在的肾动脉狭窄继续发展所致。支架断裂的主要原因可能为动脉搏动造成的应力性金属疲劳。国际上一般将移植物较初释放时移动超过10 mm或已引发临床症状称为移植物移位[12], 但也有报道称3 mm的移位已足以造成置入支架血管的肾动脉闭塞[9]。由于分支血管位置固定, 故对于开窗支架型血管, 应更加关注其移植物移位, 微小的移位即有可能造成内脏缺血。对于此种并发症, 除术后增加随访的密度外, 还应教育患者密切关注有可能发生的症状如进食后腹痛等, 以便及早加以干预。
[1] Parodi JC, Palmaz JC, Barone HD.Transfemoral intraluminal graft implantation for abdominal aortic aneurysms[J]Ann Vasc Surg, 1991, 5(6): 491-499.
[2] Faruqi RM, Chuter TA, Reilly LM,. Endovascular repair of abdominal aortic aneurysm using a pararenal fenestrated stent-graft[J]J Endovasc Surg, 1999, 6(4): 354-358.
[3] Browne TF, Hartley D, Purchas S,. A fenestrated covered suprarenal aortic stent[J]Eur J Vasc Endovasc Surg, 1999, 18(5): 445-449.
[4] Stanley BM, Semmens JB, Lawrence-Brown MM,. Fenestration in endovascular grafts for aortic aneurysm repair: new horizons for preserving blood flow in branch vessels[J]. J Endovasc Ther, 2001, 8(1): 16-24.
[5] Anderson JL, Berce M, Hartley DE. Endoluminal aortic grafting with renal and superior mesenteric artery incorporation by graft fenestration[J]. J Endovasc Ther, 2001, 8(1): 3-15.
[6] 郭伟, 刘小平, 尹太, 等. 开窗式支架型血管重建主动脉弓1例[J]中国实用外科杂志, 2007, 27(12): 1014.
[7] Sun Z, Mwipatayi BP, Semmens JB,. Short to midterm outcomes of fenestrated endovascular grafts in the treatment of abdominal aortic aneurysms: a systematic review[J]. J Endovasc Ther, 2006, 13(6): 747-753.
[8] Amiot S, Haulon S, Becquemin JP,. Fenestrated endovascular grafting: the French multicentre experience[J]. Eur J Vasc Endovasc Surg, 2010, 39(5): 537-544.
[9] O'Neill S, Greenberg RK, Haddad F,. A prospective analysis of fenestrated endovascular grafting: intermediate- term outcomes[J]. Eur J Vasc Endovasc Surg, 2006, 32(2): 115-123.
[10] Troisi N, Donas KP, Austermann M,. Secondary procedures after aortic aneurysm repair with fenestrated and branched endografts[J]. J Endovasc Ther, 2011, 18(2): 146-153.
[11] Nordon IM, Hinchliffe RJ, Holt PJ,. Modern treatment of juxtarenal abdominal aortic aneurysms with fenestrated endografting and open repair——a systematic review[J]. Eur J Vasc Endovasc Surg, 2009, 38(1): 35-41.
[12] Cao P, Verzini F, Zannetti S,. Device migration after endoluminal abdominal aortic aneurysm repair: analysis of 113 cases with a minimum follow-up period of 2 years[J]. J Vasc Surg, 2002, 35(2): 229-235.
(编辑: 任开环)
Fenestrated endovascular stent graft for juxtarenal abdominal aortic aneurysms: preliminary results
ZUO Shangwei, JIA Xin, DU Xin, LIU Xiaoping, XIONG Jiang, MA Xiaohui, ZHANG Hongpeng, ZHANG Minhong, XU Yongle, ZHANG Jia, GUO Wei
(Department of Vascular Surgery, Chinese PLA General Hospital, Beijing 100853, China)
To analyze the early outcome of juxtarenal abdominal aortic aneurysms(AAA) repair with fenestrated endovascular stent graft.Four juxtarenal AAA patients with severe comorbidities who were not suitable for open surgery were included. Fenestrated endovascular stent graft was customized according to CT data. The stent graft was implanted together with two small stent grafts into the renal arteries under general anesthesia.After operation, digital subtraction angiograph(DSA) showed the patency of the visceral arteries and the renal arteries and favorable morphology of the stent graft. Minimal proximal typeⅠendoleak was found in 2 cases. The follow-up results at 3 months after the operation showed that the morphology of the stent graft was normal in all 4 patients; typeⅠendoleak found immediately after the operation in two patients disappeared; type Ⅱ endoleak was detected in another patient.Fenestrated endovascular stent graft yields satisfactory short-term therapeutic effects on patients with juxtarenal AAA.
fenestrated endovascular stent graft; endovascular repair; aortic aneurysm, abdominal
R543.1
A
10.3724/SP.J.1264.2012.00028
2011-05-27;
2011-07-22
郭 伟, Tel: 010-66938049, E-mail: pla301dml@vip.sina.com
——导丝概述及导丝通过病变技巧

