磺达肝癸钠用于心房颤动导管消融术围术期的抗凝疗效观察
刘 婧, 王祖禄, 梁延春, 杨桂棠, 李世倍, 于海波, 韩雅玲
磺达肝癸钠用于心房颤动导管消融术围术期的抗凝疗效观察
刘 婧, 王祖禄*, 梁延春, 杨桂棠, 李世倍, 于海波, 韩雅玲
(沈阳军区总医院全军心血管病研究所, 心血管内科, 沈阳 110016)
评估皮下注射磺达肝癸钠用于心房颤动(房颤)导管消融术围术期抗凝治疗的疗效及安全性、对华法林的起效时间有无影响及在局部注射部位瘀斑的形成是否优于依诺肝素及达肝素。将射频导管消融术治疗房颤的患者随机分为依诺肝素组24例, 达肝素组20例及磺达肝癸钠组50人。消融术前皮下注射依诺肝素、达肝素或磺达肝癸钠5~10d, 消融术后皮下注射至少3~5d(同时应用华法林治疗), 待国际标准化比率(INR)上升至1.8~2.0时停用。(1)三组患者基线特征的比较差异无统计学意义(>0.05)。(2)三组疗效性及安全性的比较: 依诺肝素组、达肝素组、磺达肝癸钠组血栓栓塞事件发生率分别为0/24、0/20、1/50人, 比较三组血栓栓塞率差异无统计学意义; 三组均无大出血事件发生。(3)三组药物在华法林INR不同的达标时间例数上差异无统计学意义(>0.05)。(4)三组患者注射部位瘀斑情况比较: 用药7天时, 磺达肝癸钠注射部位皮下瘀斑的发生率明显降低(磺达肝癸钠组、依诺肝素组、达肝素组无瘀斑患者所占比例分别为: 0.66, 0.21, 0.15,<0.05), 瘀斑长径明显减小(磺达肝癸钠组、依诺肝素组、达肝素组瘀斑长径分别为: 0.7, 2.3, 3.3 cm,<0.05), 且优于依诺肝素及达肝素。与依诺肝素和达肝素组相比, 磺达肝癸钠用于房颤射频导管消融术围术期抗凝治疗未增加严重出血及血栓栓塞, 也不影响INR的达标时间, 但可以减少注射部位皮下瘀斑的发生率和范围。
心房颤动; 导管消融术; 磺达肝癸钠; 抗凝药; 低分子肝素
心房颤动(房颤)是临床最常见的心律失常之一, 且随年龄增长该发病率增高[1], 除因症状导致住院率升高和生活质量下降外, 可使致残率、死亡率明显增加。抗心律失常药物转复和维持窦性心律疗效欠佳, 近年来射频导管消融治疗房颤已成为Ⅰ类或Ⅱa类适应证[2,3]。对于行导管消融的患者, 围术期的抗凝治疗对于减少血栓栓塞并发症非常重要, 然而, 目前对于房颤导管消融围术期抗凝治疗的药物及其方案并未统一, 多在消融术前3~5d停用华法林, 给予低分子肝素作为华法林桥接治疗[4], 待国际标准化比率(international normal ratio, INR)降至1.5以下时行射频导管消融, 且术后继续应用低分子肝素, 同时服用华法林, 待INR达1.8以上时停用低分子肝素。但低分子肝素需每日2次注射, 根据患者体质量调整剂量(通常1mg/kg), 仍有少数患者发生血小板减低症, 且注射局部出现瘀斑的发生率较高和范围较大[5]。磺达肝癸钠是继低分子肝素后的新一代抗凝药物,是一种人工戊多糖, 可以选择性地与抗凝血酶结合, 从而快速抑制因子Ⅹa; 与低分子肝素不同的是磺达肝癸钠不与Ⅱa因子、血小板、蛋白等相互作用, 极少发生血小板减低症, 该药起效迅速, 而且其半衰期长达17~21h, 因此只需一日一次用药, 且在不同患者中应用剂量相同, 由于上述特点, 磺达肝癸钠已在肺栓塞治疗、外科手术围术期防止深静脉血栓、急性冠脉综合征(acute coronary syndrome, ACS)治疗中广泛应用[6], 但其在房颤围术期抗凝治疗中的有效性和安全性上研究较少。本研究通过与低分子肝素相比较, 研究磺达肝癸钠在房颤导管消融围术期应用是否同样安全、有效, 在减少局部注射部位瘀斑形成方面是否有优势。
1 对象与方法
1.1 对象
1.1.1 入选标准 选择2011年2月至2011年11月, 连续在沈阳军区总医院接受射频消融术治疗的房颤患者115例。(1)诊断为房颤行射频消融术需要抗凝治疗的患者; (2)患者性别不限、18岁≤年龄<80岁; (3)从抗凝开始到抗凝结束必须选用同一种抗凝药物。
1.1.2 排除标准 (1)对此类药物或肝素类过敏史; (2)慢性肾脏病4、5期, 肌酐清除率<20ml/min; (3)严重肝功能异常(>3倍正常值); (4)血小板< 7×104/m3; (5)先天性或获得性血液疾病; (6)胃肠活动性溃疡; (7)近期颅内性出血; (8)近期脊髓或眼科术后; (9)经食管超声检查(transesophageal echocardiography, TEE)发现左心房血栓; (10)经电生理检查证实不是房颤的患者; (11)术后患者均服用华法林抗凝。
1.1.3 记录内容 三组患者用药前均化验并记录血液分析、凝血全项、肝功能、肾功能、甲状腺功能等, 同时记录患者的年龄、性别、体质量、联合用药(包括术前服用抗血小板、抗凝药物, 以及经证实能有增强或降低华法林抗凝作用的药物如胺碘酮、普罗帕酮、奥美拉唑、安体舒通、喹诺酮类抗生素、头孢类抗生素、地高辛、肝素)、伴随疾病(如高血压、冠心病、糖尿病、心力衰竭、肝功能异常、甲状腺功能异常及脑卒中病史)、服药前INR值等基线情况。
1.2 药物
低分子肝素: 依诺肝素(Enoxaparine, 克赛), 达肝素钠注射液(FragminTM, 法安明), 磺达肝癸钠(FondaparinuxNa, 安卓)。
1.3 方法
1.3.1 随机化分组 应用1到100随机数字表按顺序规定1~25为A组(依诺肝素组, 1mg/kg, 皮下注射, 2次/d), 26~50为B组(达肝素组,100U/kg, 皮下注射, 2次/d), 51~100为C组(磺达肝癸钠组, 2.5mg, 皮下注射, 1次/d。根据患者入院的先后顺序编号1~100所对应的随机数字表的位置, 随机分入3组, 如试验过程中发现不符合试验标准的患者则从本试验剔除。
1.3.2 给药方法 如患者入院前服用华法林抗凝治疗, 入院后停用华法林, 根据随机分组结果给予依诺肝素、达肝素或磺达肝癸钠皮下注射5~10d, 皮下注射按标准方法对护士进行培训[7,8], 每次更换注射部位。术前数天行TEE检查[4,9], 如TEE未发现左心房血栓, 期间继续给予抗凝治疗, 并于术前8~12h停用低分子肝素, 术前24h停用磺达肝癸钠。TEE发现心房血栓的患者, 近期不行射频导管消融, 从本试验剔除。导管消融术中, 当完成房间隔穿刺术后, 静脉给予普通肝素100U/kg, 以后每小时追加1000~1500 U, 维持激活凝血时间250~350s。术后4~6h开始继续按原剂量给予依诺肝素、达肝素或磺达肝癸钠抗凝, 术后当天服用华法林, 口服起始剂量为4.5mg, 之后于每晚16:00服用, 与依诺肝素、达肝素、磺达肝癸钠重叠至少3~5d。术后第4天开始检测INR值, 如INR≥1.8后停用低分子肝素或磺达肝癸钠, 继续口服华法林3mg, 1次/d,调整华法林剂量使INR控制在2~3之间, 消融术后通常服用华法林2~3个月。
1.4 观察指标
1.4.1 疗效性 死亡率、脑栓塞、肺栓塞、体循环栓塞。
1.4.2药物安全性 出血并发症的严重程度根据TIMI分级作为标准。大量出血: 包括颅内出血, 明显出血使血红蛋白降低≥50 g/L或血细胞压积降低≥15%。少量出血: 自发血尿、呕血, 可察觉出血使血红蛋白降低≥30 g/L或血细胞压积降低≥10%, 未察觉出血使40 g/L≤血红蛋白降低≤50 g/L, 或12%≤血细胞压积降低≤15%。不明显出血: 血液丢失未达到以上标准。
1.4.3 INR达标时间 观察3种抗凝药物对华法林达标时间有无影响。
1.4.4 患者用药7d后的瘀斑测量和测量标准[10]如瘀斑形状不规则, 以测量瘀斑长径为标准, 长径<0.5cm为“无瘀斑”, 长径>0.5cm为有瘀斑, 其中长径0.5~2.0cm为“轻度”、长径3.0~4.0cm为“中度”、长径>5.0cm为“重度”, 若已形成硬结, 则归入重度。
1.5 门诊定期复查或电话随访
术后门诊和电话随访患者血栓栓塞事件及出血事件的发生率。
1.6 统计学处理
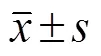
2 结 果
2.1 入选病例基本情况
试验共入选115例患者, 按上述入选标准及排除标准严格筛查后实际入选94例, 男57例, 女37例。依诺肝素组24例, 达肝素组20例, 磺达肝癸钠组50例。
2.2 三组患者基线特征的比较
三组的年龄、性别、体质量、合并用药(术前服用抗凝药、抗血小板药物及已证实有增强或降低华法林抗凝作用的药物、伴随疾病、起始INR值等基线特征差异无统计学意义(>0.05; 表1)。
2.3 三组患者疗效性及安全性的比较
随机分配到磺达肝癸钠组的50例患者中, 有1例于术后第二天出现左侧肢体行动不灵活、左手麻木, 立即行头CT检查, 右侧基底节区多发低密度影, 诊断为脑梗死, 继续给予抗凝治疗, 患者于术后第3天症状消失, 随访中再无上述症状出现。依诺肝素组及达肝素组均无血栓栓塞事件, 三组中无一例患者死亡。三组均无大出血事件发生。三组在疗效及安全性方面差异均无统计学意义(>0.05)。这一结果证实了2.5mg, 1次/d、皮下注射磺达肝癸钠在疗效性及安全性方面与依诺肝素、达肝素相比呈非劣效性。
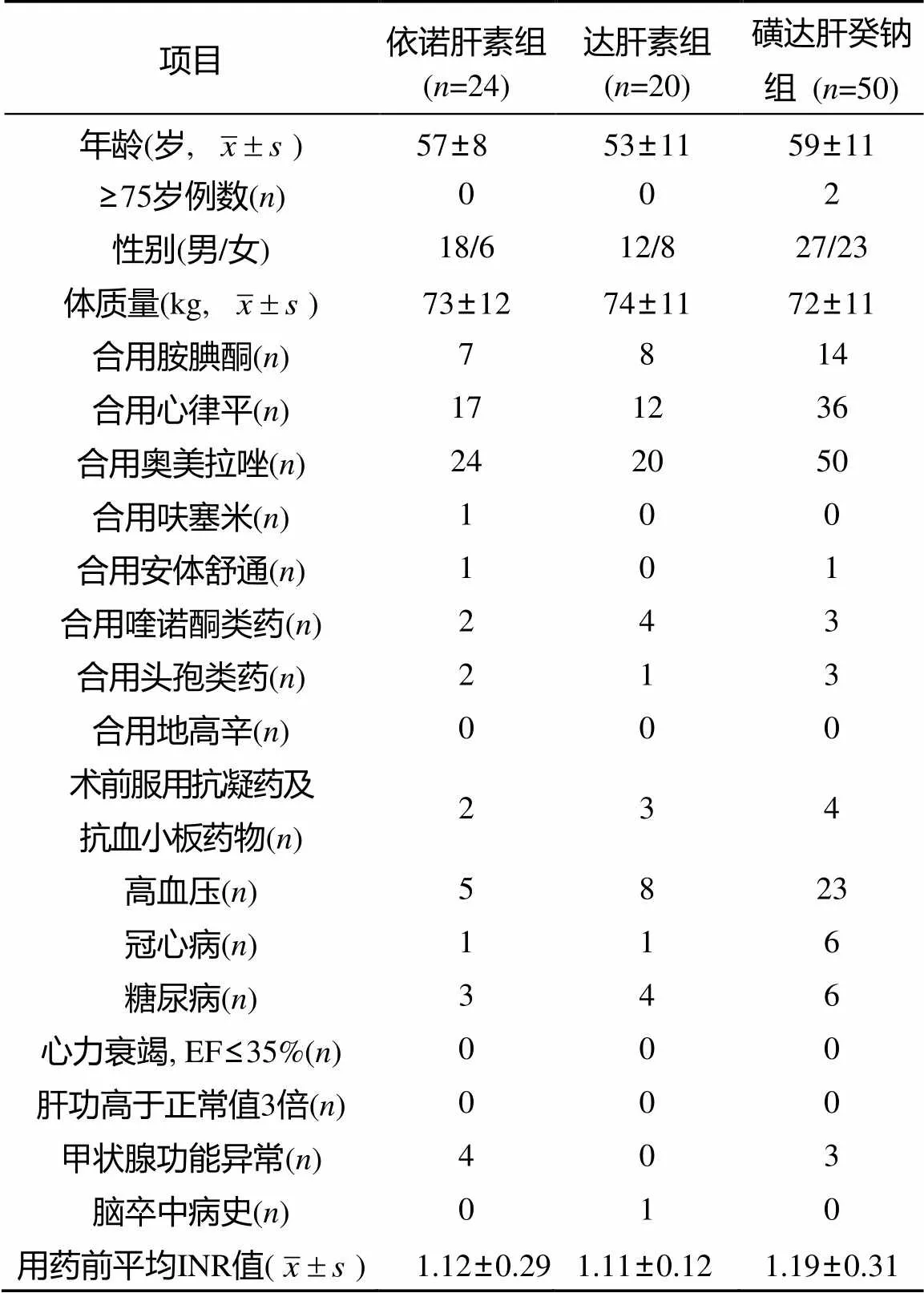
表1 三组患者基线资料比较
注: INR: 国际标准化比率
2.4 三组华法林达标时间比较
三组患者达标时间集中在第4天至第7天, 第4天三组达标人数共36例, 第5天达标人数17例, 第6天达标人数17例, 第7天达标人数14例。分别在第4天、第5天、第6天、第7天时, 进行三种药物对不同达标时间的达标例数的比较, 差异均无统计学意义(>0.05; 表2)。结果提示应用磺达肝癸钠对INR的达标时间无影响。
2.5 三组患者注射部位形成瘀斑情况比较
用药第7天时, 三组患者无瘀斑、轻度、中度、重度在依诺肝素组分别为5, 10, 4, 5例, 所占比例分别为0.21、0.42、0.17、0.20, 平均瘀斑长径2.3cm; 在达肝素组分别为3, 5, 4, 8例, 比例分别为0.15、0.25、0.20、0.40, 平均瘀斑长径3.3cm; 在磺达肝癸钠组分别为33, 13, 2, 2例, 比例分别为0.66、0.26、0.04、0.04, 平均瘀斑长径0.7cm。三组无瘀斑人数所占比例以磺达肝癸钠组为最高, 且显著高于依诺肝素组和达肝素组, 差异具有统计学意义(<0.05); 三组中、重度瘀斑人数所占比例以磺达肝癸钠组为最低, 且显著低于依诺肝素组和达肝素组, 差异具有统计学意义(<0.05); 磺达肝癸钠组患者瘀斑长径显著小于依诺肝素组和达肝素组, 且差异具有统计学意义(<0.05), 但比较依诺肝素组与达肝素组两组患者在注射部位形成瘀斑长径差异无统计学意义(>0.05; 图1, 2)。结果提示磺达肝癸钠可以减小注射部位皮下瘀斑的面积, 降低瘀斑发生率, 且优于依诺肝素及达肝素。
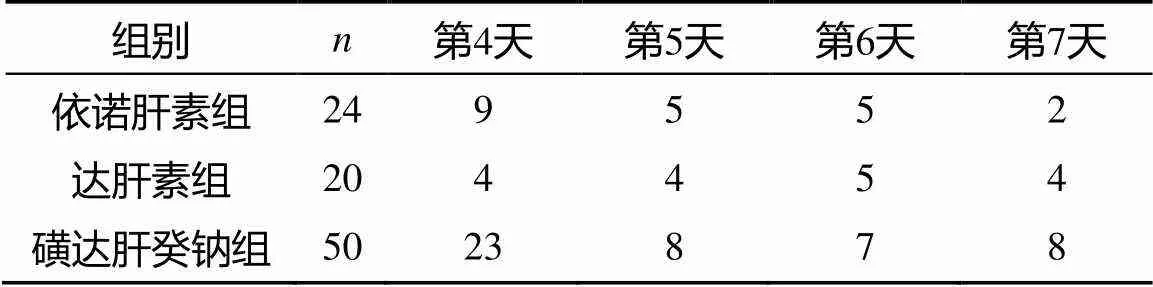
表2 三组INR不同达标时间例数的比较
注: INR: 国际标准化比率
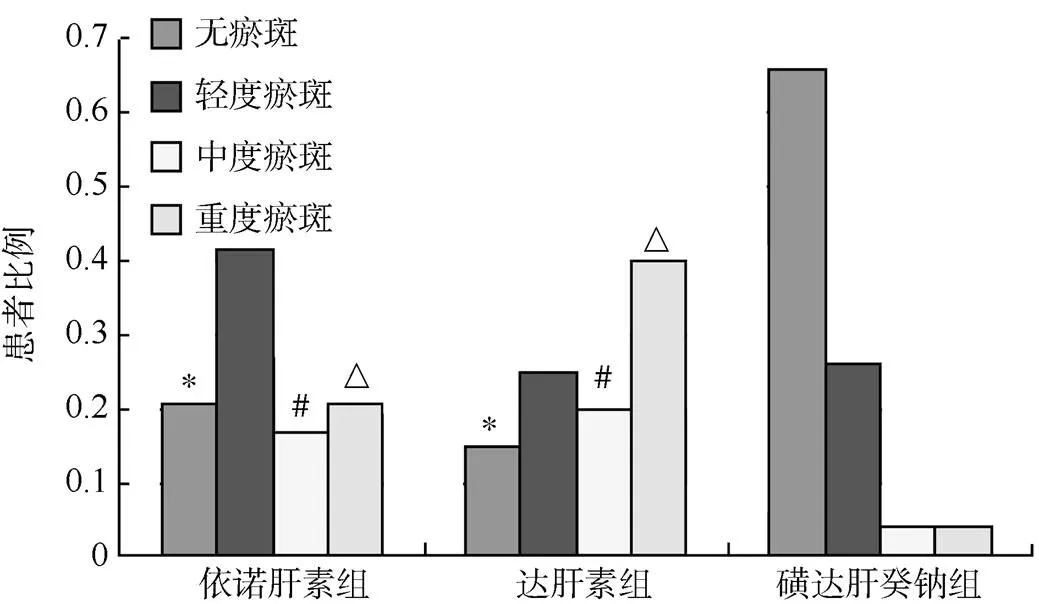
图1 三组患者皮下注射部位形成瘀斑严重程度分布比例
Figure 1 Distributions of the severity of ecchymosis formation in subcutaneous injection sites in three groups
与磺达肝癸钠组无瘀斑比较,*<0.05; 与磺达肝癸钠组中度瘀斑比较,#<0.05; 与磺达肝癸钠组重度瘀斑比较,△<0.05
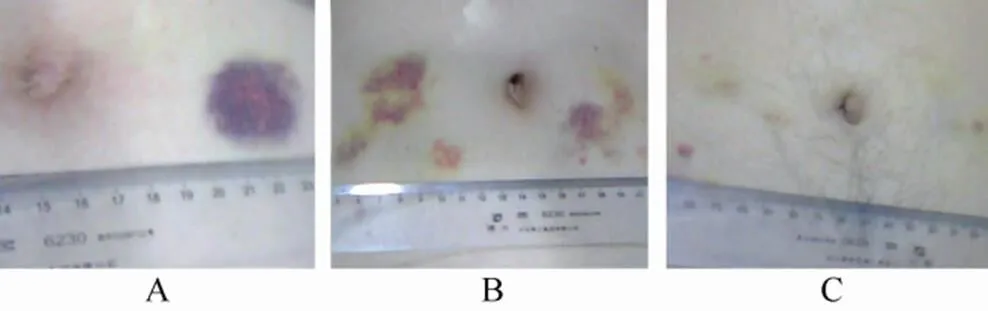
图2 依诺肝素、达肝素、磺达肝癸钠三组各1例典型病例平均瘀斑长径测量
Figure 2 Average length measurement of ecchymosis of one of the typical patients in three different groups
A: 依诺肝素组; B: 达肝素组; C: 磺达肝癸钠组
3 讨论
随着人口老龄化, 房颤对人类健康与生命的危害(包括增加死亡率、脑卒中率、住院率、降低生活质量和运动耐量、降低左室功能)日趋严重。近年来房颤的导管消融治疗已取得令人瞩目的进展, 但围绕房颤导管消融的围术期治疗, 尤其是抗凝治疗并未达成共识。低分子肝素用于深静脉血栓预防、肺栓塞和ACS、房颤等疾病的抗凝治疗已取得较好效果, 依诺肝素及达肝素是临床上常用的两种低分子肝素, 与普通肝素相比具有以下特点: ⑴无需实验室监测凝血指标, 使用方便。⑵生物利用度高, 半衰期长, 是普通肝素的2~4倍。⑶抗Xa/IIa活性的比率明显高于普通肝素, 抗血栓作用强。⑷对血小板功能影响小, 较少引起血小板减少症等。但低分子肝素多是从动物内脏中提取混合物后通过不同方法裂解而成, 成分不稳定, 作用的靶目标选择性较差, 凝血因子抑制强度的批间差异较大。磺达肝癸钠是人工合成的单一的化合物, 不含来源于动物的成分[11, 12],减少了病原微生物污染和资源短缺的潜在风险, 特异性对靶目标(Xa因子)高度选择。磺达肝癸钠的问世很大程度上解决了要么过分关注抗凝强度造成大出血风险增加, 要么追求减少出血又无法保证抗凝强度足够这一问题。多个在骨科术后预防深静脉血栓和肺栓塞[13-16], 肺栓塞治疗[17, 18]和ACS抗凝治疗[19]等所进行的临床试验已证实磺达肝癸钠在抗凝疗效和安全性方面优于或不劣于低分子肝素或普通肝素。已被多种疾病治疗指南推荐为上述疾病抗凝治疗的I类适应证。
目前房颤导管消融围术期抗凝治疗多应用低分子肝素, 主要用于消融术前替代华法林和消融术后桥接华法林INR尚未达标时的治疗。目前对于房颤(尤其阵发性房颤)消融术前是否应用华法林抗凝治疗及抗凝治疗应持续多长时间尚无定论, 而应用华法林时INR值达标并维持稳定多需要较长时间, 故国内较多中心在房颤导管消融术前应用低分子肝素皮下注射替代华法林抗凝治疗的时间(≥5~10d)长于术前已应用华法林抗凝治疗的患者(3~5d)。但低分子肝素需每日2次皮下注射, 需按患者体质量调整剂量, 且注射局部出现瘀斑的发生率较高和范围较大, 给患者的躯体和精神造成一定痛苦。
磺达肝癸钠是一种间接Xa因子抑制剂, 具有不与IIa因子、血小板、蛋白等相互作用、极少发生血小板减低症、只需每日用药1次、且在不同患者中应用剂量相同等优点, 其主要通过肾脏排泄, 不通过肝脏的P450酶代谢, 理论上与华法林等通过肝脏代谢的药物应无明显相互作用。本试验结果表明磺达肝癸钠在房颤抗凝治疗疗效和安全性方面不劣于低分子肝素, 且在INR达标方面与低分子肝素相比也不影响华法林的起效和INR达标时间。
经腹壁皮下注射低分子肝素引起的皮下瘀斑是临床中常见的并发症, 影响其发生率及范围大小有较多因素, 如:(1)局部药液残留, 渗入毛细血管和刺激局部神经,导致瘀斑和疼痛;(2)皮下注射时过浅进针和反复注射部位距离太近;(3)皮下脂肪很薄,刺入腹部肌肉;(4)按压时间及力度不当;(5)注射时是否垂直进针和是否保留气泡等。本实验中均统一培训采用垂直进针注射方法,注射前不排气泡, 尽量避免了由于注射方法不同而影响瘀斑形成。用药第7天时统一测量瘀斑长径, 试验结果表明磺达肝癸钠在减少注射部位皮下瘀斑的出现或减小瘀斑的面积方面优于依诺肝素及达肝素。其原因可能与磺达肝癸钠仅每日皮下注射1次, 且其仅具有Xa因子抑制作用, 而不具有抗IIa因子、血小板等作用有关。
4 结 论
与依诺肝素和达肝素相比, 磺达肝癸钠用于房颤射频导管消融术围术期抗凝治疗未增加严重出血及血栓栓塞事件, 也不影响INR的达标时间, 且具有只需每日1次皮下注射、在不同患者中应用剂量相同和可以减少注射部位皮下瘀斑的发生率和范围等优势。
[1] Prystowsky EN, Benson DW Jr, Fuster V,. Management of patient with atrial fibrillation.A Statement for Healthcare Professionals. From the Subcommittee on Electrocardiography and Eletrophysiology, American Heart Association[J]. Circulation, 1996, 93(6): 1262-1277.
[2] Camm AJ, Kirchhof P, Lip GY,. Guidelines for the management of arial fibrillation: the Task Force for the Management of Arial Fibrillation of the European Society of Cardiology(ESC)[J]. Europace, 2010, 12(10): 1360-1420.
[3] Fuster V, Ryden LE, Cannom Ds,. ACC/AHA/ESC 2006 guidelines for the management of patients with atrial fibrillation —executive summary: a report of the American College of Cardiology/American Heart Association Task Force on practice guidelines and the European Society of Cardiology Committee for Practice Guidelines (Writing Committee to Revise the 2011 Guidelines for the Management of Patients with Atrial Fibrillation)[J]. Eur Heart J, 2006, 27(16): 1979-2030.
[4] Calkins H, Brugada J, Packer DL,. HRS/EHRA/ECAS expert Consensus Statement on catheter and surgical ablation of atrial fibrillation: recommendations for personnel, policy, procedures and follow-up. A report of the Heart Rhythm Society(HRS) Task Force on catheter and surgical ablation of atrial fibrillation[J]. Heart Rhythm, 2007, 4(6): 816-861.
[5] 王爱英, 金艳宏, 王玲娜, 等. 低分子肝素皮下注射按压方法的研究[J]. 护理研究, 2004, 18(10): 852.
[6] Douketis JD, Berger PB, Dunn AS,. The perioperative management of antithrombotic therapy: American College of Chest Physicians Evidence-Based Clinical Practice Guidelines (8th Edition)[J].Chest, 2008, 133(6 Suppl): 299S-339S.
[7] 程 立, 梅瑞杰. 低分子肝素钠皮下注射方法探讨[J]. 中原医刊, 2003, 30(21): 60.
[8] 徐 艳. 腹部皮下注射低分子肝素减少瘀斑的发生[J]. 首都医科大学学报, 2001, 22(2): 140.
[9] Natale A, Raviele A, Arentz T,. Venice chart international consensus document on atrial fibrillation ablation[J]. J cardiovasc electrophysiol, 2007, 18(5): 560- 580.
[10] 杨秀梅, 潘冬梅, 杨东辉. 改良低分子肝素注射方法对局部皮下出血的影响[J]. 护理学报, 2007, 14(2): 16-17.
[11] van Boeckel CA, Petitou M. The unique antithrombin III binding domain of heparin: a lead to new synthetic antithrombotics [J]. Angew Chem Int Ed Engl, 1993, 32(6): 1671-1690.
[12] Petitou M, Lormeau JC, Choay J. Chemical synthesis of glycosaminoglycans: new approaches to antithrombotic drugs[J]. Nature, 1991, 350(6319 Suppl): 30-33.
[13] Shorr AF, Kwong LM, Sarnes M,Venous thromboembolism after orthopedic surgery: implications of the choice for prophylaxis[J]. Thromb Res, 2007, 121(1): 17-24.
[14] Eriksson BI, Bauer KA, Lassen MR,Fondaparinux compared with enoxaparin for the prevention of venous thromboembolism after hip-fracture surgery[J]. N Engl J Med, 2001, 345(18): 1298-1304.
[15] Bauer KA, Eriksson BI, Lassen MR,. Fondaparinux compared with enoxaparin for the prevention of venous thromboembolism after elective major knee surgery[J]. N Engl J Med, 2001, 345(18): 1305-1310.
[16] Turpie AG, Bauer KA, Eriksson BI,. Postoperative fondaparinux versus postoperative enoxaparin for prevention of venous thromboembolism after elective hip-replacement surgery: a randomised double-blind trial[J]. Lancet, 2001, 359(9319): 1721-1726.
[17] Büller HR, Davidson BL, Decousus H. Fondaparinux or enoxaparin for the initial treatment of symptomatic deep venous thrombosis: a randomized trial[J]. Ann Intern Med, 2004, 140(11): 867-873.
[18] Büller HR, Davidson BL, Decousus H,. Subcutaneous fondaparinux versus intravenous unfractionated heparin in the initial treatment of pulmonary embolism[J]. N Engl J Med, 2003, 349(18): 1695-1702.
[19] Yusuf S, Mehta SR, Chrolavicius S,. Comparison of fondaparinux and enoxaparin in acute coronary syndromes[J]. N Engl J Med, 2006, 354(14): 1464-1476.
(编辑: 周宇红)
Anticoagulation efficacy and safety of fondaparinux during perioperative period of radiofrequency catheter ablation of atrial fibrillation
LIU Jing, WANG Zulu*, LIANG Yanchun, YANG Guitang, LI Shibei, YU Haibo, HAN Yaling
(Department of Cardiology, Cardiovascular Institute of PLA, Shenyang General Hospital, Shenyang Military Command, Shenyang 110016, China)
To evaluate the efficacy and safety of subcutaneous injection of fondaparinux during perioperative period of radiofrequency catheter ablation of atrial aibrillation (AF), figure out whether it will affect the targeted time of INR after using warfarin, and compare with dalteparin and enoxaparin for ecchymosis effects at the injection sites.Ninety-four AF patients undergoing catheter ablation were randomly divided into 3 groups, including 24 patients in enoxaparin group, 20 patients in dalteparin group, and 50 patients in fondaparinux group. Enoxaparin, dalteparin or fondaparinux was subcutaneously injected for 5-10 days before catheter ablation, and continued for at least 3-5 days after ablation before INR achieving the target of 1.8-2.0 under the use of oral warfarin.There was no statistical difference in baseline characteristics among three groups (>0.05). The thromboembolic events were 0/24 patients in enoxaparin group, 0/20 in dalteparin group and 1/50 in fondaparinux group, and there was no statistical difference in the incidence of thromboembolic events among three groups. There was no serious bleeding events in all three groups. The time for achieving the targeted INR after ablation had no statistical difference among three groups (>0.05). The incidence and the long diameter of ecchymosis in injection sites were significantly lower/less in fondaparinux group than in enoxaparin and dalteparin groups on the seventh day after injection of fondaparinux or LMWH (non-ecchymosis ratio: fondaparinux, 0.66; enoxaparin, 0.21; dalteparin, 0.15;<0.05; long diameter of ecchymosis: fondaparinux, 0.7cm; enoxaparin, 2.3cm; dalteparin, 3.3cm;<0.05).Compared with enoxaparin and dalteparin, fondaparinux in perioperative anticoagulation therapy of catheter ablation of AF neither increases the major bleeding and thromboembolic events, nor affects the targeted time of INR after using warfarin. Fondaparinux could reduce the incidence and scope of ecchymosis in subcutaneous injection sites.
atrial fibrillation; catheter ablation; Fondaparinux; anticoagulants; low molecular weight heparin
R541.7+5
A
10.3724/SP.J.1264.2012.00023
2012-01-04;
2012-01-14
王祖禄, Tel: 024-28851121, E-mail: wangzl@medmail.com.cn

