多层螺旋CT血管成像评估多支肾动脉
刘小琨,赵小虎,杨红兵,王 涛,王 勇
(1.上海市嘉定区南翔医院放射科,上海 201802;2.复旦大学附属上海市第五人民医院放射科,上海 200240)
正常每侧肾由发自腹主动脉的单一肾动脉供血,但如胚胎期供应中肾的多支原始动脉部分退化不全,则可存在多支肾动脉,正常人群中约1/3存在此种血管变异[1-2]。评估多支肾动脉对于肾脏手术、肾血管介入和肾移植等非常重要,一旦手术误伤或误扎多支肾动脉,可导致严重并发症[1-4]。此外,多支肾动脉的存在还可能与高血压、肾盂积水等相关[1]。本研究回顾性分析多层螺旋CT血管成像(multislice spiral CT angiography, MSCTA)中多支肾动脉表现,探讨MSCTA评估多支肾动脉的可行性。
1 资料与方法
1.1 一般资料 回顾性分析2018年6月—2019年5月500例接受上腹部动态CT增强扫描患者,均因临床需要而接受腹部增强CT检查,检查前均签署知情同意书,包括部分罹患肾脏相关疾病、但对肾血管成像无明显影响者。排除标准:年龄<18岁或>85岁;肾脏先天畸形;肾脏疾病影响肾功能及肾动脉;腹部其他疾病影响观察肾动脉;图像质量差。最终460例纳入研究,男268例,女192例,年龄18~85岁,平均(56.9±15.9)岁。
1.2 仪器与方法 嘱患者检查前空腹>6 h,扫描前20~40 min饮水600~800 ml。采用GE BrightSpeed Elite 16排螺旋CT扫描仪行上腹部动态CT增强扫描,管电压120 kV,管电流200 mA,螺距1.375,层厚5 mm,层距5 mm,采用高压注射器以流率3~3.5 ml/s经肘前静脉注射非离子型对比剂碘佛醇(350 mgI/ml)90~100 ml,分别于注射对比剂后20~25 s、55~60 s采集动脉期、门静脉期图像。将原始数据薄层(1.25 mm)重组后传至ADW 4.5工作站。
1.3 图像分析 根据原始横断面图像,结合多种重建技术,包括多平面重建(multi-planner reformation, MPR)、最大密度投影(maximum intensity projection, MIP)和容积再现(volume rendering, VR)等行肾血管成像。由2名放射科副主任医师共同分析图像,意见不同时经讨论达成一致,观察肾动脉数目、起源、走行及入肾位置,并对多支肾动脉进行分型。
多支肾动脉的定义及分型:正常肾动脉为左右各1支,如肾脏由1支以上动脉供血,无论其径线,均判定为多支肾动脉。根据文献[1,5-7]方法将多支肾动脉分为Ⅰ型(副肾动脉型)和Ⅱ型(多支相仿型)。
1.4 统计学分析 采用SPSS 19.0统计分析软件。计数资料以率表示,采用χ2检验比较男、女性及左、右肾之间多支肾动脉发生率及其分型。P<0.05为差异有统计学意义。
2 结果
460例CT图像均可清晰显示肾动脉数目、起源、走行及入肾位置。141例存在多支肾动脉,发生率30.65%(141/460);左肾、右肾多支肾动脉发生率分别为21.08%(97/460)和17.83%(82/460),差异无统计学意义(χ2=1.560 6、P=0.221 6);其中38例(38/460,8.26%)双侧同时存在多支肾动脉。141例中,128例(128/460,27.82%)存在2支、11例(11/460,2.39%)3支和2例(2/460,0.43%)存在4支肾动脉,未见存在5支及以上肾动脉者。见表1。

表1 460例中男性与女性、左肾与右肾间多支肾动脉发生情况比较[例(%)]
141例存在多支肾动脉患者中,119例(119/460,25.87%)为Ⅰ型,CT表现为1支主肾动脉发自腹主动脉、伴1支或多支副肾动脉自肾门或肾上、下极入肾,或双侧副肾动脉并存(图1);22例(22/460,4.78%)为Ⅱ型,CT表现为2支及以上直径相仿的主肾动脉发自腹主动脉并自肾门入肾,可双侧肾同时发生(图2)。男性与女性间多支肾动脉发生率及其分型差异均无统计学意义(P均>0.05),见表2。
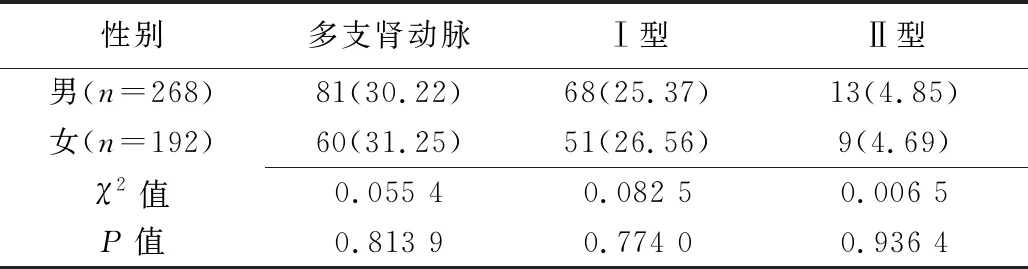
表2 460例中男性与女性间多支肾动脉发生率及其分型比较[例(%)]
3 讨论
3.1 多支肾动脉的概念、发生率及分型 肾脏及肾血管发育过程复杂。胚胎期中肾、后肾和性腺由来自背主动脉的9对中肾动脉供血,可分为头侧、中间、尾侧3组,中间组最后发育为肾动脉,如其部分动脉不退化而持续存在,则形成多支肾动脉[1],即一侧肾接受多支动脉供血;多支动脉直径可大小不等或相仿,直径最大且经肾门入肾者称为主肾动脉,其他相对细小者称为副肾动脉。据此可根据血管直径将多支肾动脉分为主+副(Ⅰ型,即副肾动脉型)和主+主两大类型(Ⅱ型)。副肾动脉绝大多数起源于腹主动脉,少数起源于腹主动脉主要分支[5,8]。也有学者[9]将不经肾门入肾的动脉称为副肾动脉,或将自主肾动脉但不经肾门入肾的动脉视为副肾动脉,后者易与单支主肾动脉产生概念混淆。既往文献[6-7,10]对副肾动脉定义存在分歧,认为副肾动脉的起源应为腹主动脉及其(不包括肾动脉在内的)分支动脉。明确相关概念有利于国内外交流和统计分析等。

图1 多支肾动脉Ⅰ型(副肾动脉型) A.患者男,39岁,右侧2支肾动脉,VR重建显示右侧主肾动脉上方细小副肾动脉自肾上极入肾; B.患者女,60岁,左侧2支肾动脉和右侧3支肾动脉并存,VR重建显示左侧主肾动脉下方细小副肾动脉自肾下极入肾,右侧主肾动脉下方2支副肾动脉分别从肾门和肾下极入肾; C.患者男,57岁,左侧3支肾动脉,VR重建显示左侧主肾动脉偏低,其上方2支副肾动脉自肾门入肾; D.患者男,49岁,左侧4支肾动脉,VR重建显示左侧主肾动脉偏高,其下方3支副肾动脉自肾门入肾,中间2支管径纤细

图2 多支肾动脉Ⅱ型(多支相仿型) A.患者男,80岁,双侧同时存在2支主肾动脉,VR重建显示双肾均有2支管径相仿的主肾动脉自腹主动脉发出、从肾门入肾,左侧1支主肾动脉位置偏低;B.患者女,65岁,左侧3支主肾动脉,VR重建显示左肾3支管径相仿的主肾动脉自腹主动脉发出、从肾门入肾
SEBASTIA等[3]观察活体肾移植供体术前MSCT,发现多支肾动脉的检出率为29%,其中2支检出率24%,≥3支为5%。CLNAR等[5]采用64排CT对504例患者行腹部CT检查,其中多支肾动脉的检出率为31.3%,包括2支22.2%、3支7.5%和4支1.4%。陈振东等[10]报告,肾动脉CTA对于副肾动脉的检出率为29.2%。本研究多支肾动脉和副肾动脉的检出率分别为30.65%和25.87%,与文献[10]数据相近。
3.2 MSCTA评估多支肾动脉 目前可用于评估肾动脉的影像学方法主要包括DSA、MSCTA、MR血管造影(MR angiography, MRA)和多普勒超声等。DSA为诊断肾血管疾病的金标准,但有创,费用高,存在电离辐射,且操作复杂。MSCTA安全、便捷、可精确评估血管,且有多种后处理重建技术,但存在电离辐射。MRA是新兴血管成像技术,但对存在变异及直径较细的肾动脉显示不佳。超声检查方便快捷,但结果易受操作者经验影响。目前MSCTA评估肾血管的价值已得到公认,许多移植中心采用MSCTA作为供者术前影像学评价方法[11]。MSCTA诊断肾动脉变异与手术所见具有高度一致性,准确率达90%~94%[8]。ZHANG等[11]发现MSCTA对直径>1.5 mm副肾动脉的检出率达100%。赵修义等[12]报道,MSCT诊断副肾动脉的准确率达98.5%。MSCTA常用后处理技术包括MPR、MIP、VR等,原理和特点各不同,对小动脉的显示率亦不同。实际工作中一般先以VR、MIP初步观察肾动脉,发现疑点时结合横断面图像及MPR进一步追踪细小动脉的起止点。本组460例经MSCTA检查后进行图像重建,CT图像均可清晰显示肾动脉数目、起源、走行及入肾位置,且明确了多支肾动脉分型。
3.3 多支肾动脉的临床意义 正常肾动脉无吻合支,由少血管的段间组织分隔。多支肾动脉供应肾脏不同区域,供血量取决于动脉管径。多支肾动脉管径相仿时,其供血比例亦相仿;而当主肾动脉管径为副肾动脉的4~5倍甚至更大时,前者供血比例可达到甚至超过90%[13]。目前多支肾动脉的存在与分型对于肾脏手术和肾移植尤为重要,有助于术中避免误伤导致大出血,或误扎副肾动脉导致移植肾相应供血区发生梗死。SEBASTIA等[3]提出,供应肾上极直径<2 mm的副肾动脉供血区域小于10%,可安全进行结扎,即使发生肾梗死也不会严重影响肾功能;而对下极副肾动脉则不能进行类似结扎,以免术后发生输尿管坏死。下极副肾动脉还可因机械性压迫肾盂输尿管连接部而导致肾盂积水[14]。此外,有学者[15]认为副肾动脉是原发性高血压发生的原因之一,可能与副肾动脉侧主肾动脉直径减小、致主肾动脉终末分支供应肾段灌注不足有关。
综上所述,多支肾动脉为常见变异,肾脏普通手术或肾移植术前需加以明确。MSCTA可准确评估多支肾动脉并对其进行分型,对指导外科医师制定手术方案、避免严重并发症具有重要意义。但本研究仅观察了多支肾动脉的MSCTA表现,未与其他成像方法进行对比,有待进一步完善。

