CO2分析仪表便携式标校装置的实验研究
,,
(海军工程大学 船舶与动力学院,武汉 430033)
目前,密闭空间中使用的CO2分析仪器需要定期标校校准以确保测量数据的准确性。其常用的标校办法是,用事先配好的CO2标气钢瓶对仪器进行标校。此标校方法存在以下问题:①标气采用动态配气,方法复杂,制备时间比较长,且费用高;②空间有限,钢瓶体积较大,携带不便,因此其对仪表的标校操作不便。解决上述问题的关键是解决标气的来源问题,即如何以简便的方式获得定量的CO2。
产生定量CO2有两种方法:其一是对在特定的压力和温度下吸附了一定量CO2的活性炭、沸石等吸附材料进行减压加热,使其释放CO2,其优点是吸附材料的吸附容量大,解吸方法简单;缺点是成本较高,样品制作困难,解吸难以控制,吸附反应需要在低温高压下进行,条件相对苛刻。其二是热分解碳酸盐,碳酸盐分解机理明确,分解温度固定可控,气体含量严格一定,成本低廉,能够稳定存放,由此可见第二种方法更具有可行性。S·J·埃克霍夫和R·A·伍德所申请的一份专利中介绍了封装在固定传感器外壳内的自校准用CO2发生装置的实例[1],但其只适用于其自身校准,且涉及的碳酸盐分解温度太高,装置在运行时不可避免会对周围环境产生影响。
为了研制出便携式CO2分析仪表标校装置,本文选择分解温度较低的碳酸盐(碳酸氢钠、碳酸氢钾)进行热分解试验,对定量制备标准气体进行试验研究,并设计CO2分析仪表便携式标校装置。
1 实验部分
1.1 碳酸盐种类选择
碳酸盐种类繁多,结合密闭空间中CO2浓度监测仪表标校的实际,所选碳酸盐必须满足以下要求。
1)单位质量碳酸盐中CO2含量尽可能高。
2)在常温以及一定的温度范围内有较好的稳定性。
3)分解温度在比较合理的尽可能低的范围内(400~600 K)。
4)主要产生CO2气体,尽量少产生其它气体,以减少对CO2的影响。
5)在较窄的温度区间能够快速地分解,分解速率快。
6)所需碳酸盐容易获得,价格便宜,便于制备、储存、运输。
通过查阅资料,得到符合上述条件的8种碳酸盐的化学式、相对分子质量、完全分解温度[2-4],见表1。考虑到药品的相对分解温度和毒性等理化特性,碳酸氢钠和碳酸氢钾成为首选。
1.2 实验试剂及仪器
高压氮气瓶(14 MPa,40 L)、减压阀、气体流量计(LZB-4型,16~160 L/h)、ZNHW-1型数字控温仪(误差±1 ℃)、万用电炉(2 kW)、自制铝块加热元件(在尺寸16 mm×4 mm×4 cm的实心铝块中放入热功率400 W的加热棒,并横向开凿圆柱形孔洞用于放置装药玻璃管)、玻璃管(4 mm×6 mm,7 mm×9 mm)、三口烧瓶(50 mL)、微型抽气泵(0~1 L/min)、铝簿双活塞气体采样袋(15 L)、GXH-1050型红外二氧化碳分析仪(量程0~3%)、分析天平(型号AL204,0~210 g 精度0.1 mg)、高温温度计(0~500 ℃)、石棉手套、白胶塞、秒表、橡胶管、直型冷凝管、石英砂、导气管、硅胶、碳酸氢钠和碳酸氢钾(纯度>99.5%)。

表1 碳酸盐性质
1.3 CO2标气规格及用量
由相关资料获得如下数据:校准CO2监测仪器所用标气体积分数为1%,以500 mL/min流速通过仪器,保持该状态15~20 min。取标校时间为20 min,可得到标校一次所用CO2的体积最大为100 mL,则CO2的摩尔数为4.464 3 mmol(标况),氮气总量为9 900 mL。
1.4 实验流程
碳酸盐热分解实验装置见图1,碳酸盐分解产生的CO2由氮气载带并经冷却和干燥后被收集,并导入CO2分析仪进行体积分数测定。

图1 碳酸盐热分解实验流程
2 结果与讨论
2.1 碳酸氢钠二氧化碳定量释放实验
2.1.1 温度和载气流量对碳酸氢钠热分解的影响
取0.753 9 g样品10份,设定温度分别取275、305、335、365、395 ℃(石英砂升温速率变化:前期6 ℃/min,中期12 ℃/min,后期24 ℃/min),载气流量分别取0.5、0.8、1.0、1.2、1.4 L/min,CO2的体积分数随时间的变化见图2,时间从开始分解后计时。
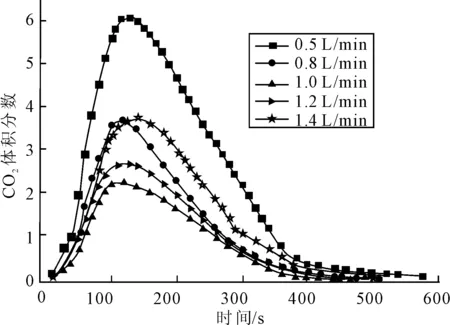
图2 275 ℃设定温度下,不同载气流量下CO2体积分数的变化
由图2可见,在275 ℃条件下,载气流量对于碳酸氢钠的热分解速率影响不大,测得烧瓶出口气体温度值均小于40 ℃,说明载气的影响远小于温度,从图2、3可以看出,275 ℃分解温度是比较合适的,为了确保该盐分解完全,后续实验取300 ℃。通过CO2分析仪上显示数据的变化得知,碳酸氢钠在70~90 ℃之间即开始分解,在150 ℃左右其分解速率开始急剧增加,取设定温度300 ℃,在不同载气流量下进行实验,测得碳酸氢钠在逐渐升温条件下完全分解完所需时间约为13 min。为了节省载气用量,载气流量可取0.5 L/min。
由图3中可见,在载气流量一定时,随着分解温度升高,CO2体积分数变化率峰值右移,且相对于275 ℃而言反而有所减小,其原因可能是当温度升高后碳酸氢钠分解产生的水分急剧增加,从而吸收了大量的热量。但温度升高,其总的分解时间变短。
2.1.2 CO2体积分数对盐的分解速率的影响
取碳酸氢钠样品10份,设定温度300 ℃,前5份在150 ℃后开始计时,不通载气加热15 min,再以1.0 L/min流量载带;后5份在150 ℃时以同样流量开始载带,各样品分解时间见表2。
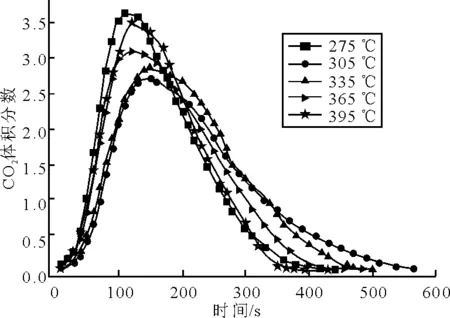
图3 1.0 L/min载气流量下,不同温度下CO2体积分数的变化
表2300℃、流量1.0L/min时不同处理方式下样品的分解时间

样品时间/min样品时间/min128.5615.2226.3713.8325.7813.5429.6912.9527.91014.8
不通载气时碳酸氢钠完全分解完所需时间为25~30 min,及时将CO2载带出去的样品分解时间为13~15 min,说明大体积分数CO2的存在会降低碳酸氢钠的分解速率。
2.1.3 升温速率的影响
石英砂和烧瓶的传热效率相对较慢,烧瓶对气体的缓冲会影响仪器读数的连续性且烧瓶内药品分散不均匀。用玻璃管取代烧瓶,用自制的铝块加热元件取代电炉进行实验,结果表明小管径的玻璃管由于气阻太大不适合实验,采用较大尺寸的玻璃管进行实验,在1.0 L/min流量下测得碳酸氢钠的分解时间约为10 min。说明升温速率增加,碳酸氢钠分解速率加快。
2.1.4 加热时间对盐分解率的影响
取设定温度300 ℃,载气流量0.5 L/min,在不同加热时间下碳酸氢钠的分解率见图4。

图4 碳酸氢钠分解率及加热介质温度变化曲线
图4中曲线1和曲线2分别为150 ℃起及开始分解起碳酸氢钠分解率随时间的变化,曲线3为加热介质温度随时间的变化。
实验中应尽量减少载气用量,剩余所需的氮气单独充入后既能使CO2快速均匀混合,又能对混合气进行冷却。
图4表明,碳酸氢钠在初始分解和150 ℃时开始计时,并以0.5 L/min载气进行载带,其分解率随时间的变化相差不大,分解率达到99%以上所需时间约为10 min。将药品加热13 min通过称重算得的CO2的体积为98~102 mL,盐的分解率在99.5%以上,冷却后气体温度低于35 ℃,通过测定,采样袋中CO2的体积分数在0.95%~1.08%。这说明采用碳酸氢钠,在150 ℃后以0.5 L/min载气载带13 min,再充入剩余氮气制取标气的方案可行,通过精确控制流量完全可以使CO2的体积分数达到1%的要求。
2.2 碳酸氢钾热分解实验
碳酸氢钾的热分解规律与碳酸氢钠相似,其开始分解的温度在140 ℃~170 ℃之间,170 ℃左右时其分解速率急剧增加,大的体积分数的CO2的同样会降低碳酸氢钾的分解速率。取碳酸氢钾0.898 4 g分别于药品温度为140、170、200 ℃时开始载带,设定温度分别取200、250、300、350 ℃,载气流量取0.5、0.8、1.1、1.4 L/min进行正交试验。结果表明,在减少载气总量方面,载气流量的影响最大,设定温度次之,通气时药品温度影响最小;在缩短盐分解时间方面,设定温度的影响最为明显,而载气流量的影响最小。200 ℃以下盐分解完的时间均超过40 min。 正交试验的最优组合结果表明,在300 ℃下,载气流量取0.5 L/min,在药品200 ℃时开始通气载带,碳酸氢钾14 min可以分解完毕,需要的载气量最少。测量采样袋中CO2的体积分数为0.95%~1.06%,这说明通过载气总量的精确控制,利用碳酸氢钾热分解同样可以满足动态配气的要求。
3 装置设计
CO2分析仪表便携式标校装置设计如图5虚线框内容所示。将质量流量控制器、标气发生装置(热解析仪)和冷却干燥装置集成在一起,通过电磁阀控制气路的开关。热分解产生的CO2气体被载气载带,经冷却干燥后被采样袋收集。进行仪器标校时只需携带一个充有标气的采样袋即可,平时采样袋折叠存放于集成装置外侧,而CO2则是以碳酸盐的形式稳定存在于装药管内,当需要标校时,只需要将药管放入加热室加热分解即可。整个装置的体积会很小,重量也将很轻,在装置外侧可以设计背带或提手以方便携带,这些不仅能节省许多空间而且还将在很大程度上提高对仪器标校的可操作性。

图5 便携式CO2分析仪表标校装置流程
4 结论
1)300 ℃下,以0.5 L/min载气流量载带时,碳酸氢钠、碳酸氢钾分别在13 min和14 min内分解完毕,增大升温速率可使其分解时间进一步缩短,由此制备的CO2标准气体体积分数范围分别为0.95%~1.08%和0.95%~1.06%,在误差范围内满足标气要求。
2)封闭环境下大的体积分数的CO2会在很大程度上降低碳酸氢钠和碳酸氢钾的分解速率。
3)通过对载气量、加热温度和加热时间的精确控制以减小实验误差,利用热分解定量碳酸盐获得定量CO2并与载气混合动态制备CO2标气的方案是可行的。
此外CO2分析仪表便携式标校装置的设计思路还适用于其它气体分析仪器的标校,如可热解析吸附了一定量苯系物的吸附材料制备苯系物分析仪器的标校用标准气体;通过热分解盐或者电解水等方式定量制备标校用H2标准气体;通过盐热分解生成CO制备标校用CO标准气体,等等,这些可以集成在一起制作成便携式多用途气体分析仪标校装置,这将为仪器仪表标校提供更大的便利。密闭空间中的复杂环境对于该装置进行仪表标校是否存在影响还有待于进一步研究,在装置自动化设计方面还有提升的空间。
[1] 埃克霍夫S J,伍德R A.包括二氧化碳校准气体发生器的二氧化碳传感器[P].中国专利:200680027039.6,2008,7.23.
[2] 董建峰.碳酸盐热稳定性初探[J].陕西广播电视大学学报,1999(3):87-89.
[3] 实用化学手册编写组.实用化学手册[M].北京:科学出版社,2001.
[4] 顾庆超,楼书聪,戴庆平,等.化学用表[M].南京:江苏科学技术出版社,1979.

