双孔道管状有序介孔炭对维生素B12的吸附缓释性能
王小蓉 郝广平 陆安慧 李文翠
(精细化工国家重点实验室,大连理工大学化工学院,辽宁大连116023)
双孔道管状有序介孔炭对维生素B12的吸附缓释性能
王小蓉 郝广平 陆安慧 李文翠*
(精细化工国家重点实验室,大连理工大学化工学院,辽宁大连116023)
通过纳米铸型法,以硅基介孔分子筛SBA-15为模板,糠醇为碳源,草酸作为聚合催化剂合成了具有双孔道管状有序介孔炭CMK-5.利用粉末X射线衍射(XRD)、扫描电子显微镜(SEM)和氮气物理吸附法等对其结构进行了表征.结果表明合成的CMK-5具有有序结构,比表面积和孔容积分别高达1856 m2·g-1和2.10 cm3· g-1,在3.1和5.5 nm具有集中的双孔分布.由于独特的双孔道结构特点,CMK-5在120 min内快速吸附维生素B12至平衡,吸附量高达943 mg·g-1,远高于商用活性炭.CMK-5吸附维生素B12后可以直接用于缓释,动态缓释浓度维持在~9 mg·L-1,适用于维生素B12分子在人体内的缓释.
有序介孔炭;双孔道;维生素B12;吸附;药物缓释
1 引言
维生素B12(VB12)作为参与体内多种代谢的水溶性维生素,其针剂药物需要频繁给药,给患者造成不便.药物缓释剂能在较长时间内维持体内有效浓度,可大大提高药效.因此药物缓释材料是目前热门的研究课题之一.1-4自2001年Vallet-Regi等5首次使用介孔硅MCM-41作为药物载体,介孔材料在控制药物缓释载体方面的应用引起广泛的关注.介孔炭材料由于具有高比表面积、尺寸可调、形貌可控、表面易官能化、无生理毒性等优点被认为是极具潜力的药物缓释载体.但一些介孔材料对药物分子的吸附效率低,6-9药物缓释速率快,10-12不能满足人体的需求.如Zhai等13对介孔炭CMK-3进行表面改性再注入热响应聚合物来作为布洛芬的缓释载体,它对布洛芬的负载量仅为25%,因此需要选择合适的载体来提高载药量.以硅基介孔分子筛SBA-15为模板,通过纳米铸型法合成的介孔炭CMK-5由于具有高比表面积,有序的双孔道结构和化学稳定性而被广泛应用于催化、氢存储、分离提纯和吸附大分子等领域,14-17但在药物缓释载体方面还未见报道.鉴于这种纳米铸型法合成的炭含有丰富的中孔,且中孔尺寸主要集中在3-6 nm,因此其特别适合于大分子的吸附富集.本文以大分子药物VB12(分子尺寸为1.84 nm×1.41 nm×1.14 nm)18为例,研究了CMK-5对VB12的吸附及缓释能力.
2 实验部分
2.1 实验试剂
糠醇购自上海金山亭新化学试剂厂,为化学纯;草酸购自华北地区特种化学试剂开发中心,为分析纯;1,3,5-三甲苯、碳酸氢钠、磷酸氢二钾、氯化镁、氯化钙、硫酸钠、三羟甲基氨基硅烷、VB12均购自国药集团化学试剂有限公司,其中VB12为生物纯,其它均为分析纯;氢氧化钠、氯化钠、氯化钾均购自天津市科密欧化学试剂有限公司,为分析纯;浓盐酸、乙醇购自天津市富宇精细化工有限公司,为分析纯.
2.2 CMK-5的合成
硅基介孔分子筛SBA-15参照文献19合成. CMK-5是以SBA-15为模板,糠醇为碳源,草酸作为聚合催化剂合成.具体的合成过程13如下:分别量取4 mL糠醇,4 mL 1,3,5-三甲苯于10 mL玻璃瓶中,加入40 mg草酸作为聚合催化剂,溶解摇匀.称取0.5 g SBA-15模板放到10 mL玻璃瓶中,加入上面配置好的聚合物溶液900 μL,等体积浸渍.密封后50°C老化24 h,再90°C老化24 h.将干燥后的聚合物在氮气气氛下于850°C热解4 h.用质量分数为7%的氢氧化钠-乙醇水溶液去除氧化硅模板,取出后过滤得到CMK-5,水洗至pH=7,再用乙醇洗涤3次并于50°C干燥后得到CMK-5有序介孔炭产品.
2.3 样品表征
粉末X射线衍射(XRD)在德国STADI P衍射仪上测定,扫描范围0.85°-2°,扫描速率0.02(°)· min-1;使用美国Micromeritics公司的ASAP 2020型全自动氮吸附比表面积测试仪在-196°C下测试氮气吸附-脱附曲线,比表面积采用Brunauer-Emmett-Teller(BET)法计算,孔径分布采用Barret-Joyner-Halenda(BJH)法计算;用日本Hitachi S-5500电子扫描显微镜(SEM)观察介孔材料的形貌;透射电子显微镜(TEM)为日本Hitachi HF 7500高分辨透射电子显微镜,加速电压为200 kV;VB12溶液的浓度测定采用上海天美科学仪器有限公司UV2300型紫外可见分光光度计.
2.4 维生素B12的吸附
配制质量浓度为500 mg·L-1的VB12溶液.将25 mg CMK-5加入到50 mL的VB12溶液中,恒温25°C磁力搅拌,转速为400 r·min-1.用紫外可见分光光度计在λmax=361 nm处测吸附后VB12溶液的浓度.按下式计算吸附量:qt=V×(C0-Ct)/m,qe=V× (C0
-Ce)/m.其中,qt为t时刻VB12的吸附量,qe为平衡吸附量,V为溶液体积,C0为溶液起始浓度,Ct为t时刻溶液浓度,Ce为平衡浓度,m为吸附剂的质量.
2.5 维生素B12的缓释
首先将VB12负载在CMK-5上:将250 mg CMK-5加入到500 mL质量浓度为500 mg·L-1的VB12溶液中,吸附温度为25°C,400 r·min-1磁力搅拌24 h.我们研究了两种缓释条件:在固定体积溶液中的静态缓释和在流动相液体中的动态缓释.静态缓释过程如下:将吸附后的溶液过滤,干燥后得到CMK-5/VB12样品,放入500 mL的类人体液中,室温磁力搅拌24 h,为第一轮缓释.第二轮缓释是将第一次缓释后的样品过滤干燥,再放入500 mL新鲜的类人体液中,室温磁力搅拌24 h.依次做第三轮.动态缓释采用带有过滤膜的玻璃管,将第三轮静态缓释后的样品担载在膜上,新鲜的类人体液以一定的速度流经样品,缓释的溶液再慢慢地渗透从玻璃管下方流出,定时取样进行测量,共缓释6 d.类人体液按文献20配制.
3 结果与讨论
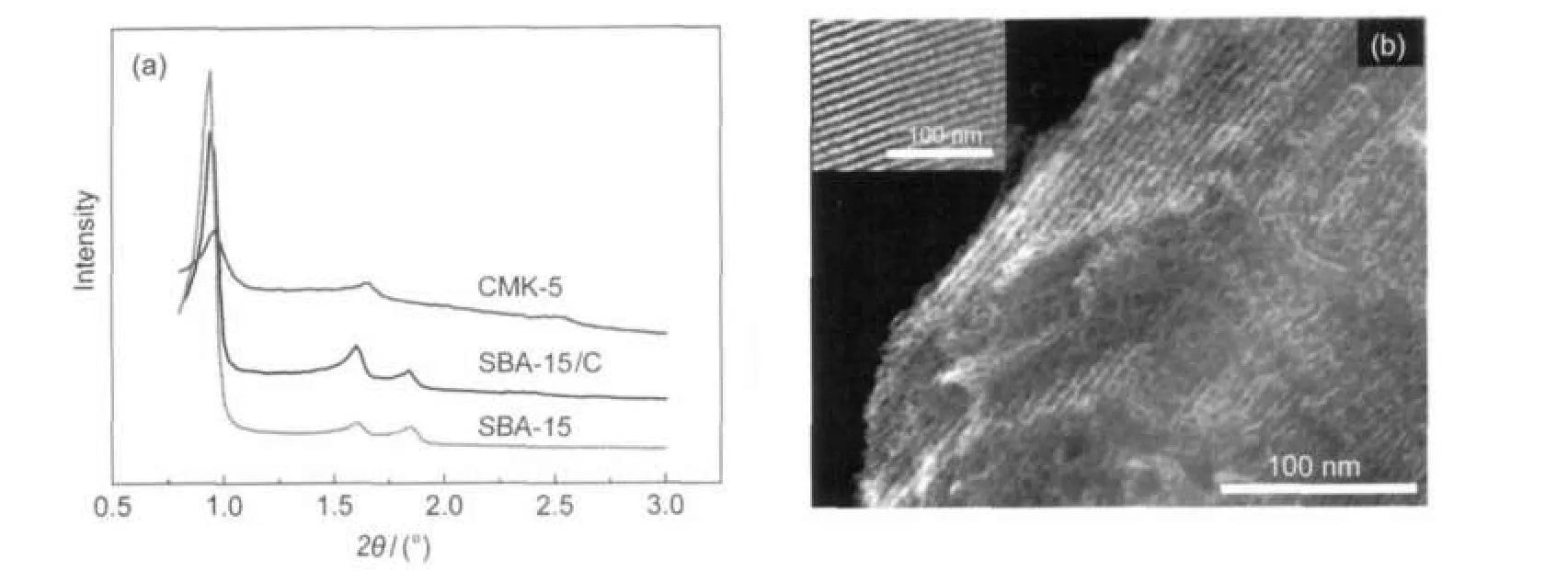
图1 (a)SBA-15,SBA-15/C,CMK-5的小角XRD图;(b)CMK-5的扫描电镜图Fig.1 (a)XRD patterns of SBA-15,SBA-15/C,and CMK-5;(b)SEM image of CMK-5Inset in Fig.1(b)is the TEM image of SBA-15.
3.1 介孔炭CMK-5的结构表征
图1(a)为模板SBA-15,炭硅复合物(SBA-15/C)及产品CMK-5的小角XRD衍射图.从图中可以看出,SBA-15/C及CMK-5在2θ=0.80°-1.80°区间内均出现三个明显的衍射峰,分别对应(100)、(110)、(200)晶面,这是六方相介孔结构的典型特征衍射峰.21说明CMK-5很好地复制了SBA-15的结构.13
图1(b)为CMK-5平行于孔道方向观察到的扫描电镜图,从图中可以看出CMK-5具有两种孔道.其六方有序的环状结构平行于CMK-5的孔道方向,孔道结构规整.对照图1(b)中插入部分的SBA-15透射电镜图,可以发现CMK-5很好地复制了SBA-15规整的二维六方孔道结构.
进一步采用物理吸附法测试了样品的吸脱附曲线.从图2(a)中可以看出SBA-15,SBA-15/C和CMK-5的氮气吸附等温线都是IV型,为典型的介孔材料的吸附特征.从图2(b)中可以看出CMK-5为双孔分布,分别为脱除模板孔壁后产生的3.1 nm的孔道和未填满SBA-15产生的5.5 nm的孔道.样品的织构参数列于表1中,脱除模板后,CMK-5的比表面积及孔容高达1856 m2·g-1和2.10 cm3·g-1.
3.2 CMK-5吸附VB12性能
图3中显示了CMK-5对VB12的吸附量随时间的变化曲线.由图3可见,在刚开始的30 min内,吸附量快速增加,VB12负载量达到平衡负载量的89.10%.在120 min CMK-5对VB12达到吸附饱和,平衡吸附量为943 mg·g-1,远高于文献22-24报道的其它规则的介孔炭.CMK-5具有高比表面积,大孔容及双孔道有序结构,有利于VB12分子的运载和传输.为了进行对比,本文选取规则的介孔炭CMK-3及不规则的介孔椰壳活性炭(AC)来吸附VB12.前期的研究结果证明CMK-3和CMK-5是分别由体相填充和表面涂层SAB-15孔道而复制的介孔炭.25-28CMK-3的介孔孔道结构与CMK-5双孔体系中的一种孔道结构相似,即脱除模板后产生的孔隙.因此通过对比这两种炭吸附VB12的结果可以反应出双孔道结构与材料性能之间的构效关系.表1列出了这两种材料的织构参数及对VB12的平衡吸附量,其吸附曲线见图3.
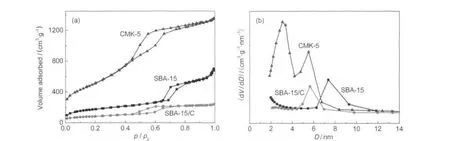
图2 SBA-15,SBA-15/C,CMK-5的氮气吸附-脱附曲线(a)和BJH孔径分布(b)Fig.2 N2adsorption-desorption isotherms(a)and BJH pore size distributions(b)of SBA-15,SBA-15/C,and CMK-5

表1 样品的织构参数和平衡吸附量Table 1 Textural parameters of the samples and equilibrium adsorption capacities
由图3可见,CMK-3对VB12的平衡吸附量为471 mg·g-1,在4 h后基本达到吸附平衡.AC对VB12的平衡吸附量仅为200 mg·g-1.CMK-3和AC的吸附速率较CMK-5要慢,一方面是因为CMK-5具有大孔容及高比表面积,对VB12的吸附容量大;另一方面是CMK-5具有双孔道结构,5.5 nm的大孔道有利于VB12快速扩散到内部.因此,它达到吸附平衡的时间短.而CMK-3虽然都为介孔,但孔径稍大于VB12分子,分子扩散运动进入内部需要一定的时间,因此吸附速率较CMK-5要慢.AC具有不规则的大孔、介孔和微孔.VB12经过AC表面的大孔快速进入内部,但是AC的介孔小且不规则,分子很难进入孔道内部或在孔道内部的扩散运动受阻碍,因此AC对VB12的吸附速率及吸附量都很低.这些都说明CMK-5的双孔道规则结构有利于维生素B12的吸附.
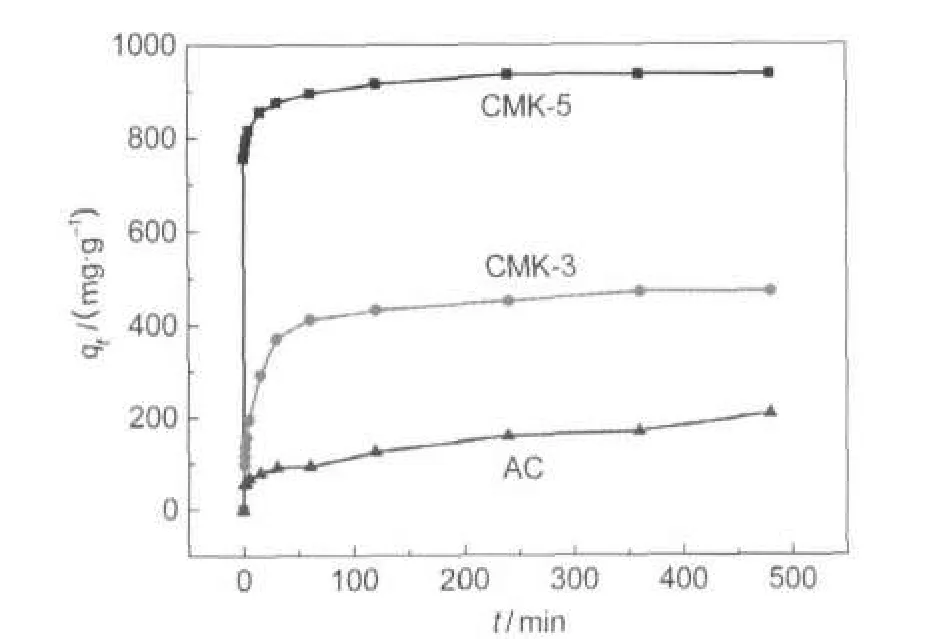
图3 CMK-5,CMK-3,AC对VB12的吸附量随时间变化曲线Fig.3 Time-resolved adsorption capacity of VB12 on CMK-5,CMK-3,andAC
3.3 CMK-5/VB12在类人体液中的缓释性能
与CMK-3及AC相比,CMK-5对大分子药物VB12的吸附效果最好.因此我们选取CMK-5作为VB12的载体,研究其负载VB12后在类人体液中的缓释性能.
图4(a)是三轮静态缓释的浓度随时间的变化曲线,第一轮缓释的速率很快,浓度在2 h就基本达到平衡,为28 mg·L-1.后两轮的缓释浓度要低于第一轮,这可能是因为CMK-5对VB12的吸附量大.由于浓度差,在CMK-5表面及5.5 nm大孔道里的药物分子快速脱附下来扩散至溶液中.随时间的延长,溶液与CMK-5表面浓度达到平衡.比较三轮静态缓释,浓度及速率随次数的增加依次降低,这可能是由于表面的药物分子脱附后,孔道内壁的药物分子先脱附下来至孔道中,然后再由孔道慢慢扩散至材料表面,最后扩散至溶液当中.
图4(b)是CMK-5/VB12样品动态缓释浓度随时间的变化曲线,研究发现,溶液的浓度维持在9 mg· L-1左右(该浓度是每天多次取样测量的平均值),这表明经过前三轮的静态缓释,CMK-5表面的VB12已经全部释放出来.动态缓释的VB12是来自于孔道内部及孔壁上的.经过6天的缓释,其浓度维持不变,表明孔道内部及孔壁上吸附的VB12是以相同的速率扩散至溶液中.CMK-5介孔材料作为VB12的高载药量载体,在动态缓释过程中能一直源源不断地缓释,并且其吸附VB12后就能直接用于缓释,不需要做其他处理如热响应或pH响应.29,30上述研究结果表明CMK-5介孔材料在流动液中对VB12具有显著的缓释行为,并且能够保持流动液中VB12的浓度基本恒定.人体内的液体是流动的,并且对VB12是一个消耗的过程.试想,如果将其用于人体药物缓释,这将是一个边消耗边缓释补充和维持VB12浓度稳定的过程.基于能够在流动相中长时间维持药物的浓度恒定这一显著特点,CMK-5的性能要优于其它快速释放药物的缓释剂.31,32当然,需要指出的是由于这类介孔炭材料的生物相容性及毒性研究尚不明确,因此能否将其作为药物的缓释载体进行实际应用,还需要开展后续的研究.我们希望本文的研究工作能为未来如何设计高效的药物吸附和缓释材料提供一点参考.
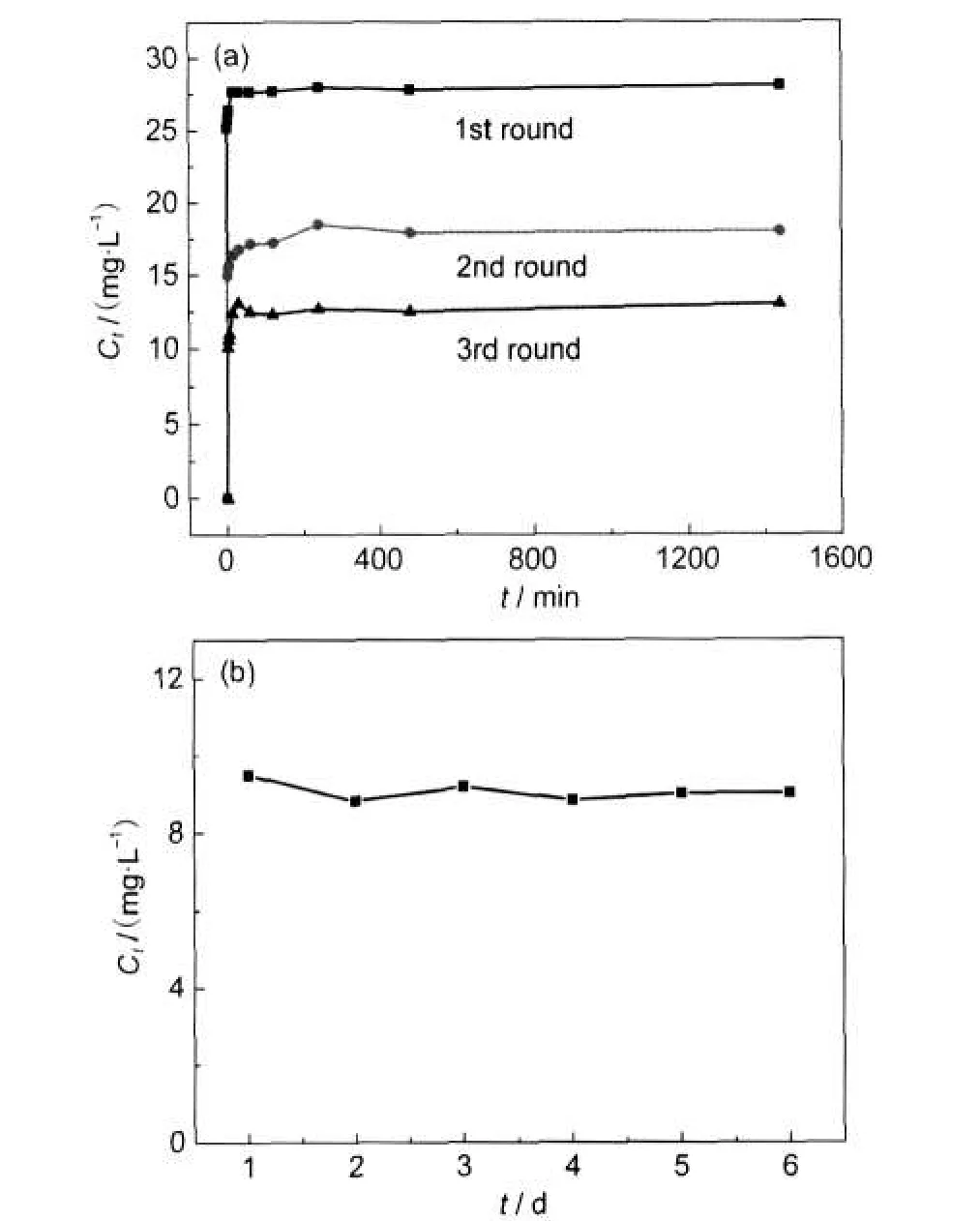
图4 CMK-5/VB12静态缓释浓度(a)和动态缓释浓度(b)随时间变化曲线Fig.4 Cumulative release of VB12 under static condition(a)and dynamic condition(b)
4 结论
以硅基介孔分子筛SBA-15为模板,糠醇为碳源,草酸为聚合催化剂合成的CMK-5具有双孔道管状有序介孔结构,大孔容及高比表面积.CMK-5对大分子药物VB12的吸附量高达943 mg·g-1,是一种非常好的高载药量载体.其吸附VB12后能直接用于缓释并且具有很好的可控性能,动态缓释能维持在一定的浓度,适合用于人体内VB12分子的定量释放.
(1) Hartmann,M.Chem.Mater.2005,17,4577.
(2)Wang,S.B.Microporous Mesoporous Mat.2009,117,1.
(3) Uhrich,K.E.;Cannizzaro,S.M.;Langer,R.S.;Shakesheff,K. M.Chem.Rev.1999,99,3181.
(4) He,Q.J.;Shi,J.L.J.Mater.Chem.2011,21,5845.
(5) Vallet-Regi,M.;Rámila,A.;Real,R.P.;Pérez-Pariente,J. Chem.Mater.2003,15,500.
(6)Yang,J.B.;Ling,L.C.;Liu,L.;Kang,F.Y.;Huang,Z.H.;Wu, H.Carbon 2002,40,911.
(7) Lu,Y.M.;Gong,Q.M.;Liang,J.Acta Phys.-Chim.Sin.2009, 25(8),1697.[卢月美,巩前明,梁 吉.物理化学学报,2009, 25(8),1697.]
(8) Yang,J.B.;Kang,F.Y;Huang,Z.H.J.Tsinghua.Univ.(Sci. Tech.)2002,16(5),688.[杨俊兵,康飞宇,黄正宏.清华大学学报(自然科学版),2002,16(5),688.]
(9) Sheng,W.Z.;Zheng,J.T.J.Mater.Sci.2004,39,4693.
(10)Yang,Q.;Wang,S.C.;Fan,P.W.;Wang,L.F.;Di,Y.;Lin,K. F.;Xiao,F.S.Chem.Mater.2005,17,5999.
(11) Doadrio,A.L.;Sousa,E.M.B.;Doadrio,J.C.;Pariente,J.P.; Izquierdo-Barba,I.;Vallet-Regí,M.J.Control.Release 2004, 97,125.
(12) Arcos,D.;López-Noriega,A.;Ruiz-Hernάndez,E.;Terasaki, O.;Vallet-Regí,M.Chem.Mater.2009,21,1000.
(13)Yu,H.;Zhai,Q.Z.Microporous Mesoporous Mat.2009,123, 298.
(14) Lu,A.H.;Nitz,J.J.;Comotti,M.;Weidenthaler,C.;Schlichte, K.;Lehmann,C.W.;Terasaki,O.;Schüth,F.J.Am.Chem.Soc. 2010,132,14152.
(15)Peng,X.;Cao,D.P.;Wang,W.C.Langmuir 2009,25(18), 10863.
(16) Korάnyi,T.I.;Vít,Z.K.;Nagy,J.B.Catal.Today 2008,130,80. (17)Hao,G.P.;Li,W.C.;Wang,S.;Zhang,S.F.;Lu,A.H.Carbon 2010,48,3330.
(18) He,J.L.Preparation of Porous Carbons and Its Performance on Adsorption.Master Dissertation,Hunan University,Changsha, 2006.[何姣莲.中孔炭的制备及其吸附性能研究[D].长沙:湖南大学,2006.]
(19)Lu,A.H.;Li,W.C.;Schmidt,W.;Kiefer,W.;Schüth,F.Carbon 2004,42,2939.
(20)Oyane,A.;Kim,H.M.;Furuya,T.;Kokubo,T.;Miyazaki,T. J.Biomed.Mater.Res.A 2003,65A(2),188.
(21) Lu,A.H.;Schmidt,W.;Spliethoff,B.;Schüth,F.Adv.Mater. 2003,15,1602.
(22) Zhuo,G.;Zhu,G.S.;Gao,B.;Zhang,D.L.;Tian,G.;Chen,Y.; Zhang,W.W.;Qiu,S.L.Carbon 2005,43,2344.
(23)Zhuo,G.;Wang,L.F.;Gao,Z.;Zhang,W.W.Chin.Chem.Lett. 2007,18,233.
(24)Liu,C.Y.;Wang,S.Y.;Rong,Z.H.;Wang,X.Q.;Gu,G.N.; Sun,W.J.J.Non-Cryst.Solids 2010,356,1246.
(25) Joo,S.H.;Choi,S.J.;Oh,I.;Kwak,J.;Liu,Z.;Terasaki,O.; Ryoo,R.Nature 2001,412,169.
(26) Ryoo,R.;Joo,S.H.;Kruk,M.;Jaroniec,M.Adv.Mater.2001, 13,677.
(27) Lu,A.H.;Schüth,F.Adv.Mater.2006,18,1793.
(28)Lund,K.;Muroyama,N.;Terasaki,O.Microporous Mesoporous Mat.2010,128,71.
(29) Luo,B.;Song,X.J.;Zhang,F.;Xia,A.;Yang,W.Y.;Hu,J.H.; Wang,C.C.Langmuir 2010,26,1674.
(30) Shome,A.;Debnath,S.;Das,P.K.Langmuir 2008,24,4280.
(31) Song,F.;Zhang,L.M.;Shi,J.F.;Li,N.N.Colloids.Surf.B: Biointerfaces 2010,79,142.
(32)Wen,X.;Cao,X.L.;Yin,Z.H.;Wang,T.;Zhao,C.S. Carbohydr.Polym.2009,78(5),193.
April 18,2011;Revised:June 14,2011;Published on Web:June 27,2011.
Adsorption and Release Behavior of Vitamin B12 in Tubular Structured Ordered Mesoporous Carbon
WANG Xiao-Rong HAO Guang-Ping LU An-Hui LI Wen-Cui*
(State Key Laboratory of Fine Chemicals,School of Chemical Engineering,Dalian University of Technology, Dalian 116023,Liaoning Province,P.R.China)
Ordered mesoporous carbon with hexagonal arrays consisting of tubular-type pores(CMK-5) was synthesized via a nanocasting process by the direct use of SBA-15 as a template,furfuryl alcohol as a carbon source and oxalic acid as the catalyst.The structure of CMK-5 was analyzed by different techniques including scanning electron microscopy,powder X-ray diffraction and N2adsorption analysis. The specific surface area and pore volume were found to be 1856 m2·g-1and 2.10 cm3·g-1,respectively, with mesopore sizes concentrated at 3.1 and 5.5 nm.Because of the unique structure the adsorption capacities of CMK-5 towards vitamin B12 was found to be as high as 943 mg·g-1in a short period of 120 min,which is significantly higher than that of commercial activated carbon.The composites of CMK-5 and vitamin B12 without any treatment gave slow-release performance in a simulated body fluid.The concentration of the release solutions remained 9 mg·L-1under dynamic conditions.A high loading capacity and slow release rate of vitamin B12 on the CMK-5 support suggested that CMK-5 might have a potential application in drug delivery.
Ordered mesoporous carbon;Dual-model pore channel;Vitamin B12;Adsorption; Drug release
∗Corresponding author.Email:wencuili@dlut.edu.cn;Tel/Fax:+86-411-84986122.
The project was supported by the Specialized Research Fund for the Doctoral Program of Higher Education of China(20100041110017).
高等学校博士学科点专项科研基金(20100041110017)资助项目
O647

