新型含氟聚醚链修饰的咪唑离子液体的合成及其热稳定性
温志勇, 黄焰根
(东华大学 化学化工与生物工程学院,上海 201620)
与传统有机溶剂和电解质相比,离子液体作为新型绿色溶剂具有一系列突出的优点[1~3],已成为当今化学的学科前沿和研究热点,并在精细有机合成、催化、电化学、材料科学、生物工程以及能源等领域得到了广泛地应用[4,5]。
近年来化学家尝试将全氟烷基链引入离子液体中以期获得独特的性能。全氟烷基链的引入可以改变离子液体原有的熔点、密度、黏度、表面张力、耐水性、耐温性、液体范围的宽度、电导性等[6]。全氟烷基链可以选择性地引入到离子液体的阴离子或阳离子中,这些离子液体作为表面活性剂或相转移催化剂显示了优异的性能[7~9]。但全氟烷基链本身难降解,具有生物累积性,从而限制了其实际应用。
全氟聚醚(PFPE)和氢氟聚醚(HFPE)因其较低的温室效应、低的臭氧层破坏能力而在工业上得到广泛应用[10]。PFPE分子主链中C-O共价键的存在,使得PFPE在保持较高热稳定性的同时又具备易降解的特点。分子量较大的PFPE还具有低挥发性、较宽的液体温度范围及优异的黏度—温度特性。基于PFPE的这些特点,我们设想将低分子量的PFPE链引入离子液体中以降低离子液体的熔点和黏度,提高其表面活性。
本文以N-[1,1-二氢-2,5-二(三氟甲基)-3,6-二氧杂-全氟壬基]咪唑(1)与碘代烷烃(2a~2d)经季铵化反应高产率地制备了4个新型的1-烷基-3-[1,1-二氢-2,5-二(三氟甲基)-3,6-二氧杂-全氟壬基]咪唑碘盐(3a~3d);通过3的复分解反应合成了4个新型的1-烷基-3-[1,1-二氢-2,5-二(三氟甲基)-3,6-二氧杂-全氟壬基]咪唑六氟磷酸盐(4a~4d)离子液体和4个新型的1-烷基-3-[1,1-二氢-2,5-二(三氟甲基)-3,6-二氧杂-全氟壬基]咪唑四氟硼酸盐离子液体(5a~5d, Scheme 1),其结构经1H NMR,19F NMR, IR和元素分析确证。用热重分析研究了4和5的热稳定性。


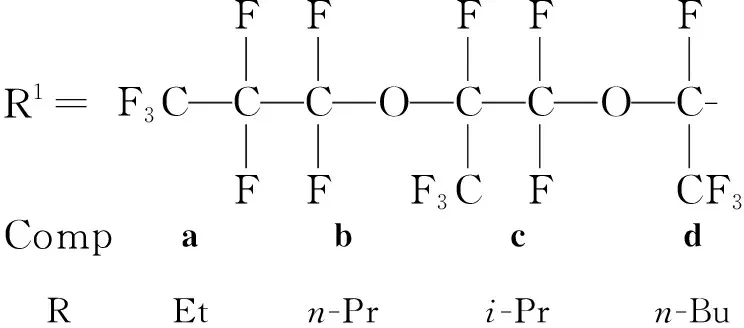
R1=F3CCFFCFFOCCF3FCFFOCCF3F-CompabcdREtn-Pri-Prn-Bu
Scheme1
1 实验部分
1.1 仪器与试剂
Bruker AV 400(400 MHz)型核磁共振仪(氘代丙酮为溶剂,TMS为内标);Bruker AV 400(376.5 MHz)型核磁共振仪(氘代丙酮为溶剂,FCCl3为外标,高场为负);Nicolet 380 FT-IR型傅立叶变换红外光谱仪(KBr压片);Germany NETZSCH TG 209 F1型热重分析仪;Italian Carlo-Erba 1106型和Perkin-Elmer 2400 CHN型元素分析仪。
1参考文献[11,12]方法合成;其余所用试剂均为分析纯。
1.2 合成
(1) 3的合成通法
在反应瓶中加入1 3.75 mmol, 2 5.63 mmol和乙腈20 mL,搅拌使其溶解;于80 ℃反应20 h~48 h。冷却至室温,减压蒸除溶剂和过量的2,残留物用乙醚(3×10 mL)洗涤得3a~3d。
(2) 4和5的合成通法
在反应瓶中加入3 3 mmol, KPF6或NaBF44.5 mmol及混合溶剂[V(丙酮) ∶V(水)=3 ∶1]20 mL,搅拌下于室温反应5 h。旋干丙酮,粗品分别用水(3×10 mL)和乙醚(3×10 mL)洗涤得4和5。3~5的实验结果和元素分析数据分别见表1和表2; NMR和IR数据见表3。
2 结果与讨论
2.1 合成
(1) 3的合成
以乙腈为溶剂,1与不同的烷基碘化物发生季铵化反应制备3。从实验结果(表1)可以发现,1与不同烷基碘化物反应的时间和产率都呈现一定的规律性:(1)烷基链越长,反应所需的时间越长,反应产率也越低;(2)与伯烷基碘化物相比,仲烷基碘化物(2c)与1的反应时间最长,需要48 h才能反应完全,且产率也较低(71.5%)。
室温下3在乙醚中的溶解性较差,我们试图用乙醚多次洗涤粗产物来实现产物的分离纯化,但是1H NMR检测发现,图谱中除了3的信号峰以外,还有很多的杂质峰,说明乙醚的洗涤难以除净粗产物中的杂质。根据相似相容原理,通过多次尝试,最终得到了纯化3的方法:将乙醚(30 mL)加入粗品3a(2 g)中,搅拌下滴加甲醇至粗产物刚好全部溶解;滴加乙醚,离子液体析出,继续滴加直至离子液体层不再增加即可;分层,将离子液体层重复此分离方法2~3次即可得到深黄色的油状液体,久置后变为蜡状固体。1H NMR和元素分析检测纯度很高。3a的1H NMR分析显示咪唑环上三个质子的特征峰分别出现在8.05, 8.11和9.91处。
(2) 4和5的合成
为了提高咪唑盐离子液体的性能,通常需要对成盐的阴阳离子进行调控。本文选取了KPF6和NaBF4作为交换对象,合成了相应的含氟聚醚链修饰的咪唑六氟磷酸盐4a~4d和四氟硼酸盐5a~5d。在合成4和5过程中,最初选择丙酮作溶剂,4a~4d的产率较高(79.5%~83%),但5a~5d的产率却很低,可能是由于NaBF4在丙酮中的溶解性较差,导致产率较低。经过工艺考察,最终用V(丙酮) ∶V(水)=3 ∶1作为溶剂,获得了不错的效果,产率在80%以上。

表1 3的实验结果和元素分析数据Table 1 Experimental results and elemental analysis data of 3
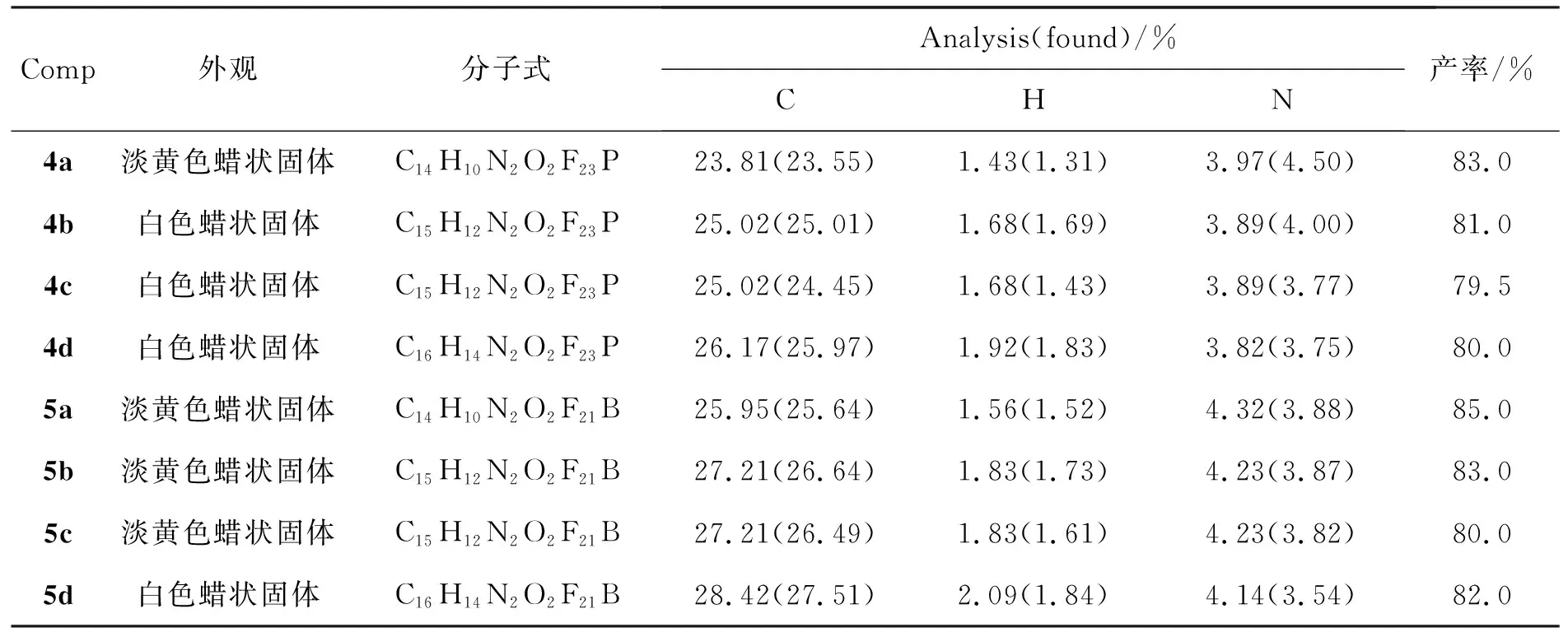
表2 4和5的实验结果和元素分析数据Table 2 Experimental results and elemental analysis data of 4 and 5

表3 3~5的NMR和IR数据Table 3 NMR and IR data of 3~5
续表3

Comp1H NMR δ19F NMR δIR ν/cm-14a1.61(t, 3H), 4.57(q, 2H), 5.65(m, 2H), 8.01(d, 1H), 8.06(t, 1H), 9.47(s, 1H)-71.7(s, 6F), -80.4(m, 2F), -80.5(m, 3F), -82.0(m, 2F), -82.1(m, 3F), -82.4(d, 3F), -130.1(s, 2F), -135.4(m, 1F), -145.0(m, 1F)447, 837, 1 240, 1 621, 3 438, 3 6954b0.97(t, 3H), 2.00(m, 2H), 4.47(t, 2H), 5.63(d, 2H), 7.99(d, 2H), 9.46(s, 1H)-71.6(s, 6F), -80.5(m, 2F), -80.6(m, 3F), -82.1(m, 2F), -82.2(m, 3F), -82.4(d, 3F), -130.2(s, 2F), -135.4(m, 1F), -145.0(m, 1F)449, 842, 991, 1 242, 1 569, 3 439, 3 6954c1.67(d, 6H), 4.99(m, 1H), 5.57(m, 2H), 7.98(s, 1H), 8.10(s, 1H), 9.44(s, 1H)-71.6(s, 6F), -80.4(m, 2F), -80.6(m, 3F), -82.1(m, 2F), -82.2(m, 3F), -82.4(d, 3F), -130.2(s, 2F), -135.3(m, 1F), -144.9(m, 1F) 447, 1 628, 3 439, 3 6954d0.96(t, 3H), 1.43(m, 2H), 2.01(m, 2H), 4.55(t, 2H), 5.87(m, 2H), 8.06(d, 1H), 8.15(s, 1H), 9.62(s, 1H)-71.6(s, 6F), -80.4(m, 2F), -80.6(m, 3F), -82.1(m, 2F), -82.2(m, 3F), -82.4(d, 3F), -130.2(s, 2F), -135.3(m, 1F), -144.9(m, 1F)447, 834, 1 166, 1 593, 2 970, 3 176, 3 443, 3 6955a1.60(t, 3H), 4.54(q, 2H), 5.63(d, 2H), 7.96(s, 1H), 8.03(s, 1H), 9.47(s, 1H)-80.5(m, 2F), -80.6(m, 3F), -82.1(m, 2F), -82.3(m, 3F), -82.6(d, 3F), -130.2(s, 2F), -135.2(m, 1F), -144.9(m, 1F), -151.2(s, 4F).448, 1 121, 1 629, 3 439, 3 6965b0.94(t, 3H), 1.97(m, 2H), 4.44(t, 2H), 5.59(d, 2H), 7.94(s, 1H), 7.98(d, 1H), 9.38(s, 1H)-80.4(m, 2F), -80.6(m, 3F), -82.2(m, 2F), -82.4(m, 3F), -82.6(d, 3F), -130.2(s, 2F), -135.3(m, 1F), -145.0(m, 1F), -151.1(s, 4F) 454, 1 621, 3 433, 3 6935c1.63(d, 6H), 4.96(m, 1H), 5.54^5.57(m, 2H), 7.96(m, 1H), 8.08(s, 1H), 9.46(s, 1H)-80.4(m, 2F), -80.6(m, 3F), -82.2(m, 2F), -82.4(m, 3F), -82.7(d, 3F), -130.2(s, 2F), -135.3(m, 1F), -145.1(m, 1F), -151.1(s, 4F)448, 1 628, 3 439, 3 6955d0.92(t, 3H), 1.34^1.39(m, 2H), 1.94(m, 2H), 4.48(t, 2H), 5.58(s, 1H), 5.63(s, 1H), 7.95(d, 1H), 8.00(s, 1H), 9.44(s, 1H)-80.5(m, 2F), -80.6(m, 3F), -82.2(m, 2F), -82.4(m, 3F), -82.6(d, 3F), -130.2(s, 2F), -135.3(m, 1F), -145.2(m, 1F), -151.0(s, 4F)1 102, 1 628, 2 967, 3 440, 3 694

2.2 3~5的热稳定性
3~5的TGA曲线见图1。从图1可见,低于180 ℃,3a~3d均没有出现明显的重量损失,证明其在该范围内具有耐热稳定性,起始热分解温度依次为199 ℃, 185 ℃, 218 ℃和198.9 ℃;同时可以看到3a~3d的分解是分步进行的。经过对3a~3d结构和TGA曲线分析可以推断,首先分解的是PFPE链,500 ℃高温时的残炭量依次为5.87%, 10.29%, 7.91%和7.07%。
从图1也可以看出,4a~4d比3a~3d的热稳定性要高,在220 ℃前,4a~4d均没有出现明显的重量损失,其起始热分解温度依次为223 ℃, 220 ℃, 243 ℃和232 ℃。与3a~3d的分解过程相似,热分解也是分步进行的,500 ℃高温时的残炭量依次为15.77%, 14.65%, 14.4%和16.07%。
从图1还可见,5a~5d的热分解情况与4a~4d非常相似,其起始热分解温度依次为200 ℃, 252 ℃, 245 ℃和226 ℃。500 ℃高温时的残炭量依次为13.85%, 11.1%, 7.12%和14%。 4a~4d和5a~5d的起始热分解温度和残炭量都比相应化合物3a~3d的要高,说明4a~4d和5a~5d比3a~3d具有更好的热稳定性。

图1 3~5的TGA曲线Figure 1 TGA curves of 3~5
3 结论
合成了一系列含氟聚醚链修饰的咪唑离子液体,热重分析表明这些离子液体具有较高的热稳定性。对这些含氟离子液体的表面性能和耐摩擦性能测试及潜在应用研究正在进行当中。
[1] Hagiwara R, Ito Y. Room temperature ionic liquids of alkylimidazolium cations and fluoroanions[J].J Fluorine Chem,2000,105(2):221-227.
[2] Liu W M, Ye C F, Chen Y X,etal. Tribological behavior of sialon ceramics sliding against steel lubricated by fluorine-containing oils[J].Tribology International,2002,35(8):503-509.
[3] Bermudez M D, Jimenez A E. Surface interactions and tribochemical processes in ionic liquid lubrication of aluminium-steel contacts[J].Int J Surf Sci Eng,2007,1(1):100-110.
[4] Welton T. Room-temperature ionic liquids.Solvents for synthesis and catalysis[J].Chem Rev,1999,99(8):2071-2084.
[5] Earle M J, Seddon K R. Ionic liquids,green solvents for the future[J].Pure Appl Chem,2000,72(7):1391-1398.
[6] Xue H, Shreeve J M. Ionic liquids with fluorine-containing cations[J].Eur J Inorg Chem,2005,(13):2573-2580.
[7] Merrigan T L, Bates E D, Dorman S C,etal. New fluorous ionic liquids function as surfactants in conventional room-temperature ionic liquids[J].Chem Commun(Cambridge),2000,(20):2051-2052.
[8] Broeke J, Winter F, Deelman B-J,etal. A highly fluorous room-temperature ionic liquid exhibiting fluorous biphasic behavior and its use in catalyst recycling[J].Org Lett,2002,4(22):3851-3854.
[9] Emnet C, Weber K M, Vidal J A,etal. Syntheses and properties of fluorous quaternary phosphonium salts that bear four ponytails; new candidates for phase transfer catalysts and ionic liquids[J].Adv Synth Catal,2006,348:1625-1634.
[10] Caporiccio G, Flabbi L, Marchionni G,etal. The properties and applications of perfluoropolyether lubricants[J].J Synth Lubric,1989,6(2):133-149.
[11] Lu H Y, Chen Q Y. The synthesis of acrylates of fluorinated alcohols[J].Acta Chimica Sinica,1985,43:970-975.
[12] Kysilka O, Rybackova M, Skalicky M,etal. HFPO trimer-based alkyl triflate,a novel building block for fluorous chemistry.Preparation,reactions and19F gCOSY analysis[J].Collect Czech Chem Comm,2008,73(12):1799-1813.

