SGLT2抑制剂治疗糖尿病研究进展
丁海峰,曹永兵,安毛毛,贾鑫明,姜远英
(第二军医大学药学院新药研究中心,上海 200433)
SGLT2抑制剂治疗糖尿病研究进展
丁海峰,曹永兵,安毛毛,贾鑫明,姜远英
(第二军医大学药学院新药研究中心,上海 200433)
近年来,钠-葡萄糖协同转运蛋白2(type 2 sodium glucose co-transporters,SGLT2)抑制剂作为一种新型的治疗糖尿病药物成为研究热点。SGLT2在肾近端小管葡萄糖重吸收中起着非常重要的作用;抑制肾脏SGLT2可以促进Ⅱ型糖尿病人尿糖的排泄,使其血糖恢复正常而不会有低血糖的风险。临床实验表明,SGLT2抑制剂对Ⅱ型糖尿病的治疗效果明显,且具有降低体重、无低血糖风险等优点,目前,许多SGLT2抑制剂已经进入临床评价后期。
Ⅱ型糖尿病;钠-葡萄糖协同转运蛋白;抑制剂
Ⅱ型糖尿病,又名非胰岛素依赖型糖尿病(non-insulin-dependent diabetes mellitus,NIDDM),主要表现为组织对胰岛素不敏感(胰岛素抵抗)和β细胞机能障碍从而导致高血糖。长期的高血糖可以导致微血管和大血管并发症(如心脏疾病、失明、肾病和中风等)。2010年,全球糖尿病患者已经超过2.85亿,其中中国地区患病人数为9 240万,居世界首位。治疗糖尿病主要通过摄入胰岛素或口服降糖药物使血糖维持在正常水平,目前治疗糖尿病药物的机制主要集中在胰岛素,促进胰岛素的释放,增加胰岛素的敏感性,控制肝糖释放或抑制小肠葡萄糖重吸收等方面。但是只有37%的病人能够将糖化血红蛋白(glycohemoglobin,HbA1c)水平控制在7%以下,并且有很多的与药物相关的不良反应,如体重增加、加重胰岛素抵抗、胰岛素分泌减少、低血糖、胃肠道不良反应及增加心肌梗塞的风险等,Ⅱ型糖尿病的治疗仍然是一个难题。和目前使用的抗糖尿病药物不同,钠-葡萄糖协同转运蛋白2(SGLT2)抑制剂通过抑制肾糖重吸收以促进尿糖排泄,使平衡朝着能量消耗的方向移动,从而降低体内血糖,且没有体重增加和低血糖风险,是一类治疗糖尿病的新型药物。
1 钠-葡萄糖协同转运蛋白(SGLT)的作用
肾脏在调节血糖水平中起着极其重要的作用,葡萄糖在肾小球滤过,并在肾近曲小管重吸收,90%的葡萄糖在近端小管的S1段重吸收,其余10%的葡萄糖在肾脏近端小管的直部重吸收[1]。SGLT蛋白属于SLC5A基因家族,SLC5A基因家族共有12个成员,负责肾葡萄糖的重吸收的SGLT蛋白主要有2种,他们均分布于转运上皮细胞,其中钠-葡萄糖协同转运蛋白1(type 1 sodium glucose co-transporters,SGLT1)是SLC5A1基因的产物,以钠-葡萄糖2:1的比率转运,存在于肠、脑、心肌、肝、肺和肾等部位,肠黏膜上的SGLT1负责将食物中的葡萄糖吸收进入血液,在肾近曲小管S3段SGLT1负责肾部分葡萄糖的转运。SGLT2是SLC5A2的产物,其59%基因序列和SGLT1相同,在肾近曲小管S1和S2段表达,以钠-葡萄糖1:1的比率转运,负责肾90%的葡萄糖重吸收,可以逆浓度转运葡萄糖穿过细胞膜[2~7]。所以,SGLT2的抑制剂可以通过阻断近曲小管对葡萄糖的重吸收降低血糖。
2 SGLT2抑制剂的作用机制
SGLT2抑制剂的作用机制是影响肾近曲小管S1段的钠糖转运蛋白,但目前对于SGLT2抑制剂的分子水平的作用机制仍知之甚少。Pajor等[8]认为,其抑制作用包括SGLT2抑制剂的葡萄糖基竞争性结合转运蛋白葡萄糖基的结合位点,以及糖苷元可能与SGLT疏水基或芳香残基相互作用;人SGLT2保守的半胱氨酸615残基使得抑制剂的结合位点的结构得以保持,并不直接与抑制剂结合。
3 目前研发的SGLT2抑制剂
3.1根皮苷phlorizin[9](结构式见图1) 根皮苷于1835年从苹果、苹果树皮及叶中提取而得,它是苹果树体内的酚类物质,是第一个SGLT抑制剂,根皮苷最早被用于降热研究,用以治疗疟疾,但是进一步的实验发现根皮苷具有促进尿糖排出的作用,随后根皮苷被用于糖尿病治疗的研究,根皮苷可以选择和竞争性抑制SGLT1和SGLT2,研究证明根皮苷可以通过增加肾中尿糖的排出,降低血糖,而不增加胰岛素的分泌,改善糖尿病动物模型的胰岛素抵抗。但是由于口服生物利用度比较低,除了抑制SGLT2还能抑制其它的载体,副作用比较大,所以没有被开发为治疗糖尿病的药物。但是它被用来作为研究SGLT2抑制剂的工具,多数SGLT2抑制剂具有和根皮苷类似的结构。
3.2T-1095和canagliflozin[10,11](结构式见图1) Tanabe Seiyaku和Johnson & Johnson公司根据phlorizin的化学结构,共同开发了第一个口服SGLT2抑制剂T-1095A,它是甲基碳酸酯前药T-1095的活性成分。T-1095口服后在小肠里很快就转化为活性体T-1095A,具有更好的生物利用度,在体外实验中,它对人的SGLT2抑制作用四倍于SGLT1(IC50分别为50 nM和200 nM),由于其选择性不高,其在Ⅱ期临床试验中被终止。随后,它们共同开发了另一SGLT2选择性抑制剂canagliflozin。其在SD大鼠中药代动力学参数见表1,单次给予正常雄性SD大鼠30 mg/kg的canagliflozin后,平均24 h尿糖排出量为3 696 mg/200 g体重。单次口服该药3 mg/kg可以持续抑制葡萄糖的重吸收,降低高脂诱导的KK小鼠血糖水平,6 h后降糖达48%,目前该药在日本处于Ⅰ期临床研究阶段,同时作为JNJ-28431754,在美国和欧洲进行Ⅲ期临床阶段。在2010年第70届美国糖尿病协会科学年会上Johnson & Johnson制药公布了canagliflozin的Ⅱ期临床数据,实验结果表明,该药能够改善使用二甲双胍治疗的Ⅱ型糖尿病人的血糖,控制并降低体重。Ⅲ期临床试验将评估超过10 000名的Ⅱ型糖尿病患者单独给予该药100、300 mg以及联合其它糖尿病药物(如胰岛素)治疗的安全性和药效,以及约4 500名无心血管疾病史的Ⅱ型糖尿病病人的心血管安全。
3.3sergliflozin和remogliflozin(结构式见图1) 2007年,Kissei制药公司研发了SGLT2选择性抑制剂sergliflozin,这是一种不同于根皮苷的苄基苯酚苷结构,其活性形式sergliflozin-A,对SGLT2具有较高的选择比(296:1),口服该药能够促进正常动物(小鼠、大鼠和犬)尿糖的排出,且对正常动物的电解质(钠、钾、氯)没有影响,不会引起电解质失衡。该药不会降低大鼠空腹血糖(fasting plasma glucose,FPG),引起低血糖的风险很低,其降血糖作用不依赖刺激胰岛素分泌。在链脲佐菌素(streptozocin,STZ)诱导的糖尿病大鼠口服糖耐量实验中,它能抑制口服葡萄糖后大鼠血糖水平的上升,降低给药后血糖-时间曲线下面积,降低胰岛素的分泌[12]。单剂量口服sergliflozin临床实验中,14名健康受试者口服该药5~500 mg,能够剂量依赖性的促进尿糖的排出;另一个8名Ⅱ型糖尿病受试者口服该药50~500 mg的实验显示,500 mg组能够使平均血糖由18.3 mmol/L降至11.2 mmol/L,对尿液电解质只有短暂且轻微的影响[13]。
remogliflozin(GSK189075)是由Kissei制药公司合成的另一SGLT2抑制剂。该抑制剂的结构不同于根皮苷,T-1095和sergliflozin,比sergliflozin-A具有更高的SGLT选择性,拥有365:1的高选择比。口服该药,能够剂量依赖性的促进正常小鼠和大鼠的尿糖排出,抑制正常大鼠静脉注射葡萄糖后血糖升高,且不会增加胰岛素分泌。口服糖耐量实验中,remogliflozin可以抑制STZ诱导的糖尿病大鼠的血糖升高,长期口服给药还可以降低db/db糖尿病小鼠FPG及HbA1c,改善高脂诱导GK糖尿病大鼠的高血糖,高胰岛素血症,高甘油三酯血症以及胰岛素抵抗[14]。
由于sergliflozin具有增加糖尿病人的体重的不良反应,并且考虑到竞争对手的其它SGLT2抑制剂的开发进展,Kissei制药与Glaxo-SmithKline在Ⅱ期临床时停止sergliflozin和remogliflozin的开发。
3.4dapagliflozin(结构式见图1) Bristol-Myers Squib和AstraZeneca公司开发的dapagliflozin(BMS-512148)是目前处于临床研究的SGLT2抑制剂中的领先者。在体外,其对人的SGLT2和SGLT1的EC50分别为(1.1±0.06)nM和(1 390±7)nM,选择性(hSGLT2>hSGLT1)为1 200倍,具有超高的选择比。dapagliflozin在SD大鼠中药代动力学参数见表1,口服该药可以显著促进正常大鼠和糖尿病大鼠体内葡萄糖通过尿液排泄,改善正常大鼠的糖耐量[15]。单次口服该药0.1~1.0 mg/kg可以降低ZDF(zucker diabetic fatty)大鼠的血糖。单次给予64名健康受试者和连续14 d给予40名健康受试者dapagliflozin,显示其半衰期约为17 h,血药浓度呈剂量依赖性的增加,同时对尿糖的排泄作用也呈剂量依赖性的增加[16]。在14 d的临床实验中,47名Ⅱ型糖尿病受试者在未经治疗或只服用固定剂量的二甲双胍的情况下,连续口服给药14 d(安慰剂、5 mg、25 mg和100 mg)[17]。在首次给药后24 h内,给药后尿糖量随剂量依赖性增加。第14天,安慰剂组、5 mg、25 mg和100 mg组肾内葡萄糖重吸收(0~4 h)的平均抑制率分别为0.88%、19.77%、40.88%、44.01%。与实验前FPG水平相比,dapagliflozin各剂量组第13天的FPG水平显著降低(11.7%~21.8%),并具有剂量依赖性,口服糖耐量实验中,口服75 g葡萄糖后血糖-时间下曲线面积(AUC0h~4 h)也显著下降(18.8%~22.9%)。与健康受试者相同,Ⅱ型糖尿病受试者对dapagliflozin的耐受性很好,常见不良反应为胃肠性的,且不良反应发生率与服用二甲双胍相同。Ⅱ型糖尿病受试者参加的12周的随机双盲对照临床试验中,389名未经药物治疗的受试者被随机分为7组,分别给予dapagliflozin(2.5~50 mg),二甲双胍,或者安慰剂[18]。给药12周后,FPG(0.88~1.72 mmol/L)剂量依赖性降低,所有剂量组的HbA1c下降程度(-0.55%~-0.90%)均显著大于安慰剂组。给药后没有死亡和严重的不良反应,各给药组的常见的不良反应为低血糖和尿路感染,其发生率各组基本相同,无严重的低血糖发生。给予dapagliflozin 12周后,24 h的尿量有轻微的升高,血清中尿素氮的含量有轻微的变化,但肌酐的含量不变;各给药组24 h肌酐清除率有轻微的升高但肾小球滤过率没有明显的变化。因此,dapagliflozin对肾糖重吸收抑制作用还需要进一步研究。2010年,第46届欧洲糖尿病研究协会年会上公布的Ⅲ期临床研究结果表明,与单独使用格列美脲相比,两者联合使用可以降低Ⅱ型糖尿病人的FPG、HbA1c和体重,改善口服糖耐量。若其获美国食品与药物管理局批准,则有望成为第一个治疗糖尿病的SGLT2抑制剂。

A: phlorizin B: T-1095 C: sergliflozin
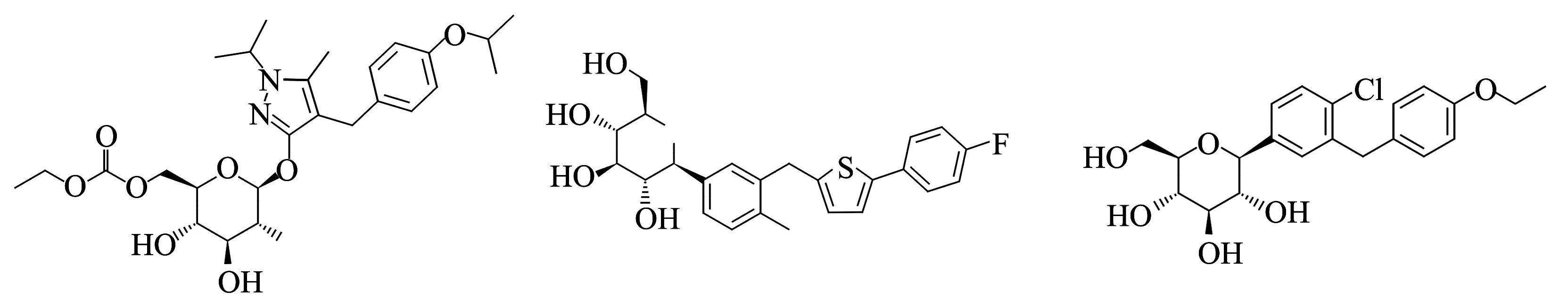
D: remogliflozin E: canagliflozin F: dapagliflozin
图1SGLT2抑制剂的化合物结构
3.5ASP1941 SGLT2抑制剂ASP1941是Astellas制药开发的me-too化合物, 目前在日本处于Ⅲ期临床研究,在美国和欧盟处于Ⅱ期临床开发。在2010年第70届美国糖尿病联合会科学年会上Astellas制药公布了ASP1941在日本的Ⅱ期临床数据,361个Ⅱ型糖尿病患者连续12周口服ASP1941(12.5、25、50、100 mg)和安慰剂,数据显示,相对于口服安慰剂组,口服ASP1941能够剂量依赖性的降低HbA1c和体重,50 mg组降HbA1c达到1.3%,100 mg组12周体重下降高达2 kg,所有病人都对该药有良好的耐受。
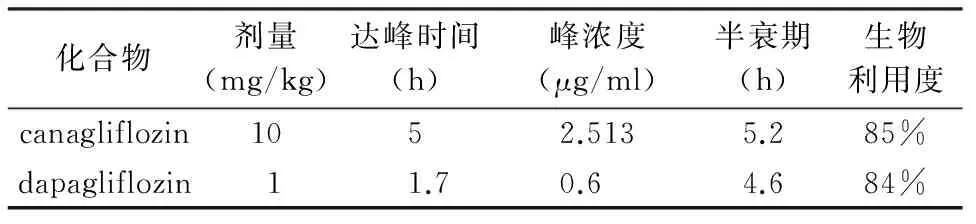
表1 口服canagliflozin和dapagliflozin在SD大鼠中的药代动力学参数
3.6目前公布的SGLT2抑制剂临床开发情况 见表2。
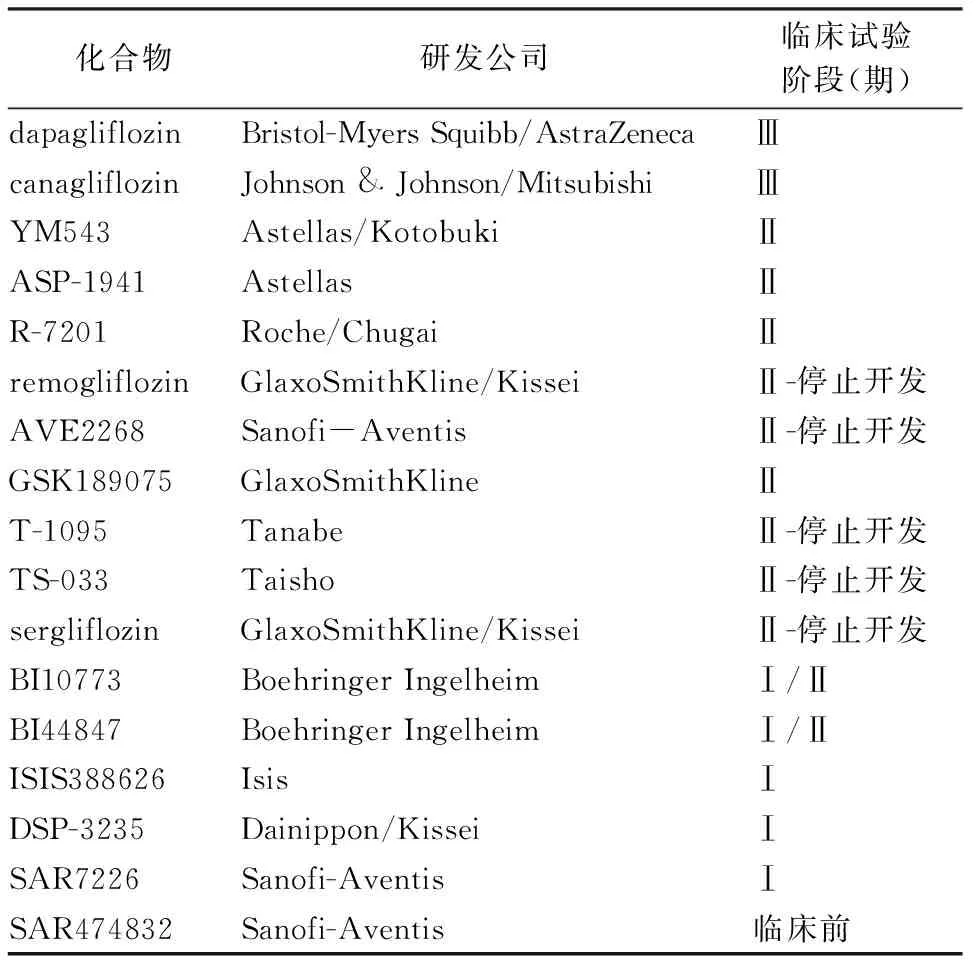
表2 SGLT2 抑制剂的临床开发情况总结
资料来源: http://www.clinicaltrials.gov
4 SGLT2抑制剂的优点和副作用
SGLT2抑制剂能够抑制肾脏葡萄糖的重吸收,促进尿液中葡萄糖排泄,使平衡朝着能量消耗的方向移动,降低体内血糖水平,降低高糖毒性,利于糖尿病的控制,且引起低血糖的风险很低。此外部分抑制剂能增加钠的排泄,可以降低血压,但是并非所有的SGLT2抑制剂都有此作用[12, 18, 19]。SGLT2抑制剂只在肾糖转运中起作用,不刺激胰岛素的分泌,可以改善胰岛素的敏感性,保护胰岛β细胞,改善长期糖尿病引起的肾病和糖尿病并发症,同时还不会引起体重增加,可降低心血管病的风险。SGLT2抑制剂的副作用表现为增加生殖器霉菌感染以及泌尿道感染机会,增加24 h尿量,此作用与弱利尿剂的作用基本相符,常见的不良反应还有红疹,但其发生率与安慰剂组大致相同。
5 结论与展望
SGLT2抑制剂口服方便,能够通过影响“能量平衡”,降低血糖,长期给药能够降低HbA1c,改善糖尿病人的高糖毒性以及糖尿病相关症状,且没有体重增加和低血糖风险;因此SGLT2抑制剂有望成为一类有效治疗Ⅱ型糖尿病的新型药物。但药物使尿糖的排泄增加所引起的副作用,以及对于Ⅰ型糖尿病,高血压,肥胖和高血脂症的治疗,还需要进一步评估。
[1] Wright EM,Hirayama BA,Loo DF.Active sugar transport in health and disease[J].Intern Med,2007,261:32.
[2] Kanai Y,Lee WS,You G,etal.The human kidney low affinity Na/glucose cotransporter SGLT2: delineation of the major renal reabsorptive mechanism for D-glucose[J].Clin Investig,1994,93:397.
[3] Van den Heuvel LP,Assink K,Willemsen M,etal.Autosomal recessive renal glucosuria attributable to a mutation in the sodium glucose cotransporter (SGLT2) [J].Hum Genet,2002,111:544.
[4] Calado J,Soto K,Clemente C,etal.Novel compound heterozygous mutations in SLC5A2 are responsible for autosomal recessive renal glucosuria[J].Hum Genet,2004, 114:314.
[5] Pajor A,Wright EM.Cloning and functional expression of a mammalian Na+/nucleoside cotransporter. A member of the SGLT family[J].Biol Chem,1992,267:3557.
[6] Wright EM.Renal Na+-glucose cotransporters[J].Am J Physiol,2001,280:F10.
[7] Turk E,Zabel B,Mundlos S,etal.Glucose/galactose malabsorption caused by a defect in the Na+/glucose cotransporter[J].Nature,1991,350:354.
[8] Pajor AM,Randolph KM,Kerner SA,etal.Inhibitor binding in the human renal low-and high-affinity Na+/glucose cotransporters[J].J Pharmacol Exp Ther,2008,324:985.
[9] Ehrenkranz JRL,Lewis NG,Kahn CR,etal.Phlorizin: a review[J].Diabetes Metab Res Rev,2005,21:31.
[10] Oku A,Ueta K,Arakawa K,etal.T-1095, an inhibitor of renal Na+- glucose cotransporters, may provide a novel approach to treating diabetes[J].Diabetes,1999, 48:1794.
[11] Adachi T,Yasuda K,Okamoto Y,etal.T-1095, renal Na+-glucose transporter inhibitor, improves hyperglycemia in streptozotocin induced diabetic rats[J].Metabolism,2000,49:990.
[12] Katsuno K,Fujimori Y,Takemura Y,etal.Sergliflozin, a novel selective inhibitor of low-affinity sodium glucose cotransporter (SGLT2), validates the critical role of SGLT2 in renal glucose reabsorption and modulates plasma glucose level[J].Pharmacol Exp Ther,2007,320:323.
[13] Hussey EK,Clark RV,Amin DM,etal.Early clinical studies to assess the safety, tolerability, pharmacokinetics and pharmacodynamics of single doses of sergliflozin, a novel inhibitor of renal glucose reabsorption, in healthy volunteers and subjects with type 2 diabetes mellitus[J].Diabetes,2007,56 (Suppl 1):189.[14] Fujimori Y,Katsuno K,Nakashima I,etal.Remogliflozin etabonate, in a novel category of selective low-affinity/high-capacity sodium glucose cotransporter (SGLT-2) inhibitors, exhibits antidiabetic efficacy in rodent models[J].Pharmacol Exp Ther,2008,327:268.
[15] Wei M,Bruce AE,Alexandra AN,etal.Discovery of dapagliflozin: A potent, selective renal sodium-dependent glucose cotransporter 2 (SGLT2) inhibitor for the treatment of type 2 diabetes[J].J Med Chem,2008,51(5):1145.
[16] Komoroski B,Vachharajani N,Boulton D,etal.Dapagliflozin, a Novel SGLT2 Inhibitor, Induces Dose-Dependent Glucosuria in Healthy Subjects[J].Clin Pharmacol Ther,2009,85:520.
[17] Komoroski B,Vachharajani N,Feng Y,etal.Dapagliflozin, a novel, selective SGLT2 inhibitor, improved glycemic control over 2 weeks in patients with type 2 diabetes mellitus[J].Clin Pharmacol Ther,2009,85:513.
[18] List JF,Woo V,Morales E,etal.Sodium-glucose cotransport inhibition with dapagliflozin in type 2 diabetes mellitus[J].Diabetes Care,2009,32:650.
[19] Calado J,Loeffler J,Sakalliouglu O,etal.Familial renal glucosuria: SGLC5A2 mutation analysis and evidence of salt-wasting[J].Kidney Int,2006,69:852.
2010-11-09
[修回日期] 2011-02-22
Researchontype2sodiumglucoseco-transportersindiabetestreatment
DING Hai-feng, CAO Yong-bing, AN Mao-mao, JIA Xin-ming, JIANG Yuan-ying
( The center of new drug development, second military medical university, Shanghai 200433, China)
In the last few years, inhibitors of the type 2 sodium glucose co-transporters (SGLT2) had been the subject of novel approach to treating diabetes. SGLT2 played a major role in physiology of glucose reabsorption from proximal part of kidney. The blockade of SGLT2 in the kidney had the potential to prompts urinary excretion of glucose and promotes normalization of blood glucose without hypoglycemia in the setting of type 2 diabetes. Clinical trails showed that their efficacy in the treatment of type 2 diabetes was promising; Weight loss and very low risk of hypoglycemia were the potential benefits of these inhibitors. Some of these inhibitors had been developed and advanced to late phase clinical testing.
type 2 diabetes; sodium-glucose co-transporters (SGLT);inhibitor
丁海峰(1980-),男,硕士研究生. Tel: 15995423234, E-mail:vetdhf@sina.com..
姜远英. Tel:(021)818171357, E-mail:jiangyycn@yahoo.com.cn.
R977
A
1006-0111(2011)02-0089-05

