氯离子在有机涂层中的渗透及涂层失效过程的电化学阻抗谱研究
陈家才,王旭东,2,孙冬柏
(1北京科技大学腐蚀与防护中心,北京100083;2北京市腐蚀、磨蚀与表面技术重点实验室,北京100083)
氯离子在有机涂层中的渗透及涂层失效过程的电化学阻抗谱研究
陈家才1,王旭东1,2,孙冬柏1
(1北京科技大学腐蚀与防护中心,北京100083;2北京市腐蚀、磨蚀与表面技术重点实验室,北京100083)
采用渗透实验和电化学阻抗谱(EIS)分别研究了氯离子在氟碳涂层游离膜中的渗透规律以及不同温度、不同溶液对复合涂层体系耐蚀性能的影响。渗透实验结果表明:氯离子在氟碳涂层游离膜中的扩散存在一个时间临界点。在临界点之前,氯离子在游离膜两侧浓差作用下迅速达到动态平衡;在临界点之后,氯离子在游离膜中的扩散则呈线性增加趋势,并且氯离子在复合涂层游离膜中的渗透速率比在单层游离膜中的渗透速率慢。EIS结果表明:溶液和温度对氯离子在复合涂层体系中的渗透有较大的影响,虽然涂层电容值在不同条件下均呈上升趋势,但在15℃下,人造海水溶液对复合涂层体系的腐蚀性比3.5%(质量分数)NaCl溶液对复合涂层体系的腐蚀性强。
氟碳涂料;游离膜;电化学阻抗谱
由于有机涂层能够抵抗电解质离子如氯离子的透过,避免水与氧在较短时期渗透到金属表面而引起早期腐蚀,因此,有机涂层成为目前最经济、应用最普遍的一种对金属加以保护、延长金属使用寿命的有效防腐手段[1-8]。Mayne等[9]指出,涂层抗电解质离子渗透的性能决定着涂层的最终防腐效果,并且涂层在溶液中的浸泡时间对其电化学参数的变化有着直接的影响。Miskovic等[10]研究发现,电解质透过涂层完全是通过涂层中存在的孔道实现的,并测量得到其直径在3~7.2μm之间。张鉴清等[11]研究了水和氯离子在有机涂层中传质的三个阶段。但是,针对电解质离子在涂层中的渗透机理,目前仍然存在着较大的争议。在海水飞溅区[12,13]中,高浓度海雾和飞溅水滴就含有大量的腐蚀性氯离子,因此,研究有机涂层在此区域的腐蚀机理和规律,特别是氯离子在涂层中的传质具有重要的意义。
氟碳涂料是以氟烯烃聚合物或氟烯烃和其他单体的共聚物等为成膜物质的涂料,由于分子链中高键能C—F键的存在及稳定的分子结构使其具有优异的防腐蚀性、耐候性、耐玷污性等性能而日益受到广泛的重视和使用。本工作以氟碳面漆游离膜、环氧富锌底漆/环氧云铁中间漆/氟碳面漆复合涂层游离膜和金属基环氧富锌底漆/环氧云铁中间漆/氟碳面漆复合涂层体系为研究对象,采用渗透装置和电化学阻抗谱(EIS)研究了不同温度、不同溶液条件下氯离子在游离膜中的渗透规律和复合涂层体系失效过程的电化学行为,为进一步建立典型有机涂层体系海水飞溅区腐蚀的室内模拟方法积累数据。
1 实验
1.1 实验材料及制备
基体选用海水飞溅区广泛使用的A3钢。使用的涂料为环氧富锌底漆(牌号:HI-EPOXY 1495)、环氧云铁中间漆(牌号:HI-EPOXY 4465)、氟碳面漆(牌号:HI-FLORO 6738)。
调整涂料的黏度为20s(涂-4杯)左右,按氟碳面漆和环氧富锌底漆/环氧云铁中间漆/氟碳面漆的顺序依次涂覆于聚四氟乙烯衬垫膜上,分别制得两种游离膜。复合涂层游离膜中每道涂层间涂装间隔时间为24h。待膜干后,剥离游离膜,使原先未暴露的膜表面至少和空气自由接触一周,以确保游离膜两面充分干燥。游离膜的厚度如表1所示。

表1 涂层的厚度Table 1 The thicknesses of coating
基体尺寸为50mm×30mm×2mm,试样表面用120#砂纸打磨,焊接铜线后分别依次用乙醇、丙酮处理,干燥后按环氧富锌底漆、环氧云铁中间漆、氟碳面漆的顺序涂覆在基材上,每道涂层间涂装间隔时间为24h。全部涂覆完成后室温下干燥一周。复合涂层体系的厚度亦如表1所示。
1.2 氯离子渗透实验
将制备好的完全连续、厚度均匀和光滑的游离膜制成直径合适的圆片,置于渗透装置中部。游离膜两边分别放置蒸馏水和3.5%(质量分数,下同)NaCl溶液,按实验周期使用 TU-1901型双光束紫外可见分光光度计检测蒸馏水部分的氯离子含量。渗透实验装置如图1所示。
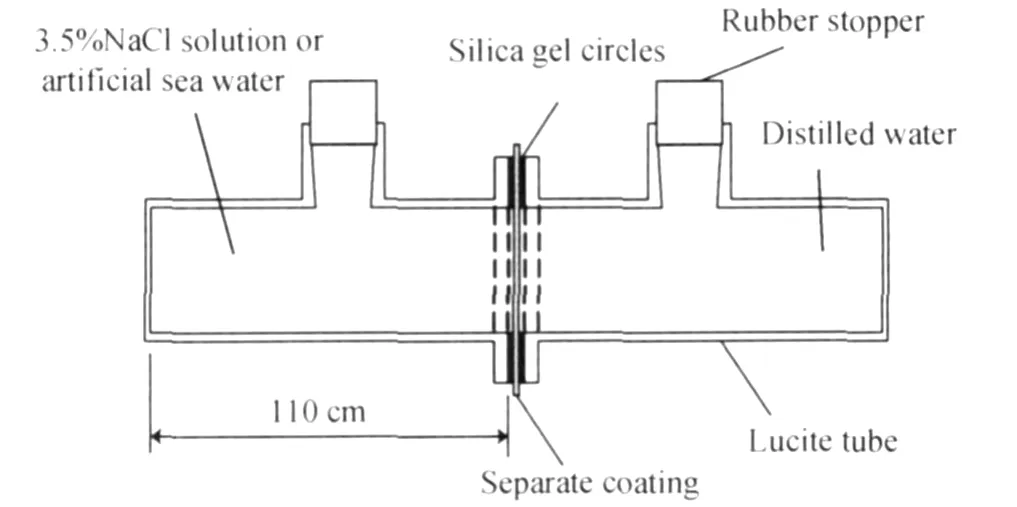
图1 渗透装置示意图Fig.1 Schematic diagram of permeability apparatus
1.3 浸泡实验
在实验前将涂层试片的棱边和背面用硅胶密封,露出的涂层表面有效面积为13cm2。然后分别浸泡于3.5%NaCl溶液和人造海水中,在不同阶段取出进行EIS测试。
使用人造海水浸泡时,人造海水按照 G B/T 19746—2005《金属和合金的腐蚀盐溶液周浸试验》配制。
1.4 电化学测试
电化学交流阻抗测试采用CHI660D电化学工作站测试系统。测试频率范围为105~10-2Hz,正弦波信号振幅为10mV。电解池采用三电极体系,参比电极为饱和甘汞电极(SCE),辅助电极为铂电极,工作电极为带有涂层的A3钢。测试面积为13cm2。电解质溶液为3.5%NaCl溶液或人造海水。并利用ZSimp-Win软件对阻抗谱数据进行解析,根据等效电路对EIS数据进行拟合,以得到涂层电化学参数值。
1.5 实验过程
分别在25,35℃下进行3.5%NaCl溶液的氯离子渗透实验,以及在15,25℃下进行3.5%NaCl溶液和人造海水的浸泡实验。
2 实验结果与分析
2.1 氯离子渗透实验分析
氟碳面漆游离膜(SC1)和环氧富锌底漆/环氧云铁中间漆/氟碳树脂面漆复合涂层游离膜(SC2)在25℃下,3.5%NaCl溶液中氯离子的渗透浓度随时间的变化如图2所示。
可见,对氯离子在 SC1游离膜中的渗透,初始阶段(0~24h),氯离子在膜两侧的浓差作用下,沿着膜中的毛细微孔逐渐透过游离膜;从48h开始至96h,氯离子的渗透浓度几乎不变(0.6mg·dm-3),达到早期动态平衡,表明膜的物理孔隙结构、化学分子结构均未发生变化;到96h时,渗透达到一临界点,此时,漆膜性能开始发生变化,前阶段渗入游离膜中的氯离子与膜中的树脂、颜料发生作用,破坏了动态平衡;渗透96h后,氯离子在膜中的扩散速率逐渐增大,渗透浓度呈线性增加,表明膜内的孔隙率增加、孔隙结构增大,导致氯离子在膜中的传输速度明显加快,从而降低了膜耐腐蚀性离子的渗透性能。
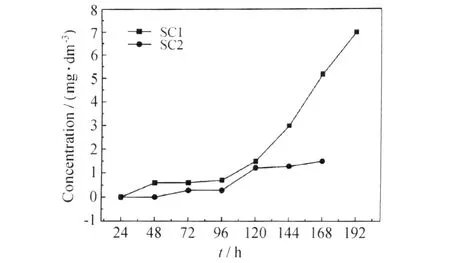
图2 25℃下,氯离子在两种游离膜中渗透浓度随时间的变化Fig.2 Permeability-time curved of chloride ion in the fluorocarbon separate coatings at 25℃
由渗透96h后线性阶段直线的斜率,根据Fick扩散定律可求得氯离子在游离膜中的扩散系数D[9,11]:
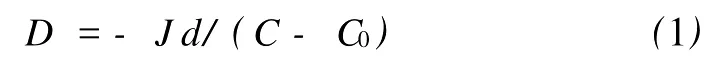
式中:J为扩散通量;d为试样厚度;C,C0分别是试样两侧溶液的浓度。由于C较小,相对于C0可以忽略,因此,C0可视为常数。

式中:q为通过游离膜的氯离子量;A为游离膜暴露于溶液中的面积;t为单位时间。由此可得:
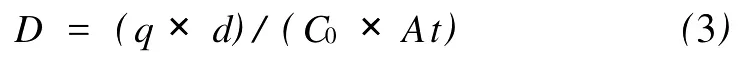
分别测定式中各值,可计算得到氯离子在SC1游离膜中的扩散系数为4.6×10-10cm2/h。
对氯离子在SC2游离膜的渗透,由图2可见,整个渗透阶段,氯离子的渗透浓度都较小(低于1.2mg·dm-3)。这是由于环氧富锌底漆、环氧云铁中间漆、氟碳面漆的叠加,相互间填补了由于溶剂挥发留下的微小孔洞,降低了膜中毛细微孔连续贯通的概率,阻断了氯离子和水分子在其中传输的通道,使得整体的致密性提高,从而提高了膜的防渗透性能。
图3为氯离子在SC2游离膜中不同温度下渗透浓度随时间的变化。由图3可见,不同温度下氯离子的渗透浓度都较小,且随着时间的延长均呈上升趋势。渗透120h后,氯离子在35℃下的扩散速率增大的更快,表明随着温度的升高,经过一段时间的渗透后,涂层的一些物化性能发生变化,孔隙率增大,水和氯离子的扩散传输速率加快。
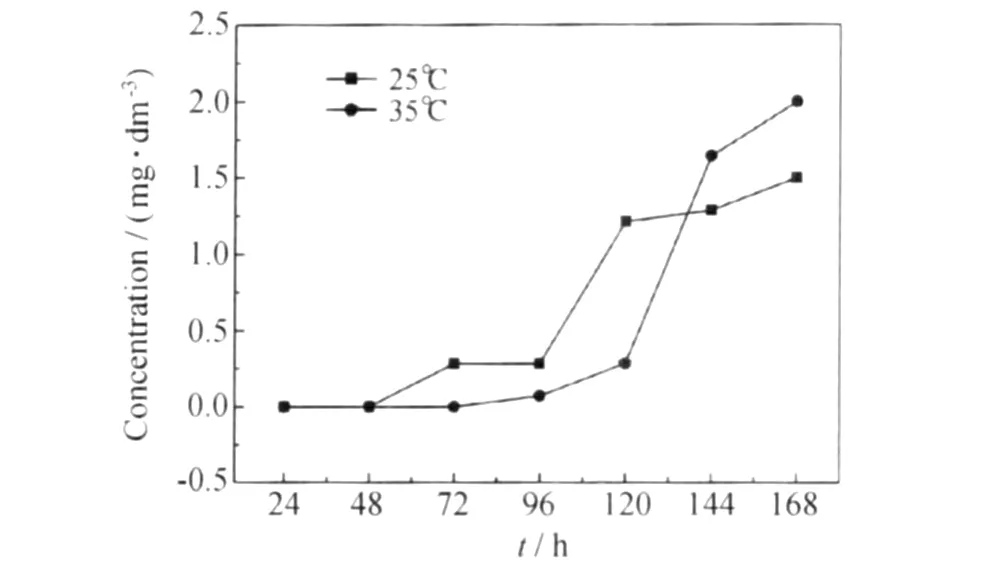
图3 不同温度下,氯离子在SC2游离膜中渗透浓度随时间的变化曲线Fig.3 Permeability-time curved of chloride ion in the SC2 fluorocarbon separate coating at different temperatures
2.2 浸泡实验分析
在15℃和25℃下,金属基环氧富锌底漆/环氧云铁中间漆/氟碳面漆复合涂层体系(MC)随浸泡时间的EIS变化如图4~7所示。

图4 25℃下,复合涂层体系在人造海水中浸泡不同时间的阻抗谱图 (a)Nyquist图;(b)Bode图Fig.4 EIS of fluorocarbon coating at the different time of immersion in artificial sea water at 25℃(a)Nyquist plot;(b)Bode plot

可见,在25℃下,浸泡于人造海水中的复合涂层体系在2h的 EIS图谱上出现较大半径的半圆(Nyquist图),阻抗的模值为108(Bode图),其等效电路模型如图8(a)所示,复合涂层体系可看做是一个大电阻与一个小电容并联而成,具有较好的防护性能;随着浸泡时间的延长,EIS图谱呈现两个时间常数,高频段容抗弧半径逐渐减小,低频段容抗弧半径先减小后增大,说明电解质逐步扩散到金属基体和涂层的界面处,高频段容抗弧表示复合涂层体系的腐蚀反应,其半径的减小表明渗透到基体界面的氯离子引起了基体金属的腐蚀,低频段容抗弧表示底漆中锌粉的腐蚀反应,其半径的先减小后增大表明锌粉发生腐蚀反应,但生成的腐蚀产物又抑制了反应的继续进行,这一时期阻抗的模值下降很快,从浸泡初期的108很快下降到105,其等效电路模型如图8(b)所示;随着浸泡时间的进一步延长,到120h时,EIS图谱开始出现了 Warburg阻抗弧[14-20],表明锌粉腐蚀生成的腐蚀产物不再抑制腐蚀反应的继续进行,水和氯离子等腐蚀性介质的浸入导致金属基体持续发生腐蚀,此时的等效电路模型如图8(c)所示。
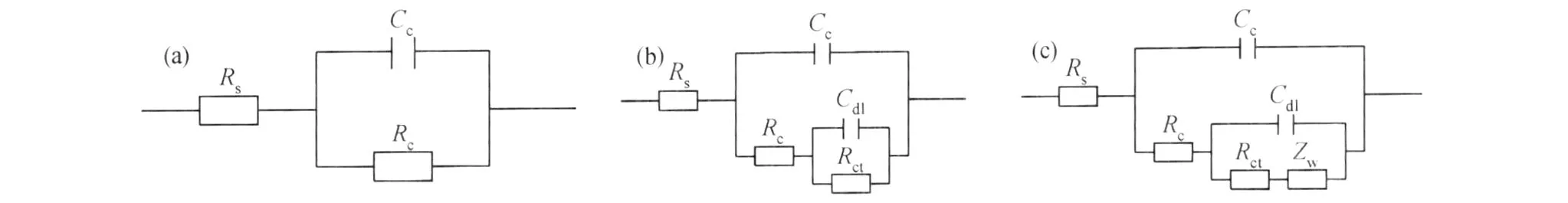
图8 复合有机涂层在不同腐蚀时期的等效电路模型(a)浸泡初期;(b)浸泡中期;(c)浸泡末期Fig.8 The equivalent electrical circuit of organic coated at the different time of immersion(a)beginning time of immersion;(b)medium-term of immersion;(c)final stage of immersion
图8中,Rs是溶液电阻;Cc和Rc分别为涂层电容和涂层电阻,Cdl为界面双电层电容,Rct为电荷转移电阻,Zw为Warburg阻抗。
同样,复合涂层体系在25℃下,3.5%NaCl溶液中的EIS图谱的变化也显示出复合涂层体系经历了上述浸泡初期、中期和末期的过程。但是,在3.5%NaCl溶液中,浸泡初期阻抗的模值为109,并且随着浸泡时间的延长,阻抗的模值下降得较同样温度下人造海水中的慢,浸泡时间到168h时,才出现 Warburg阻抗弧。可见,人造海水对复合涂层体系的腐蚀性比3.5%NaCl溶液对复合涂层体系的腐蚀性更大。
15℃下,人造海水和3.5%NaCl溶液中复合涂层体系在浸泡中期经过同样浸泡时间时,其低频段容抗弧半径均比25℃时相应溶液中的容抗弧半径大。说明15℃时,锌的腐蚀电阻较大,水、氧和腐蚀性氯离子扩散速度较25℃时慢,在涂层中传质时间延长,到达富锌底漆层后与锌粉接触而使锌粉先发生腐蚀。此外,15℃下,人造海水中阻抗的模值下降的较3.5%NaCl溶液中的快,因此,人造海水在15℃温度下对复合涂层体系的影响也比3.5%NaCl溶液对复合涂层体系的影响大。
当复合涂层体系在浸泡过程中发生吸水后,水和电解质离子在涂层微孔中持续扩散,涂层发生溶胀,孔隙的数量和尺寸相应增加。反映在等效电路上就是涂层吸水后导致涂层的电容不断增大。不同条件下复合涂层体系的电容值如图9所示。
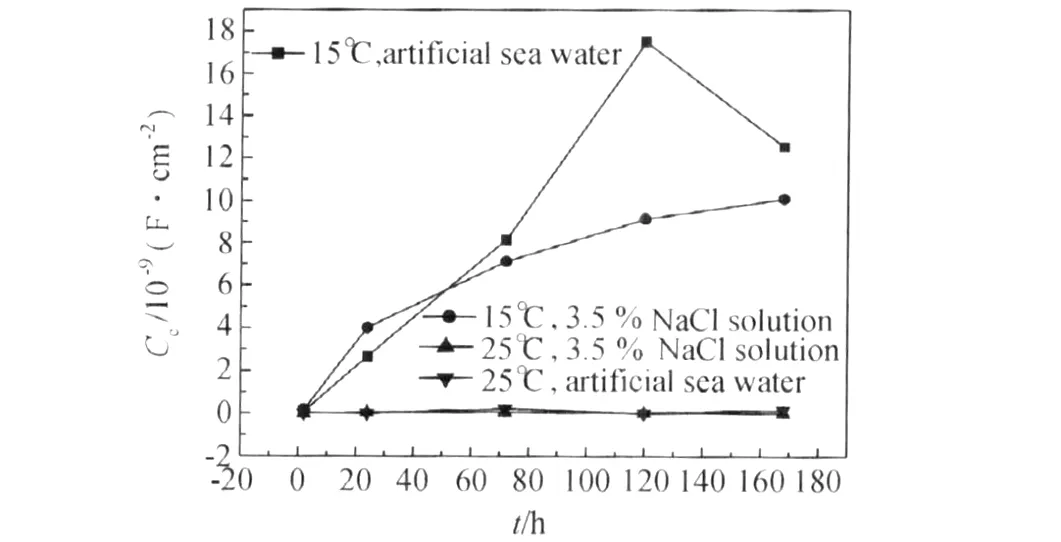
图9 不同条件下复合涂层体系的电容值随时间的变化Fig.9 Coating capacitance-time curved at different conditions
由图9可见,在 15℃下,浸泡 120h之前,复合涂层体系在人造海水和3.5%NaCl溶液中的涂层电容均随着浸泡时间的延长而增大,并且复合涂层体系的涂层电容值在人造海水中变化的斜率更大,增大的更快。这是由于人造海水与3.5%NaCl溶液相比,人造海水中含有MgCl2,NaCl和Na2SO4,并且加入了微量的F-,Ca2+等离子,这些离子可使复合涂层体系的结构发生变化,致使涂层孔隙的数量和尺寸都增大,从而使复合涂层体系在人造海水中的抗渗透性减弱。浸泡在120~168h时,复合涂层体系在人造海水中的涂层电容值有一个降低过程,说明腐蚀性氯离子与富锌底漆后的锌粉发生腐蚀反应,生成的腐蚀产物在一定程度上填补了前期的孔隙,降低了孔隙的数量和尺寸,抑制了腐蚀的继续进行。而在25℃下,分别浸泡在人造海水和3.5%NaCl溶液中的复合涂层体系的电容值变化都比较小。不过可以看出,在浸泡末期,人造海水的涂层电容值比3.5%NaCl溶液中的涂层电容值稍大一些。这说明不同溶液中的水和氯离子等腐蚀性介质在25℃温度下复合涂层体系中扩散受到的阻力相差不大,复合涂层体系阻挡不同溶液中水和氯离子等腐蚀性介质的能力、水在其中的传输都大致相同,但到浸泡末期,人造海水中多种离子对复合涂层体系的破坏开始显露出来。
3 结论
(1)氯离子在氟碳游离膜中的扩散存在一个时间临界点。在渗透初期,临界点之前,氯离子在漆膜中的扩散达到动态平衡;临界点之后,氯离子在漆膜中的扩散随时间呈线性增加趋势。
(2)对氯离子在三层涂层游离膜中的渗透,短期内随时间呈缓慢上升的趋势。氯离子在三层涂层游离膜中的渗透量明显小于单层氟碳游离膜。升高温度,能加速氯离子的扩散。
(3)人造海水和3.5%NaCl溶液对氯离子在复合涂层体系中扩散的影响不同,人造海水对复合涂层体系影响更大。
[1] AMIRUDIN A,THIERRY D.Application of electrochemical impedance spectroscopy to study the degradation of polymer-coated metals[J].Progress in Organic Coatings,1995,26(1):1-28.
[2] RANJBAR Z,MORADIAN S,ATTAR M R M Z.EIS investigation of cataphoretically electrodeposited epoxy coatings having different EEWs[J].Progress in Organic Coatings,2004,51(2):87-90.
[3] LAVAERT V,COCK M D,MOORS M,et al.Influence of pores on the quality of a silicon polyester coated galvanised steel system[J].Progress in Organic Coatings,2000,38(3-4):213-221.
[4] KRALJ IC M,MANDIC Z,DUIC L.Inhibition of steel corrosion by polyaniline coatings[J].Corrosion Science,2003,45(1):181-198.
[5] STRUNZ W.Dielectric relaxation in barrier coatings:A square root of time process[J].Progress in Organic Coatings,2000,39(1):49-60.
[6] TRACHLI B,KEDDAM M,TAKENOUTI H,et al.Protective effect of electropolymerized 2-mercaptobenzimidazole upon copper corrosion[J].Progress in Organic Coatings,2002,44(1):17-23.
[7] DESTRERI M D G,VOGELSNAGJ,FEDRIZZI L,et al.Water up-take evaluation of new waterborne and high solid epoxy coatings.Part II:electrochemical impedance spectroscopy[J].Progress in Organic Coatings,1999,37(1-2):69-81.
[8] PEN C L,LACABANNE C,PEBERE N.Structure of waterborne coatings by electrochemical impedance spectroscopy and a thermostimulated current method:influence of fillers[J].Progress in Organic Coatings,2000,39(2-4):167-175.
[9] CORTI H,FERNADEZ-PRINI R,GOMEZ D.Protective organic coatings:Membrane properties and performance[J].Progress in Organic Coatings,1982,10(1):5-33.
[10] MISKOVIC-STANKOVIC V B,DRAZIC D M,TEODOROVIC M J.Electrolyte penetration through epoxy coatings electrodeposited on steel[J].Corrosion Science,1995,37(2):241-252.
[11] ZHANG Jian-qing,ZHANG Jin-tao.Studies of water transport behavior and impedance models of epoxy-coated metals in NaCl solution by EIS[J].Progress in Organic Coatings,2004,51(2):145-151.
[12] ZEN K.Corrosion and life cycle management of port structures[J].Corrosion Science,2005,47(10):2353-2360.
[13] HOU B R,DUAN J Z,ZHANG J L,et al.Tests for hanging steel specimens in seawater[J].Materials Performance,2002,41(10):45-48.
[14] OLIVEIRA C G,FERREIRA M G S.Ranking high-quality paint systems using EIS.Part I:intact coatings[J].Corrosion Science,2003,45(1):123-138.
[15] OLIVEIRA C G,FERREIRA M G S,FERREIRA.Ranking high-quality paint systems using EIS.Part II:defective coatings[J].Corrosion Science,2003,45(1):139-147.
[16] 曹楚南,张鉴清.电化学阻抗谱导论[M].北京:科学出版社,2002.
[17] ZHANG J T,HU J M.ZHANG J Q,et al.Studies of water transport behavior and impedance models of epoxy-coated metals in NaCl solution by EIS[J].Progress in Organic Coatings,2004,51(2):145-151.
[18] CASTELA A S,SIMOES A M.An impedance model for the estimation of water absorption in organic coatings.PartⅡ:A complex equation of mixtures[J].Corrosion Science,2003,45(8):1647-1658.
[19] CASTELA A S,SIMOES A M.An impedance model for the estimation of water absorption in organic coatings.PartⅠ:A Linear dielectric mixture equation[J].Corrosion Science,2003,45(8):1631-1646.
[20]CASTELA A S,SIMOES A M.Assessment of water uptake in coil coationgs by capacitance measurements[J].Progress in Organic Coatings,2003,46(1):55-61.
Penetration of Chlorine Ion in Organic Coating and Deterioration Process by Electrochemical Impedance Spectroscopy
CHEN Jia-cai1,WANG Xu-dong1,2,SUN Dong-bai1
(1 Center for Corrosion and Protection,University of Science and Technology Beijing,Beijing 100083,China;2 Beijing Key Laboratory for Corrosion-Erosion and Surface Technology,Beijing 100083,China)
The penetration law of chloride ion in the fluorocarbon separate coating and the deterioration process of fluorocarbon coating were investigated by permeability test and EIS,respectively.The results show that the diffusion of chlorine ion in fluorocarbon separate coating have a time critical point.The spread of chlorine ion in coating reach a dynamic balance stage before the critical point,then the chlorine ion in coatings diffusion present linear increase trend.The permeability of chlorine ion in fluorocarbon coatings slower than fluorocarbon resin layer.And solution and temperature on the infiltration of chloride ion in fluorocarbon coating have clear influence on the transmission.The EIS result also indicates that the coating capacitance(Cc)all have ascendant trend.Besides,the artificial seawater had more corrosive effect than 3.5%(mass fraction)NaCl solution at 15℃.
fluorocarbon coating;separate coating;electrochemical impedance spectroscopy
TG174.4
A
1001-4381(2011)06-0052-06
国家科技支撑计划(2007BAB27B05);北京市科技新星计划(2008A029);北京市教委共建项目(SYS100080419)
2010-07-15;
2010-12-08
陈家才(1976—),男,博士研究生,主要从事涂层的室内模拟加速实验方法的研究,E-mail:gz_cjc@sina.com
王旭东,联系地址:北京市海淀区学院路30号,北京科技大学腐蚀与防护中心223室(100083),E-mail:xdwang@ustb.edu.cn

