酶法交联对食物蛋白的改性作用研究进展
吴进菊,汤尚文,黄升谋,豁银强
(襄樊学院化学工程与食品科学学院,湖北襄樊 441053)
酶法交联对食物蛋白的改性作用研究进展
吴进菊,汤尚文,黄升谋,豁银强
(襄樊学院化学工程与食品科学学院,湖北襄樊 441053)
食物蛋白通过分子间或分子内的交联作用,可有效地改善功能特性,有利于在食品加工中的应用。可用于蛋白交联的酶主要有转谷氨酰胺酶、多酚氧化酶、过氧化物酶等。主要阐述了转谷氨酰胺酶、多酚氧化酶、过氧化物酶交联蛋白的作用机理及最新研究进展。
交联,食物蛋白,多酚氧化酶,转谷氨酰胺酶
蛋白质是人体必需的六大营养素之一,是影响食品质地的重要组分。然而,天然蛋白质的性质无法满足食品加工的需要,蛋白质改性研究已引起了广大学者的广泛重视。蛋白质的改性是指通过物理、化学和生物(酶)的方法改变蛋白质的结构,从而改善它们的功能特性,使之达到食品所需要的品质特性,以扩大蛋白质在不同类型食品体系中的应用范围[1]。蛋白质的功能特性,与其化学结构、分子大小、表面疏水性等密切相关。蛋白质通过分子间或分子内的交联作用,分子结构发生明显变化,分子量大大提高,可有效地改善功能特性,如保水性、乳化性、起泡性、流变学特性及凝胶特性等,减少食品添加剂的使用,有利于在食品加工中的应用。蛋白交联的方法有化学法、物理法和酶法。利用酶进行蛋白交联以改良食品的功能特性,比化学法更好,因为酶所需条件温和,具有较高的特异性,不会产生有毒物质,并且消费者感觉酶比化学剂更“天然”[2]。目前研究发现,可用于蛋白交联的酶有转谷氨酰胺酶、多酚氧化酶、过氧化物酶等,它们可催化蛋白质形成分子内或分子间交联,从而改善蛋白质的功能特性。
1 转谷氨酰胺酶对食物蛋白的交联作用
转 谷 氨 酰 胺 酶 (Transglutaminase,TG,E.C.2.3.2.13,全称为蛋白质-谷氨酰胺-γ谷氨酰胺基转移酶)可催化转酰胺基反应,形成ε-(γ-谷氨酰胺基)赖氨酸键的交联,从而导致蛋白质(或多肽)之间发生共价交联形成共价化合物。转谷氨酰胺酶的作用机理如下[3]∶a.它可催化肽键中谷氨酰胺残基γ-羰基和伯胺之间酰胺基转移反应(图1a),利用该反应可共价导入蛋白质、氨基酸、多肽至同种或异种蛋白,或将氨基糖类、磷脂导入蛋白质形成多相共轭蛋白质,从而改善蛋白质营养特性[4]。b.当蛋白质中赖氨酸残基γ-氨基作为酰基受体时,蛋白质在分子之内或分子之间形成ε-(γ-谷氨酰胺基)赖氨酸共价键(图1b)。通过该反应蛋白质分子发生交联,使食品或其他制品发生质构变化,从而赋予产品特有的质构特性和粘合性能。c.当不存在伯胺时,水会成为酰基受体,则谷氨酰胺残基脱去胺基(图1c),该反应可用于改变蛋白质等电点及溶解性。
转谷氨酰胺酶最初是从哺乳动物的组织中提取得来的,由于提取纯化困难,价格较高,从而制约了其在食品加工中的应用。直到1989年,日本人采用微生物发酵的方法大量生产转谷氨酰胺酶,使转谷氨酰胺酶的来源得到充分保障,从而推动了转谷氨酰胺酶交联蛋白的进一步研究。采用TG对食物蛋白进行交联,可改良蛋白质的功能特性,如热稳定性、乳化性、凝胶特性、保水性、流变学特性等。目前,转谷氨酰胺酶是蛋白质酶法交联中研究最多、应用最广的一种酶,已广泛应用于乳制品、植物蛋白制品、肉制品和焙烤制品中。
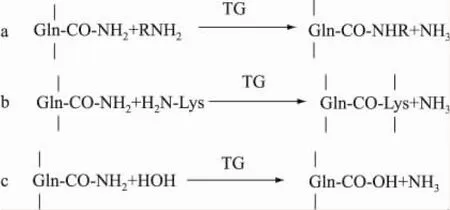
图1 转谷氨酰胺酶作用机理
Kuraishi等报道采用TG处理乳制作的凝固型酸奶的凝胶强度和搅拌型酸奶的粘性具有更易被人们接受的感官性,因为TG能增加凝胶强度,提高蛋白溶液的粘性,从而提高保水性[4]。Chambi等采用TG催化交联不同配比浓度的酪蛋白和明胶制备可食用膜,当酪蛋白和明胶配比为75∶25时,可食用膜的延展性能大大提高,而透水性却大幅度降低[5]。采用TG催化交联β-乳球蛋白,可以显著提高其热稳定性,如聚合度为1%的β-乳球蛋白在100℃下可保持30min不变性,而未交联的β-乳球蛋白在70℃下就会发生变性[6]。同样地,脱脂乳经 TG交联后,在pH6.3~7.1范围内比未处理乳的热稳定性更高[7]。Marton等研究发现采用转谷氨酰胺酶(MTG)和谷胱甘肽(GSH)的共同作用对乳蛋白进行共价交联,可使乳在不需要预热处理的情况下就能进行交联,从而增加外观粘性,比单独采用TG处理的乳具有更高的蛋白聚合度[8]。Ozer等建议 TG的使用浓度在9~14U/g蛋白质,以提高凝固型脱脂酸奶的物理、化学和感官特性。而当采用TG+GSH共同作用时,所需的酶浓度较低,只需0.6~1.0U/g蛋白质[25]。庄玮婧等研究发现TG酶的添加可以明显提高鲢鱼鱼丸的持水性、质构特性和感官品质,但对色泽无明显影响[9]。
2 多酚氧化酶对食物蛋白的交联作用
多酚氧化酶 (Polyphenoloxidase,PPO,EC 1.14.18.1),是由核编码的含铜金属酶,广泛存在于各种动物、植物和微生物中。根据作用底物的不同,多酚氧化酶又被习惯地称为单酚氧化酶、酪氨酸酶、甲酚酶、儿茶酚酶等。近些年来,多酚氧化酶催化蛋白交联反应引起了学者的广泛重视。
目前,用于蛋白交联研究的PPO多是从双孢蘑菇子实体提取得来的。Onwulata等采用经蘑菇多酚氧化酶交联的乳蛋白制作凝胶,凝胶粘度显著增加,将凝胶放置于4℃冰箱保存10d后,凝胶状态稳定,且粘弹性更高[10]。Burzio等采用蘑菇PPO对棱纹贻贝、智利贻贝和合唱壳菜蛤三种蚌类中的多酚类蛋白质进行交联,研究发现智利贻贝和合唱壳菜蛤中蛋白质的交联效果不如棱纹贻贝中好。对交联蛋白的氨基酸分析表明∶只有多巴含量明显减少,而其它氨基酸含量变化不大,这说明交联的形成可能只限于蛋白质分子中多巴衍生物的氧化[11]。Takasaki等研究发现小麦醇溶蛋白经蘑菇PPO交联后,分子量为20~60ku的峰面积显著减少,而分子量为300~1000ku的峰面积显著增加,他们通过进一步的研究表明小麦醇溶蛋白发生了分子内和分子间的交联[12]。Thalmann等在研究蘑菇PPO对α-乳白蛋白、β-乳球蛋白和溶菌酶的交联作用时发现,α-乳白蛋白和β-乳球蛋白产生交联反应的最适pH为4~5,而溶菌酶的最适pH为7.0,其中,α-乳白蛋白经交联后能产生分子量大于300ku的聚合体[13]。经双孢蘑菇PPO交联后酪蛋白的乳化性和乳化稳定性与形成的聚合物含量有着密切的关系,当PPO酶比活力为400U/mL,25℃反应4h时,交联后酪蛋白的乳化性和乳化稳定性分别为18.3m2/g和19.8min,较未交联的酪蛋白乳化性和乳化稳定性分别提高了17.3%和37.5%[14]。另外,蘑菇PPO也能催化胶原蛋白发生分子内和分子间的交联[15]。
由于双孢蘑菇的栽培具有明显的季节性,鲜菇不易贮存,且PPO分离纯化困难,近年来,少数学者将PPO的来源投向了微生物,采用里氏木霉PPO交联蛋白。研究表明,里氏木霉 PPO在3h内可使β-酪蛋白产生交联,但牛血清白蛋白在24h内都不能产生交联[16]。另外,Monogioudi等研究发现β-酪蛋白经里氏木霉PPO交联后形成的聚合物分子量大小与酶的加入量和作用时间有关,聚合物分子量在500~1700ku之间,交联度在21~71之间[17]。
3 过氧化物酶对食物蛋白的交联作用
过氧化物酶(Peroxidase,POD,E.C.1.11.1.7)是由微生物或植物所产生的一类氧化还原酶,广泛地分布于自然界中,是以过氧化氢为电子受体催化底物氧化的酶,该酶也可以催化蛋白发生交联反应。过氧化物酶可氧化酪氨酸残基,在蛋白质中形成分子间和分子内的二酪氨酸和三酪氨酸结构,从而使蛋白发生交联作用[18]。
Steffensen等采用灰盖鬼伞过氧化物酶和 H2O2交联酪蛋白,经SDS-PAGE电泳检测发现,天然酪蛋白的量明显减少,而形成了高分子量的聚合物[19]。在H2O2存在的情况下,采用辣根过氧化物酶对酪蛋白进行交联作用,酪蛋白的最佳交联条件是酶加入量4.73μkat/g,酪蛋白浓度5%,pH9.5,37℃反应2.9h;交联后酪蛋白的乳化性和乳化稳定性分别提高了10%和6%,制作的凝胶微观结构更紧密、一致[20]。
4 展望
转谷氨酰胺酶是蛋白交联中研究最深入、应用最广的一种酶,已进行商业化生产。相比而言,多酚氧化酶由于来源得不到保障,对蛋白交联方面的研究相对较少,但也取得了一定的成绩,具有广阔的开发应用前景。而过氧化物酶交联蛋白方面的报道较少。
目前,酶法交联食物蛋白方面的研究主要集中在交联后蛋白功能特性的改变,而对蛋白的营养特性研究较少,交联后蛋白在体内的消化吸收情况有待于进一步深入的研究。另外,交联后蛋白功能特性改变的机理尚不明确,交联后蛋白结构的改变与功能特性的关系有待于进一步研究。
[1]杨晓泉.大豆蛋白的改性技术研究进展[J].广州城市职业学院学报,2008,2(3):37-44.
[2]Singh H.Modification of food proteins by covalent crosslinking[J].Trends in Food Sci Technol,1991,2:196-200.
[3]张红.蛋白质交联研究概况[J].粮食与油脂,2004,12: 16-19.
[4]Kuraishi C,Yamazaki K,Susa J.Transglutaminase:Its utilization in the food industry[J].Food Reviews Int,2001,17: 221-246.
[5]Chambi H,Grosso C.Edible films produced with gelatin and casein cross-linked with transglutaminase[J].Food Res Int,2006,39(4):458-466.
[6]刘心伟,吕加平,范贵生.微生物转谷氨酰胺酶在食品工业中的研究进展[J].内蒙古农业大学学报,2005,26(4): 54-57.
[7]O’Sullivan M M,Lorenzen P C,O’Connell J E.Influence of transglutaminase on the heat stability of milk[J].Dairy Sci,2001,84:1331-1334.
[8]Marton P B,Manfred H,Kerstin W.Transglutaminase crosslinking of milk proteins and impact on yoghurt gel properties[J]. Int Dairy J,2007:1-12.
[9]Ozer B,Kirmaci H A,Oztekin S,et al.Incorporation of microbial transglutaminase into non-fat yogurt production[J].Int Dairy J,2007,17:199-207.
[10]Onwulata C I,Tomasula P M.Gelling properties of tyrosinase-treated dairy proteins[J].Food Bioprocess Technol,2010(3): 554-560.
[11]Burzio L A,Burzio V A,Pardo J,et al.In vitro polymerization of mussel polyphenolic proteins catalyzed by mushroom tyrosinase[J].Comp Biochem Phys B:Biochem Mol Biol,2000,126(3): 383-389.
[12]Takasaki S,Kawakishi S,Murata M,et al.Polymerisation of gliadin mediated by mushroom tyrosinase[J].LWT,2001,34 (8):507-512.
[13]Thalmann C L,Lötzbeyer T.Enzymatic cross-linking of proteins with tyrosinase[J].Europ Food Res Technol,2002,214 (4):276-281.
[14]吴进菊,高金燕,刘潇,等.双孢蘑菇多酚氧化酶交联作用对酪蛋白乳化性及其稳定性的影响[J].食品科学,2010,31 (15):117-120.
[15]Dabbous M K.Inter-and intramolecular cross-linking in tyrosinase-treated tropocollagen[J].J Biol Chem,1966,241 (22):5307-5312.
[16]Mattinen M-L,Lantto R,Selinheimo E,et al.Oxidation of peptides and proteins byTrichoderma reeseiandAgaricus bisporustyrosinases[J].J Biotechnol,2008,133(3):395-402.
[17]Monogioudi E,Creusot N,Kruus K,et al.Cross-linking of b-casein byTrichoderma reeseityrosinase andStreptoverticillium mobaraensetransglutaminase followed by SEC-MALLS[J].Food Hydrocolloid,2009,23:2008-2015.
[18]Matheis G,Whitaker J R.Peroxidase-Catalyzed Cross Linking of Proteins[J].J Protein Chem,1984,3(1):35-48.
[19]Steffensen C L,Mattinen M L,Andersen H J,et al.Crosslinking of tyrosine-containing peptides by hydrogen peroxideactivatedCoprinus Cinereusperoxidase[J].Eur Food Res Technol,2008,227(1):57-67.
[20]LI J,ZHAO X.Oxidative cross-linking of casein by horseradish peroxidase and its impacts on emulsifying properties and the microstructure of acidified gel[J].Afr J Biotechnol,2009,8(20):
5508-5515.
Research progress on modification of food proteins by enzymatic cross linking
WU Jin-ju,TANG Shang-wen,HUANG Sheng-mou,HUO Yin-qiang
(College of Chemical Engineering and Food Science,Xiangfan University,Xiangfan 441053,China)
Inter-and intramolecular cross-linking of food proteins can modify their functional properties,which are useful to application in food processing.The enzymes which can be used for protein cross linking are transglutaminase,polyphenol oxidase and peroxidase.Reaction principle of transglutaminase,polyphenol oxidase and peroxidase generated cross-linking of proteins,as well as the latest progresses,were Illustrated.
cross-linking;food proteins;polyphenol oxidase;transglutaminase
TS201.2+1
A
1002-0306(2011)11-0511-03
2011-03-23
吴进菊(1983-),女,讲师,研究方向:食品生物技术。

