橙皮果胶的提取及性质研究
夏天添,梁瑞红,刘成梅,刘 伟,冯 静,陈 军
(南昌大学食品科学与技术国家重点实验室,江西南昌 330047)
橙皮果胶的提取及性质研究
夏天添,梁瑞红,刘成梅*,刘 伟,冯 静,陈 军
(南昌大学食品科学与技术国家重点实验室,江西南昌 330047)
以脐橙皮为原料,经酸洗法处理后,以酸法提取橙皮果胶。通过单因素及正交实验确定果胶提取的最佳工艺为:料液比1∶25(m∶V),提取pH1.7,提取温度85℃,提取时间100min。最佳醇沉条件:果胶提取液与乙醇的体积比1∶2,提取pH3.5。提取的果胶,提取率为21.816%,半乳糖醛酸含量为70.66%,酯化度为72.49%。其他性质如水分(9.71%)、灰分(3.26%)和pH(2.93)等均满足国标要求,表明该方法适宜用于从橙皮中提取果胶。
橙皮,果胶,提取,性质
果胶是一种高分子聚合物,是植物细胞壁的组成成分,为白色、浅黄色到黄色的粉末,无固定熔点和溶解度,不溶于乙醇等有机溶剂[1-2]。果胶分子平均每100个半乳糖醛酸残基C6位上以甲酯化形式(带有甲氧基)存在的百分数称为果胶的酯化度(Degree of Esterification,DE);按照酯化度不同,通常可分为高酯果胶(High Methoxyl Pectin,HM)(DE>50%,甲氧基含量>7%)和低酯果胶(Low Methoxyl pectin,LM)(DE<50%,甲氧基含量<7%)[3-6]。果胶具有非常好的胶凝性和乳化稳定作用,且安全无毒,被广泛应用于食品、药品、化妆品等,作为稳定剂、乳化剂和增稠剂[7]。国内外对果胶的需求量都在不断增加,而我国每年从国外进口大量果胶[8],由此可见,发展果胶生产在国内市场有着十分广阔的前景。我国的橙子种植面积广大,随着食品加工业的发展,产生了大量的橙皮资源[9]。而浪费严重、转化率低和处理不当所引发的环境污染等问题,亟待解决。本研究探讨在预处理后,酸法提取赣南脐橙皮果胶的最佳工艺条件,并对所得产品进行了理化性质的分析,为橙皮的处理和利用提供了一种绿色、高效、简便、易行的方法。
1 材料与方法
1.1 材料与仪器
兴国-28脐橙 由江西某厂提供;苹果果胶、柑橘果胶、间羟基联苯、半乳糖醛酸 Sigma公司,分析纯;溴化钾 阿拉丁公司,光谱纯;盐酸、氢氧化钠、硫酸、硼砂、无水乙醇 国产,分析纯。
AR224CN 电子天平 美国 Ohaus公司; SevenMulti型 pH/电导率/离子综合测试仪 瑞士Mettler Toledo公司;Du640紫外可见分光光度计 美国Beckman Coulter公司;Nicolet FT-IR 5700型傅里叶红外光谱仪 美国Thermo Electron公司;TDL5A飞鸽牌离心机 上海安亭仪器厂;DHG-9145A电热恒温鼓风干燥箱 上海一恒仪器有限公司;HR83 (P)型水分测定仪 上海梅特勒-托利多仪器有限公司;QL-861微型旋涡混合器 海门市其林贝尔仪器制造有限公司;DV-III数字流变仪 BROOKFIELD公司。
1.2 实验方法
1.2.1 标准溶液配制 半乳糖醛酸标准溶液配制∶称取干燥至恒重的半乳糖醛酸25mg,加水溶解并定容至500mL,混匀,成0.05mg/mL的标准溶液。
0.15%间羟基联苯溶液∶称取0.15g间羟基联苯溶于5mg/mL氢氧化钠溶液中,定容至100mL,其质量浓度为1.5mg/mL。
四硼酸钠/硫酸溶液∶四硼酸钠溶解在浓硫酸中形成0.0125mol/L的溶液,备用。
1.2.2 工艺流程 原料→预处理→烘干→粉碎→提取→离心→沉淀→烘干→粉碎→筛分→成品
1.2.3 操作要点
1.2.3.1 原料预处理 新鲜橙皮切成3cm×3cm的小块后,分成三份。第一份直接在65℃烘干20h,粉碎;第二份用沸水漂烫10min后,65℃烘干20h,粉碎;第三份以一定量比例在调好pH的盐酸水溶液中浸泡、挤干,重复三次,65℃烘干20h,粉碎[10]。
1.2.3.2 果胶提取 预处理好的原料,按一定的质量体积比加入蒸馏水,用1∶1的盐酸调溶液的不同pH,水浴加热反应一段时间后,取出离心得上层果胶溶液待用。
1.2.3.3 乙醇沉淀 向固定体积的几份果胶液中加入不同体积的无水乙醇,并调节pH,以提取率为标准确定果胶醇沉的最佳工艺条件。以提取液与乙醇体积比表示,取1∶1,1∶1.5,1∶2,1∶2.5的条件进行比较。得到最优结果后,再调节乙醇的pH至3.0~4.0,以提取率和GA%衡量最佳醇沉条件。
1.2.4 果胶提取条件的确定 通过单因素实验,初步确定提取果胶的最佳料液比、提取pH、提取温度、提取时间。并在此基础上,建立4因素3水平正交实验L9(34)(见表1),以果胶提取率为指标,确定最佳提取工艺。
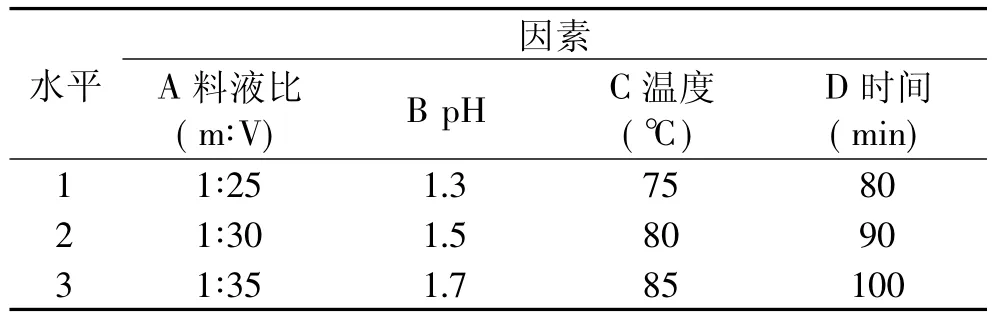
表1 正交实验因素水平表L9(34)
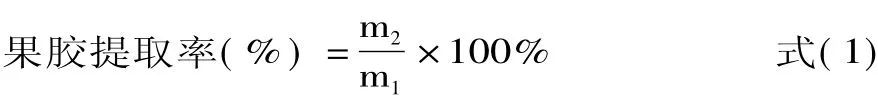
式中∶m1-橙皮粉质量(g);m2-果胶产品质量(g)。
1.2.5 果胶的红外光谱分析 把果胶研成粉末,与KBr混合压片制样,采用傅立叶红外光谱仪对样品在400~4000cm-1区内进行红外光谱分析[11-12]。
1.2.6 半乳糖醛酸含量(GA)的测定
1.2.6.1 标准曲线的制备 取标准溶液0.00,0.20,0.40,0.60,0.80,1.00mL置于具塞试管中,加蒸馏水补足至1.00mL。在冰浴中预冷后,加5.0mL四硼酸钠/硫酸溶液,用旋涡混合器混合后沸水浴5min,再冰浴冷却至室温,再加100μL间羟联苯混匀后在524nm处测吸光度,制作标准曲线[13],见图1。
1.2.6.2 测定 取1.00mL样品溶液,过程同上。最后为避免样品中半乳糖醛酸成分与四硼酸钠/硫酸试液反应的干扰,做一组对照,以100μL氢氧化钠溶
称量后果胶提取率计算如公式(1)所示。
计算公式∶
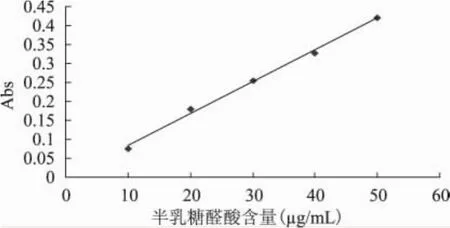
图1 间羟基联苯法制作的标准曲线图

式中∶m1-果胶产品质量(g);m2-半乳糖醛酸质量(g)。
1.2.7 果胶酯化度、水分、灰分、pH的测定
1.2.7.1 果胶酯化度 采用FCC滴定法测定果胶酯化度[14]。
1.2.7.2 水分 参考GB25533-2010测定果胶水分(以干燥失重计)。
1.2.7.3 灰分 参考QB2484-2000测定果胶总灰分含量。
1.2.7.4 pH 参考GBn246-85测定0.1%果胶溶液的pH。液代替100μL间羟基联苯,其他过程一样,测定吸光度,从样品吸收值中扣除。从标准曲线上查出半乳糖醛酸浓度(μg/mL)。
果胶纯度计算如公式(2)所示。
2 结果与讨论
2.1 三种前处理方法的比较结果
如表2所示,漂烫处理和酸洗法处理过的橙皮,提取率较高,而未经任何前处理直接烘干的橙皮,提取率比前两种低了近2.3%。三种方法分别处理的果胶,在半乳糖醛酸含量上也有很大的差异,由高到低依次是酸洗法>直接烘干>漂烫法。在25℃相同浓度的条件下分别测定了三种处理方法得到的果胶溶液的粘度随剪切速率的变化情况。从图2中可以看出,三种果胶的粘度都随着剪切速率的增大而逐渐降低,在15s-1后基本不变,溶液趋向于牛顿流体。而在剪切速率为2.5s-1时,酸洗法得到的果胶粘度达到60MPa·s,直接烘干得到的果胶粘度为48MPa· s,而漂烫法得到的果胶粘度仅为32MPa·s,可以看出酸洗法得到的果胶粘度好于其他两种处理方法。实验结果与专利CN 1703429A中所述一致,分析原因,可能是pH的选择使橙皮中的天然果胶酯酶失活,从而使得橙皮的脱酯化降到最低,分子量增大,因而也就使得果胶的粘度增大。在同等条件下具有较高的半乳糖醛酸含量和粘度值的果胶拥有更好的凝胶特性,所以综合考虑提取率、半乳糖醛酸含量和粘度值,本研究采用酸洗法来处理橙皮。
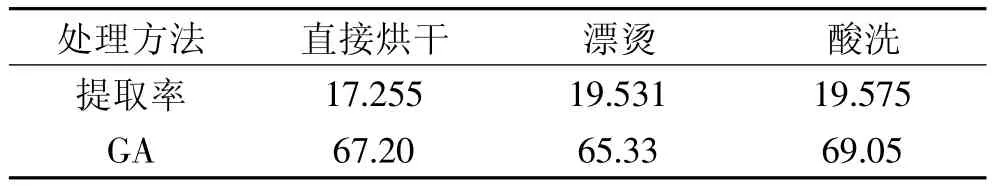
表2 不同前处理方法得到的果胶比较(%)

图2 不同前处理方法对果胶粘度的影响
2.2 果胶提取的正交方案及结果
由表3可知,因素A、D、B较显著,各因素对提取率的主次顺序是A>D>B>C,即料液比>时间>pH >温度。最佳工艺组合为A1D3B3C3即果胶提取工艺最佳条件为∶料液比1∶25,提取pH1.7,提取温度85℃,提取时间100min。做验证实验(n=3),果胶提取率 21.816% 得率较高,因此确定最优组合为A1B3C3D3。

表3 正交实验结果与分析
2.3 醇沉条件的选择
向固定体积的提取液中,加入不同体积的乙醇对果胶的提取率和GA有比较大的影响,随着乙醇体积的增大,提取率逐渐升高,而半乳糖醛酸含量在提取液与乙醇体积比为1∶2时最大。在醇沉pH3.0~4.0范围内,果胶得率随pH的增加而提高,而半乳糖醛酸含量在pH3.5时最高。据报道,果胶作为带电多糖也具有离解系数[15],因此,通过控制醇沉时的pH可以提高果胶的得率。通过实验,综合提取率与GA%两个参数,确定乙醇沉淀的最佳条件为体积比1∶2,pH3.5。
2.4 果胶的红外光谱分析结果
提取橙皮果胶的红外光谱分析见图3。在1000~2000cm-1之间的吸收峰是鉴定果胶主要化学官能团及提供用于比较不同类型果胶结构信息的特征峰。其中1650cm-1处是自由羧基官能团吸收峰,1750cm-1处是酯化羧基官能团吸收峰,这两个特征吸收峰的存在,可说明所得到的为果胶,果胶在1750cm-1处的特征峰还可用来区分果胶为高酯果胶还是低酯果胶。
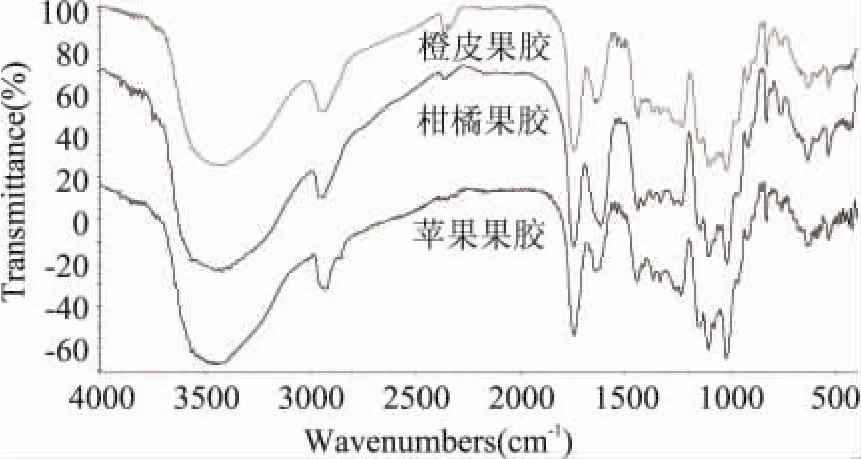
图3 三种果胶的红外光谱图
本研究提取的橙皮果胶与苹果果胶及柑橘果胶的红外光谱如图3所示。所得到的果胶在1748cm-1处的吸收很强,因此,橙皮果胶为高酯化度果胶,果胶的酯化度的化学分析也证明这一点,数据如下∶1100~1200cm-1之间的两个特征峰是R-O-R键和环C-C键的吸收峰;在1245cm-1处的特征峰是C-O-C键的伸缩振动峰,它表明有甲氧基存在。
Singthong等以已知酯化度果胶为材料进行红外光谱扫描,探讨采用红外光谱计算果胶酯化方法[12],结果发现在A1730/(A1730+A1630)与果胶酯化度之间存在明显线性关系,相关系数R2=0.9852,其中A为峰面积。以此式计算得本研究所得橙皮果胶的酯化度为70.22%。
2.5 果胶的理化性质
以D-半乳糖醛酸浓度为横坐标,吸光度为纵坐标绘制标准曲线,计算其回归方程为∶y=0.0084x-0.0009,相关系数R2=0.9985,测定样品果胶半乳糖醛酸含量为70.66%(n=3),满足国标要求。
用滴定法测得的样品果胶的酯化度平均值为72.49%(n=3),与红外图谱计算得到的酯化度70.22%,两者间相对误差小于5%,可相互验证。因赣南橙皮果胶的酯化度高于50%,该果胶属于高酯果胶。
在105℃下放置2h,用快速水分测定仪测得果胶的干燥失重最大为10.06%,样品的平均干燥失重为9.71%,低于GB25533-2010所规定的12%。果胶灰分最大值为3.57%,样品的平均灰分为3.26%,也低于QB2484-2000中规定的5%的灰分值,pH2.93也满足GBn246-85中要求的2.8±0.2。
3 结论
通过研究确定三种前处理方法中,酸洗法处理后的新鲜橙皮提取得到的果胶,提取率更高,品质更好。橙皮果胶提取的最佳工艺条件为∶料液比1∶25,提取pH1.7,提取温度85℃,提取时间100min。乙醇沉淀的最佳条件为∶提取液与无水乙醇的体积比1∶2,pH为3.5。果胶产品的提取率为21.816%,半乳糖醛酸含量为70.66%,酯化度为72.49%,水分、灰分和pH均满足国标要求。本实验筛选出的工艺条件生产的果胶品质好,提取率较高,方法简单易行。为橙皮的利用和发展提供了一项变废为宝的方法,同时有着十分广阔的市场前景。
[1]Kalapathy U,Proctor A.Effect of acid extraction and alcohol precipitation conditions on the yield and purity of soy hull pectin[J].Food Chemistry,2001,73(4):393-396.
[2]赵利,王彬.果胶的制备及其在食品工业的应用综述[J].食品科技,1999(5):32-34.
[3]Masmoudi M,Besbes S,Chaabouni M,et al.Optimization of pectin extraction from lemon by-product with acidified date juice using response surface methodology[J].Carbohydrate Polymers,2008,17(2):271-275.
[4]Pellerin P,Neil M A O'.The interaction of the pectin polysaccharide Rhamnogalacturonan II with heavy metals and lanthanides in wines and fruit juices[J].Analysis,1998(26): 32-36.
[5]孙元琳,汤坚.果胶类多糖的研究进展[J].食品与机械,2004,29(6):60-64.
[6]邸铮.苹果皮渣中果胶的提取及性质研究[M].北京:中国农业大学,2006.
[7]郭飞燕,纪明慧,舒火明,等.海南菠萝蜜果胶的提取工艺研究[J].食品工业科技,2008,29(5):212-214.
[8]张泽生,徐慧,张兰,等.辣椒果胶的提取工艺研究[J].食品工业科技,2010,31(9):212-214.
[9]毕双同.赣南脐橙皮果胶的提取工艺及其性质研究[D].南昌:南昌大学,食品科学与工程学院,2008.
[10]CP凯尔科有限公司.含有果胶的植物材料的改进处理方法[P].中国:CN 1703429A,2005-11-30.
[11]仇农学,田玉霞,邓红,等.超滤法分离苹果果胶及其理化性质[J].中国农业科学,2009,42(10):3609-3616.
[12]Singthong J,Cui S W,Ningsanond S,et al.Structural characterization,degree of esterification and some gelling proerties of Krueo Ma Noy(Cissampelos pareira)pectin[J].Carbohydrate Polymers,2004,58(4):391-400.
[13]高林,施秀芳,张文博,等.MCP中糖醛酸的含量测定[J].化学工业与工程,2005,22(6):487-489.
[14]杨大川.从柑桔皮中提取果胶[J].食品科学,1983(11): 39-42.
[15]周祖康,顾惕人,马季铭.胶体化学基础[M].北京:北京大学出版社,1987.
Study on extraction and properties of pectin from the peel of orange
XIA Tian-tian,LIANG Rui-hong,LIU Cheng-mei*,LIU Wei,FENG Jing,CHEN Jun
(State Key Laboratory of Food Science and Technology,Nanchang University,Nanchang 330047,China)
Using peel of orange as the material,pectin was extracted by acid extraction method.Through factor analysis method and orthogonal experimental,the optimal process conditions were shown as follows∶ratio(solid∶liquid)1∶25(m∶V),extracting solution pH1.7,extracting temperature 85℃,extracting time 100min,precipitated with ethanol in the ratio 1∶2 at pH3.5,and the resulting extraction yield was 21.816%.Analyzing the properties of the pectin,galactose-uronic acid,degree of methoxylation,moisture,ash content,and pH of solution were 70.66%,72.49%,9.71%,3.26%,and 2.93,respectively.All the parameters reached the Chinese standard.The method was suitable for the exaction of pecttion from the peel of orange.
peel of orange;pectin;extraction;property
TS255.1
B
1002-0306(2011)11-0234-03
2011-08-25 *通讯联系人
夏天添(1986-),女,硕士研究生,研究方向:食品质量与卫生。
国家重点实验室目标导向项目(SKLF-MB-201004)。

