甲型H1N1流感病毒感染小鼠的发病机制
鲍琳琳,孙惠惠,占玲俊,许黎黎,邓 巍,李枫棣,吕 琦,朱 华,秦 川
(中国医学科学院医学实验动物研究所,卫生部人类疾病比较医学重点实验室,国家中医药管理局人类疾病动物模型三级实验室,北京 100021)
甲型H1N1流感病毒感染小鼠的发病机制
鲍琳琳,孙惠惠,占玲俊,许黎黎,邓 巍,李枫棣,吕 琦,朱 华,秦 川
(中国医学科学院医学实验动物研究所,卫生部人类疾病比较医学重点实验室,国家中医药管理局人类疾病动物模型三级实验室,北京 100021)
目的 甲型H1N1流感病毒A/California/7/2009感染BALB/c小鼠,研究甲型H1N1流感病毒病毒性肺炎发病机制。方法 4~6周龄雌性BALB/c小鼠60只,随机分为2组,实验组和对照组,每组30只。CA7流感病毒滴鼻制备甲流病毒感染小鼠模型。攻毒后第5天解剖实验和对照组小鼠,取肺组织,测定肺组织中IL-2,IL-6,TNF-α含量。结果 结果实验组肺组织中IL-6,TNF-α,水平明显高于对照组,IL-2水平明显低于对照组,差异均有显著性(P<0.05)。结论 IL-6、TNF-α、IL-2这3种细胞因子在感染甲流病毒后的显著性变化与病毒感染后的肺组织病理损伤有密切的关系。
A/California/7/2009;BALB/c小鼠;发病机制;细胞因子
研究证明细胞因子在呼吸道合胞病毒(RSV)等病毒性肺炎发病中发挥重要作用。有研究报道通过流感病毒感染人体实验发现,呼吸道局部和血清中IL-6、TNF-α水平,与临床症状密切相关。IL-2本身无直接抗病毒作用,它能刺激T细胞产生多种淋巴因子,诱导杀伤细胞产生IFN-γ等细胞因子,而起到抗病毒作用。为研究H1N1甲型流感病毒的病原特性、致病机理建立了小鼠感染甲型H1N1病毒的动物模型。本研究应用双抗体夹心酶联免疫吸附法(ELISA)对甲型H1N1流感病毒感染模型小鼠肺组织 IL-2、IL-6、TNF-α水平进行检测,以明确其与小鼠的病毒性肺炎的发生是否存在相关性及其意义。
1 材料和方法
1.1 病毒
H1N1病毒株为 A/California/7/2009。经无特殊病原体(specific pathogen free,SPF)鸡胚增殖后收集病毒尿囊液,TCID50为107。-80℃储存备用,实验均在生物安全Ⅲ级实验室中进行。
1.2 动物
实验动物均选用SPF级雌性BALB/c小鼠,4~6周龄(体重14~16 g)。由中国医学科学院医学实验动物研究所提供(许可证号:SCXK(京)2004-0001)。
1.3 实验仪器和试剂
RVC-Ⅱ型独立送风隔离笼具 Tecniplast公司;AMV反转录酶及 RNA酶抑制剂购自 Promega公司;Taq plus DNA聚合酶及dNTP购自TaKaRa公司。ELISA试剂盒R&B公司。
1.4 感染小鼠
实验在本所的BSL-3实验室中进行。将60只4~6周龄雄性BALB/c小鼠随机分为对照组和实验组。每组30只,每笼5只。标记后分别称重。将小鼠乙醚吸入麻醉后,106TCID50病毒液通过滴鼻途径感染小鼠,每只小鼠的接种剂量为50 μL,对照组小鼠经鼻腔滴入等量的生理盐水。独立送风隔离笼具中正常饲养。实验的观察期为14 d。其中每组20只感染第5天处死,处死后取肺组织做进一步机制研究。
1.5 观察指标
每日观察记录小鼠的活动状态及临床表现,称量体重。感染小鼠第5天处死后取肺组织,做病毒载量测定。肺组织用夹心法测定 IL-2、IL-6、TNF-α,IFN-γ细胞因子。肺组织病理检查用甲醛固定、石蜡包埋、常规HE染色,光镜下观察其病理变化。称量每只死亡小鼠的体重及肺脏湿重,计算其肺指数(肺脏湿重/小鼠体重)。
1.6 检测方法
1.6.1 细胞因子检测:感染小鼠第5天放血处死,每组各取10只,取全肺,在低温条件下,按常规方法制作肺组织匀浆后取上清液,检测采用双抗体夹心ABC-ELISA法测肺组织细胞因子 TNF-α、IFN-γ、IL-2、IL–6的蛋白表达。
1.6.2 肺组织病毒载量测定:根据中国CDC公布的H1N1亚型禽流感病毒核蛋白基因的保守序列设计一对引物:SW-H1 F786:5’-AATAACATTAGAA GCAACTGG-3’;SW-H1 R920:5’-AGGCTGGTGTT TATRGCACC-3’。扩增片段的大小为134 bp。常规方法提取 RNA,并进行反转录。将反转录产物5 μL,加至 25 μL PCR 反应体系中,瞬时离心后置ABI Step One PCR仪进行扩增。扩增条件:35循环,94℃ 30 s变性,59℃ 30 s退火,72℃ 60 s延伸。95℃,15 s;60℃,1 min,60℃ ~ 95℃ 每 0.3℃ 记录Tm值,记录溶解曲线。
1.7 数据统计方法
小鼠的体重变化用体重百分比表示,即以小鼠当天体重减去其前1 d体重的差值作分子,以其前1 d的体重作分母,记录为平均体重变化百分比±标准差,数值采用每组的平均数。小鼠的平均存活天数(MSD)按照公式:MSD=Σ[f(d-1)]/n计算,其中d为天数,f为第n天幸存的小鼠数目,n为每组的小鼠数目。数据以均数±标注差表示,实用软件SOSS15.0对组间差异应用t检验分析。
2 结果
2.1 甲流病毒感染对小鼠生存质量的影响
甲型流感病毒感染小鼠后第3天,实验组小鼠体重就开始下降,体重下降最多达17.0%。感染后第3天开始出现竖毛,摄食量下降,活动度下降,严重。小鼠在感染后第3~4天开始死亡,感染8 d后10只小鼠全部死亡。对照小鼠未见异常。感染后的小鼠肺指数与对照组比较明显增加。感染后的小鼠存活情况,体重变化,及肺指数变化(表1)。
2.2 甲流病感染小鼠肺组织病毒复制
甲流病毒感染后的小鼠,第5天处死,取肺组织做病毒载量分析。结果显示小鼠感染后肺组织的病毒载量在(5.7±0.17)log10 copies/mg(表2)。
2.3 实验组与对照组小鼠血清IL-2、IL-6和INF-γ水平
各细胞因子水平在攻毒变化显示,实验组较对照组 IL-6、IFN-γ明显升高(P <0.01),IL-2明显降低(P<0.05)(表2)。
2.4 甲流病毒感染小鼠病理组织学观察
实验组小鼠支气管肺组织病理表现是毒性肺炎特点。剖检可见感染小鼠肺脏有明显充血和水肿,肺体积变大,肺组织表面有局部轻度实变,呈斑点状充血。光镜下主要改变是肺组织肺泡间隔不同程度增宽,肺内小血管及肺泡间隔的毛细血管扩张、淤血,肺泡腔不同程度缩小,可见中等量淋巴细胞和单核细胞浸润(图1,见彩插2)。
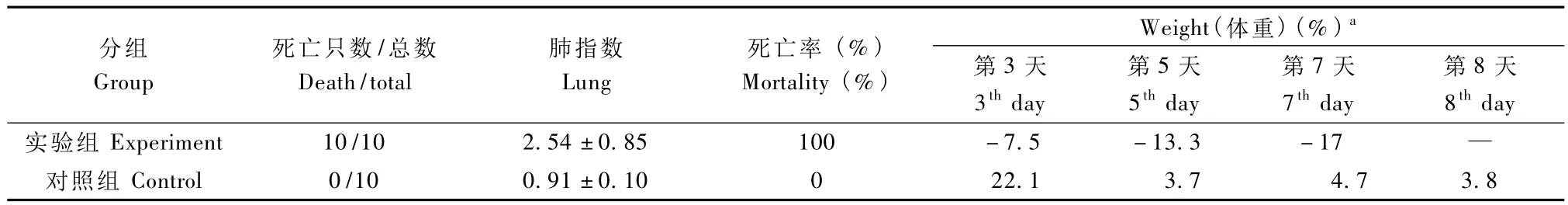
表1 小鼠感染CA7流感病毒结果Tab.1 Results of mice infected with CA7 virus

表2 小鼠感染CA7流感病毒细胞因子变化Tab.2 Virus loads and cytokines in the lung of mice infected with CA7 virus
3 讨论
感染甲型H1 N1流感病毒小鼠肺组织组织病理呈间质性肺炎变化[1-2]。09年爆发的甲型H1N1流感传播速度快感染人群多,感染的人群多,病患多以上呼吸道感染为主要症状,严重者发展成为间质性肺炎,病死率在0.1% ~0.2%之间。既往研究证明流感病毒感染可波及肺间质和肺泡而引起肺炎,细胞因子在其发病中有重要作用[3]。病毒感染后通过细胞因子的诱导作用,激活内皮细胞和粒细胞,继而调节黏附分子的合成及其在细胞表面的表达。TNF-α是一种由巨噬细胞产生的基因多显性的细胞因子,其生物活性均通过细胞表面的特异受体传递信号。TNF-α水平升高时[4],可介导炎性反应的许多病理生理过程,引起局部炎性反应、器官的损害、甚至系统的损害。它可刺激单核细胞、内皮细胞等分泌 IL-6、IL-1进入血液循环[5],诱导中性粒细胞的趋化作用和局部浸润,吞噬和杀伤病原体,从而启动炎性反应。本研究实验组小鼠血清TNF-α水平明显升高,说明甲流发病中,TNF-α是重要的炎性介质,发挥了重要作用。IL-6是一种多组织亲和性的细胞因子,调节炎性反应有关的多种过程,由单核巨噬细胞及内皮细胞产生,还可被TNF-α、IL-1诱导及多种细胞产生,在肺炎支原体感染时,IL-6的产生、释放异常,IL-6参与整个炎性反应部位的炎性损伤。IL-2主要由CD4+T细胞产生,此外CD8+T细胞和 NK细胞也可产生[6]。在小鼠,主要由Th1亚群产生。IL-2本身无直接抗病毒作用,它能刺激T细胞产生多种淋巴因子,诱导 CTL、NK、LAK等多种杀伤细胞的分化和效应功能,诱导杀伤细胞产生IFN-γ等细胞因子,而起到抗病毒作用。病毒感染后,IL-2水平降低,引起机体免疫功能的抑制和失调[7-8]。本实验中,在人工感染后的第 5天,IL-2水平降低,进一步引起机体免疫功能的抑制和失调。IL-6表达水平上升,发挥其刺激局部炎性反应,促进组织破坏作用。TNF-α水平升高,引起局部炎性反应、器官的损害。提示它们之间是相互诱导、相互协同、共同参与甲流病毒感染的发生、发展过程。
[1] 鲍琳琳,孙惠惠,占玲俊,等.A/California/7/2009与 A/California/4/2009病毒感染力比较[J],中国比较医学杂志,2010:20(1):6-9.
[2 ] Bao L,Xu L,Zhan L,et al.Challenge and polymorphism analysis of the novel A(H1N1)influenza virus to normal animals[J].Virus Res.2010,151(1):60-65.
[3] 孙惠惠,邓巍,占玲俊,等.板蓝根颗粒对甲型流感病毒小鼠的作用.[J]. 中国比较医学杂志,2010,20(7):54-57.
[4] Hussell T,Pennycook A,Openshaw PJ.Inhibitionoftumor necrosisfactor reduces the severity ofvirus-specific lung immunopathology[J].Eur J Immunol,2001,31(9):2566-2573.
[5 ] Helen C,Su Leslie P,CousensL D,et al.CD4+and CD8+T cell interactions in IFN-γ and IL-4 responses to viral infections:requirements for IL-2[J].J Immunol,1998,160:5007-5017.
[6] MacMicking J,Xie QW,Nathan C.Nitric oxide and macrophage function[J].Annu Rev Immunol,1997,15:323-350.
[7] 杨贵贞.医学免疫学[M].长春:吉林科学技术出版社,1995:45,83.
[8] 史利卿,邱全瑛,吕燕宁,等.宣肺解毒颗粒剂对流感病毒肺炎小鼠血浆中细胞因子水平的影响[J].北京中医药大学学报,1998,21(4):23-25.
Pathogenesis of Influenza A(H1N1)Virus in Infected Mice
BAO Lin-lin,SUN Hui-hui,ZHAN Ling-jun,XU Li-li,DENG Wei,LI Feng-di,LV Qi,ZHU Hua,QIN Chuan
(Key Laboratory of Human Diseases Comparative Medicine,Ministry of Health;Institute of Medical Laboratory Animal Science,Chinese Academy of Medical Sciences;Key Laboratory of Human Diseases Animal Models,State Administration of Traditional Chinese Medicine,Beijing 100021,China)
Objective To study the mechanism of the influenza virus infection in BALB/c mice with A/California/7/2009Influenza H1N1 virus.Methods Sixty BALB/c mice were randomly divided into 2 groups:experimental group and control group,each group consisted of 30 mice.The CA7 influenza virus was used to establish influenza models.The expressions of lung IL-6,TNF-α,and IL-2 in experimental group of 5thday control group were detected by enzyme linked immunosorbent assay(ELISA).Results The lung tissue IL-6,TNF-α levels were significantly higher,IL-2 levels were significantly lower than that in the control group,the differences were significant(P <0.05).Conclusions The cytokines IL-2,IL-6 and TNF-α may participate in the whole process of influenza A H1N1 virus infection and their lung levels are positively correlated with the severity of the disease.
A/California/7/2009;BALB/c mice;cytokine;mechanism
R33
A
1671-7856(2011)02-0020-03
2010-10-12
10.3969/j.issn.1671.7856.2011.02.05
科技重大专项-艾滋病和病毒性肝炎等重大传染病防治:2009ZX10004-402,009ZX10004-016;卫生公益性行业科研专项项目:200802036;中央级公益性科研院所基本科研业务费:DWS200810。
鲍琳琳,助理研究员,研究方向:病毒学。
秦川,教授,博士生导师。E-mail:chuanqin@vip.sina.com。

