LaCoO3掺杂Ba和Fe催化分解NO的研究
许树军,朱宇君,李 丽,鲁国明 袁福龙
(1.黑龙江中医药大学 教学实验中心,哈尔滨 150040;2.黑龙江大学 化学化工与材料学院,哈尔滨 150080)
0 引 言
空气中NO其主要来源于汽车内燃机的排放和含氮燃料高温下直接燃烧。NO无论对环境还是对人体都会产生很大的危害,因此国内外对消除NO进行了大量的研究[1]。
本文探讨LaCoO3的A位掺杂Ba元素对氧空位的影响,B位掺杂Fe对Co元素的影响,以及B位元素的协同作用与催化分解NO的关系。
1 实验部分
1.1 催化剂的制备
按化学计量比准确称取La(NO3)3◦6H2O,Co(NO3)2◦6H2O和Ba(NO3)2,Fe(NO3)3◦9H2O加水溶解。称取与金属离子等物质量的柠檬酸加水溶解,加热。将混合硝酸盐滴加到柠檬酸溶液中,加热搅拌浓缩,置于烘箱中得干凝胶。把所得前驱体置于马弗炉中在450℃和900℃分别焙烧4 h和6 h,得到催化剂粉体。
1.2 催化剂的表征
X射线衍射 (XRD)测试仪为日本理学公司生产的D/MAX-ⅢB型X-射线衍射仪,Cu Kα射线。比表面积 (BET)测定采用北京市北分仪器技术公司生产的ST2000比表面孔径测定仪,以氢气做吸附剂。氢气程序升温还原 (H2-TPR)测定在自制仪器上进行,热导池 (TCD)为检测器,(0.025 g)催化剂,以5%H2/N2混合气为还原气(流量25 mL/min),升温速率为10℃/min。傅立叶红外光谱 (FT-IR)测试采用美国PE公司生产的型号为Spectrum One的傅立叶红外光谱测定仪,常温常压,KBr压片,扫描范围为 350~4 000 cm-1,分辨率1 cm-1。X射线光电子能谱(XPS)测试采用Thermo ESCALAB 250电子能谱仪,AlKα射线,分析室真空度4.5×10-9mbar。谱图能量标准以污染碳 (C1s=286.4 eV)作参比。
1.3 NO直接分解的活性测试
NO直接分解反应在固定床反应器中进行,反应管为内径6 mm石英管,催化剂粒度40~60目,催化剂用量为0.50 g,原料气为1%NO(He气平衡),流量为25 mL/min。用配备有5Å分子筛色谱柱的气相色谱仪在线检测NO、O2和N2。各温度点的活性数据都在反应1 h后测得。
2 结果与讨论
2.1 XRD表征
图1给出了 LaCoO3(LC)、La0.8Ba0.2CoO3(LBC)、La0.8Ba0.2Co0.7Fe0.3O3(LBCF73)XRD表征,结果表明样品的主相都是LaCoO3相,没有杂相,并且衍射峰整体向低角度移动。图1同时还给出了它们的衍射角30°~35°放大的XRD曲线,由图1可见,LaCoO3的110晶面的衍射峰为32.94°与标准卡中的 32.91°相差很小,La0.8Ba0.2CoO3110晶面的衍射峰为32.86°,与LaCoO3比较向低角度移动了0.08°,La0.8Ba0.2Co0.7Fe0.3O3110晶面的衍射峰为32.72°,与La0.8Ba0.2CoO3比较向低角度移动了0.14°。在LaCoO3的A位掺入Ba,再掺入Fe,衍射峰都向低角度移动。由布拉格方程dsin2θ=nλ可知,衍射峰向低角度偏移,d值变大,晶面间距变大。这是由于掺入了半径比较大的离子,而使晶格参数变大,晶格膨胀的结果。在LaCoO3的A位掺入Ba,峰形不完好,说明晶面发生严重扭曲,存在大量的氧空位。在La0.8Ba0.2◦CoO3的B位掺入Fe后,峰形比较完好,这说明氧空位含量降低。这一点可从样品的XPS谱图进一步理解。各离子的半径如下[2]497:La3+,106 pm;Ba2+,134 pm;Co3+,63 pm;Fe3+,64 pm。

图1 LC、LBC、LBCF73的XRD谱图Fig.1 XRD patterns of LC、LBC、LBCF73 catalyst
2.2 XPS表征
图2给出了3种氧化物的O1s XPS的谱图及其拟合曲线。据文献报道[3-4],O1s XPS的谱图中通常得到两个峰,低结合能 (Binding Energy)的峰对应表面晶格氧 (O2-),用O(L)表示,高结合能的峰对应表面吸附氧物种 (O-、O-2或O2-2)[1],用O(A)表示。表1给出计算机对O1s XPS的谱图分峰拟合得到的表面吸附氧含量和晶格氧含量,以及晶格氧的半高宽。由表1可见,LaCoO3的A位掺入Ba后,表面吸附氧的含量明显增大,晶格氧谱峰加宽,La0.8Ba0.2CoO3的B位掺入Fe后,La0.8Ba0.2Co0.7Fe0.3O3表面吸附氧的含量又降低了,晶格氧的谱峰又进一步加宽。

图2 LC、LBC、LBCF73的O1s XPS谱图Fig.2 O1s spectra for LC、LBC、LBCF73

表1 LaCoO3,La0.8Ba0.2CoO3,La0.8Ba0.2Co0.7Fe0.3O3的表面氧物种结合能和含量Table 1 Proportion of surface oxygen and binding energy of LaCoO3,La0.8Ba0.2CoO3,La0.8Ba0.2Co0.7Fe0.3O3
在A位掺入Ba元素,由于钡离子的价态低于镧离子,钙钛矿要保持电中性,则会产生A空位或氧空位和B位元素的价态升高[5]。由表1可见,A位掺入少量Ba后,表面吸附氧明显增加,说明氧空位的含量明显增加,同时也伴随Co离子的价态变化,Co3+→Co4+价态升高。在B位掺入Fe后,表面吸附氧降低,氧空位含量降低,是由于Fe-O键的结合能比较大,不易形成氧空位,为了保持电中性必然引起更多的钴离子发生价态变化。晶格氧存在的环境也出现了多样性,从而引起谱峰加宽。
图3给出了Co2p的XPS谱图,由图3可见,Co 2p1/2 and Co 2p3/2不对称光电子峰分别在795.0 and 780.0 eV,差值是15 eV,与Giraudon等人[6]的研究成果相一致,另外在高于Co 2p3/2约10 eV有一弱强度峰,这个卫星峰是低自旋构型的Co3+的特征峰[7]。在 LaCoO3的B位掺入Fe,在高于Co 2p3/2峰约6 eV处存在一个卫星峰,这是Co4+大量存在的特征峰[7]。在 LaCoO3A位掺入Ba,晶体中也存在Co4+,但含量低,所以没有明显的谱峰出现。
为了证明Fe-O键的结合能比较大,氧物种的多样性以及钴元素的价态变化,我们对样品进行了傅立叶红外光谱和H2-TPR的表征。

图3 LC、LBC、LBCF73的 Co2p XPS谱图Fig.3 Co2p spectra for LC、LBC、LBCF73
2.3 FT-IR表征
由图 4可见,3 119 cm-1和 1 400 cm-1左右对应的是水的红外吸收峰,600 cm-1左右对应的是B-O-B键的伸缩振动频率,即ν1(F1u)峰[8]。在LaCoO3中掺入Ba可以使红外光谱谱峰整体发生红移,这是由于掺入Ba后,晶格发生膨胀使B-O键的平均键长增加,键的振动频率降低所致。而在La0.8Ba0.2CoO3B位掺入Fe元素,由于Fe(Ⅲ)离子半径比Co(Ⅲ)离子半径大,掺入Fe元素后,晶胞参数变大,Co-O键的键长增长,导致Co-O键伸缩振动频率降低,而Fe-O键受Co-O键的影响的伸缩振动频率升高,成为重叠峰,所以产生红外吸收谱峰向高频侧位移,谱带劈裂并加宽,肩峰比较明显。
2.4 H2-T PR表征
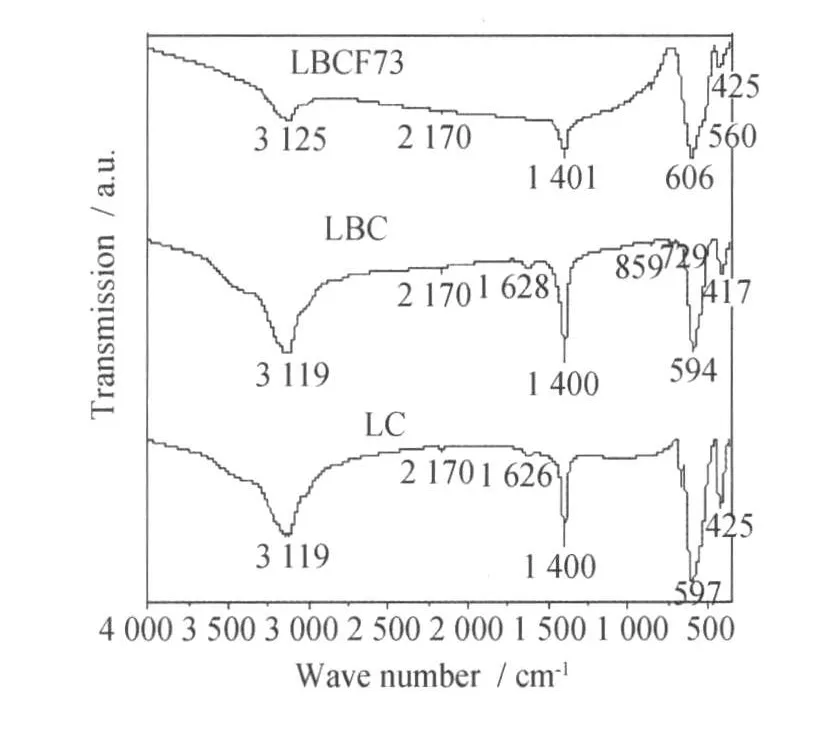
图4 LC、LBC、LBCF73的红外谱图Fig.4 Infrared spectra of LC、LBC、LBCF73
图5给出的是样品的H2-TPR曲线,由图5可见,LaCoO3的峰位置在 450℃,480℃,620℃,这与文献 [8]、文献 [9]一致。在A位掺入Ba和在B位掺入Fe时催化剂被还原的温度明显降低,在300℃左右,而且高温处的还原峰温度和强度都降低,尤其在B位掺入Fe,CoO6-δ晶格氧的还原温度进一步降低,而且都体现出多重峰的特征,这些峰都是钴离子的还原峰。在A位掺入Ba元素,钡离子的半径比镧离子的半径大,钙钛矿结构被扭曲,CoO6-δ八面体变形,出现大量的氧空位等结构缺陷,而导致晶面不完整,氢元素容易攻击氧物种,从而使Co离子容易被还原。在B位掺入Fe元素,由于Fe(Ⅲ)离子半径比Co(Ⅲ)大,而使Co-O键长变大,使Co-O键松懈,晶格氧的活动性增强,还原温度降低。还原峰的多重性是钴离子的存在环境、价态和氧缺陷多样性的结果[10]。在La0.8Ba0.2Co0.7Fe0.3O3中,Fe离子的还原温度比较高,在700℃才开始被还原[10],这进一步说明了Fe-O之间的结合能较大。

图5 LC、LBC、LBCF73的 H2-TPR谱图Fig.5 H2-TPR profiles of LC、LBC、LBCF73
LaCoO3的A位掺入Ba和La0.8Ba0.2CoO3的B位掺入Fe,掺入的都是电负性较小的元素。电负性如下[2]246:La3+,1.10;Ba2+,0.89;Co3+,1.88;Fe3+,1.83。这样相当于增大了Co元素的电负性,增大了Co与配位的氧原子的极化作用,使O2p电子云变形加大,致使从O2p至Co3d的电荷转移能 (△CT)减小,说明Co的3d电子更易于流动,这样氧物种更容易被氢还原[12-13]。无论是表面氧空位吸附氧,还是晶格氧空位吸附的氧以及晶格氧都容易脱附。
2.5 催化分解NO的活性
图6给出的是LC、LBC、LBCF73催化分解NO的活性曲线。由图 6可见,LC、LBC、LBCF73的催化活性随着温度的升高而升高,在La-CoO3的A位掺入Ba,催化活性明显提高,在B位掺入Fe催化活性也有提高。在850℃催化活性达到93.3%。在A位掺杂Ba元素,有利于NO的吸附[4],使钙钛矿的结构产生畸变,产生大量的氧空位,有利于晶格氧的迁移,Co3d电子容易流动,有利于氧的脱附,从而提高了催化活性。在B位掺杂Fe元素,虽然氧空位的含量降低,但是Fe元素与Co元素产生协同作用,使Co-O键松懈,使氧的电子云偏向Co元素,进一步增强了Co3d电子的流动性,更加有利于晶格氧的还原和脱附,从而进一步提高了催化活性。
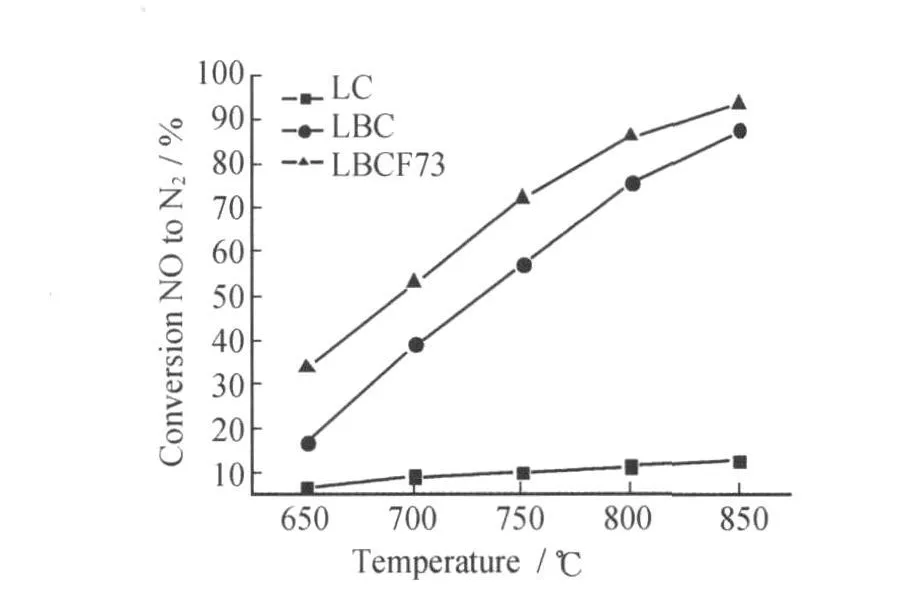
图6 LC、LBC、LBCF73催化分解NO为N2和O2的转化率Fig.6 Conversion of NO toN2and O2over LC、LBC、LBCF73
3 结 论
本文研究的是在钙钛矿的A位和B位掺杂不同元素而提高钙钛矿催化分解NO的活性。我们发现在A位掺杂Ba元素钙钛矿结构产生畸变,提高催化剂的表面氧空位的浓度,从而提高了催化剂的催化活性,在B位掺杂Fe,Fe弱化了Co-O键,二者协同作用,提高了氧的迁移能力,从而进一步提高了催化活性。无论是掺入Ba还是掺入Fe都有利于Co3d电子的流动,有利于氧的脱附。
[1]许树军,朱宇君,袁福龙,等.复合氧化物 La(1-x)BaxCoO3对NO直接分解的研究 [J].黑龙江大学自然科学学报,2008,25(5):667-670.
[2]梅若兰,石臣恩,陈伯涛,等.无机化学:上册[M].北京:高等教育出版社,1992.
[3]崔秀兰,杨桔材,刘 源,等.钙钛矿LaMnO3-δ及La1-xSrxMnO3-δ纳米粒子的 XPS表征 [J].稀土,2000,21(3):20-26.
[4]P.Wang,L.Yao,M.Wang,et al.XPS and voltammetric studies on La1-xSrx CoO3-δperovskite oxide electrodes[J].Journal ofAlloys and Compounds,2000,311:53-56.
[5]Hirohisa Tanakaa,Makoto Misonob.Advances in designing perovskite catalysts[J].Current Opinion in Solid State and Materials Science.2001,(5):381-387.
[6]J.-M.Giraudon,A.Elhachimi,F.Wyrwalski,et al.Leclercq studies of the activation process over Pd perovskite-type oxides used for catalytic oxidation of toluene[J].Applied CatalysisB:Environmental,2007,(5):147-156.
[7]M.R.Goldwasser,M.E.Rivas,M.L.Lugo,et al.Combined methane reforming in presence of CO2and O2over LaFe1-xCoxO3mixed-oxide perovskites as catalysts precursors[J].Catalysis Today,2005,107-108:106-113.
[8]刘社田,于作龙,吴 越.钙钛矿型复合氧化物LaMyM′1-yO3的结构与红外光谱研究 [J].无机材料学报,1994,2(9):184-190.
[9]Huang L,Bassir M,Serge Kaliaguine.Reducibility of Co3+in perovskite-type LaCoO3and promotion of copper on the reduction of Co3+in perovskite-type oxides[J].Applied Surface Science,2005,243:360-375.
[10]Yasutake Teraoka,Tomohiro Harada and Shuichi Kagawa.Reaction mechanism of direct decomposition of nitric oxide over Co-and Mn-based perovskite-type oxides[J].Chem.Soc.FaradayT rans,1998,94(13):1 887-1 891.
[11]白树林,傅希贤,桑丽霞,等.钙钛矿(ABO3)型复合氧化物的光催化活性变化趋势与分析 [J].高等学校化学学报,2001,22(4):663-665.
[12]桑丽霞,傅希贤.LaBO3(B=Fe,Co)中氧的迁移与光催化反应活性[J].高等学校化学学报,2003,24(2):320-323.

