疏肝脂片质量标准研究
李 燕, 晁 愚, 吴威巍, 杨 方, 庄昌龙, 吴 彤*
(1.上海医药工业研究院,上海200040;2.上海方心健康科技发展有限公司,上海200032)
疏肝脂片源于临床经验方舒肝祛脂胶囊,由柴胡、三七、枳实、白术等九味中药组成,具有疏肝消脂、清热化积、行气活血的功效,用于治疗非酒精性单纯性脂肪肝。为有效控制该制剂的质量,本实验按照中药六类新药的注册要求对该制剂进行质量研究。柚皮苷为枳实中的主要有效成分,具有降血脂、抗动脉粥样硬化的生物学活性,能降低胆固醇、减少血栓的形成[1-3],并且在该制剂中含有量较高,因此采用高效液相色谱法测定其质量分数,同时对柴胡、三七、白术进行定性鉴别。实验方法简单可靠,为该制剂质量标准的制定提供了依据。
1 仪器与试药
1.1 仪器 HP1100高效液相色谱仪(G1322A脱气机,G1311A四元泵,G1316A柱温箱,G1314AVWD检测器,美国HP公司);KQ2200超声波清洗仪(昆山市超声仪器有限公司);HHS电热恒温水浴锅(上海医疗器械二厂);BP211D型电子天平(赛多利斯科学仪器有限公司)。
1.2 试药 疏肝脂片(批号080625-1,080625-2,080625-3,上海医药工业研究院自制);柚皮苷对照品(批号110722-200610,供定量测定用);人参皂苷 Rg1(批号 110703-200424,供定量测定用);柴胡对照药材(批号 120992-200504);白术对照药材(批号120925-200407),上述对照品及对照药材均购自中国药品生物制品检定所;柴胡皂苷C对照品(批号080314,上海医药工业研究院自制,纯度﹥98%);乙腈为色谱纯,水为双蒸水,其它试剂均为分析纯。
2 定性鉴别
2.1 柴胡 取本品10片,研细,过75目筛,称取粉末0.35 g,加甲醇10mL,超声提取10min,滤过,滤液蒸干,残渣加水10 mL超声使成悬浊液,转移至分液漏斗中,以水饱和的正丁醇提取2次,每次20 mL,合并正丁醇提取液,蒸干,残渣加甲醇1 mL溶解,作为供试品溶液。另取柴胡对照药材0.1 g,加甲醇10mL,超声处理10min,滤过,滤液浓缩至约1 mL,作为对照药材溶液;取柴胡皂苷C对照品,加甲醇制成每1 mL含0.5 mg的溶液,作为对照品溶液。再取缺柴胡的阴性样品,按供试品溶液制备方法制备阴性对照品溶液。照薄层色谱法(2010版中国药典一部附录Ⅵ B)试验,吸取上述4种溶液各5μL,分别点于同一硅胶G薄层板上,以乙酸乙酯-乙醇-水(10∶2∶1)为展开剂,展开,取出,晾干,喷以2%对二甲氨基苯甲醛的40%硫酸溶液,60℃加热至斑点显色清晰,置日光下检视。供试品色谱中,在与对照品色谱相应的位置上,显相同颜色的斑点,阴性对照无斑点。结果见图1。

图1 疏肝脂片中柴胡薄层色谱图
2.2 三七 取本品10片,研细,过75目筛,称取粉末0.35 g,加甲醇10mL,超声提取10min,滤过,滤液蒸干,残渣加水10 mL超声使成悬浊液,转移至分液漏斗中,以水饱和的正丁醇提取2次,每次20 mL,合并正丁醇提取液,蒸干,残渣加甲醇1 mL溶解,作为供试品溶液。另取人参皂苷Rg1对照品,加甲醇制成每1 mL含0.5 mg的溶液,作为对照品溶液。再取缺三七的阴性样品,按供试品溶液制备方法制备阴性对照品溶液。照薄层色谱法(2010版中国药典一部附录ⅥB)试验,吸取上述3种溶液各5μL,分别点于同一硅胶G薄层板上,以三氯甲烷-甲醇-水(13∶6∶2)10℃以下放置的下层溶液为展开剂,展开,晾干,喷以10%硫酸溶液,105℃加热至斑点显色清晰,置日光下检视。供试品色谱中,在与对照品色谱相应的位置上,显相同颜色的斑点,阴性对照无斑点。结果见图2。
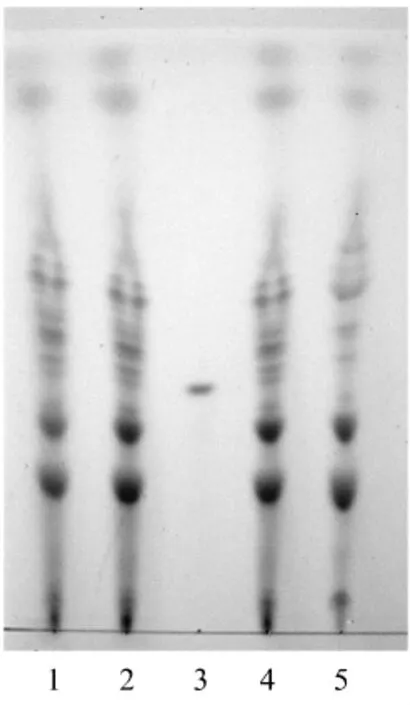
图2 疏肝脂片中三七的薄层色谱图
2.3 白术 取本品10片,研细,过75目筛,称取粉末1 g,加甲醇10 mL,超声提取20 min,滤过,滤液蒸干,残渣加水10 mL超声使成悬浊液,转移至分液漏斗中,以三氯甲烷提取2次,每次20 mL,合并三氯甲烷提取液,蒸干,残渣加0.5 mL甲醇溶解,作为供试品溶液。另取白术对照药材0.1 g,加甲醇10 mL,80℃水浴回流1 h,滤过,滤液蒸干,残渣加1 mL甲醇溶解,作为对照药材溶液。再取缺白术的阴性样品,按供试品溶液制备方法制备阴性对照品溶液。照高效液相色谱法(2010版中国药典一部附录Ⅵ D)试验,以十八烷基键合硅胶为填充剂;乙腈-水(45∶55)为流动相;检测波长为210 nm,体积流量1mL/min,柱温25℃。吸取上述3种溶液各20μL,注入液相色谱仪,测定,供试品色谱中,应呈现与对照品色谱峰保留时间相同的色谱峰,阴性对照无该色谱峰。结果见图3。
3 定量测定
3.1 色谱条件与系统适用性试验 用十八烷基硅烷键合硅胶为填充剂;乙腈-水(20∶80)为流动相;检测波长为283 nm[4-7],体积流量1 mL/min,柱温25℃。理论板数按柚皮苷峰计算应不低于5 000。结果见图4。
3.2 供试品溶液的制备 取本品10片,研细,过75目筛,取粉末约35 mg,精密称定,置于10 mL量瓶中,加50%甲醇约9 mL,超声提取20 min,放冷至室温,再加50%甲醇至刻度,滤过,取续滤液,即得。
3.2 供试品溶液的制备 取本品10片,研细,过75目筛,取粉末约35 mg,精密称定,置于10 mL量瓶中,加50%甲醇约9 m L,超声提取20 min,放冷至室温,再加50%甲醇至刻度,滤过,取续滤液,即得。

图3 白术定性鉴别的HPLC图谱

图4 柚皮苷定量测定的HPLC图谱
3.5 标准曲线的制备 精密吸取柚皮苷对照品溶液(0.337mg/mL)适量,以 50% 甲醇分别稀释至 0.168、0.084 2、0.042 1、0.003 37 mg/mL,分别精密吸取上述溶液 20 μL 注入液相色谱仪,测定,以质量浓度对峰面积进行回归,得回归方程为 Y=3.72 ×104X-43.6,r=0.999(n=5),表明柚皮苷进样量在0.067 4μg~6.74μg范围内与峰面积呈良好的线性关系。
3.6 精密度试验 精密吸取质量浓度为0.084 2 mg/m L的柚皮苷对照品溶液20μL,注入液相色谱仪,重复进样6次,测定,柚皮苷峰面积的RSD为0.22%(n=6),表明仪器精密度良好。
3.7 稳定性试验 精密吸取供试品溶液,分别在0、2、4、8 h进样20μL,测定,柚皮苷面积RSD为2.2%,表明供试品溶液中柚皮苷在8 h内稳定。
3.8 重复性试验 取同一批号的样品6份,制备供试品溶液并测定,柚皮苷的RSD为0.96%,表明该试验方法的重复性较好。
3.9 加样回收率试验 取同一批号的样品6份,分别加入一定量的柚皮苷对照品,制备供试品溶液,精密吸取20μL注入液相色谱仪,测定柚皮苷,计算加样回收率,柚皮苷回收率平均值为98.6%,RSD为2.2%,说明该测定方法回收率较好,结果见表1。

表1 加样回收率试验结果
3.10 样品的测定 取3批片剂(批号080625-1,080625-2,080625-3;平均片质量分别为 370.81 mg,370.67 mg,370.33 mg),每批取2个样品,制备供试品溶液,测定柚皮苷量,3批样品中柚皮苷量分别为 8.64 mg/片、8.60 mg/片、9.18 mg/片。
4 讨论
4.1 柴胡的鉴别方法参考2010版中国药典[8]263,考察不同比例的展开剂,包括乙酸乙酯-乙醇-水(8∶2∶1),乙酸乙酯-乙醇-水(8 ∶2 ∶1)展开两次,乙酸乙酯-乙醇-水(10 ∶2 ∶1)等。实验结果证明,后两种展开方法均有较好的展开效果,但是乙酸乙酯-乙醇-水(8∶2∶1)需要展开两次,所用时间较长,因此,选择乙酸乙酯-乙醇-水(10 ∶2 ∶1)。
4.2 三七的鉴别方法使用了多种展开剂,包括正丁醇-乙酸乙酯-水(4∶1 ∶5)、三氯甲烷-甲醇-水(13 ∶7 ∶2)下层溶液[9]、三氯甲烷-甲醇-水(13 ∶6 ∶2)下层溶液、三氯甲烷-乙酸乙酯-甲醇-水(15 ∶40 ∶22 ∶10)下层溶液[8]11等。实验结果证明,3种展开剂均有较好的分离效果,但是由于正丁醇-乙酸乙酯-水系统背景颜色较深,三氯甲烷-乙酸乙酯-甲醇-水系统不稳定,因此选择三氯甲烷-甲醇-水系统,其中三氯甲烷-甲醇-水(13∶6∶2)下层溶液展开效果更好,故最终选择三氯甲烷-甲醇-水(13∶6∶2)下层溶液作展开剂。
4.3 实验中曾采用多种提取方法制备白术鉴别的供试品溶液,更换不同的展开系统,均未找到合适的鉴别白术的薄层层析方法,因此,选择用高效液相色谱法对白术进行鉴别[10-11]。
4.4 实验中对柚皮苷的提取时间进行考察,10 min、20 min、30 min柚皮苷的提取率分别为 2.89%、2.91%、2.92%,确定20 min可将柚皮苷提取完全,因此选择超声提取20 min。
[1]杨宏亮,田 珩,李沛波,等.柚皮苷及柚皮素的生物活性研究[J].中药材,2007,30(6):752-754.
[2]杨晓泉,张海德,李 琳.柚皮黄酮类抗氧化物质的纯化及其降血脂作用研究[J].营养学报,2004,26(5):378-381.
[3]蔡逸平,曹 岚,范崔生.枳实、枳壳类药材的化学成分及药理研究概况[J].江西中医学院学报,1999,11(1):18-19.
[4]梁远园,冯 彪,祝晨筱,等.HPLC法测定枳实药材中橙皮苷和柚皮苷的含量[J].中药新药与临床药理,2006,17(5):359-361.
[5]吴卫中,李永庆,陈 蕾.RP-HPLC法测定金甲王颗粒中柚皮苷的含量[J].药物分析杂志,2007,27(7):1078-1080.
[6]刘振丽,宋志前,李林福,等.枳实炮制前后化学成分含量的变化[J].中成药,2006,28(8):1148-1150.
[7]曾祖平,何 薇,崔立山.高效液相法测定枳实中黄酮类成分[J].中国实验方剂学杂志,2006,12(7):9-10.
[8]国家药典委员会.中华人民共和国药典:2010版一部[S].北京:中国医药科技出版社,2010.
[9]国家药典委员会.中华人民共和国药典:2000版一部[J],北京:化学工业出版社,2000:10.
[10]苗明三,李振国.现代实用中药质量控制技术[M].北京:人民卫生出版社,2000:334.
[11]叶 燕,程雪梅,侴桂新.白术药材HPLC指纹图谱研究[J].江苏中医药,2009,41(4):59-60.

