硫酸庆大霉素片含量测定的不确定度评估
邢以文
本品为氨基糖苷类广谱抗生素,对多种革兰阴性菌及阳性菌都具有抑菌和杀菌作用。对绿脓杆菌、产气杆菌、肺炎杆菌、沙门氏菌属、大肠杆菌及变形杆菌等革兰阴性菌和金葡菌等作用较强,临床上用于金葡菌、绿脓杆菌、大肠杆菌、痢疾杆菌、克雷白杆菌、变形杆菌和其他敏感菌所引起的败血症、呼吸道感染、胆道感染、化脓性腹膜炎、颅内感染、尿路感染及菌痢等疾患。本品按照《中国药典》2005年版二部二剂量法[1]检验,所得结果进行不确定度分析。
测量不确定度是衡量分析测试结果的质量的尺度。不确定度越小,分析测试结果越可靠,因此,测量不确定度是测量结果质量的定量表征。根据ISO/IEC17025[2]和CNAS-CL 07:2011《测量不确定度的要求》[3]的要求,检测实验室应该建立并实施测量不确定度评估程序。
1 仪器、试药及菌种
仪器:智能抑菌圈测定仪(CAM-ⅢB型,上海波浦电脑系统工程有限公司);电恒温水浴锅(H.S型,上海医疗器械厂);隔水式电热恒温培养箱(PYX-DHS一40X5型,国营创新医疗器械厂);高压湿热蒸汽灭菌器(LMQ.C型,山东新华医疗器械有限公司);测定抗生素效价用培养皿(直径90 mm),牛津杯,陶瓦盖等;电子天平(AE240型,Mettler Toledo(中国)有限公司);数字显示移液器(200~1000 μl Finnpipette,芬兰移液器有限公司)。
试药及菌种:磷酸二氢钾(分析纯),磷酸氢二钾(分析纯),自配pH7.8磷酸盐缓冲液(简称PBS pH7.8);硫酸庆大霉素片(规格40000 U,批号为20060405,开封制药<集团>有限公司);抗生素检定培养基I(pH值为7.8~8.0,北京三药科技开发公司);短小芽孢杆菌[CMCC(B)63202,中国药品生物制品检定所]。
2 方法与结果
2.1 缓冲液、菌悬液及双碟制备 取磷酸氢二钾11.18 g与磷酸二氢钾0.82 g,加水使成2000 ml,滤过,在115℃灭菌30 min,即得磷酸盐缓冲液(pH=7.8)。取短小芽孢杆菌[CMCC(B)63202]的营养琼脂斜面培养物,接种于盛有营养琼脂培养基的培养瓶中,在35℃ ~37℃培养7 d,用革兰氏染色法涂片镜检,应有芽孢85% 以上,用灭菌水将芽孢洗下,在65℃加热30 min,即得短小芽孢杆菌菌悬液。
取直径约90 mm,高16~17 mm的平底双碟,分别注入加热融化的抗生素检定培养基120 ml,使在碟底内均匀摊布,放置水平台上使凝固,作为底层;另取抗生素检定培养基I适量加热融化后,放冷至60℃,加入短小芽孢杆菌菌悬液适量(能得清晰的抑菌圈为度,使标准品溶液的高浓度所致的抑菌圈直径为18~22 mm)摇匀,在每一双碟中分别加入5 ml,使在底层上均匀摊布,作为菌层。放置水平台上冷却后,在每一双碟中以等距离均匀放置牛津杯4个,用陶瓦圆盖覆盖,备用。
2.2 标准品溶液的制备 精密称取庆大霉素标准品25.19 mg(638U/mg×20.15 mg=12856U)置25 ml量瓶中,加灭菌水溶解,并稀释置刻度,摇匀(514.240U/ml)。

2.3 供试品溶液的制备 取供试品5片,加少量灭菌水研细,移置200 ml量瓶中,加灭菌水至刻度,摇匀(1000 U/ml)。

2.4 测定方法 照抗生素微生物检定法,使用移液枪分别吸取浓度为10.285、5.142U/ml的标准品溶液和浓度为10U/ml、5U/ml的供试品溶液各275 μl至上述准备好的双碟中的牛津杯内,盖好陶瓦盖,在36℃下培养14~16 h后,使用智能抑菌圈测定仪测量各抑菌圈的直径,并计算含量。
2.5 不确定度评估
2.5.1 建立数学模型
见含量测定公式。

T1:供试品低剂量所致抑菌圈直径或面积
T2:供试品高剂量所致抑菌圈直径或面积
S1:标准品低剂量所致抑菌圈直径或面积
S2:标准品高剂量所致抑菌圈直径或面积

P:估计效价
从检测过程和数学模型分析,不确定度主要来源于标准品、供试品的称量和溶液的配制过程、加液至牛津杯过程中移液枪以及测量用抑菌圈测定仪的误差、最后结果FL值。
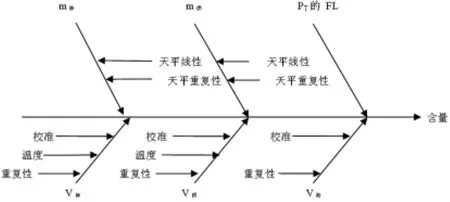
图1 不确定度分量分析图
2.5.2 标准品溶液的标准不确定度
2.5.2.1 天平称量引入的不确定度 ①天平线性:实验使用AE240电子天平,依据说明书,线性为±0.2 mg,按矩形分布,故U(m1)= 0.2/=0.12 mg;②天平重复性:AE240电子天平说明书标明重复性为0.05 mg(天平参数),由于采用减量法称量,故:

2.5.2.2 容量玻璃仪器引入的不确定度 ①25 ml量瓶;a校正:允差:±0.03 ml,中间分布,U(V1)= 0.03/=0.012 ml,b 重复性:由实验求得标准偏差;c温度:ΔV=(2.1 ×10-4-1.5×10-5)×25×(25-20)=0.024 ml
按正态分布U(V3)=0.0122/2=0.012 ml

Urel(V1)=0.072/25=0.0029
②50 ml量瓶:a校正:允差:±0.05 ml,中间分布,U(V1)=0.05/=0.020 ml
b重复性:由实验求得标准偏差U(V2)=0.08 ml
c温度:
ΔV=(2.1 ×10-4-1.5 ×10-5)×50 ×(25-20)=0.048 ml
按正态分布U(V3)=0.048/2=0.024 ml

Urel(V2)=0.086/50=0.0017
③100 ml量瓶:a校正:允差:±0.10 ml,中间分布,U(V1)= 0.10/=0.041 ml
b重复性:由实验求得标准偏差U(V2)=0.08 ml
c温度:
ΔV=(2.1 ×10-4-1.5 ×10-5)×100 × (25-20)=0.098 ml
按正态分布U(V3)=0.098/2=0.049 ml

④5 ml移液管
a校正:允差:±0.015 ml,中间分布,U(V1)= 0.015/=0.0061 ml
b重复性:由实验求得标准偏差U(V2)=0.02 ml
c温度:ΔV=(2.1×10-4-1.5×10-5)×5×(25-20)=0.0049 ml
按正态分布U(V3)=0.0049/2=0.0024 ml

Urel(V4)=0.021/5=0.0042
2.5.2.3 标准品溶液的不确定度 由于使用25 ml量瓶2个,5 ml移液管 2 支,故

2.5.3 供试品溶液的不确定度
2.5.3.1 容量玻璃仪器引入的不确定度
①200 ml量瓶:a校正:允差:±0.15 ml,中间分布,U(V1) = 0.15/=0.061 ml
b重复性:由实验求得标准偏差U(V2)=0.1 ml
c温度:
ΔV=(2.1×10-4-1.5×10-5)×200×(25-20)=0.196 ml
按正态分布U(V3)=0.196/2=0.098 ml

Urel(V3)=0.15/200=0.00075
②100 ml量瓶引入的不确定度
Urel(V6)=0.0010
③50 ml量瓶
Urel(V8)=0.0017
④5 ml移液管
Urel(V10)=0.0042
2.5.3.2 供试品溶液的不确定度 由于使用50 ml量瓶二个,5 ml移液管二支,故

2.5.4 滴加溶液 275 μl数字显示移液器
①校正:允差:± 2 μl,中间分布,U(V1)=2 μl=0.82 μl
②重复性:由实验求得标准偏差U(V2)=0.51 μl

2.5.5 抑菌圈测定
2.5.5.1 智能抑菌圈测定仪
①均匀性:由实验求得相对标准偏差Urel(V1)=0.00037
②重复性:由实验求得相对标准偏差Urel(V2)=0.00052

2.5.5.2 实验结果 测定效价PT=98.6%平均可信限率PT的FL=2.2%
由平均可信限率(PT的FL),按正态分布 k=2

2.5.6 合成相对标准不确定度的计算

2.5.7 合成标准不确定度的计算

2.5.8 扩展不确定度计算 测量结果符合正态分布,包含
因子k=2,置信概率为9 5.4 5%
U=K×u c(X)=2 ×1.6=3.2
2.6 硫酸庆大霉素片含量的表示 本品含硫酸庆大霉素为标示量的(9 8.6±3.2)%;k=2
3 结论
分析评估不确定度时,首先要尽量考虑产生不确定度的所有来源,因为合成不确定度是由各方面产生的不确定度分量合成而来的。
本方法测量结果的不确定度主要来源于实验结果的平均可信限率(PT的FL值),这也从客观上反映出抗生素微生物检定法的不足之处,就是微生物实验的重复性相对较差,这是由于细菌生长的不确定因素较多造成的。可见,测量不确定度对于反映测量过程的准确性具有重大意义。本方法能够较为准确的反映出硫酸庆大霉素片含量测定(微生物检定法)的不确定度。
[1]国家药典委员会.中华人民共和国药典(二部).北京:化学工业出版社,2005:731,附录8l-84.
[2]中国实验室国家认可委员会.ISO/IEC 17025:2005检测和校准实验室认可准则.中国实验室国家认可委员会,2005.
[3]中国实验室国家认可委员会.CNAS-CL 07:2011测量不确定度的要求.中国实验室国家认可委员会,2011.

