激素联合赛可平和他克莫司治疗狼疮性肾炎的前瞻性临床研究
胡伟新 陈樱花 刘正钊 章海涛 陈惠萍 曾彩虹 张丽华 刘志红
狼疮性肾炎(LN)的病理改变多样,其中Ⅲ型、Ⅳ型、Ⅴ型、Ⅴ+Ⅳ型及Ⅴ+Ⅲ型称为重症LN,仍是国际公认的治疗难题。传统疗法采用激素联合一种免疫抑制剂如环磷酰胺(CYC)、吗替麦考酚酯(MMF)或他克莫司(FK506),疗效低,尤其Ⅴ+Ⅳ型LN的治疗缓解率仅20%左右,5年终末期肾病(ESRD)的发生率达15%左右。最近十年,国际上试图努力改变现状,但临床试验未能取得满意结果[1-2]。
近年来,由激素联合MMF和FK506组成的多靶点免疫新疗法(简称多靶点)在难治性LN的治疗上有所突破[3-5]。该疗法利用不同药物作用于LN免疫机制不同环节的协同作用提高疗效,并减小药物剂量以减少不良反应。临床对照研究发现,多靶点疗法治疗V+IV型LN的完全缓解率是传统CYC疗法的4倍。对其他重型LN,包括Ⅲ型、Ⅳ型、Ⅴ型和Ⅴ+Ⅲ型,该疗法同样有显著疗效。因此,多靶点疗法成为目前治疗LN最为引人注目的新疗法。但该疗法中,MMF和FK506的进口产品价格昂贵,患者常难以承受,更无法长期使用。为了让更多的患者能够接受多靶点疗法,更好地控制病情活动,提高疗效,本研究在以往观察了赛可平(吗替麦考酚酯分散片,杭州中美华东制药有限公司)血药浓度和治疗LN疗效的基础上[6,7],前瞻性观察激素联合赛可平和FK506(杭州中美华东制药有限公司)组成的多靶点疗法,观察该疗法诱导治疗LN的疗效和安全性,并与激素联合环磷酰胺静脉冲击疗法(IV-CYC)进行比较。
对象和方法
入组标准 所有进入本试验的患者符合以下条件:(1)符合美国风湿病协会的系统性红斑狼疮(SLE)的诊断标准(1997)的活动性狼疮患者,SLEDAI>10分;年龄18~60岁,性别不限;(2)入组前12周内行肾活检,病理类型为活动性Ⅳ型、Ⅴ+Ⅳ型及Ⅴ+Ⅲ型LN(ISN/RPS2003病理分型标准)[8],慢性化指数(CI) <3;(3)Ⅳ型、Ⅴ +Ⅳ型、Ⅴ+Ⅲ型:蛋白尿≥1.5 g/24h,伴或不伴活动性尿沉渣表现(尿沉渣红细胞计数>10万/ml,或白细胞>5个/HP,或出现红细胞管型);(4)经伦理委员会批准通过,签署书面知情同意书。
排除标准 存在以下临床情况者不纳入研究:(1)血清肌酐(SCr) >265.2 μmol/L(3.0 mg/dl),或肌酐清除率(CCr)<30 ml/(min·1.73m2)(Cockcroft-Gault公式);(2)肝酶或总胆红素超过正常上限2倍以上;(3)糖代谢异常,定义为空腹血糖>6.1 mmol/L和(或)进食2h后血糖>7.8 mmol/L;(4)3个月内使用过MMF、CYC、FK506、环孢霉素 A、丙种球蛋白静脉注射、大剂量甲泼尼龙冲击治疗;(5)已知对MMF、FK506、CYC或糖皮质激素中的任何成分过敏或有禁忌证;(6)目前或以往有:(a)在随机分组前3个月内有活动性乙肝(包括大三阳或小三阳)、丙肝、肺结核、巨细胞病毒、真菌或HIV感染;(b)在随机分组前3个月内有未愈的活动性消化道溃疡;(c)滥用毒品或酗酒;明显营养不良(体质量指数<18.5 kg/m2)或体重<45 kg。(7)其他活动性疾病,如:(a)严重的心血管疾病;(b)慢性阻塞性肺病,或需要应用口服激素治疗的哮喘;(c)排除SLE活动导致的骨髓抑制:白细胞计数<3×109/L,绝对中性粒细胞计数<1.3×109/L,血小板计数<50×109/L。(8)存在狼疮性脑病等危及生命的并发症。
治疗方案
符合条件的患者随机进入多靶点组及IV-CYC组。
多靶点组 采用激素、MMF和FK506三联治疗。患者均先接受甲泼尼龙(methylprednisolone,MP)0.5g,静脉滴注,每日一次,共3d。以后口服泼尼松[起始剂量为 0.8 mg/(kg·d),最大剂量45 mg/d],分 3次口服,4周后减量,每 2周减 5 mg/d至20 mg/d,再每2周减2.5 mg/d直到每日10 mg维持。MMF(赛可平,中美华东制药公司):诱导期治疗剂量0.5g每日2次,间隔12h空腹服用。根据血吗替麦考酚酸(MPA)浓度(MPA-AUC0~12h)调整 MMF 剂量[5],MPA-AUC0~12h目标值为 20 ~ 30 mg·h/L。FK506(中美华东制药公司)目标治疗剂量4 mg/d,每日2次间隔12h空腹服用。根据FK506血药谷浓度调整剂量,要求 FK506浓度 4~7 ng/ml。治疗期间如果出现不良反应或血药浓度超过靶目标水平,MMF和FK506均可减量直至停用,但停药时间不得超过2周,否则退出本试验。
诱导治疗时间为6~9个月:如6个月获得完全缓解,进入维持期治疗,可继续多靶点维持(MMF减为0.5~0.75 g/d,FK506减至2~3 mg/d),或改硫唑嘌呤1~2 mg/(kg·d)维持,若6个月获部分缓解,则继续诱导至9个月后转入维持期。如6个月治疗无反应(未达部分缓解标准),则退出本试验。
IV-CYC组 采用激素联合间断静脉CYC冲击疗法。激素用法与多靶点组相同。在MP使用2周开始首次CYC冲击治疗。CYC用法:首剂0.75 g/m2BSA,以后根据首次CYC冲击后白细胞数量调整CYC剂量为0.5~1.0 g/m2BSA,最大剂量不超过1.2g。
诱导治疗时间6~9个月,如果6个月获得完全缓解,转入维持期治疗[硫唑嘌呤1~2 mg/(kg·d)],若6个月仅获部分缓解,则继续诱导至9个月后转入维持期。如6个月治疗无反应(未达部分缓解标准),则退出本试验。
合并用药 均口服缬沙坦(代文)80 mg/d,要求血压控制在120/75 mmHg以下。如单用缬沙坦血压仍未达标,加用二氢吡啶类钙拮抗剂、β受体阻滞剂、利尿剂或α受体阻滞剂控制血压,但不增加缬沙坦剂量或加用ACEI。禁止合并使用来氟米特、甲氨喋呤等免疫抑制剂。可使用利尿剂、抗凝剂、红细胞生成素及粒细胞集落刺激因子等药物。避免使用可能影响MMF和FK506血药浓度的药物,如大环内酯类抗生素(如红霉素)、氟康唑、己炔雌二醇、利福平、苯巴比妥及卡马西平等。
观察指标 治疗前记录所有患者的病史及实验室检查结果(包括:性别、年龄、狼疮病程、肾脏病程、SLE-DAI、尿蛋白定量、尿沉渣红细胞计数、SCr、血清白蛋白、ANA、ds-DNA和补体等)。所有患者入选前12周内均在B超引导下行经皮肾穿刺术,肾组织常规行 HE、PAS、PASM、Masson染色,半定量评分肾组织狼疮活动指数(AI)及CI。
疗效判断 主要指标为完全缓解率,即尿蛋白<0.4 g/24h、血清白蛋白≥35 g/L、SCr正常。次要疗效为部分缓解率、不良反应发生率、尿蛋白和免疫学指标的变化。部分缓解定义为尿蛋白较基础值减少50%以上且尿蛋白<3.5 g/24h、血清白蛋白≥30 g/L和SCr稳定(升高不超过基线值25%)。总缓解率为完全缓解率与部分缓解率之和。
统计分析方法 计量资料以均数±标准差表示,组间比较采用t检验;计数资料以百分率表示,组间比较采用χ2检验。累积缓解率采用Kaplan-Meier法估算,log-rank检验比较组间差异。使用SPSS16.0统计软件,P<0.05为差异有统计学意义。
结 果
患者基础资料 2009年6月至2010年4月共纳入79例患者,随机分为多靶点组(n=45)和IV-CYC组(n=34)。两组患者的基础临床和病理资料无显著差异(表1)。
FK506剂量及浓度 FK506的起始剂量平均为(2.36±0.82)mg/d,平均血药浓度(5.06±2.42)ng/ml。治疗期间FK506剂量及血药浓度变化如图1,FK506平均剂量为(2.65±0.94)mg/d,血药浓度平均为(4.23 ±1.97)ng/ml。

表1 多靶点组和IV-CYC组患者基本资料

图1 他克莫司(FK506)剂量及血药浓度
MMF(赛可平)剂量和血药浓度 MMF的起始剂量平均为(0.62±0.22)g/d,平均血药浓度(29.06±10.32)mg·h/L。治疗期间 MMF的平均剂量为(0.71±0.23)g/d,平均血药浓度(29.56±8.60)mg·h/L(图2)。
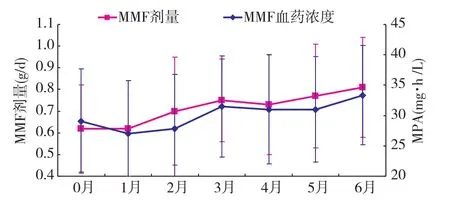
图2 赛可平(MMF)剂量及血药浓度
临床疗效 所有患者完成6~9月的诱导期治疗,多靶点组 28例(62.2%),IV-CYC组 13例(38.2%)获得完全缓解,多靶点组的完全缓解率显著高于IV-CYC组(P<0.05)(图3)。6月和9月多靶点组的累积完全缓解率分别为53.3%和62.2%,IV-CYC组则分别为29.4%和42.6%,两组相比有统计学差异(P<0.05)(图4)。6月的累积总缓解率多靶点组显著高于IV-CYC组(95.6%vs76.5%,P<0.01)。
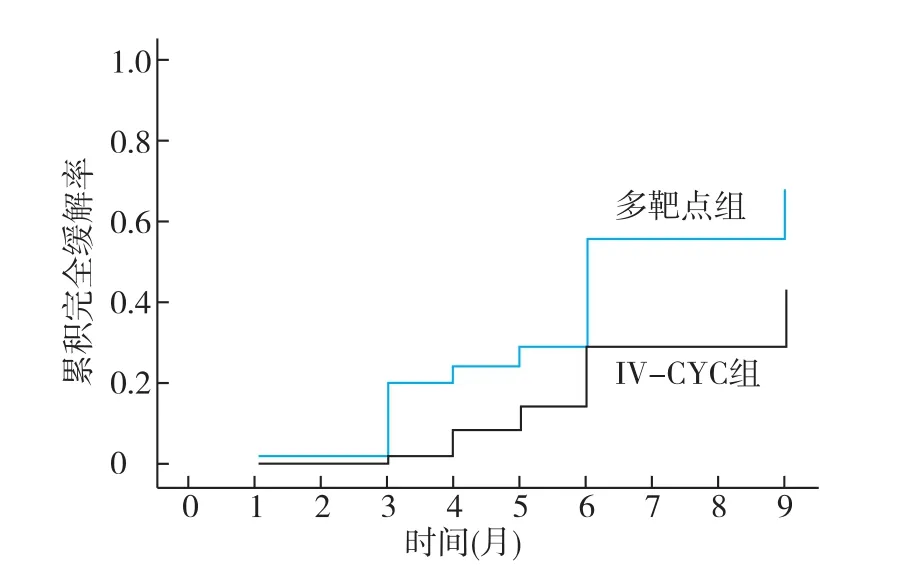
图3 多靶点组与IV-CYC组累积完全缓解率比较
比较不同病理类型LN的缓解率(表2),多靶点组Ⅴ+Ⅳ型的完全缓解率显著高于IV-CYC组(50.0%vs16.7%,P<0.05),Ⅴ+Ⅲ型的完全缓解率多靶点组也高于IV-CYC组(54.5%vs22.2%,P>0.05),但未达统计学差异。Ⅳ型的完全缓解率和总缓解率两组无差异。
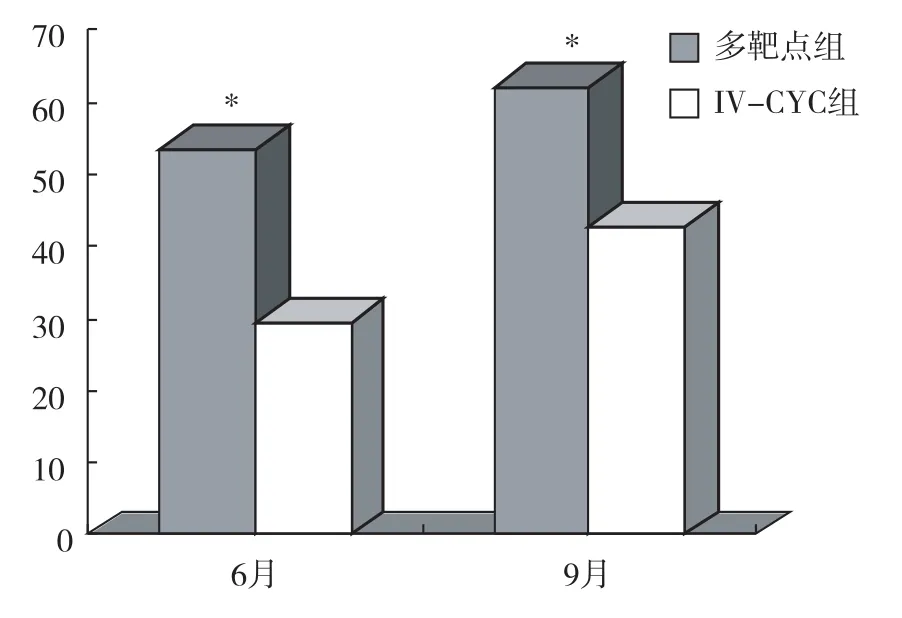
图4 多靶点组与IV-CYC组不同治疗时间的完全缓解率
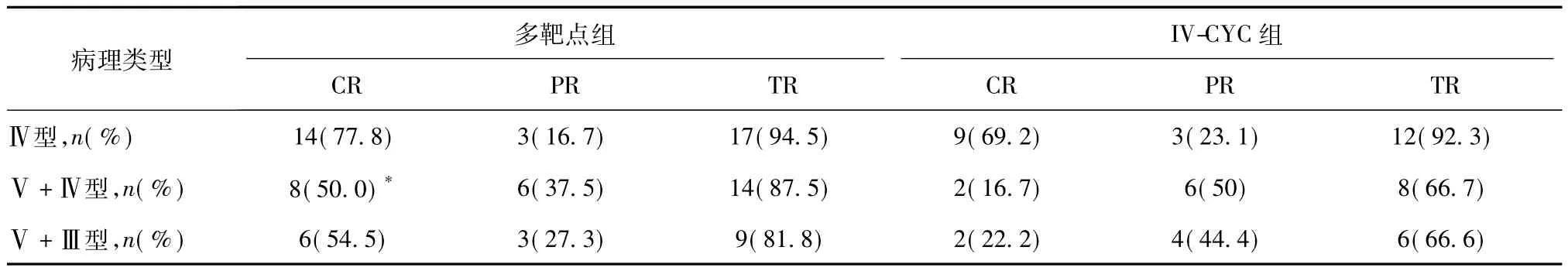
表2 不同病理类型狼疮性肾炎患者的缓解率
临床指标变化 治疗期间多靶点组尿蛋白下降较IV-CYC组显著。与基线值相比,6月时多靶点组尿蛋白下降幅度显著高于IV-CYC组[(79.36±18.30)%vs(59.68±39.75)%,P<0.01](图5)。两组血清白蛋白水平及SCr变化均无显著差异(图6)。抗-dsDNA的转阴率(75%vs57%,P>0.05)、补体C3恢复正常的比例(50%vs42.6%,P>0.05)多靶点组高于IV-CTX组,但均未达统计学差异。
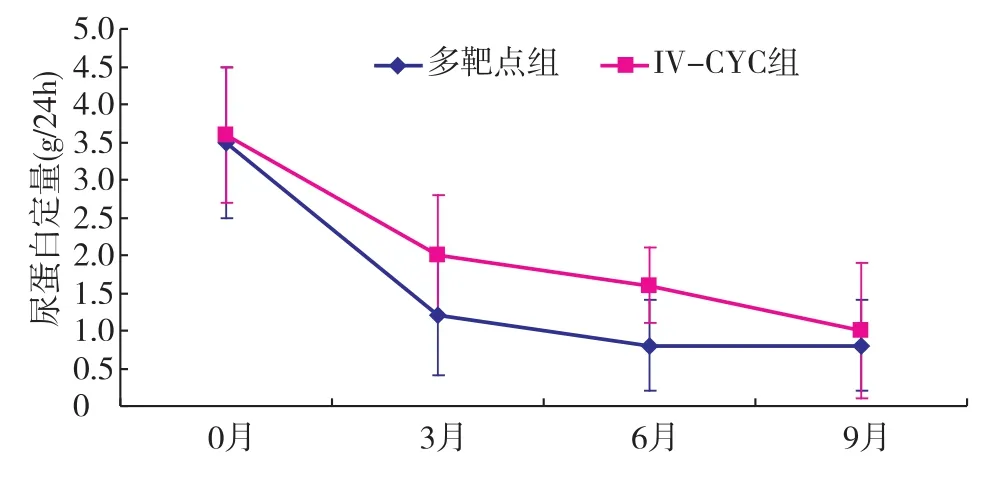
图5 多靶点组和IV-CYC组尿蛋白排泄量变化
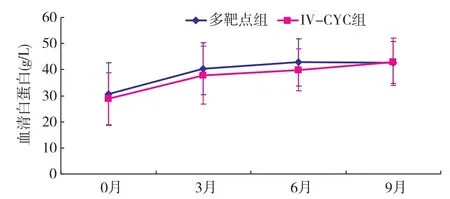
图6 多靶点组和IV-CYC组血清白蛋白变化
不良反应 多靶点组总不良反应发生率低于IV-CYC(31.1%vs70.6%,P<0.01),其中多靶点组的不良反应主要为新发高血压(11.1%)和带状疱疹(6.7%),IV-CYC组的主要不良反应为胃肠道症状(23.5%)、白细胞减少(14.7%)、皮肤感染(8.8%)和月经紊乱(6.7%)。多靶点组 2例,IV-CYC组1例并发肺部感染,无一例死亡(表4)。
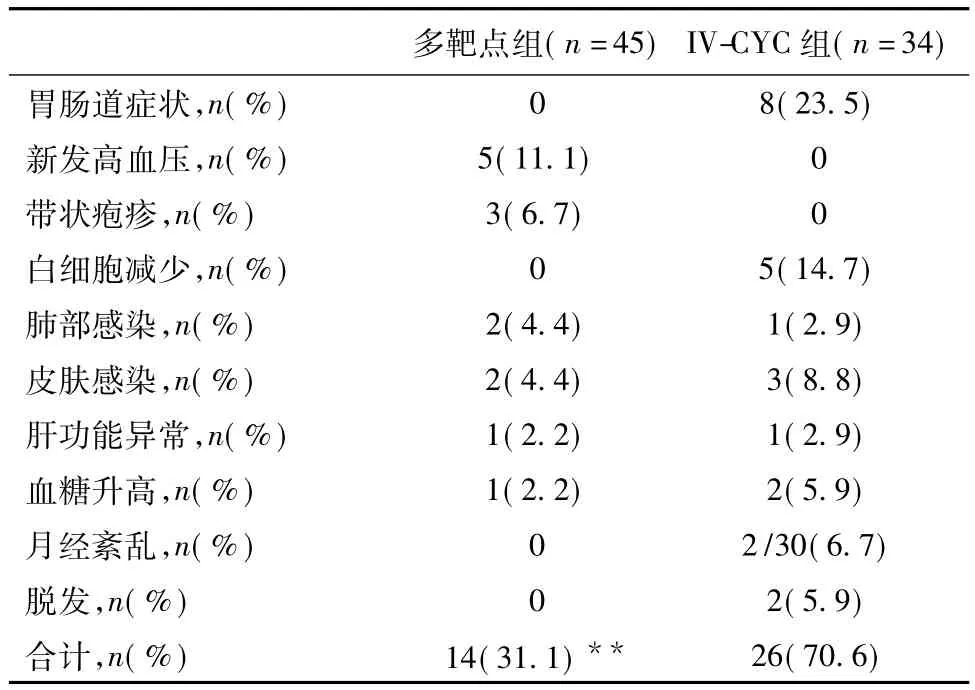
表4 多靶点组和IV-CYC组患者的不良反应
讨 论
经临床对照研究证实,由激素联合 MMF和FK506组成的多靶点新疗法,其疗效优于传统CYC静脉冲击疗法[3-5],尤其显著提高了Ⅴ+Ⅳ型 LN的完全缓解率,而且由于药物剂量相应减少,不良反应发生率降低。本研究的多靶点方案中,MMF和FK506均采用国产制剂:赛可平和他克莫司,探讨其临床疗效和安全性。作者以往观察了赛可平治疗LN患者药代动力学特点,发现赛可平的药代动力学与MMF胶囊制剂相似[6]。作者同时前瞻性观察了赛可平治疗LN的临床疗效,证明了其治疗Ⅳ型及Ⅲ型LN有效且安全[5],并发现根据MMF血药浓度调整MMF剂量的方法可降低不良反应发生率[6,9]。因此,在本试验中,激素和赛可平剂量和方法与以往报道相同。基于安全考虑,本研究中他克莫司的目标浓度为 4 ~ 7 ng/ml,低于以往研究[4,5]。随访中FK506平均治疗剂量3 mg/d左右,谷浓度平均为4 ng/ml。结果发现多靶点疗法治疗LN的完全缓解率显著高于IV-CYC疗法,6个月和9个月累积完全缓解率多靶点组分别达53.3%和62.2%,而CYC组仅为29.4%和38.2%,多靶点组完全缓解率均显著高于CYC组,从而再次证实了多靶点疗法治疗LN的临床疗效。本文作者将继续多靶点维持治疗的研究,观察多靶点维持缓解的疗效及对远期预后影响。
以往研究发现,多靶点疗法对不同类型LN的疗效存在差异,与CYC比较,多靶点治疗显著提高了Ⅴ+Ⅳ型的完全缓解率,而对单纯Ⅳ型LN,多靶点疗法的缓解率与CYC无显著差异,其他类型LN由于病例数较少难于评价多靶点与CYC之间的疗效差异[3-5]。由于Ⅲ型、Ⅴ型在LN中所占比例较低,难于收集足够的病例数,因此,本试验仅纳入Ⅳ型、Ⅴ+Ⅳ型和Ⅴ+Ⅲ型LN。研究发现,多靶点疗法对Ⅳ型、Ⅴ+Ⅳ型和Ⅴ+Ⅲ型LN均有较高的缓解率,但对Ⅴ+Ⅳ型和Ⅴ+Ⅲ型LN,多靶点的疗效与CYC相比更加明显,而对Ⅳ型LN,多靶点的疗效与CYC无明显差异,这与以往的临床研究结果一致[5]。表明多靶点疗法对Ⅳ型或Ⅲ型与Ⅴ型合并的LN有更强的适应证。
本研究还发现,多靶点组不良反应的发生率显著低于CYC组(31.1%vs70.6%,P<0.01)。两组不良反应类型存在一定差异,多靶点疗法的主要不良反应为新发高血压和带状疱疹,而CYC静脉冲击疗法主要引起胃肠道症状、白细胞减少和皮肤感染。多靶点组2例和CYC组1例发生肺部细菌感染,但均治愈,无一例死亡。表明激素联合赛可平和他克莫司组成的多靶点疗法安全。本研究中多靶点疗法的严重不良反应发生率较低,与随访中监测血药浓度和淋巴细胞亚群从而及时调整药物剂量有关,而且本试验中他克莫司和赛可平的目标浓度也低于以往研究[4-5]。
小结:激素联合赛可平和他克莫司治疗LN的疗效高于间断CYC静脉冲击疗法,尤其对Ⅴ+Ⅳ型疗效更为显著,不良反应发生率低。多靶点疗法的临床疗效和对远期预后的影响还需要多中心和长期随访的临床研究。
1 Melander C,Sallée M,Trolliet P,et al.Rituximab in severe lupus nephritis:early B-cell depletion affects long-term renal outcome.Clin J Am Soc Nephrol,2009,4:579-587.
2 Garcia-Carrasco M,Mendoza-Pinto C,Sandoval-Cruz M,et al.Anti-CD20 therapy in patients with refractory systemic lupus erythematosus:a longitudinal analysis of 52 Hispanic patients.Lupus,2010,19(2):213-219.
3 鲍 浩,章海涛,张 馨,等.难治性狼疮性肾炎多靶点治疗前瞻性临床研究.肾脏病与透析肾移植杂志,2007,16(1):5-13.
4 Bao H,Liu ZH,Xie HL,et al.Successful treatment of classⅤ +Ⅳlupus nephritis with multitarget therapy.J Am Soc Nephrol,2008,19(10):2001-2010.
5 鲍 浩,刘志红,胡伟新,等.多靶点诱导治疗增殖性和膜性狼疮性肾炎前瞻对照性临床研究.肾脏病与透析肾移植杂志,2009,18(3):201-206.
6 鲍 浩,胡伟新,秦卫松,等.霉酚酸酯分散片治疗狼疮性肾炎的血药浓度分析.肾脏病与透析肾移植杂志,2008,17(5):427-431,452.
7 胡伟新,刘正钊,鲍 浩,等.霉酚酸酯分散片治疗狼疮性肾炎的疗效及安全性.肾脏病与透析肾移植杂志,2008,17(5):422-426.
8 Weening JJ,D'Agati VD,Schwartz MM,et al.The classification of glomerulaonephritis in systemic lupus erythematosus revisited.J Am Soc Nephrol,2004,15(2):214-250.
9 谢红浪,胡伟新,章海涛,等.霉酚酸酯治疗狼疮性肾炎的血药浓度与不良反应的联系.肾脏病与透析肾移植杂志,2007,16(5):414-420.

