2型糖尿病的外科治疗体会
任辉明,蔡崇元,上官昌盛
湖北省荆门市第二人民医院普外科,湖北 荆门 448000
2 型糖尿病(type 2 diabetes mellitus,T2DM)已经成为严重威胁人类健康的慢性疾病之一,由其所引起的冠心病、肾病、视网膜病及神经病变等是造成患者致死及致残的主要原因。随着减肥外科在国外的发展,许多肥胖患者并存的糖尿病(DM)在接受外科手术后得到缓解甚至治愈,近年来胃转流术(gastric bypass,GBP)治疗肥胖伴T2DM在国外的治愈率达83%~86%[1]。我院对2007年12月~2010年12月对收治的11例T2DM行GBP手术治疗,取得了良好的效果,现分析报道如下:
1 资料与方法
1.1 一般资料
选取我院11例2型糖尿病患者。其中,男5例,女6例;年龄49~62岁,平均53.6岁;并发高血压3例,糖尿病眼底病变3例,糖尿病足2例,糖尿病肾病1例,胆总管结石1例,胃癌 1 例。 其中,体重指数(body mass index,BMI)≥25 kg/m2的肥胖者8例。采用开腹手术7例,腹腔镜手术4例。手术方式均征得患者同意,并自愿接受为期2年以上的随访。术后10~18 d(平均 14 d)出院。
1.2 入选诊断标准
根据美国糖尿病(DM)学会2007年版DM诊断标准:有DM症状和随机血糖≥11.1 mmol/L;空腹血糖 (FBG)≥7.0 mmol/L;口服葡萄糖耐量试验(OGTT)2 h餐后血糖(2 h PG)≥11.1 mmol/L。本组均未发现有垂体前叶、甲状腺及肾上腺皮质功能紊乱的证据。
1.3 GBP手术要点
全麻常规开腹或腹腔镜,然后分离胃体部,于胃中部用手工或缝合器闭合胃远端及近端胃小弯侧,在Trietz韧带下50~80 cm处分离空肠袢,切断空肠后用手工或吻合器将远端空肠与近端胃大弯侧吻合,将近端空肠吻合于距胃空肠吻合口远端60~120 cm处,完成GBP手术。其中,1例胃癌患者加做远端胃癌根治术。
1.4 统计学方法
所有数据用SPSS 11.0软件进行统计分析。计量资料采用均数±标准差()表示,手术前后比较用 t检验,以 P<0.05为差异有统计学意义。
2 结果
2.1 手术前后血糖水平及相关值的变化比较
与术前相比,胃转流术后,患者平均FBG由术前的(12.4±2.6) mmol/L 降至术后的(6.3±1.4)mmol/L,2 h PG 由(16.1±3.7)mmol/L 降至(8.5 ±3.2) mmol/L,6个月后 HbA1c由术前的(7.9±1.5)mmol/L 降至术后(6.8±0.6)mmol/L,胰岛素抵抗指数(IRI)由(6.6±0.9)mmol/L 降至(3.2±0.4)mmol/L,差异均有高度统计学意义(均P<0.01)。见表1。
表1 手术前后血糖水平及相关值的改变比较 (,n=11)
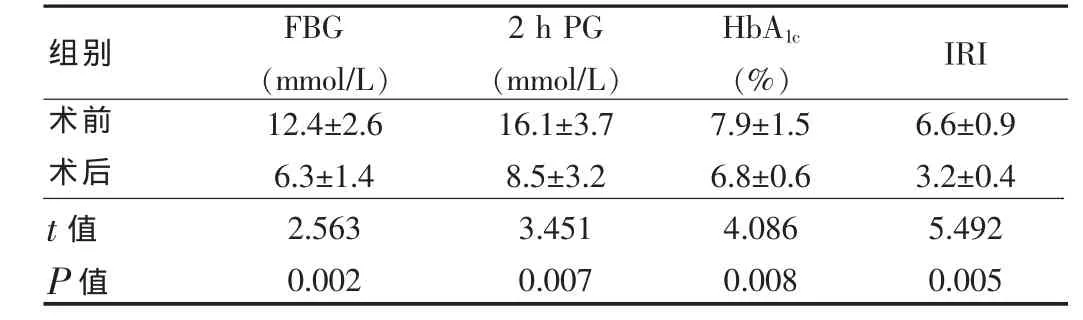
表1 手术前后血糖水平及相关值的改变比较 (,n=11)
术前术后t值 P值组别 FBG(mmol/L)12.4±2.66.3±1.42.5630.0022 h PG(mmol/L)16.1±3.78.5±3.23.4510.007 HbA1c(%)7.9±1.56.8±0.64.0860.008 IRI 6.6±0.93.2±0.45.4920.005
2.2 糖尿病及并发症的转归
11例术后6个月按T2DM诊断标准对照,治愈8例(72.8%),好转3例 (27.2%)。术前T2DM患者出现的眼底病变、高血压及肾病等并发症均有不同程度的缓解;2例糖尿病足患者术前经久不愈的皮肤溃疡在术后2个月内治愈;2例高血压病患者术后半年血压恢复正常;有2例仍需依靠药物控制血糖,但用药剂量较前明显减少;另有2例由术前注射胰岛素控制血糖改为口服降糖药控制。
3 讨论
3.1 外科治疗适应证和禁忌证
现已明确GBP手术的适应证是肥胖症并存T2DM。患者无严重并发症,病程<5年,越早手术治疗,血糖恢复可能性越大,病程长的疗效较差,这可能与β细胞功能受损后能否完全恢复有关[2]。但约有60%的T2DM不伴有肥胖,章勇等[3]报道采用手术治疗非肥胖的T2DM患者或动物实验,取得良好效果。王瑜等[4]研究证实GBP手术对非肥胖T2DM有较好的治疗作用,而不依赖于体重的降低。张新国等[5]对42例T2DM(其中,20例为非肥胖者,BMI<24)实施GBP术后1个月治愈40例,好转2例。上述报道均提示GBP对非肥胖T2DM也同样有效果。本组中3例非肥胖T2DM患者行GBP术,术后随访1年,血糖控制水平稳定,与上述研究基本相符。值得注意的是,只有术前检查提示血清胰岛素和C肽值升高或正常才适合做GBP,如降低,则可能提示胰岛功能不全或衰竭,应考虑为T1DM或晚期T2DM大量β细胞损害,分泌功能几乎消失,这是GBP手术治疗DM的禁忌证。
3.2 外科治疗机制探讨
GBP手术治疗T2DM的确切机制尚未完全明了,可能与以下机制有关。
3.2.1 术后胃肠激素的变化 GBP术后十二指肠和部分空肠旷置,以致未完全消化的食物较早被送至回肠、十二指肠和部分空肠被排斥出肠-胰岛轴。体内胃肠激素,如抑胃肽(gastricinhibitory polypeptide,GIP)、胰高血糖素样肽(glucagonlike peptide 1,GLP-1)、Ghrelin、肽 YY(peptide YY,PYY)、瘦素(leptin)、脂连素(adiponectin)和胰岛素样生长因子-1(insulin growth factor-1,IGF-1)等,发生一系列变化,有前肠和后肠两种假说。目前认为,GLP-1是肠-胰岛轴中控制T2DM最核心的介导因子[6]。GBP术后GLP-1水平升高可能与未消化食物直接到达回肠末端刺激L细胞分泌有关。GLP-1能促进糖原合成及脂肪分解,抑制胃排空及胰高血糖素分泌,增加胰岛素的基因表达和胰岛素前体的合成,促进β细胞增生与抑制凋亡,改善β细胞功能。
3.2.2 体重下降和饮食减少 肥胖症患者术后DM得到控制曾被认为是体重下降的原因,但目前资料表明可能与体重下降无关,通常术后血糖和胰岛素恢复正常远远早于显著体重下降[7]。GBP手术使胃容积明显缩小,减少进食量及减肥,但与此相似的胃束带术及袖状胃减容术却很难达到降低血糖的效果[8]。大多数学者认为,GBP后饮食减少不是控制血糖的主要原因。本组3例T2DM患者无病理性肥胖,术后摄食量并无减少,体重亦无明显变化,由此说明GBP手术控制T2DM的机制可能与摄入的热量减少和体重变化无关。
糖尿病是一种古老的内科疾病,传统的内科治疗方法很难从根本上治愈,也无法阻止糖尿病各种并发症的发生和发展,患者迫切需要一种能良好控制糖尿病及其并发症的治疗手段。本组11例T2DM患者术后均取得了良好的疗效,结合国内外相关文献研究,证明GBP是治疗T2DM的一种安全有效可行的方法,对经历长期的非手术治疗后效果不佳或不能耐受的T2DM患者,可考虑行此类外科手术治疗。
[1]Buchwald H,Avidor Y,Braunwald E,et al.Bariatric surgery:a systematic review and meta-analysis[J].JAMA,2004,292(14):1724-1737.
[2]John B,dixon,Waltcr J,et al.Surgery as an effective early intervention for diabesily[J].Diabetes Care,2005,28(2):472-474.
[3]章勇,陈宗祜,朱江帆,等.胃转流术治疗2型精尿病的实验研究[J].中国临床医学,2006,13(6):960-962.
[4]王瑜,王燕婷,王烈.胃转流术对非肥胖型2型糖尿病的治疗作用[J].中国普通外科杂志,2008,17(10):1003-1006.
[5]张新国,杨学军,徐红,等.胃转流手术治疗2型糖尿病胰岛素抵抗改变的临床研究[J].武警医学,2007,11(4):309-310.
[6]Aylwin S.Gastrointestinal surgery and gut hormones[J].Curr Opin Endocrinol Diabetes,2005,12:89-98.
[7]Anderson JW,Cenley SB,Nicholas AS.One hundred pound weight losses with an intensive behavioral program:changes in risk factors in l18 patients with long-term follow-up [J].Am J Clin Nutr,2007,86(2):301-307.
[8]Meneghini LF.Impact of hariatric surgery on type 2 diabetes [J].Cell Biochem Biophys,2007,48(2/3):97-102.

