二氧化碳捕获材料的研究进展
付 新
(渭南师范学院化学与生命科学学院,陕西 渭南 714000)
随着全球气候变暖加剧,减少二氧化碳(CO2)等温室气体排放、保护环境成为当前要解决的全球核心问题之一。CO2是引起温室效应的主要气体之一,是化石燃料和生物质燃烧以及动物新陈代谢的产物,其中化石燃料燃烧产生的CO2是其主要来源。CO2过量排放使区域生态环境系统中碳含量失衡,引起全球变暖,将导致冰山融化、海平面上升、海岸线退后以及洪水频增等一系列后果,对社会和经济发展以及人类生存产生恶劣的影响。然而,CO2同时也是一种潜在的碳资源,作为化工原料、致冷剂、油田驱油增产剂、惰性介质、溶剂和压力源等在国民经济各领域有着广泛的用途[1]。因此,如何将排放到大气中的CO2变废为宝受到了广泛的关注。由于在实现CO2富集再利用的过程中捕获成本最高,也最为核心,为了实现CO2减排和碳资源的有效利用,各种高效、环保、节能的CO2捕获材料已成为当前各国研究的重点。
1 传统捕获材料
1.1 醇胺类吸附剂
溶液吸附在传统意义上主要是利用含有胺基官能团的溶液,通过化学吸收法捕获CO2,目前常用的吸附剂是醇胺类溶液,包括一级醇胺(如乙醇胺)、二级醇胺(如二乙醇胺、二异丙醇胺)、三级醇胺(如甲基二乙醇胺、三乙醇胺)及立体障碍醇胺,在立体障碍醇胺方面,目前最常用也最常见于文献报道的为AMP,这也是国外相当多研究及工业单位所重视的研发项目之一[2]。
化学吸收法是利用吸收剂与CO2发生化学反应达到回收CO2的目的,并利用其逆反应进行吸收剂再生。该法脱除率较高,是目前回收最有效的方法之一,并且适合于处理分压低的混合气体。但仍有许多缺点:胺容易发生氧化降解使得吸收性能降低,同时还会造成溶液粘度增加,不利于气体的传输;胺及其降解物在吸收剂再生时易挥发,使其吸收能力下降;胺溶液的强碱性对仪器设备的腐蚀作用特别严重;操作较繁琐,再生耗能高[3]。
1.2 离子液体吸附材料
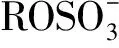
吴永良等[5]以N-甲基咪唑和3-溴丙胺氢溴酸盐为起始原料,合成了一种含氨基的离子液体1-(1-氨基丙基)-3-甲基咪唑溴盐(简写为[NH2p-mim]Br),吸收实验结果表明,该离子液体能够有效地吸收CO2,在40 ℃、106 kPa下,质量分数为45%的离子液体水溶液吸收CO2至饱和时,溶液中CO2的摩尔分数可达0.444 molCO2·(mol ILs)-1,接近理论吸收量0.5 molCO2·(mol ILs)-1;在90 ℃、真空状态下,吸收的CO2能够完全解吸,重复吸收实验表明,该离子液体吸收CO2的能力无明显下降。
1.3 金属化合物材料
用来捕获CO2的金属化合物材料主要分为两类:一类是金属氧化物如Na2O、K2O、CaO、MgO、Al2O3、Li2O及ZrO2;另一类是碱性金属盐,如碳酸钙、硅酸盐、硅酸锂、锆酸锂等。由于CO2是酸性气体,容易吸附在略带碱性的材料表面,且在高温下金属氧化物均有较好的吸附能力,因此此类吸收剂通常属于高温吸附剂,反应生成的碳酸盐在高温下能重新分解成金属氧化物和CO2。目前钙基吸收剂、锆基吸收剂和锂基吸收剂是研究的重点。
白涛等[6]对CaO吸收进行了研究,CaCO3在高温下受热分解,产生具有大比表面积的多孔CaO。CaO与CO2发生气-固反应生成CaCO3吸收烟气中的CO2,降低CO2排放量。同时,生成的CaCO3煅烧产生的CO2因纯度较高可以直接存储,易于工业利用。CaO因具有高的CO2吸附容量、低的制备成本、较长的使用寿命及良好的抗磨性而成为优选的高温CO2脱除剂。但CaO颗粒表面易形成CaCO3膜,CO2难以扩散到颗粒内部与CaO进一步反应,导致转化率下降,且煅烧温度超过900 ℃时,生成的颗粒容易烧结从而降低CO2吸收能力。
1.4 陶瓷材料
锆酸锂、硅酸锂等含锂陶瓷材料具有很好的吸附CO2性能,目前已有学者投入到吸收CO2的新型陶瓷材料的研究中。
2001年,日本东芝公司成功开发出一种用于吸收CO2的新型陶瓷材料——硅酸锂。该材料吸收CO2的能力超过其它陶瓷材料,且可在室温下吸收CO2。硅酸锂的CO2吸收率比传统的锆酸锂和锆过渡金属氧化物高出30倍。在CO2浓度为20%的条件下,1 g硅酸锂每分钟可吸收62 mg CO2[7]。
王银杰等[8]在500~800 ℃下合成了Li2ZrO3(ZrO2+Li2CO3= Li2ZrO3+CO2),该吸收剂吸收性能较优异,在含20%CO2的空气气氛下,于500 ℃下保持3 h,吸收量达到(25±0.6)%(质量分数)。
王银杰等[9]以SiO2和碳酸锂为原料,采用高温固相反应法于500~750 ℃下合成了一系列可在高温下直接吸收CO2的硅酸锂材料(Li4SiO4)。结果表明,在750 ℃下煅烧6 h可合成出CO2吸收性能良好的硅酸锂材料。在CO2气氛下,于750 ℃保温15 min即可达到吸收平衡,吸收量约为43%。
中川和明等[10]在进行熔融碳酸盐陶瓷的稳定性实验时,发现了如下的反应:Li2ZrO3+CO2→ZrO2+Li2CO3。他们推测该反应可以扩大到含锂复合氧化物与CO2的反应,生成新的氧化物和碳酸锂。通过一系列实验,发现除锆酸锂以外,硅酸锂等也可以发生可逆反应:Li4SiO4+CO2→Li2SiO3+Li2CO3。多孔体的硅酸锂材料,在500 ℃左右同含有CO2的气体接触而发生化学反应,CO2以碳酸锂的形态存在于多孔体的微孔中,700 ℃以上碳酸锂分解放出CO2气体。
吕国强等[11]以Li2CO3、SiO2和无水乙醇为原料采用固相法合成Li4SiO4,该材料在600~720 ℃吸附CO2反应最为活跃,最高吸附量可达29.16%(质量分数)。锂基吸附剂相对其它金属化合物吸附剂而言CO2前后体积变化不大,Li2ZrO3经过18次吸附-解吸循环后,材料的吸附量仅衰减1.1%(质量分数)左右。锂基吸附剂的理论吸附量为36.66%,仍存在极大的发展潜力,是一种有前途的高效吸附剂。
总的来说,陶瓷材料对CO2的吸附量很高,可以进行多次循环吸附,无污染,对环境友好,是一类比较理想的CO2捕获材料。
1.5 沸石分子筛材料
沸石分子筛是天然或人工合成的含碱金属或碱土金属氧化物的结晶硅铝酸盐,有严格的结构和孔隙,孔隙大小因结构差异略有变化,可对不同分子量物质进行分离。沸石分子筛材料的吸附性能主要取决于两方面:一是其丰富的孔道结构和大的比表面积,可为吸附质提供足够的吸附中心;二是其表面的电性质,由阳离子和带负电荷的硅铝氧骨架所构成的沸石分子筛本身是一种极性物质,其表面具有很强的色散力和静电力,表现为对极性、不饱和及易极化分子强大的亲和力。沸石分子筛吸附剂常用于气体分离和净化,如空气制氮、CO2的分离与纯化等。
赵忠林等[12]以凹凸棒土为粘结剂制备了13X分子筛吸附剂。凹凸棒土丰富的孔隙结构、纳米颗粒的大表面效应和表面负电性,使得该分子筛吸附剂具有较大的吸附量,最大达到24.6%(质量分数),且CO2与凹凸棒土相互作用较弱,有利于脱附。但在分压低的高温烟道气中,此类吸附剂不适用。
美国加州大学洛杉矶分校科研人员研制出了一种新型的多孔晶体材料——沸石咪唑酯骨架结构材料(ZIFs)。该材料是将传统沸石中的硅元素和铝元素用锌离子和钴离子等取代,而桥氧用咪唑酯取代。ZIFs材料具有多孔和化学稳定结构,有着更大的比表面积(2000 m2·g-1)来吸收CO2,而且在高温下加热也不会分解,甚至在水或有机溶液中煮一个星期仍能保持稳定。ZIFs材料的内部可以存储气体分子,在化学结构上,它有一个类似于旋转门的薄盖,能够让大小合适的分子进入并将其存储,而将较大或者形状不同的分子阻挡在外。与传统的沸石分子筛体系相比,该材料具有产率较高、微孔尺寸和形状可调、结构和功能变化多样等特点,但是其合成对设备和材料的要求高、合成条件不易控制,现阶段还不能大规模生产。
1.6 碳基吸附材料
碳质吸附剂包括活性炭及活性碳纤维、多孔炭材料、炭分子筛材料以及碳纳米管等纯碳结构的吸附剂,它们具有发达的孔隙结构、大的比表面积、优良的吸附性能和稳定的物理化学性质,广泛应用于吸附分离、净化和催化等领域[13]。
活性炭是一种最常见的大比表面积的黑色孔性吸附剂,其主要成分为无定型碳,还有少量的氢、氧、氮、硫及灰分。原材料、制备工艺和活化方法不同,使得活性炭的理化性质和表面化学性质都会有很大差异。决定活性炭吸附能力大小的主要因素是比表面积、孔结构、表面性质和吸附质的吸附特性。
活性碳纤维由有机纤维经炭化、活化而得到,是继活性炭粉末、活性炭颗粒后的第三代炭材料,活性碳纤维较颗粒状活性炭比表面积更大、微孔直径更小,且微孔体积占总孔体积的90%以上,同时直接开口于纤维表面,因而具有吸附容量大、吸附效率高、吸脱附速度快等优点。由于其结构和性能的特殊性,用活性碳纤维吸附空气污染物已成为研究热点,并表现出巨大的应用前景。
离子交换纤维可用于净化、分离气体。离子交换纤维吸附气体具有化学吸附的特征,且吸附剂可以再生。吴政等[14]通过NaOH(2 mol·L-1)溶液浸泡的方法制得强碱性阴离子交换纤维。纤维含水量越大,对CO2的吸附效果越好,且CO2的流速只要不超过某个极限都利于吸附,CO2浓度对吸附效果影响较小。
1.7 硅胶材料
硅胶是由多聚硅酸经分子内脱水而形成的一种多孔性物质,其化学组成为SiO2·xH2O,属于无定型结构。硅胶的基本结构质点为Si-O四面体,由Si-O四面体相互堆积形成硅胶的骨架堆积时,质点内的空间即为硅胶的孔隙。
梅华等[15]比较了两种硅胶型吸附剂对CO2的吸附性能,测定了N2和CO2在硅胶和活性炭吸附剂上的吸附等温线,并考察了不同体系中CO2动态吸附穿透曲线。结果表明,硅胶吸附剂对CO2的吸附量与活性炭相当,吸附选择性优于活性炭;较大的比表面积和较高的细孔含量对吸附有利,而合适的孔分布则有利于降低硅胶吸附剂的内扩散阻力。
2 新型捕获材料
2.1 复合型捕获材料
复合材料(Composite materials),是由两种或两种以上不同性质的材料通过物理或化学的方法在宏观上组成的具有新性能的材料。不同材料在性能上互相取长补短,产生协同效应,使复合材料的综合性能优于原组成材料而满足各种不同的要求。
近年来,复合材料由于其优越的性能也越来越多的用在CO2吸附方面,具有代表性的有水滑石类混合吸附材料(HTlcs)、复合型胺基吸附纤维、介孔复合材料以及复合纳米材料等。
2.1.1 水滑石类混合吸附材料
天然复合材料水滑石含有碱性金属化合物,同时具有微孔结构,是一类带阴离子的碱性粘土,可用通式表示:
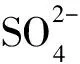
有关实验表明[16]:CO2在水滑石EXM696上的吸附量随温度的变化而变化,当温度从20 ℃升至200 ℃时,吸附量减小;继续升温至300 ℃,吸附量反而增大。这是由于低温时主要表现为物理吸附,吸附量随温度的升高而减小,高温时为化学吸附,温度升高吸附量反而增大,而且大于20 ℃时的吸附量。由于化学吸附的吸附热较大,约为8.37×104~41.9×104J·mol-1,化学吸附速度随温度升高而加快,故吸附宜在高温下进行,对吸附气体有较高的选择性。反应一般不可逆或只能在1000 ℃以上的高温下分解,因而其脱附难于实现,只能进行单层或不满单层吸附,吸附量的大小与可进行化学反应的基团和物质的量成正比。
2.1.2 复合型胺基吸附纤维
李培源等[17]以玻璃纤维作为基底复合聚乙撑亚胺(PEI),制得含多胺基的复合型吸附纤维,系统考察了不同原料比例下该吸附纤维的化学结构、热稳定性能及交换容量,测定了该吸附纤维的吸水率,在饱和水蒸气和干燥条件下对CO2的吸附性能,以及作为CO2气体吸附材料的重复使用及再生性能。研究表明,适当的交联剂用量可使该吸附纤维在250 ℃左右仍保持热稳定。该吸附纤维具有较高的交换容量,最高可达3 mmol·g-1以上;在饱和水蒸气环境中,该吸附纤维对CO2的吸附量可达20%(质量分数)以上,但吸附量随着交联程度的提高而减小。该吸附纤维具有良好的重复使用及再生性能,经再生处理后,吸附纤维对湿态CO2的吸附量变化不大。
2.1.3 介孔复合材料
方建慧等[18]以介孔分子筛原粉作载体,负载不同有机胺制备CO2吸附材料。固体胺吸附剂通过化学作用,可选择性吸附酸性气体CO2,受水蒸气影响较小。采用具有高比表面积和孔体积的介孔材料为载体,制备的固体胺吸附剂表现出了高吸附量的特性。特别是保留了介孔材料原粉里所含的模板剂胶束,在介孔空间里组成不同尺度的“网孔”对气流中的CO2进行拦截和吸附,吸附效率较高,与微孔材料相比,这种复合材料可以达到很高的气体流通量;与普通介孔材料相比,其拦截效率和孔分布又高出一筹。这种复合新材料的特点在于直接利用原粉样品中胶束的疏松结构。胶束径向呈轮辐状态分布,为客体提供足以支撑网格结构的几何位置,从而形成密集的空间拦截构型。另外,与采用去除模板剂的介孔分子筛相比,介孔分子筛合成原粉作为载体,既节省去除模板剂所需的能源与时间,在提高CO2吸附量的同时又降低吸附剂的成本。但相对于工业实际应用,以介孔分子筛为基体的固体胺吸附剂还是存在制备成本高、循环使用寿命短的缺点。因此,固体胺吸附剂的研究仍要围绕解决成本(吸附剂制备成本和使用成本)、吸附量以及使用寿命的问题。
2.1.4 复合纳米材料
法国国家科研中心于2008年研制出一种名为MIL-101的新型材料,能大量吸附CO2气体,这种材料由铬元素和对苯二甲酸合成,是一种多孔的复合纳米材料,材料表面布满了直径3.5 nm的小孔,因此吸附能力十分强大,1 m3MIL-101在25 ℃下可以吸附400 m3的CO2,而目前通用的吸附材料在同等条件下的CO2吸附量不过200 m3,这种新型材料可以安放在汽车上,对其排出的CO2进行过滤,从而达到减排温室气体的目的。
2.2 负离子选择性吸附材料
丁浩等[19]对负离子选择性吸附材料进行了研究。这类材料是以天然极性矿物电气石为基体,复合具有选择性吸附功能物质的空气净化材料,通过电气石释放负氧离子的功能和对CO2及有害气体的吸附、去除作用,完成对室内居住环境中空气污染的净化治理,其无源释放负氧离子产生的节能作用、直接吸收CO2气体和复合制备绿色建筑材料产生的环境效应代表了这一空气净化材料的低碳生活理念。
3 结语
随着人们环保意识的逐渐加强,各个国家对环境保护力度加大,必然会对CO2捕获材料的发展起到积极的促进作用。近年来,CO2捕获材料的研究已取得了很大进展,CO2捕获技术正向价廉、操作简单、运行成本低、可循环使用的方向发展。这就要求CO2捕获材料必须具有生产原料价廉易得、生产工艺简单且环保、再生能力好、可循环使用等特点,并要求能同时处理CO2、硫化氢、氮的氧化物等多种污染物。因此,智能性CO2捕获材料成为未来发展的趋势,要求新材料能在不同气氛下,根据环境变化,适当调节自身的表面性质,增强吸附性。
[1]杨圣儒.二氧化碳应用进展[J].广东化工,2005,32(8):1-4.
[2]顾洋,邱炳嵌.台湾在二氧化碳捕获及再利用中的技术研究状况[J].太原理工大学学报,2010,41(5):670-674.
[3]岳明波,朱建华.从介孔分子筛原粉研制高效吸附CO2的有机胺-介孔复合材料[J].催化学报,2008,29(10):1051-1057.
[4]王仲妮,王洁莹,司友华,等.咪唑类离子液体的研究进展[J].化学进展,2008,20(8):1057-1063.
[5]吴永良,焦真,王冠楠,等.用于二氧化碳吸收的离子液体的合成、表征及吸收性能[J].精细化工,2007,24(4):324-327.
[6]白涛,王春波,李永华,等.CaO颗粒吸收CO2特性研究[J].电站系统工程,2007,23(5):21-26.
[7]张永伟,税安泽,曾令可,等.CO2吸收剂的研究进展[J].陶瓷,2008,(3):5-8.
[8]王银杰,其鲁,王祥云.高温下锆酸锂吸收CO2的研究[J].无机化学学报,2003,19(5):918-922.
[9]王银杰,其鲁,王祥云.高温下硅酸锂吸收CO2的研究[J].无机化学学报,2006,22(2):268-272.
[10]中川和明,胡溯帆,胡海泉,等.吸收CO2特陶的开发[J].陶瓷研究,2004,(2):39-40.
[11]吕国强,王华,马文会,等.Li4SiO4吸收CO2的实验研究[J].工业加热,2007,36(5):4-7.
[12]赵忠林,李鹏飞,马静红,等.凹凸棒土粘结剂对13X分子筛吸附性能的促进作用[J].离子交换与吸附,2008,24(1):25-32.
[13]吕伟,杨全红,康飞宇.碳质吸附剂对CO2的吸附、捕集和分离[J].化工进展,2009,28(6):1054-1058.
[14]吴政,崔成民,田树盛,等.强碱性离子交换纤维对二氧化碳吸附的研究[J].劳动保护科学技术,1999,19(2):25-28.
[15]梅华,陈道远,姚虎卿,等.硅胶的二氧化碳吸附性能及其与微孔结构的关系[J].天然气化工,2004,29(5):21-25.
[16]李莉,袁文辉,韦朝海.二氧化碳的高温吸附剂及其吸附过程[J].化工进展,2006,25(8):918-922.
[17]李培源,陈水挟,张其坤,等.复合型胺基吸附纤维及其对二氧化碳的吸附性能[J].离子交换与吸附,2008,24(3):232-239.
[18]方建慧,沈霞,包伯荣.分子筛对微量二氧化碳的吸附[J].离子交换与吸附,1999,15(2):190-193.
[19]丁浩,陈荣坤.负离子-选择性吸附材料的功能与低碳理念[J].中国非金属矿工业导刊,2010,(4):11-12.

