老年下肢动脉疾病患者中CXCL16与血管新生的关系
诸葛欣,孙 宁,王丽莉,陈翊玲,张 蕴
(1天津医科大学总医院,天津300052;2 Old Dominion University,USA)
周围动脉性疾病是老年人中的高发病,其中下肢动脉疾病(PAD)可导致老年人活动能力下降,进一步影响患者的生活质量。有研究提示,PAD的加重是远期心血管事件死亡的独立危险因素[1]。动脉粥样硬化性血管闭塞导致了组织的缺血和不同程度的侧支血管形成,其中由血管内皮生长因子(VEGF)为代表的一系列血管生长因子对血管新生过程的调控决定了侧支循环的程度,影响着临床表现和预后。巨噬细胞趋化因子配体16(CXCL16)是近年来被发现的具有清道夫受体功能的炎性趋化因子[2],体外实验提示该分子具有对内皮细胞的促血管新生作用[3],本研究旨在探索老年PAD患者中CXCL16的水平及其促血管新生的意义。
1 资料与方法
1.1 临床资料 选择2007年1月~2009年12月在天津医科大学总医院干部病房查体和就诊的老年男性50例,年龄60~92岁。将入选者随机分为对照组[踝臂指数(ABI)>1.0]和 PAD组(ABI<0.9)。PAD有间歇性跛行或行下肢血管重建、有明确影像学诊断证据。排除心肌梗死、心衰、脑血管病、肾脏功能异常、恶性肿瘤、免疫系统疾病以及其他研究者认为不适合入选的疾病。
1.2 方法
1.2.1 血生化指标的检测 对照组和PAD组于清晨空腹采集静脉血,送生化室按照规定方法进行空腹血糖(FPG)、总胆固醇(TC)、甘油三酯(TG)、高密度脂蛋白(HDL)、低密度脂蛋白(LDL)等指标的检测。
1.2.2 ABI的检测 采用日本Colin公司的全自动动脉硬化检测仪,在清晨安静状态下,让患者取平卧位,在上臂和踝部分别绑扎传感器,输入相关信息由机器自动完成。
1.2.3 血管生长因子的检测 研究对象于清晨空腹静脉采血,立即放入4℃ 冰箱,1 h内4℃离心(2 500 r/min),取上层血清-80℃保存待测。CXCL16、VEGF的检测采用R&D Systems试剂盒,酶联免疫分析法进行检测,操作按试剂盒说明进行,批内差异<10%,批间差异<15%。
1.2.4 EPCs的分离和检测 按常规方法分离外周血的单核细胞[4],并悬浮于 200 μl的 PBS 中(含0.5%小牛血清和2 mm的EDTA),加入标记的单克隆抗体 CD133/CD34,经流式细胞仪(BD FACS ArisTM,美国BD公司)计数测定。
1.3 统计学方法 采用SPSS13.0统计软件,计量资料符合正态分布以±s表示,不符合正态分布的用中位数(四分位数间距)表示,组间比较符合正态分布的用方差分析,不符合正态分布的用Mann-Whitney检验;计数资料用百分比表示,比较采用列联表χ2检验。CXCL16与EGFR、EPCs之间的相关性用Spearman相关检验。P≤0.05为有统计学差异。
2 结果
2.1 两组基本资料比较 PAD组中糖尿病、高血压、高血脂的患病例数分别为9、16、11例。两组基线资料的比较见表1。
2.2 两组促血管新生因子和EPCs的比较 见表2。
2.3 CXCL16与VEGF和EPCs的相关分析 对照组中 CXCL16与VEGF和EPCs均呈正相关(r=0.463,P=0.033;r=0.359,P=0.043);PAD 组中CXCL16 与 VEGF 呈正相关(r=0.307,P=0.031),与 EPCs不相关(r=0.114,P=0.265)。

表1 两组基本资料比较
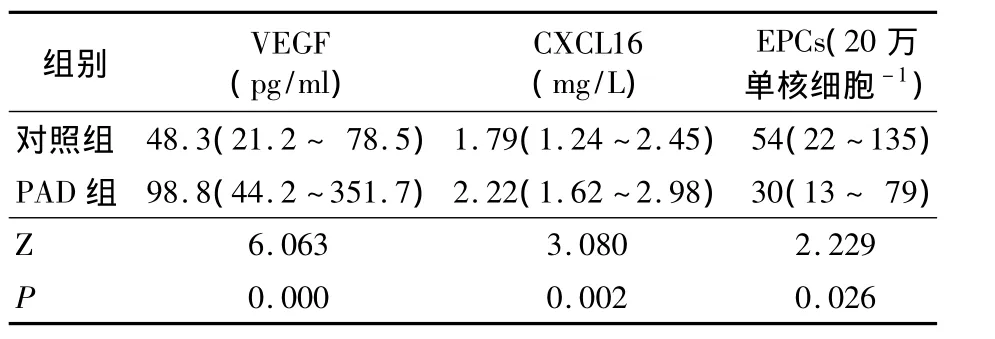
表2 两组促血管新生因子和EPCs的比较
3 讨论
PAD是老年人中的高发病,特征主要为周围动脉特别是下肢动脉的粥样硬化性病变导致的组织缺血,以及不同程度的侧支循环形成,并因此决定了临床症状的严重程度和预后。
CXCL16是近年来被发现的具有清道夫受体功能的炎性趋化因子[2],体外实验证明,该分子可以促进内皮细胞增殖、迁移和管状结构的形成[3],并在小鼠体内Matrigel血管新生模型中得到验证[5],推论CXCL16是一个具有促血管新生作用的化学趋化因子。
血管新生是一个极其复杂的过程,需要多种生长因子协同参与。缺血、缺氧是血管生成的触发因素,促进VEGF等一系列调节血管生成的细胞因子表达,激活内皮细胞,启动血管生成过程,使细胞对缺氧作出反应。有研究认为,CXCL16可显著增强MMP-2和MMP-9的活性[6],而后者可以促进包括VEGF在内的细胞外基质结合因子的生成,从而诱导EPCs并增强因组织缺血而引发的血管新生[7]。
EPCs是一种能直接分化为血管内皮细胞的前体细胞,具有高增殖潜能及内皮特性,主要定居于骨髓中,外周血中含量很少[8],它具有较强的增殖、迁移、分化能力,在血管新生和维持血管完整性中起重要作用[9]。研究表明,具有血管并发症的糖尿病患者与无血管并发症的糖尿病患者相比,循环EPCs数目显著降低,并且其数目与血管并发症的严重程度密切相关[10]。
本研究显示,PAD患者CXCL16、VEGF水平较对照组显著增高,而EPCs水平显著降低,反映了机体对组织缺血代偿性上调促血管新生因子,动员EPCs到外周血,参与缺血组织的血管新生过程。该结果与Findley等[11]研究结果相一致。进一步相关分析显示,两组中CXCL16均与VEGF呈正相关,对照组中与EPCs数量呈正相关,提示CXCL16具有与VEGF类似的促血管新生作用。虽然相关研究中的P<0.05,但相关性不是很好,原因可能为样本量较小,因此需要进一步较大样本的研究对结论加以证实和完善。
[1]Sakamoto S,Yokoyama N,Tamori Y,et al.Patients with peripheral artery disease who complete 12-week supervised exercise training program show reduced cardiovascular mortality and morbidity[J].Circ J,2009,73(1):167-173.
[2]Matloubian M,David A,Engel S,et al.A transmembrane CXC chemokine is a ligand for HIV-coreceptor Bonzo[J].Nat Immunol,2000,1(4):298-304.
[3]Zhuge X,Murayama T,Arai H,et al.CXCL16 is a novel angiogenic factor for human umbilical vein endothelial cells[J].Biochem Biophys Res Commun,2005,331(4):1295-1300.
[4]Hildbrand P,Cirulli V,Prinsen RC,et al.The role of angiopoietins in the development of endothelial cells from cord blood CD34 progenitors[J].Blood,2004,104(7):2010-2019.
[5]诸葛欣,孟艳玲,孙宁,等.CXCL16对小鼠Matrigel种植体内促血管新生的作用[J].细胞与分子免疫学杂志,2010,26(11):1095-1096.
[6]Dahl CP,Husberg C,Gullestad L,et al.Increased production of CXCL16 in experimental and clinical heart failure:a possible role in extracellular matrix remodeling[J].Circ Heart Fail,2009,2(6):624-632.
[7]Huang PH,Chen YH,Wang CH,et al.Matrix metalloproteinase-9 is essential for ischemia-induced neovascularization by modulating bone marrow-derived endothelial progenitor cells[J].Arterioscler Thromb Vasc Biol,2009,29(8):1179-1184.
[8]Werner N,Kosiol S,Schiegl T,et al.Circulating endothelial pro-genitor cells and cardiovascular outcomes[J].N Engl J Med,2005,353(10):999-1007.
[9]Mukai N,Akahori T,Komaki M,et al.A comparison of the tube forming potentials of early and late endothelial progenitor cells[J].Exp Cell Res,2008,314(3):430-440.
[10]Fadini GP,Sartore S,Albiero M,et al.Number and function of endothelial progenitor cells as a marker of severity for diabetic vasculopathy[J].Arterioscler Thromb Vasc Biol,2006,26(9):2140-2146.
[11]Findley CM,Mitchell RG,Duscha BD,et al.Plasma levels of soluble Tie2 and VEGF distinguish critical limb ischemia from intermittent claudication in patients with peripheral arterial disease[J].J Am Coll Cardiol,2008,52(5):387-393.

