超声造影在经皮微波凝固治疗肝细胞癌前的应用
黄国喜,付文生,魏国兴,孔学军
经皮微波凝固治疗(percutaneous microwave coagulation therapy,PMCT)可实现肝癌组织的凝固性坏死[1],已经成为肝癌非手术治疗的重要手段。该疗法具有升温快、热效率高,凝固彻底等优点,最常用的引导方法是超声,而常规多普勒超声引导的 PMCT原位复发率相对较高。本研究将肝细胞癌的常规彩色多普勒超声 (color Doppler flow imeging,CDFI)与超声造影(contrast-enhanced ultrasonography,CEUS)图像特点的差异进行比较,探讨PMCT前超声造影对制定肝细胞癌PMCT治疗方案的应用价值。
1 资料与方法
1.1 一般资料 2007-11~2009-12,83例拟行 PMCT 肝细胞癌(hepatocellular carcinoma,HCC)患者,男 60 例,女 23例;年龄38~71岁,平均61岁。诊断均经穿刺活检病理证实。
1.2 仪器方法 采用Vivid 7彩色多普勒超声诊断仪,具有低机械指数谐波超声造影功能。常规二维超声及彩色多普勒血流检查,记录病灶数目、大小,观察病灶内血流信号。采用意大利博莱科(Bracco)公司生产的微气泡造影剂 SonoVue冻干粉,使用前注入生理盐水5 ml,振荡混匀后抽取2.4 ml,经肘静脉注入人体,所有患者均采用团注法。利用低机械指数(0.06~0.08)观察病灶内造影剂的灌注情况,并对资料进行录像。造影后由2名医师负责常规彩色多普勒超声及造影资料的整理分析。
1.3 统计分析 采用SPSS 11.0软件进行统计学处理,计数资料数据显著性分析采用配对χ2检验。
2 结 果
超声造影显示83例86个病灶中有85个病灶 (98.8%)动脉期快速增强,静脉期及延迟期强度变弱,具有典型的HCC超声造影特征。51个病灶(59.3%)超声造影显示肿瘤大小较彩色多普勒超声增大,其中,边界欠清晰的肿瘤造影后71.7%范围增大。超声造影后,6个直径>6 cm的病灶和3个邻近重要结构(分别为距肝门、膈肌、胆囊距离<1.0 cm)的病灶改为手术治疗。CEUS与CDFI显示肿瘤主滋养动脉的病灶数分别为 76个(88.4%)和53个(61.6%),前者高于后者(P<0.01,表1)。
3 讨 论
经皮微波凝固治疗肝细胞癌的最佳效果是癌细胞完全性坏死,适应证的选择对指导临床治疗起着至关重要的作用[2,3]。PMCT前制定合理的排除标准,既保证患者肿瘤的彻底灭活效果,又减少了治疗过程中出现更加严重的并发症。
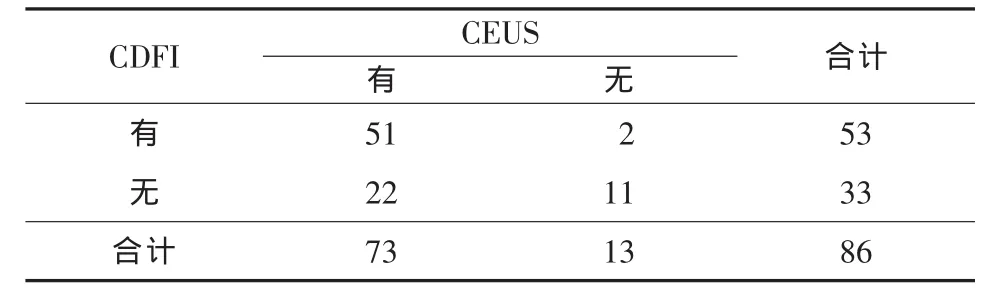
表1 CDFI及CEUS显示主滋养动脉肝细胞癌病灶结果(个)
本研究PMCT排除标准见于:①巨大(直径超过6 cm)或多于2个HCC病灶;②肝、肾功能严重受损;③严重黄疸、腹水者;④高热、恶病质、出血性疾病;⑤病灶距肝门部、胆囊及周围重要脏器<1 cm的HCC。可见,肿瘤的大小是PMCT纳入和排除标准的一项重要参考指标,同时,病灶边界的显示对于选择合理的无瘤治疗安全边缘非常重要,目前有学者认为以0.5~1.0 cm作为无瘤治疗安全边缘可有效减少肿瘤复发率,同时又不过多损伤正常肝组织[4]。本研究统计结果显示,59.3%HCC病灶在超声造影后测值较造影前明显增大。图像分析发现肿瘤的增大与造影前肿瘤边界密切相关。边界欠清晰的肿瘤造影后71.7%范围增大;CEUS动脉期有49个病灶(46.7%)显示形态不规则,部分病灶呈现分叶状或局部不规则增强特征,有助于了解肿瘤的浸润生长特征和浸润范围,并可清晰显示周围微血管浸润所显示出的肿瘤形状。
CEUS可准确识别主滋养动脉血管,微气泡造影剂到达肿瘤主滋养动脉时,由于动脉血流速度快,主滋养动脉血管的显像时间短,可为闪烁的强回声迅速充盈肿瘤血管,部分可见主干分支呈抱球样在肿瘤周边增强,之后造影剂进入瘤内致整体增强。超声造影显示肿瘤主滋养动脉的病灶数高于CDFI(P<0.01)。部分学者认为,对于病灶内血供过于丰富的患者,采用先阻断供血,再进行射频消融治疗的方法,获得的疗效将比单纯射频治疗治疗效果好[5,6]。本研究治疗过程中,在超声造影的指导下重点加强对部分病例滋养血管进入肿瘤区域的热凝固,或配合必要的动脉栓塞,有利于封断肿瘤的血供,从而减少或阻止血液流动带走一定的热量,使肝细胞癌的凝固治疗更加彻底。CEUS后可更加准确地显示肿瘤与肝门、胆囊及膈肌的关系,有助于制定更加合理的治疗方案,增加肿瘤的灭活率和减少并发症。
综上,在PMCT前进行肝细胞癌的CEUS,可更加准确地显示肿瘤的大小,肿瘤与重要邻近脏器的距离,更加清楚地呈现主滋养动脉血管的位置,为PMCT治疗方案的选择和实施提供重要的参考指标。
[1]代文杰,马 威,姜洪池.肝细胞癌的局部消融治疗[J].肝胆胰外科杂志,2006,18(5):326.
[2]罗葆明,智 慧,文艳玲,等.低机械指数谐波超声造影在局灶性肝病治疗适应证选择中的应用[J].中国临床医学影像杂志,2006,17(9):512.
[3]付文生,杨一林,朱少君,等.编码谐波造影在超声导向微波凝固治疗肝肿瘤前的应用[J].现代肿瘤医学,2008,16(3):403.
[4]Gazelle GS,Goldberg SN,Solbiati L,et al.Tumor ablation with radiofrequency energy.Radiology,2000,217:633.
[5]Ahrar K,Gupta S.Hepatic artery embolization for hepatocellular carcinoma:technique,patient selection,and outcomes.Surg Oncol Clin North Am,2003,12(1):105.
[6]罗葆明,杨海云,文艳玲,等.冷循环射频消融治疗肝细胞癌的疗效分析[J].中华超声影像学杂志,2005,14(3):208.

