环孢素治疗药物监测质控规则的比较与评价*
刘 云,欧 宁,刘 婷,张宏文,王蔚青
(南京医科大学第一附属医院·江苏省人民医院,江苏 南京 210029)
治疗药物监测已在国内普遍开展,其质量控制也日益受到临床药师的重视,但该项工作在我国尚处于研究和自愿参加阶段,没有形成完善的系统和规范。目前常见的做法是定期或每次测定患者样品时测定标准质控品,只要质控结果落在允许的误差范围内,则判断本批次结果正确。但这种做法忽略了质控评价的连续性,因而不能及时发现影响测定准确性的潜在因素。为此,笔者按照国家实验室管理的有关要求,对可能影响检测结果的人员、设备、方法等因素进行控制,对治疗药物监测实行全过程、全范围的质量管理;同时针对现行治疗药物监测质控对失控规则无明确规定的问题,参照临床检验质控设计评价方法,对本院随行质控数据进行分析评价,并建立适当的质控规则。现报道如下。
1 材料
质控数据来源于我院治疗药物监测实验室2009年全年的环孢素随行质控测定值。每次测定患者样品时测定质控样品,每次带1个质控样品,按低、中、高顺序循环进行。共测定低质控59份,中质控62份,高质控57份。测定方法为荧光偏振免疫法。
2 方法与结果
2.1 年度质控分析
依据2010年版《中国药典(二部)》[1]生物样品分析方法质量控制要求,按治疗药物监测常规做法,低质量浓度以靶值±15%、靶值±20%为限,中、高质量浓度分别以靶值±10%、靶值±15%为限,将数据划分为合格、警告、失控3个区段。低、中、高3种质量浓度质控数据在合格区段的分布比例分别为93.2%,91.9%,91.2%;在警告区段的分布比例分别为 6.8% ,8.1% ,8.8%;在失控区段均无分布。
2.2 Levey-Jennings控制方法[2]
计算出各质量浓度的平均值(X)和标准差(s),见表 1。将X,X ±2 s,X±3 s标在纵坐标轴上,通过各点作与横坐标轴平行的直线,分别称为靶值线、上警戒线、下警戒线和上失控线、下失控线,以测定值为纵坐标、测定时间为横坐标绘制环孢素年度质控图,见图1。2009年质控品均未超过X±3 s的失控线,据此规则判断均在控。
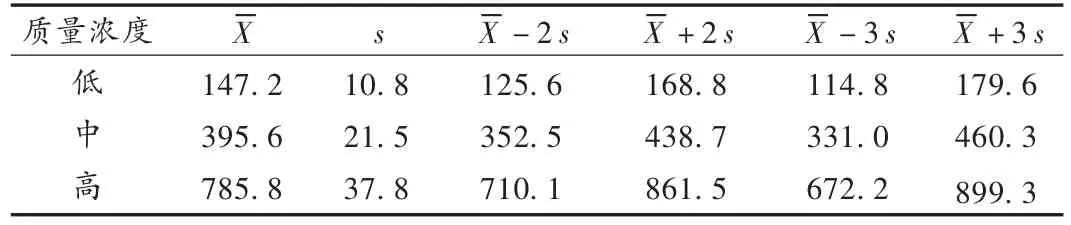
表1 2009年随行质控各质量浓度的X,X ±2 s,X±3 s值(ng/mL)
2.3 累计和质量控制方法[3]
本法主要用来监测测定方法的系统误差,在此选用CS-(1.0 s∶2.7 s)规则。计算出 k 值(ku=X+1.0 s,kl=X -1.0 s)和控制限(hu=2.7 s,hl= -2.7 s),计算质控测定值与阈值(k)之差,再求其累计和,然后由累计和是否超出控制限(h)来判断测定结果是否失控。根据累计和控制规则,2009-06-01低质控失控,2009-06-09中质控失控,2009-09-11中质控失控。
2.4 Westgard多规则控制方法[1]
采用多规则控制方法,12s/13s/22s/R4s/41s/10X,控制规则的逻辑图见图2。22s是指两个连续的控制测定值同时超过X+2 s或X-2 s控制限,R4s指在同一批内高、低控制测定值之间的差值超过4 s,41s指4个连续的控制测定值同时超过X+s或X - s,10X指10个连续的控制测定值落在平均数(X)的同一侧。
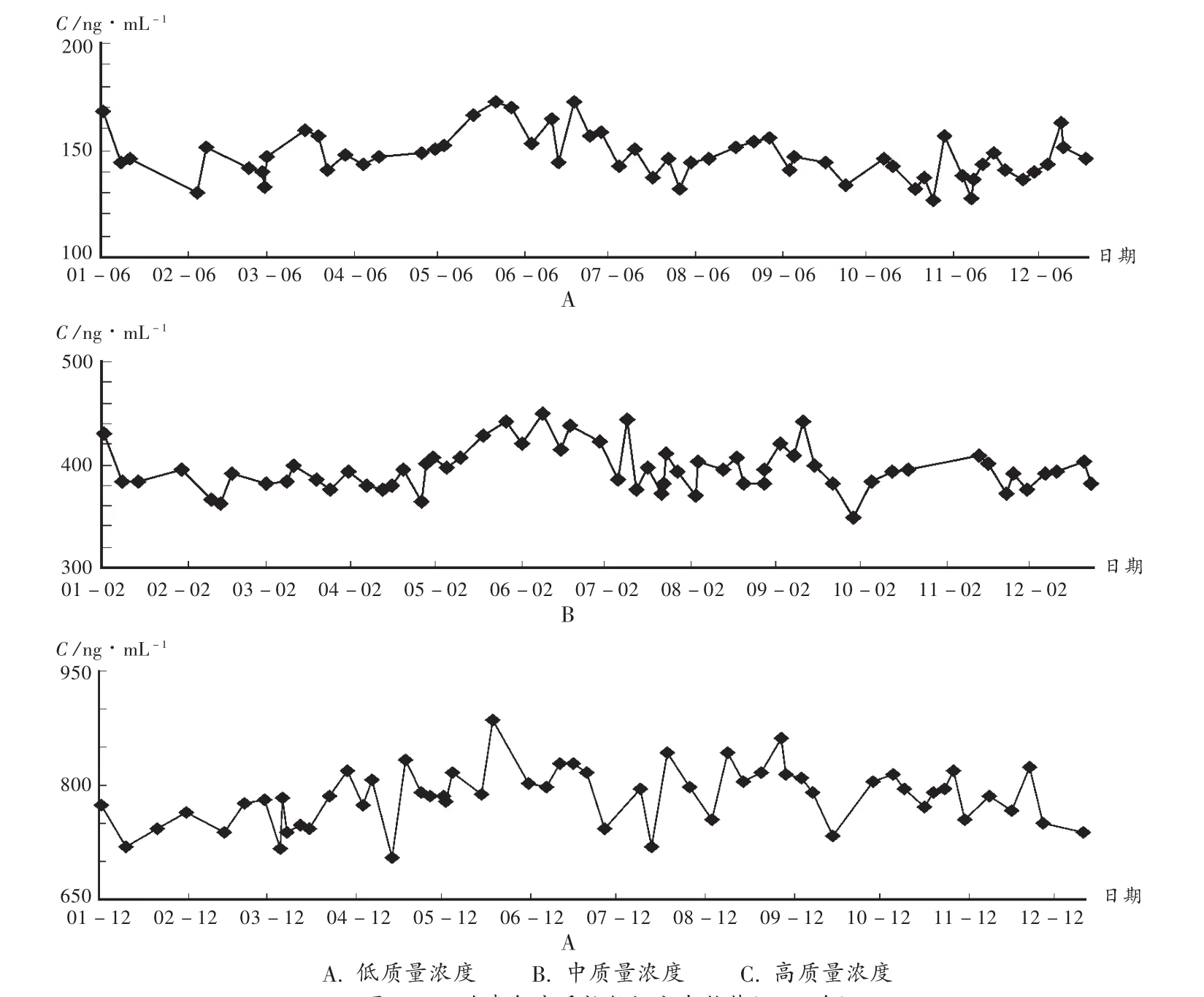
图1 环孢素年度质控数据分布趋势(2009年)
由于本室采用3个质量浓度质控品,按低、中、高顺序循环使用,评价时将不同浓度水平的质控测定值转换成 Z-分数形式,绘制在单个质控图上进行比较。Z-分数指质控测定值与其平均数之差再除以该质控品的标准差,Z-分数=(Ximat-Xmat)/Smat。结果见图3。从年度 Z-分数控制图上共发现8次失控,包括3次违背22s质控规则,5次违背41s质控规则。
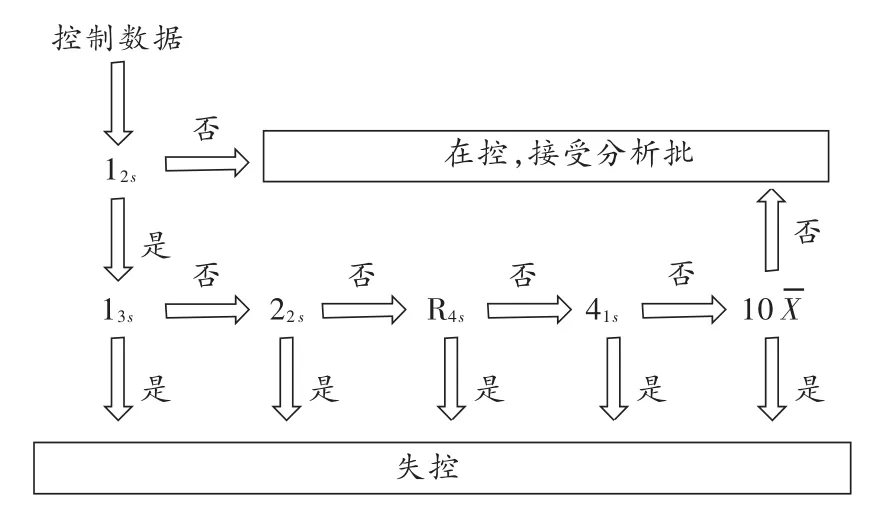
图2 应用12s/13s/22s/R4s/41s/10X系列控制规则的逻辑图
2.5 质控方法选择与设计[3]

图3 Z-分数数据分布
参照临床检验质控设计评价方法,确定允许总误差(allowable total error,TEa)、方法的相对标准偏差(RSD)、偏移(bias),计算临界系统误差,ΔSEc=[(TEa-|bias|)/s]-1.65,以及临界随机误差,ΔREc=(TEa-|bias|)/1.65 s,判断仪器性能稳定性;从质控表格中查出质控规则和质控品的个数,根据误差检出率和假失控概率,选出最佳的质控方法。质控规则设计参数的计算结果见表2。将过程稳定性定位良好,查单规则、多规则质量控制设计的表格,得可选质控规则和控制测定值个数(n)为 12.0s(1),12.5s(2),13.0s(4),13.5s(6),13s/22s/R4s/41s(n=2)。从实用性考虑,每批检测带1~2个质控比较可行,筛选出 12.0s(1),12.5s(2),13s/22s/R4s/41s(n=2)3 种方法,查质控方法的性能特征表得,不同控制设计的误差检出概率和假失控概率,相对而言,13s/22s/R4s/41s(n=2)具有较高的误差检出概率和较低的假失控概率。
3 讨论
依据2010年版《中国药典(二部)》生物样品分析方法质量控制要求[2],2009年所有质控样品数据均符合要求。运用Levey-Jennings控制方法后,其规定的范围要比2010年版《中国药典(二部)》生物样品分析方法质量控制要求小,也均在控,显示该方法在长期的检测中稳定性较好。累计和质量控制方法检出3次失控。Z-分数控制图上共发现8次失控,包括3次违背22s质控规则,5次违背41s质控规则,本实验室失控违背的质控规则是22s和41s,提示存在系统误差,由于以前的单规则不能检出,故这8次系统误差未得到及时的纠正。经查证,有4次都是更换试剂盒而导致的基值漂移,检测中发现仪器对试剂的批间差异有时可显示小的偏移且无法消除,此时对很小的系统误差相当敏感的41s规则将提供失控信号,而其实际上又具有假失控性质。因此,有必要对经典的多规则质控方法进行适当修改使用。修改的Westgard多规则控制方法,可达到极高的误差检出率和较低的假失控概率,提高了实验室测定数据的准确性,能够为临床提供更加真实有效的数据。
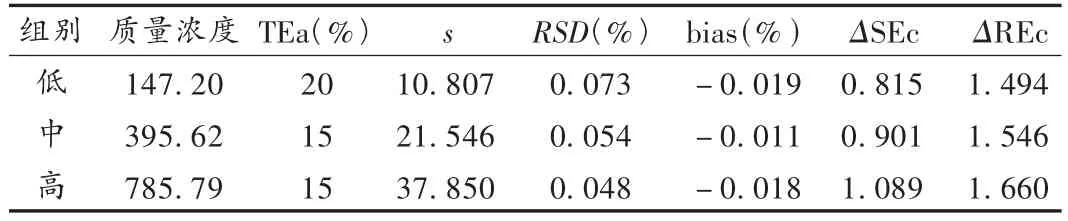
表 2 低、中、高质控的 Tea,bias,ΔSec,ΔRec
[1]国家药典委员会.中华人民共和国药典(二部)[M].北京:中国医药科技出版社,2010:附录196.
[2]王大建,王惠明,侯永生.临床试验室管理学[M].第2版.北京:科学出版社,2009:93.
[3]黄立方.实用医学分析与应用[M].北京:人民卫生出版社,2002:630-672.

