拉米夫定及恩替卡韦治疗非何杰金淋巴瘤相关性HBV再激活的疗效对比研究
黄 晶,陈小苹,陈学福,陈文莉
(广东省人民医院感染科,广东广州,510080)
近年来淋巴瘤(NHL)发病率呈逐年上升趋势,并以每年4%的比率递增,加之治疗药物的不断发展,NHL合并HBV感染患者接受化疗后乙肝病毒再激活已成为常见的临床问题而受到人们的重视。2005年我国的乙肝防治指南中指出,在HBV表面抗原阳性患者开始化疗前1周,即开始预防性使用拉米夫定进行抗病毒治疗,持续至化疗结束后4~6周,或根据患者病情决定拉米夫定停药时间。尽管拉米夫定在HBV病毒再激活的预防和治疗上具有优势,但其本身也存在局限性,例如用药时间延长后出现的耐药和病毒变异等。恩替卡韦因强效、低耐药在临床上得到广泛应用,现就本院近4年的HBsAg阳性的NHL患者应用拉米夫定或恩替卡韦抗病毒治疗的疗效作一回顾性对比分析。
1 资料与方法
1.1 一般资料
2006年6月~2010年6月期间,本院收治的NHL合并HBV感染患者84例(除外抗病毒治疗不足3个月的NHL患者),其中男66例,女18例,平均年龄(47.8±15.5)岁。所有病例在接受化疗同时服用拉米夫定或恩替卡韦抗乙肝病毒治疗。84例患者中22例抗乙肝病毒治疗前HBV DNA<103copies/mL,其中16例服用拉米夫定(100 mg/d),6例服用恩替卡韦(0.5 mg/d);62例患者抗乙肝病毒治疗前 HBV DNA>103copies/mL,其中38例服用拉米夫定,24例服用恩替卡韦。
乙型肝炎诊断符合2005年中华医学会传染病与寄生虫病学会修订的慢性病毒性肝炎诊断标准。
1.2 观察指标
病毒学突破率(病毒学突破定义为在治疗过程中,相隔1个月的连续 2次检查,血清HBV DNA载量比获得应答后的最低值的上升值均大于1 log210);原发耐药率(原发耐药定义为核苷(酸)类似物治疗12周,HBV DNA载量的下降幅度小于1 log210 U/mL);病毒学突破出现时间;是否出现病毒突破相关性肝炎突发而导致化疗中断(肝炎突发定义为当ALT水平上升大于5倍正常值上限);是否出现肝衰竭;抗乙肝病毒治疗前HBV DNA>103copies/mL患者观察基线ALT、HBV DNA,HBV DNA低于检测下限(HBV DNA<103copies/mL)时间。
2 结 果
观察拉米夫定的使用时间6~36个月,平均18个月;观察恩替卡韦使用时间7~26个月,平均14.3个月。
2.1 抗乙肝病毒治疗前HBV DNA<103 copies/mL组的转归
拉米夫定治疗16例患者中1例于第12月出现病毒学突破,并出现肝衰竭,病毒学突破率7.14%。恩替卡韦治疗6例患者中无病毒学突破情况,无肝炎突发情况发生,病毒学突破率0%。两者病毒学突破无统计学差异(P>0.05)。
2.2 抗乙肝病毒治疗前HBV DNA>103 copies/mL组的转归
2.2.1 接受拉米夫定或恩替卡韦治疗患者的基线情况及疗效比较:分别予以拉米夫定及恩替卡韦治疗的2组间在年龄、性别、基线ALT及HBV DNA水平等方面具有可比性,在原发无应答及肝衰竭发生率方面未见明显差异,但在病毒学突破率及肝炎突发率方面,拉米夫定治疗组明显高于恩替卡韦治疗组,26.3%的拉米夫定治疗者因病毒学突破后随之而来的肝炎突发而需要中断化疗(见表1)。

表1 拉米夫定、恩替卡韦治疗HBsAg阳性的NHL患者基线情况及抗病毒疗效
2.2.2 拉米夫定治疗组不同转归患者的基线情况及HBV DNA阴转时间比较:就上述抗乙肝病毒治疗前HBV DNA>103copies/mL组病例进一步分析,拉米夫定治疗者中发生病毒学突破的13例,平均病毒学突破时间为(11.3±2.8)月,发生原发性无应答的4例,持续病毒学应答者21例。表2就拉米夫定治疗者中病毒学突破和持续病毒学应答及原发性无应答的病例基线情况进行统计,3者年龄、基线ALT、基线HBV DNA未见统计学差异。提示上述基线信息对拉米夫定耐药的提示作用不大。此外,病毒学突破和持续病毒学应答患者治疗至HBV DNA低于检测下限所需时间分别为(4.1±1.7)个月和(2.9±1.3)个月,差异无统计学意义(F=0.002,P>0.05)。
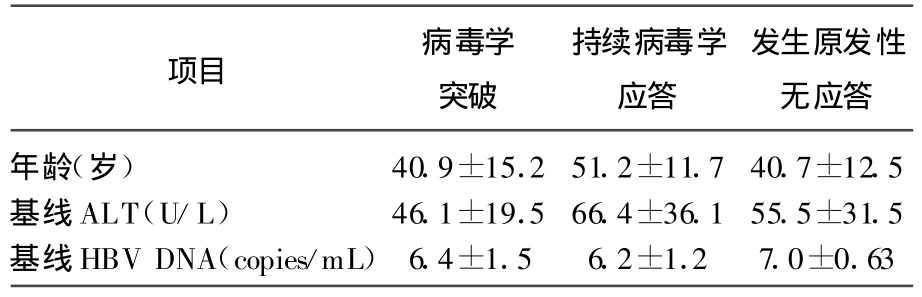
表2 拉米夫定组病毒学突破和持续病毒学应答的患者相关情况*
3 讨 论
我国的流行病学统计数据显示,我国非何杰金淋巴瘤(NHL)患者HBsAg阳性率为24%~77%[1-2]。HBsAg阳性的淋巴瘤患者在化疗后出现HBV再激活的概率为20%~55%,高于其他肿瘤2~3倍[3-4]。分析其原因,很大程度上是由于化疗方案中含有蒽环类和皮质类固醇类。Yeo等[5]报道淋巴瘤是HBV激活的危险因子,蒽环类是以剂量相关的方式在体外刺激HepG2.215分泌HBV DNA,而HBV DNA含有糖皮质激素应答元件,能促进HBV再感染。同时,糖皮质激素可以溶解淋巴细胞,也降低了B淋巴细胞和T淋巴细胞的功能。但多种化疗药物的联合引起的机体免疫功能抑制仍是HBV激活的主要原因。近年来,R-CHOP方案(美罗华、环磷酰胺、多柔比星、长春新碱和泼尼松)作为一线方案治疗NHL已被广泛应用。有报道指出,接受RCHOP方案治疗停用预防性拉米夫定治疗后,可发生延迟性HBV再激活[6]。因此,随着该方案的广泛应用,HBsAg阳性的NHL患者面临着更长时间的抗病毒治疗。
拉米夫定预防和治疗HBV再激活的的有效性得到公认,能明显降低HBsAg阳性的肿瘤患者化疗后的HBV再激活率,使发生率降低79%以上[7]。本研究显示,抗乙肝病毒治疗前HBV DNA<103copies/mL的患者服用拉米夫定或恩替卡韦均可获得良好疗效,如从经济学角度出发,拉米夫定则更有优势。但拉米夫定本身也存在用药时间延长后出现的耐药和病毒变异局限性。一般而言,YMDD突变常发生在拉米夫定治疗6个月以后,并随继续治疗时间延长发生率逐渐增高。普通慢性乙肝人群拉米夫定初始治疗1年时YMDD突变发生率为14%~32%,2、3、4年发生率分别为38%、49%、66%。但本研究中,HBsAg阳性的NHL患者平均应用拉米夫定11.3个月的病毒学突破率高达34.2%,更有10.5%的患者原发性不应答,由于病毒学突破,出现肝炎突发,导致26.3%的患者化疗中断。鉴于此,HB-sAg阳性的NHL患者比普通慢性乙肝人群有着更高的拉米夫定耐药率。
相比之下,在本研究中,恩替卡韦有更低的病毒学突破率及肝炎突发率,与其他报道[8]一致,就保证NHL化疗的顺利进行及提高无事件生存率方面有更好的作用。因此,HBsAg阳性的NHL患者接受抗乙肝病毒前如HBV DNA阳性,恩替卡韦可能是更好的选择。
本研究分析发现抗乙肝病毒治疗前HBV DNA>103copies/mL服用拉米夫定的患者出现病毒学突破组和持续病毒学应答及原发性不应答的3部分患者的年龄、基线ALT水平、HBV DNA水平及均无统计学差异,与免疫力正常的乙肝人群不同,本组患者无法通过基线情况及HBV DNA低于检测下限时间得到耐药风险的提示。
[1]袁 昕,刘晓丹,童建东,等.非何杰金淋巴瘤患者β2-微球蛋白检测的临床意义[J].实用临床医药杂志,2004,8(1):74.
[2]郑荣生,秦凤展,翟云芝,等.感染HBV的NHL化疗方案的研究[J].实用癌症杂志,2001,16(2):181.
[3]Yeo W,Chan P K,Zhong S,et al.Frequency of hepatitis B virus reactivation in cancerpatients undergoing cytotoxic chemo-therapy:a prospective study of 626 patients with identification of risk factors[J].J Med Virol,2000,62(3):209.
[4]冯洪玲,曹武奎.淋巴瘤化疗导致的乙型肝炎病毒再激活及其预防[J].医学综述,2009,15(21):3256.
[5]Yeo W,Hui E P,Chan A T,et al.Prevention of hepatitis B virus reactivation in patients with nasopharyngeal carcinoma with Lamivudine[J].Am J Clin Oncol,2005,28(4):379.
[6]Dai M S,Chao T Y,Kao W Y,et al.Delayed hepatitis B virus reactivation after cessation of preemptive Lamivudine in lymphoma patients treated with rituximab plus CHOP[J].Ann Hematol,2004,83(12):769.
[7]翟东兴.拉米夫定预防HBV再激活20例临床分析[J].齐齐哈尔医学院学报,2010,31(9):1393.
[8]Lalazar G,Rund D,Shouval D.Screening,prevention and treatment of viral hepatitis B reactivation in patients with haematological malignancies[J].Br J Haematol,2007,136(5):699.

