WHO与我国基本药物目录中心血管用药的比较研究Δ
杨 悦,邹 韵,田丽娟,傅书勇,胡 欣,武志昂#(.沈阳药科大学工商管理学院,沈阳市 006;.卫生部北京医院,北京市 00780)
1975年,世界卫生组织(WHO)提出了基本药物的概念,经过30余年的发展,基本药物体系已经建立,涵盖基本药物遴选评价、目录更新和推广、WHO基本药物图书馆等方面。2009年3月,WHO发布第16版《基本药物示范目录》(以下简称“WHO目录”)。同年,我国发布了《国家基本药物目录·基层医疗卫生机构配备使用部分》(2009版)(以下简称“我国目录”),其中仅有部分药物标明了剂型限制,而规格没有限定,实质是扩大了基本药物的范围,这给基本药物的招标采购和临床使用等带来不少障碍。由于WHO目录的遴选调整程序和方法已经比较成熟,特别是剂型和规格遴选方面的标准对我国基本药物目录的完善具有直接的指导意义,笔者选择了临床需求比较大的心血管用药作为基础,分析我国与WHO目录心血管基本药物品种、剂型、规格遴选上的差异,旨在为我国基本药物遴选提供实证参考证据。
1 WHO与我国基本药物遴选原则比较
从2000年起,WHO对基本药物的遴选必须基于可靠且足够的证据,其中包括药物在多种临床条件下的相对有效性证据、药物的安全性证据以及同一治疗类别内相对成本-效用(Cost-effective)证据等。如果两种同类药品具有相似作用,要对两者相对的安全性、有效性、质量、价格以及可获得性进行评价。WHO对剂型规格的遴选主要基于药物的效用以及广泛的可获得性。在大部分情况下,应对药物进行剂型选择,尤其是固体制剂。片剂通常情况下要比胶囊价格便宜,但是在考虑成本因素的同时,应该基于药动学、生物利用度、受环境气温等因素影响下的稳定性等进行选择。在没有统一的片剂规格规定的情况下,适合的片剂规格应以当地的可获得性以及需求为依据。在没有规定精确的规格时,推荐刻痕片可使剂量调整更为灵活[1]。
我国基本药物遴选原则为“防治必需、安全有效、价格合理、使用方便、中西药并重、基本保障、临床首选和基层能够配备”。虽有遴选原则,但缺乏统一的技术标准,多基于专家意见,缺少评价的证据。对于剂型的遴选,我国仅在基本药物目录说明中概括的指出剂型适宜,未有具体遴选原则,而对规格的遴选,也没有说明。
2 WHO与我国心血管类基本药物比较
2.1 两目录心血管基本药物的类别比较
2.1.1 品种比较 WHO目录分为核心目录与补充目录,核心目录中的药品为WHO优先推荐使用的药品,进入核心目录的药品必须安全、有效、成本低廉;补充目录的药品为治疗重点疾病的基本药物,这些重点疾病需要专科诊断或监测设施,或专业医疗保健和专业培训。在有疑问时,很多情况下也可将价格较高或成本-效用不低的药物列入补充目录。WHO目录中的心血管基本药物共19种,我国目录共29种,两目录重合的药物为10种;同时,我国目录中收录了WHO补充目录中的胺碘酮、硝普钠以及多巴胺。
WHO目录中对一些药物用方框符号(“□”)进行标注,用以说明在一类具有相似临床作用的药物中,列入目录的药物应是有最佳证据证明其安全性和有效性的该类药物中的代表药物。在有效性和安全性数据方面没有差别的情况下,列入目录的药物应根据国际药物价格信息来源以确保其最低价格能够广泛获得。WHO也指出,国家基本药物目录不应使用类似的符号,并应在最后的遴选中体现本国的独特性,列入目录的药品应取决于本地区的可获得性和价格。WHO目录中7种方框符号标注的药物以及我国目录中的具有相似治疗效果的药物详见表1。
WHO与我国基本药物目录的分类方式不同,WHO基本药物目录根据解剖-治疗-化学代码分类法(ATC法)进行分类,而我国目录按照临床药理学作用进行分类。WHO采用的ATC分类法是一种药物系统分级分类法。在19世纪70年代初挪威医学供应部扩展了已有的欧洲制药市场研究协会解剖和治疗3级分类系统,并增加了2个化学级。后来,ATC分类获得WHO药物应用研究组的认可,并由WHO药物统计方法合作中心(WHO Collaborating Centre for Drug Statistics Methodology)负责维护。ATC分类法既考虑了治疗分类,又考虑了化学分类,这个特征是其他分类方法所缺乏的。我国目录按照临床药理学作用进行分类,缺少了对化学分类的考虑。

表1 与WHO目录方框标注治疗效果相似的我国目录中心血管药物Tab 1 Cardiovascular medicine in EML of China which have similar therapeutic efficacy to those stated in EMML of WHO
两目录中心血管用药的二级目录均为6类,重合的类别有5类,分别为抗心绞痛、抗心律失常药、抗高血压药、心力衰竭用药和降脂药;WHO特有的类别为抗血栓药,收录了在核心目录中的阿司匹林以及作为补充目录的链霉素,而我国心血管基本药物并未收录这2种药物。我国特有的类别为抗休克药,其中肾上腺素被WHO收录在抗心律失常药中;我国抗休克药中的多巴胺,同时也收录在WHO目录中的心力衰竭药补充目录中。
2.1.2 心血管基本药物品种差异 我国目录与WHO目录心血管用药相重合的药品有10种。对于WHO目录中具有方框符号标注的7种药物中,WHO指出国家基本药物目录应根据本地区的可获得性和价格具有独特性,而我国并没有完全体现出遴选的独特性,详见表1。如早在2004年,WHO专家委员会就提出用依那普利来替代卡托普利进行方框符号标注,2007的系统评价显示依那普利可以应用于儿童,但是当时卡托普利还没有应用于儿童的足够证据,故没有将卡托普利列入目录[1]。而我国目录中却收录了依那普利和卡托普利2种药物。
2.2 新旧版目录心血管基本药物的调入调出比较
2003年,WHO在《基本药物的遴选与使用》914号专家委员会报告中明确指出,对基本药物的遴选要基于证据,并对WHO目录中的药物进行调整,形成第13版WHO目录,WHO对药品的遴选正式进入了循证阶段。我国基本药物的遴选程序在2002-2004年开始由专家评价向循证评价过渡,自2004版目录遴选调整开始,逐渐重视循证评价,最终调整形成2009版目录。故以下比较仅从两目录重视循证评价后进行比较,即仅比较WHO目录的第13、14、15、16版,我国目录的2004版、2009版的调入和调出情况。
2.2.1 新旧版目录调入调出心血管基本药物的数量 WHO心血管基本药物的数量从第13版开始基本没有变化,而我国心血管基本药物的数量调整较大,由2004版的68种到2009版的29种(见图1),每类药品的数量均有所减少,详见表2。
2.2.2 新旧版目录药品品种调入调出比较 WHO与我国对成人心血管基本药物的调整情况详见表3。我国2009版目录在2004版的基础上调出了41种药品,其中我国和WHO目录均调出了奎尼丁。尽管WHO目录中调出了异丙肾上腺素、普鲁卡因胺和利血平,然而我国目录中却保留着异丙肾上腺素、普鲁卡因胺及含有利血平的复方制剂。
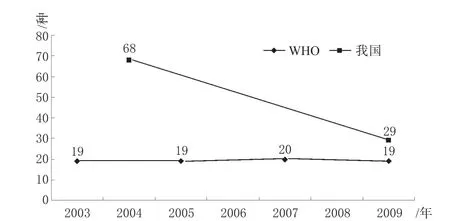
图1 新旧版目录心血管基本药物数量调整情况Fig 1 Number adjustment of cardiovascular essential drugs in new and old edition of list
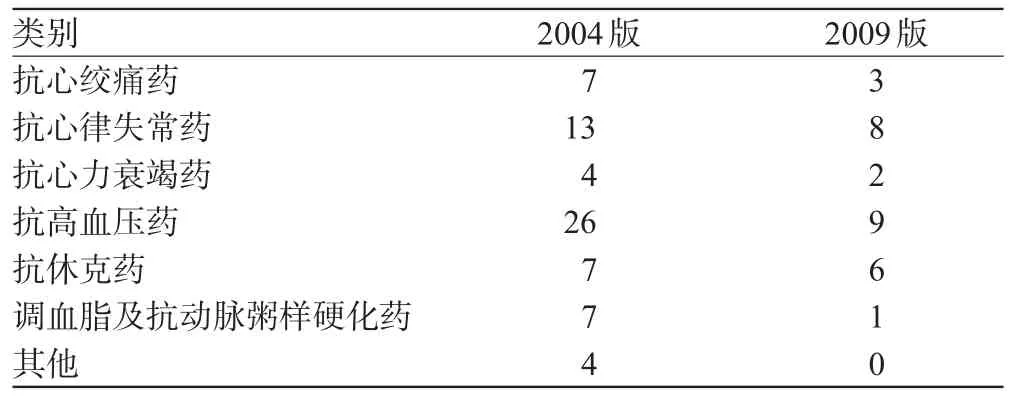
表2 我国新旧版目录各类心血管基本药物数量调整情况Tab 2 Number adjustment of cardiovascular essential drugs in new and old edition of list in China

表3 两目录心血管基本药物调入调出情况Tab 3 Input and output of cardiovascular essential drugs in 2 lists
2.2.3 新旧版目录比较情况差异分析 两目录在重视循证评价后,调入调出的药品品种也存在差异。我国目录中仍收录的异丙肾上腺素、普鲁卡因胺及含有利血平的复方制剂等WHO已调出的药品,其原因很大程度上是因为缺乏循证评价证据,无法判断收录普鲁卡因胺、卡托普利以及含有利血平的复方制剂的合理性。而WHO目录调整依据的是系统评价结果,如WHO从2007年开始对胺碘酮进行评价,当时提交的随机对照试验(RCT)以及系统评价均支持胺碘酮应用于心律失常的有效性和安全性,但是不支持胺碘酮应用于心律失常的常规治疗,同时其应用是要对甲状腺及肝功能进行长期评估,同时也要警惕其与地高辛等联合用药时的相互作用[2]。从2007年开始,WHO通过Cochrane评价[3]及大量的RCT[4]评价抗心律失常药普鲁卡因胺以及奎尼丁,认为与其他抗心律失常药物相比,它们并没有更优的有效性和安全性,故将两者从目录中调出。
2.3 对不同作用机制心血管基本药物收录情况的比较分析
2.3.1 不同作用机制心血管基本药物收录情况比较详见表4。由表4可知,WHO和我国共同收录了2种抗心绞痛的硝酸酯类药物,WHO仅收录了2种抗心力衰竭的利尿药,其中氢氯噻嗪同时在抗高血压药中列出;其余各种作用机制的心血管用药均仅收录1种。而我国β受体阻断药、Na+通道阻滞药、强心苷、肾素-血管紧张素系统抑制剂中均收录了2种或2种以上药物。同时,我国并没有收录抗心力衰竭的利尿药。

表4 两目录中不同作用机制心血管用药收录情况Tab 4 Application of cardiovascular medicines with different mechanisms in 2 lists
2.3.2 对不同作用机制心血管用药收录差异分析 经上述分析可以看出,我国较WHO按不同作用机制收录的心血管基本药物品种重复或缺乏现象并存。如抗心律失常药中β受体阻断药,WHO仅收录了阿替洛尔,而我国收录了阿替洛尔、普萘洛尔、美托洛尔3种基本药物。国内、外研究都证实,阿替洛尔治疗心律失常有效,另一项研究显示,美托洛尔与传统抗心律失常药物疗效相当,但价格高于阿替洛尔[5];WHO在抗力衰竭的药物中收录了利尿药呋塞米和氢氯噻嗪,而我国在抗心力衰竭药物中并没有收录利尿药。WHO曾经对利尿药进行Cochrane评价证明其可以改善心力衰竭患者的运动能力[6]。我国较WHO缺少对药物的循证评价,使得心血管基本药物在数量以及品种上都没有达到最优化。
2.4 药品剂型比较分析
2.4.1 药品剂型比较 我国心血管基本药物标注的剂型有口服常释剂、口服缓释剂等,我国目录说明中规定,化学药品和生物制品中的口服常释剂型包括口服普通片剂、肠溶片、分散片、硬胶囊、肠溶胶囊、软胶囊(胶丸);口服缓释剂型包括缓释片、控释片,缓释胶囊、控释胶囊。经查阅四川美康医药软件研究开发有限公司与卫生部合理用药专家委员会合作开发的“MCDEX合理用药信息支持系统”(MCDEX)数据库,我国批准上市的29种心血管基本药物其制剂品种共48种。
WHO目录中的19种心血管基本药物中仅有氢氯噻嗪标为口服固体制剂,未规定具体剂型,其余18种药物均明确标明具体剂型,共29种,详见表5。
2.4.2 心血管用药剂型差异分析 由表5可以看出,我国心血管基本药物剂型没有WHO明确。早在1985年,WHO召开第2次专家委员会时便在剂型遴选指南中提到对剂型遴选的目的是为那些希望简化或标准化基本药物目录的国家提供示范目录。剂型的选择要基于效用及广泛的可获得性。大部分情况下应选择一种剂型,特别是对于固体制剂,通常情况下,片剂较胶囊成本低,但是在考虑成本的同时,也应该考虑药动学、生物利用度等[2]。2009年3月,WHO召开的第17次专家委员会会议上,进一步对剂型和规格进行了规范[7]。WHO提出了两条原则,其中一条便是对于多种剂型的药物,应选择常见的剂型。而我国卫生部等9部委2009年颁布的《关于实施基本药物制度的意见》中仅提到了“剂型适宜”,并没有对剂型的选择有具体的规定。
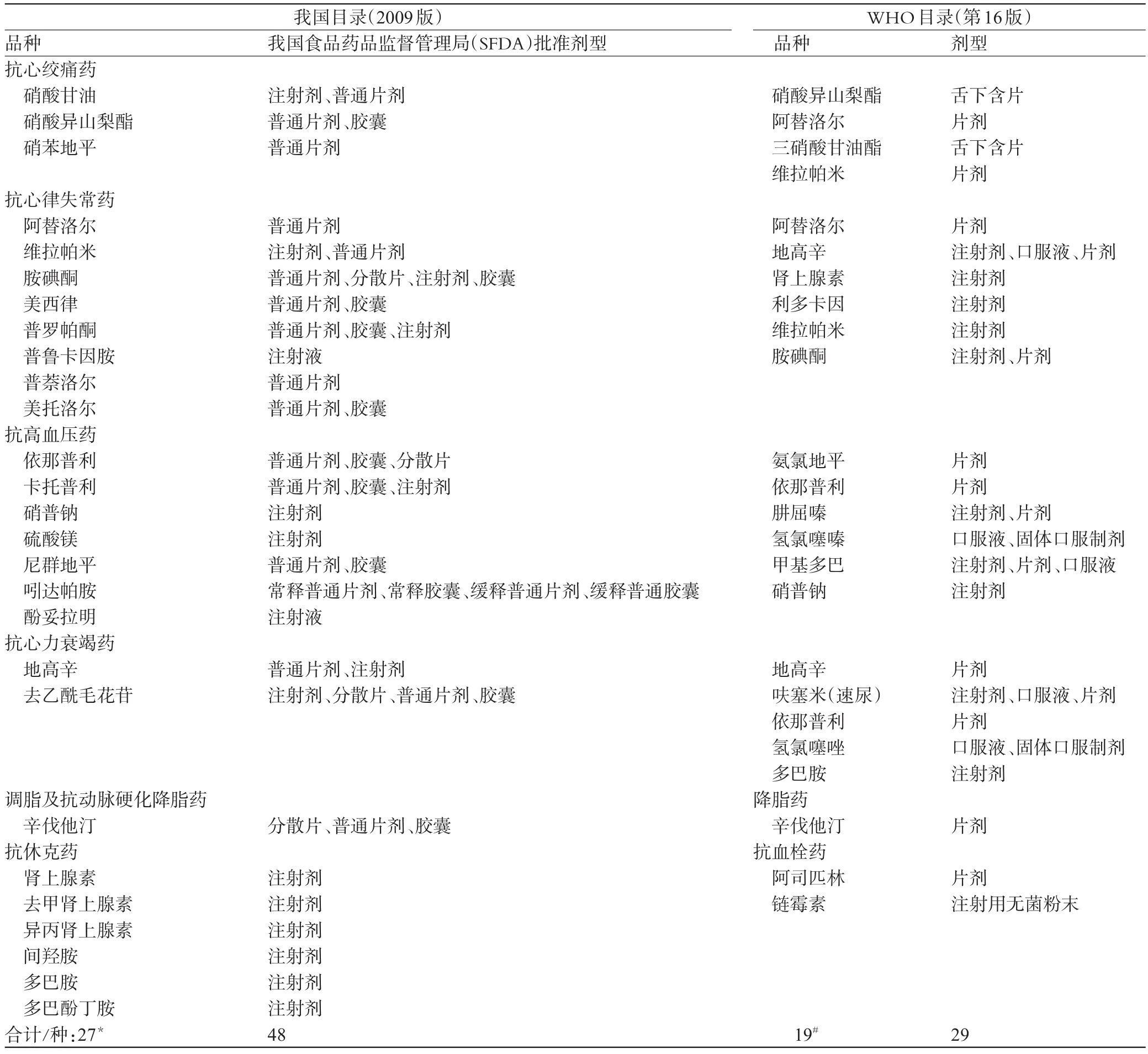
表5 两目录中心血管基本药物剂型比较Tab 5 Comparison of dosage form of cardiovascular essential drugs in 2 lists
WHO心血管基本药物中除了氢氯噻嗪只标明固体口服制剂外,其余心血管用药均明确规定了剂型,而我国目录中仅标明了口服常释剂型,由于口服常释剂型还包括片剂、胶囊等剂型,故导致列入目录的药品实际生产厂家和药品数量众多,已经不能体现基本药物“基本”的特点,给基本药物生产、招标采购和使用等方面带来混乱,导致资源浪费。
2.5 心血管基本药物规格比较
基本药物的剂型、规格众多,但并非都适合列入基本药物目录。从两目录的比较可以看出,我国目录中未标明规格,而WHO中却明确规定了每种基本药物的规格。
2.5.1 国家食品药品监督管理局(SFDA)批准的符合我国目录心血管用药的口服常释剂型规格 由于我国基本药物目录中没有明确规定规格,本研究检索了MCDEX数据库,统计了心血管用药基本药物剂型在我国获批的药品批准文号数量。我国目录中有16种口服常释剂型的心血管用药,获批了共43种规格,平均每种药品有2.68种规格,平均每种规格的药品获批生产的批准文号数为37.56个,详见表6。
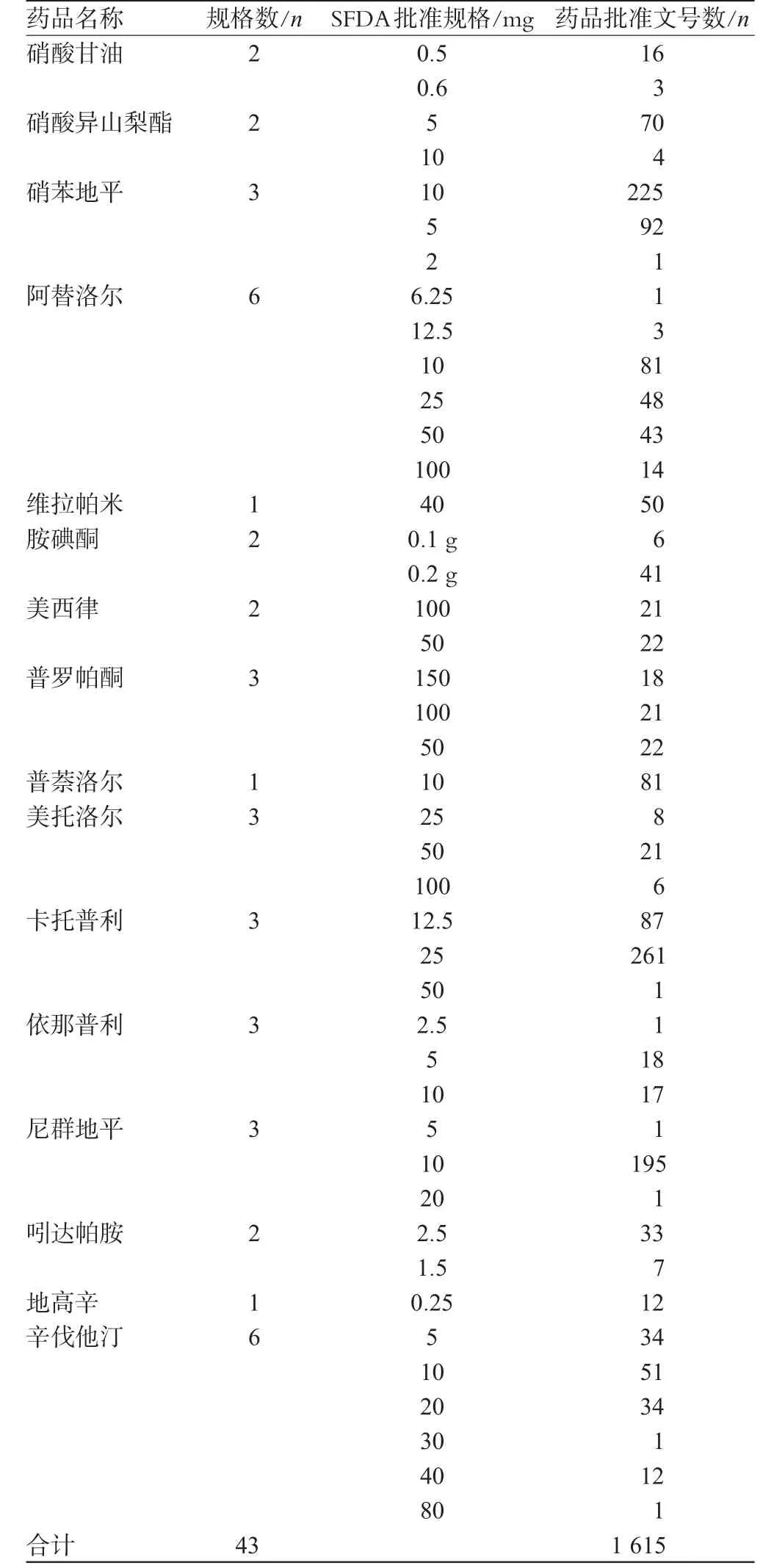
表6 我国符合心血管基本药物的口服常释剂型规格情况Tab 6 Specifications of oral conventional release dosage forms of cardiovascular essential drugs in China
2.5.2 固体口服制剂规格与成人口服单次最低剂量的比较 (1)WHO固体口服制剂规格与成人口服单次最低剂量的比较。参照前述WHO的规格遴选原则,笔者查阅《WHO基本药物处方集》中心血管基本药物的剂量规定,找出固体口服制剂最适合成人口服的单次最低剂量,与目录中的药品规格进行比较,详见表7。结果,WHO共12种固体口服制剂,有10种药品的规格与成人口服单次最低剂量相符,占心血管基本药物口服固体制剂总数的83.3%;不符合成人口服单次最低剂量的2种药品为呋塞米和阿司匹林,其中WHO规定的呋塞米剂型还包括口服液,便于服用时根据情况调整剂量。
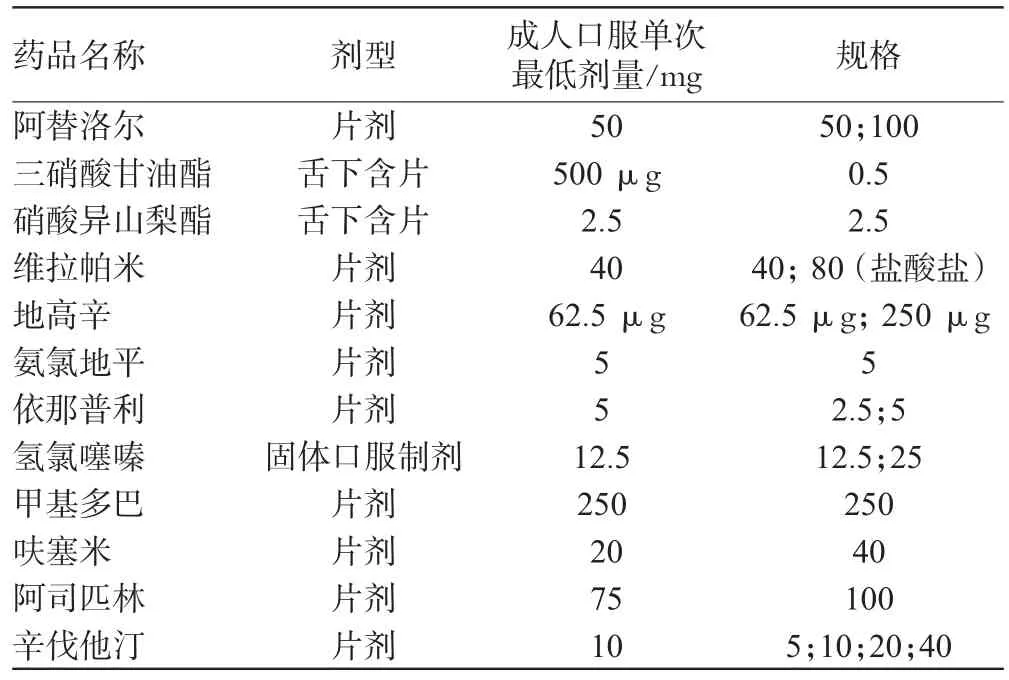
表7 WHO固体口服制剂规格与成人口服单次最低剂量Tab 7 Specifications of solid oral preparation of WHO and single minimum oral dose for adult
(2)我国固体口服制剂规格与成人口服单次最低剂量的比较。我国目录中未列药品规格,也无遴选规格的标准和原则。根据SFDA所批准的常见规格与2009版《国家基本药物目录处方集(化学药品和生物制品)》中推荐的成人口服单次最低剂量进行比较,其中“常见规格”界定为该规格占该药品所有获批规格批准文号数量的10%以上,该规格便为常见规格。我国心血管基本药物共有16种固体口服制剂,其中仅有7种药品的常见规格与成人口服单次最低剂量相符,占心血管基本药物口服固体制剂总数的43.8%,详见表8。
2.5.3 心血管用药规格差异分析 由上述分析可以看出,我国心血管基本药物未标明规格。WHO目录中按照药物组成成分(API)和活性成分的不同,采用2种规格标示方法:(1)如果基本药物目录的右侧栏中的规格标示的是药物活性基团的含量,则其API的类型(盐类、酯类和化合物)列在规格后面用括号括起来。(2)如果基本药物目录右侧栏中的规格代表的是API的含量,则规格后应列出API(盐类、酯类和化合物)全称。
我国心血管基本药物并没有规定剂量规格,适合的片剂规格为SFDA批准的常见药品规格。据统计,SFDA批准的16种心血管基本药物仅有5种药品的常见规格符合成人口服单次最低剂量,满足了患者服药的依从性,其余11种规格并没有满足成人口服单次最低剂量,而其生产的剂型也缺乏类似刻痕片等可分割的剂型以便于患者服用。
2.6 两目录差别原因分析
经过比较发现,WHO目录与我国目录存在差异,其根本原因在于遴选原则的差异和以循证为基础的评价方法的差异。我国基本药物遴选原则均为定性描述,没有细化的可操作的原则,特别是缺乏对药品剂型、规格的遴选原则,也缺乏在同类药品中如何选择首选药的具体原则。遴选原则缺乏操作性制约了基本药物目录遴选和调整的合理性。
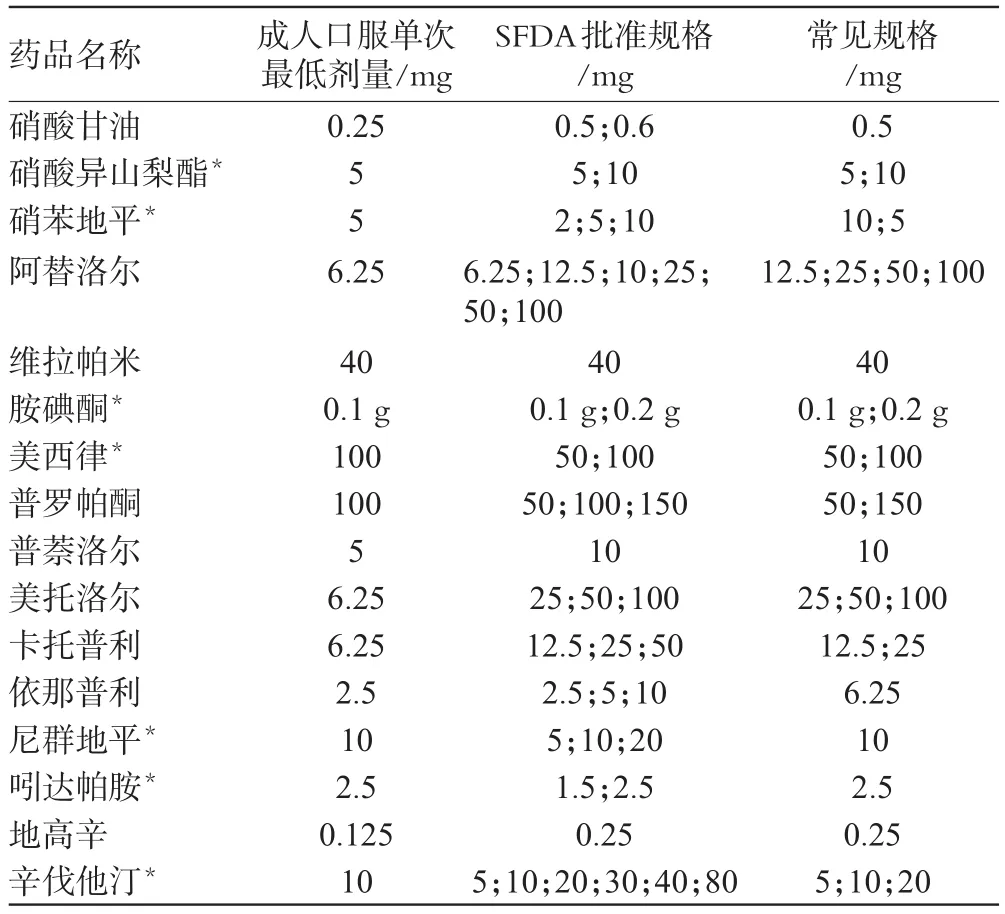
表8 我国心血管基本药物固体口服制剂规格与成人口服单次最低剂量Tab 8 Specifications of solid oral preparation of WHO and single minimum oral dose for adult of cardiovascular essential drugs in China
WHO基本药物遴选原则强调,对于药品疗效、安全性、相对成本-效益等指标的评价应当基于证据。尽管从2004年开始我国也逐渐重视循证评价,但是并未规定遴选程序中的证据提供方式和提供程序,对证据缺乏具体要求,这使得循证评价并未得到有效运用。
3 对完善我国心血管基本药物遴选调整的建议
3.1 在基本药物同类品种遴选中注重循证证据的运用
自2000年WHO正式提出在遴选中需要对所有相关的证据进行系统评价后,WHO开始采用系统评价方法对基本药物进行评价,对某一具体临床问题(如疾病的病因、诊断、治疗、预后)系统、全面地收集全世界所有已发表或未发表的临床研究、采用临床流行病学评价文献的原则和方法,筛选出符合质量标准的文献,进行荟萃分析(Meta-analysis),得出综合可靠的结论[8]。WHO于2003年将Grading of Recommendations Assessment,Development and Evaluation(GRADE)引入WHO指南制定手册。GRADE对证据的质量和推荐强度进行分级,在WHO对基本药物的调整申请中广泛应用。
尽管我国对基本药物的遴选已经参考WHO经验,心血管基本药物的数量在逐渐接近WHO目录,但是对循证证据的运用较为缺乏,遴选方法相对来说缺乏科学性和客观性。因此,应在最佳科学证据的基础上,将专家评价与客观的科学证据结合起来,获得定量化的评价,有助于精简目录中的心血管基本药物,提高心血管用药的合理性、安全性,使心血管基本药物更体现其基本的特征。
3.2 确定适合我国国情的基本药物剂型规格遴选原则
WHO提出对剂型遴选指南的目的在于给那些希望简化基本药物目录的国家提供参考,WHO在剂型遴选指南中提到了对固体制剂剂型的选择最好为1种。当没有统一的片剂规格规定的情况下,适合的片剂规格应以当地的可获得性以及需求为依据。在没有规定确切的规格时,推荐刻痕片等易于调整剂量的剂型可使剂量调整更为灵活。
结合我国国情,笔者建议对固体口服制剂的遴选应借鉴WHO经验,制订符合我国国情的剂型规格遴选原则,每种基本药物尽量选择1种固体制剂剂型,而对于规格可以选择常见规格以及符合成人口服单次最低剂量的规格来提高患者的依从性。在无法确定统一的片剂规格的情况下,对适合的片剂规格应当以当地的可获得性以及需求为依据。确定基本药物剂型规格意味着减少我国基本药物数量,也相应减少了在基本药物招标采购时进行二次剂型、规格遴选的工作量。
3.3 补充完善我国基本药物目录的剂型、规格信息
心血管疾病病情变化快且后果严重,大多数的心血管药物起效极快,具有血管活性,所以对患者的观察必须认真仔细,选用的治疗药物及其剂量必须精确无误[9]。我国心血管基本药物的剂型规格应根据上述建议的遴选原则进行补充,明确选择1种固体口服制剂剂型列入目录,对片剂等口服固体制剂选择常见规格列入目录,若其常用规格不符合成人口服单次最低剂量,建议考虑刻痕片等可分割剂型来方便服用,提高患者依从性。
4 结语
WHO基本药物目录与我国基本药物目录的差异来源于遴选原则可操作性的差异。目前,我国2009版《国家基本药物目录》再次面临调整变化,迫切需要建立适合我国国情的剂型、规格、同类药品循证评价比较的遴选原则和标准。补充完善我国基本药物目录中的剂型、规格信息,可以使药品的处方更加规范,药品的使用更加合理,心血管用药的安全性、有效性更加具有保障。
[1]WHO.The selection and use of essential medicines[R].WHO Technical Report Series 772,Geneva,Switzerland,1985:9-10.
[2]Faris RF,Flather M,Purcell H,et al.Cochrane review:Diuretics for heart failure[EB/OL].http://www.mrw.interscience.wiley.com/cochrane/clsysrev/articles/CD003838/frame.html.2006-04.2011-05-11.
[3]WHO.The selection and use of essential medicines[R].WHO Technical Report Series 958,Geneva,Switzerland,2009:38.
[4]Lafuente-Lafuente C,Mouly S,Longas-Tejero MA,et al.Antiarrhythmias for maintaining sinus rhythm after cardioversion of atrial fi brillation[J].Cochrane Database of Systematic Reviews,2007,4:CD005049.
[5]Wyse DG,DiMarco JP,Domanski MJ,et al.The atrial fibrillation follow-up investigation of rhythm management(AFFIRM)investigators.A comparison of rate control and rhythm control in patients with a trial fi brillation[J].N Eng J Med,2002,347(43):1825.
[6]王 莉,李幼平,张 川,等.我国和WHO基本药物目录2009年版比较分析[J].中国循证医学杂志,2009,9(11):1173.
[7]WHO.The selection and use of essential medicines[R].WHO Technical Report Series 958,Geneva,Switzerland,2009:5-6.
[8]CEBM.Levels of Evidence[EB/OL].http://www.cebm.net/index.aspx?o=1025.2010-06-20.
[9]黄 健,张明雄,纳爱飞.利用DDDs排序分析我院心血管类药物使用情况[J].中国药师,2004,7(7):554.

