对氯苯氧异丁酸甲氧基苯丙烯酸酯的小鼠急性毒性和大鼠长期毒性
赵 坡,许 军,陈小兵,黄洪林,徐远成
(江西中医学院药物化学学科组,江西南昌 330004)
对氯苯氧异丁酸甲氧基苯丙烯酸酯{(E)-4-〔2-(4-chlorophenoxy)-2-methylpropanoyloxy〕-3-methoxyphenyl acrylic acid,AZ},是以中药活性成分阿魏酸为先导化合物所合成的阿魏酸衍生物,系经过筛选得到的一种兼有降血脂和抗血栓作用的药物,可以用作预防和治疗高脂血症与血栓[1]。本实验观察AZ对小鼠的急性毒性反应及其对大鼠的长期毒性反应,以评价AZ的安全性,并为临床剂量的拟定提供依据。
1 材料与方法
1.1 动物
昆明种小鼠,雌雄各半,体质量18~22 g,由江西中医学院动物实验中心提供,许可证号:SCXK(赣)2005-0001;SD种大鼠,雌雄各半,体重110~130 g,由江西中医学院实验动物中心提供,许可证号:SCXK(赣)2005-0001。
1.2 药物
AZ,由江西中医学院药物化学学科组提供,批号:090805,使用前用 0.5%羧甲纤维素纳(CMC-Na)生理盐水溶液配制为混悬液,2~4℃冰箱避光保存。
1.3 主要仪器
Dimension RXL Max型全自动生化分析仪,德国西门子公司;XT-1800i血细胞测定仪和CA-530血凝测试仪,日本东亚公司。
1.4 小鼠急性毒性实验[2-3]
根据预实验确定ig及ip给予AZ的剂量范围。小鼠ig给予AZ的急性毒性剂量范围为3000~1001 mg·kg-1,剂量公比为 0.76,分别为 3000,2280,1733,1317 和1001 mg·kg-1。取小鼠按性别和体质量随机分成6组,每组10只,溶媒对照组ig给予等体积0.5%CMC-Na生理盐水溶液。小鼠 ip给予AZ 剂量为1600 ~983 mg·kg-1,剂量公比 0.85,分别为1600,1360,1156 和 983 mg·kg-1。小鼠随机分成6组,每组10只,溶媒对照组ip给予等体积0.5%CMC-Na生理盐水溶液,正常对照组ip给予等体积生理盐水,给药体积0.2 ml。给药后立即观察各组动物毒性反应的体征及死亡数目和时间,并连续观察14 d。根据死亡情况使用SPSS13.0软件计算LD50。
1.5 大鼠长期毒性实验[3]
1.5.1 分组
SD种大鼠,雌雄各半,实验前适应性观察2周,取一般状况良好的大鼠80只,按性别体质量随机分为4组,每组20只,雌雄分笼饲养,每笼5只。AZ组大鼠 ig给予 AZ 500,291.7 和166.7 mg·kg-1,溶媒对照组ig给予等体积的0.5%CMC-Na生理盐水溶液。每日1次,连续13周。末次给药24 h后,每组选取10只大鼠(雌雄各半),ip给予3%戊巴比妥钠麻醉,腹主动脉取血,检测血液学指标,凝血时间和血液生化学指标;取主要脏器称重并作病理组织学检查。余下动物停止给药,正常饲养2周后,同法处理检测上述指标。每天观察一般情况,每周称重1次。
1.5.2 血液学和血液生化学指标检测
取血于血液细胞分析仪上测定红细胞(red blood cell,RBC)、白细胞(white blood cell,WBC)、血红蛋白(hemoglobin,HGB)、血小板(platelet,PLT)、淋巴细胞系和中性粒细胞等指标,血凝测定仪上测定部分凝血活酶时间(activated partial thromboplastin time,APTT);取血分离血清,全自动生化分析仪上测定血清中的谷丙转氨酶(alamine aminotransferase,ALT)、谷草转氨酶 (aspartate aminotransferase,AST)、总蛋白(total protein,TP)、白蛋白 (albumin,ALB)、总胆 红素 (total bilirubin,T-Bil)、碱性磷酸酶(alkaline phosphatase,ALP)、血尿素氮(blood urea nitrogen,BUN)、肌酐(creatinine,Crea)、总胆固醇(total cholesterol,T-Cho)、葡萄糖(glucose,GLU)10项血液生化学指标。
1.5.3 脏器系数和病理组织学检查
大鼠放血处死后,主要脏器进行全面尸检,肉眼观察各脏器有无病变异常情况;取心、肝、脾、肺、肾、脑、肾上腺、胸腺、睾丸、附睾、前列腺、子宫、卵巢和甲状腺等14个脏器称重,并计算脏器系数;然后对上述主要脏器及胃、大肠、小肠、胰腺和脊髓等脏器用10%甲醛固定,进行常规病理学检查。
1.6 统计学分析
2 结果
2.1 AZ对小鼠的急性毒性
小鼠ig和ip给予AZ约10 min后,出现自主活动减少、呼吸困难和后肢伸展松弛等现象,部分小鼠有流泪现象,毒性反应随剂量减小而减轻。各组小鼠死亡多发生在给药4~48 h,死亡小鼠立即尸检,除ip给药小鼠胃肠道有充血现象外,其他主要脏器无明显异常。未死亡小鼠于给药3 d后逐渐恢复正常。根据各组死亡分布情况计算得出小鼠ig及ip给予AZ的LD50分别为2053 mg·kg-1(95%置信区间为 1770 ~2438 mg·kg-1)和 1254 mg·kg-1(95%置信区间为1172~1341 mg·kg-1)。动物死亡情况见表1和表2。

表1 ig给予对氯苯氧异丁酸甲氧基苯丙烯酸酯(AZ)对小鼠存活的影响Tab.1 Effect of(E)-4-〔2-(4-chlorophenoxy)-2-methylpropanoyloxy〕-3-methoxyphenyl acrylic acid(AZ)ig given on mice survival
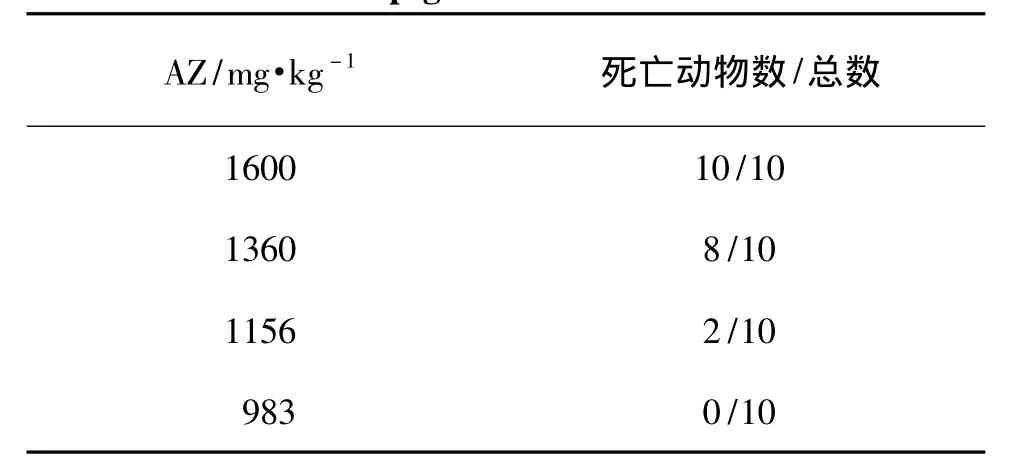
表2 ip给予AZ对小鼠存活的影响Tab.2 Effect of AZ ip given on mice survival
2.2 AZ的大鼠长期毒性
2.2.1 AZ对大鼠一般状况和体质量的影响
AZ给药期间和停药2周内,各组大鼠行为活动、外观体征和进食量及二便情况等状况均正常,未出现因药物毒性死亡现象。各给药组大鼠体质量变化与溶媒对照组相比无显著差异(表3)。
2.2.2 AZ对血液学指标的影响
AZ组大鼠给药13周及停药2周后血液学指标与对照组相比无明显改变(表4,表5)。
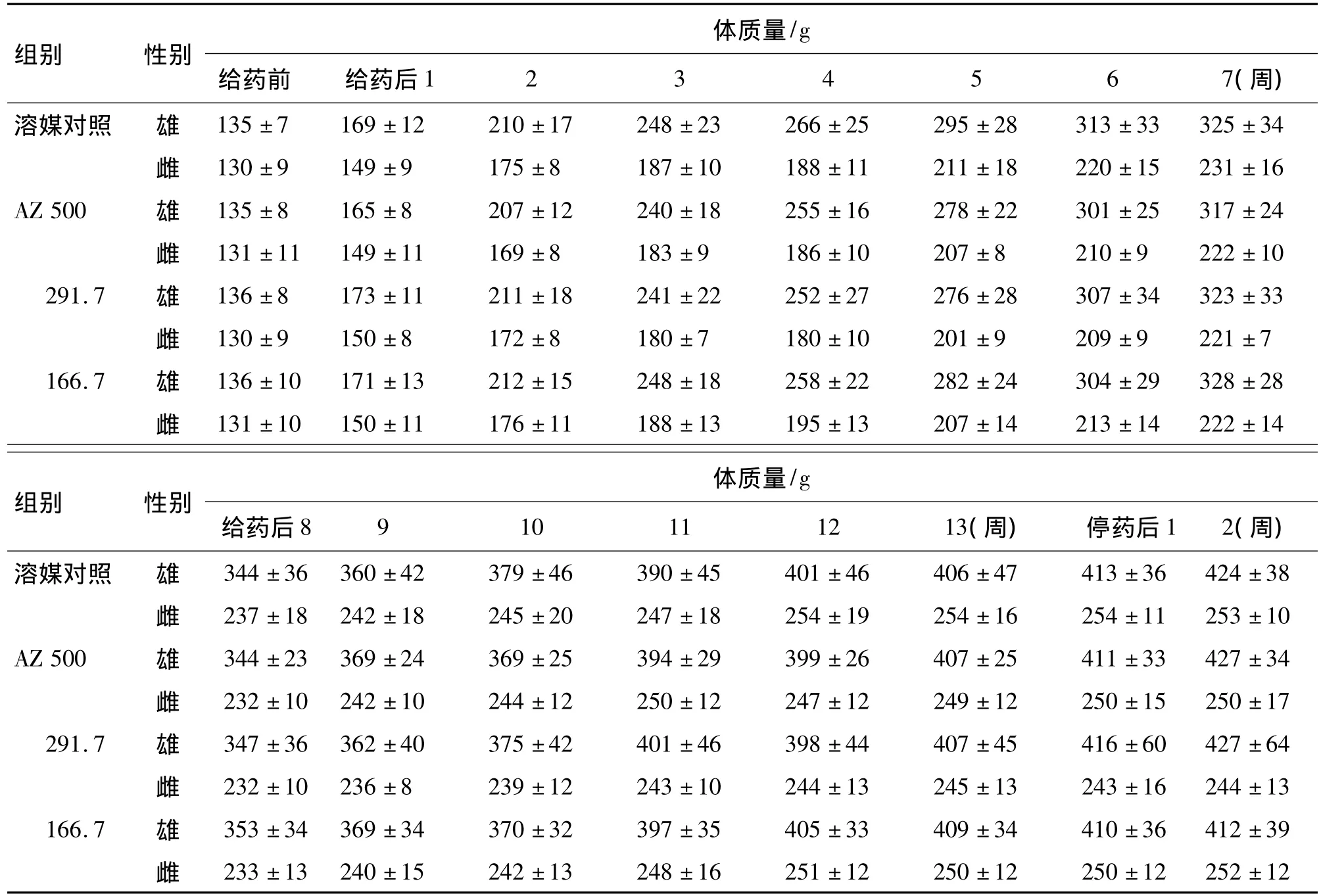
表3 AZ对大鼠体质量的影响Tab.3 Effect of AZ on body mass in rats
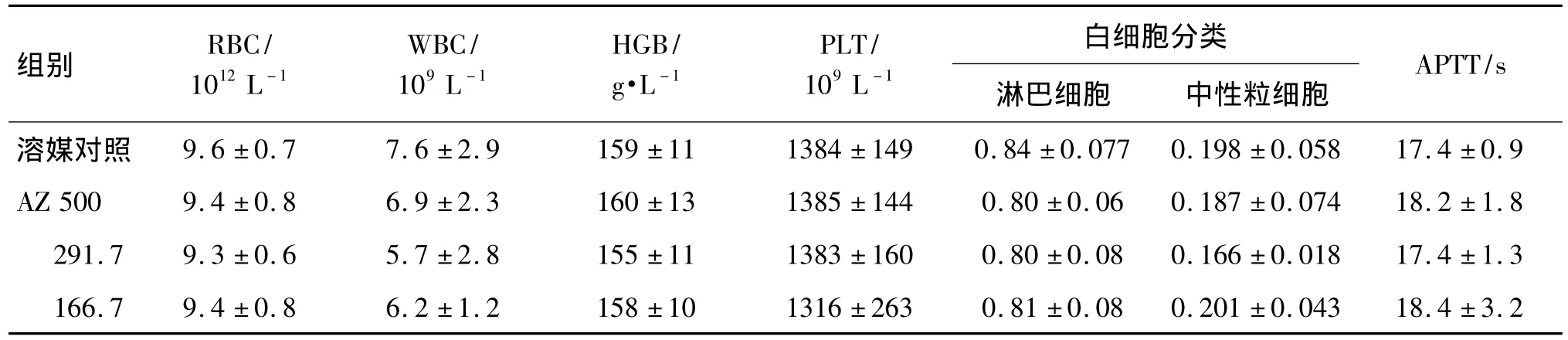
表4 AZ给药13周后对大鼠血液学指标的影响Tab.4 Effect of AZ for 13 weeks on hemotological indexes in rats
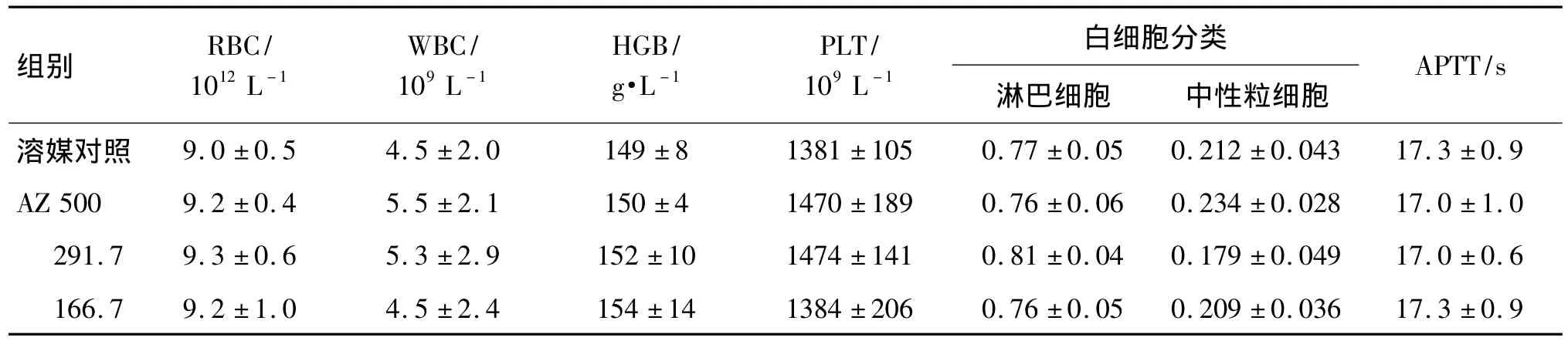
表5 AZ停药2周后对大鼠血液学指标的影响Tab.5 Effect of AZ on hemotological indexes 2 weeks after AZ was ig given in rats for 13 weeks
2.2.3 AZ对大鼠血液生化学指标的影响
与溶媒对照组相比,给AZ 13周后,AZ 500 mg·kg-1组 ALT,AST 及 BUN(P <0.05,P <0.01)有显著上升,AZ 291.7 mg·kg-1组 GOT 有显著上升(P<0.05),但基本在在正常范围内(大鼠正常参考值为 83 U·L-1)[5],AZ 500 和 291.7 mg·kg-1组T-CHO均显著降低(P <0.05,P <0.01);各给药组的其余指标与对照组比较,均无显著性差异(表6);停药2周后,各给药组生化学指标与对照组相比无显著性差异,AZ 500 和 291.7 mg·kg-1组的异常指标均恢复正常(表7)。
2.2.4 AZ对脏器系数的影响
给药期和恢复期 AZ 500,291.7和 166.7 mg·kg-1组动物处死后尸检,肉眼观察各脏器无明显病变异常情况。与对照组相比,给药13周后AZ 500 和 291.7 mg·kg-1组肝系数显著升高(P <0.05),停药2 周后 AZ 500 和291.7 mg·kg-1组肝系数基本恢复正常。各给药组其他主要脏器的脏器系数与对照组比较,均未见显著性差异(表8,表9)。
2.2.5 AZ对大鼠脏器组织形态的影响
病理组织学检查结果(图1)显示,AZ 500 mg·kg-1给药13周后,发现1例肝组织汇管区炎细胞浸润。溶媒对照组和AZ 500 mg·kg-1组各发现1 例局部间质性肺炎。AZ 291.7 和 166.7 mg·kg-1组大鼠其他各脏器组织形态学与溶媒对照组比较无差异,并未见与药物毒性相关的明显病变。
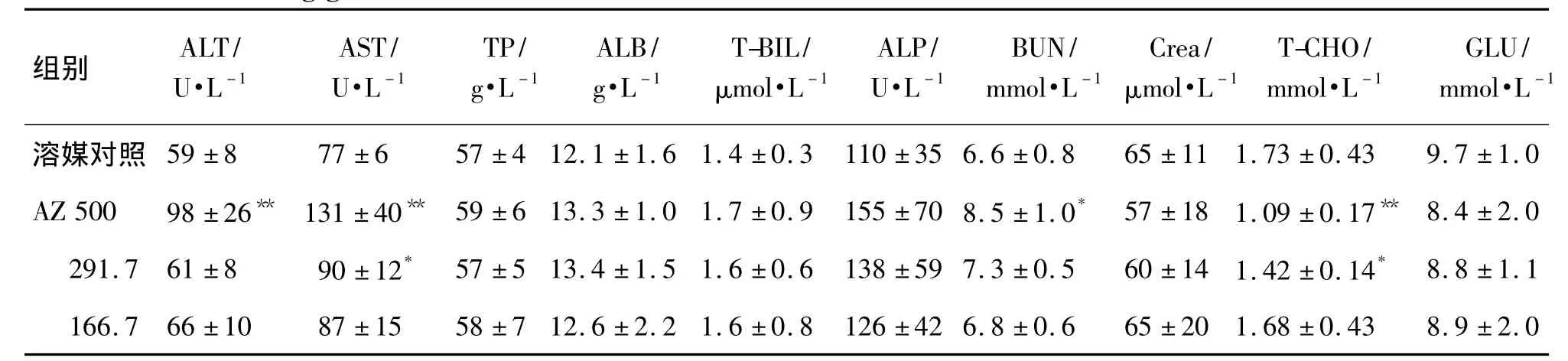
表6 AZ给药13周对大鼠血液生化学指标的影响Tab.6 Effect of AZ ig given for 13 weeks on blood biochemical indeices in rats
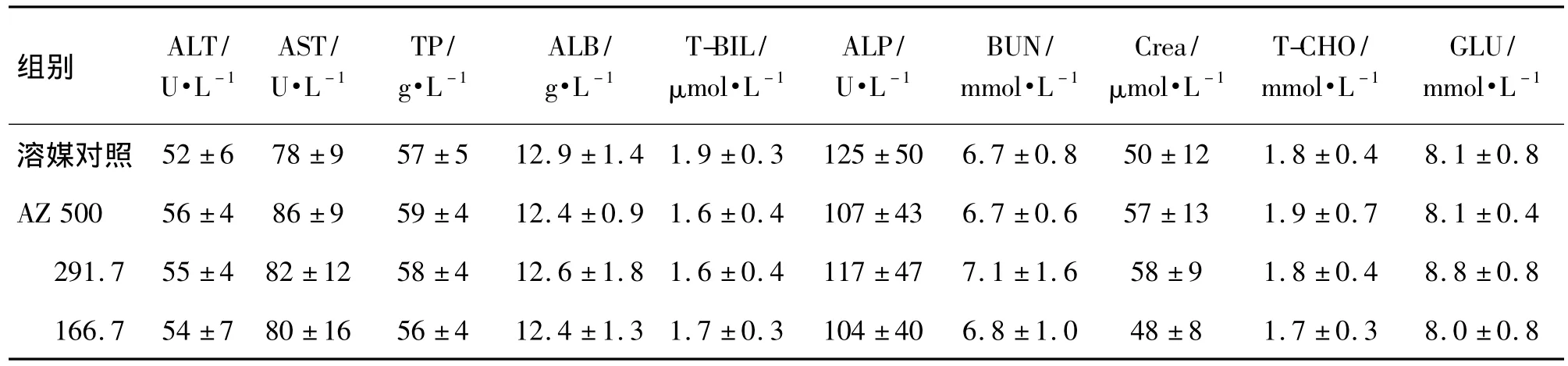
表7 AZ停药2周后大鼠血液生化学指标的变化Tab.7 Blood biochemical indexes in rats 2 weeks after AZ administration
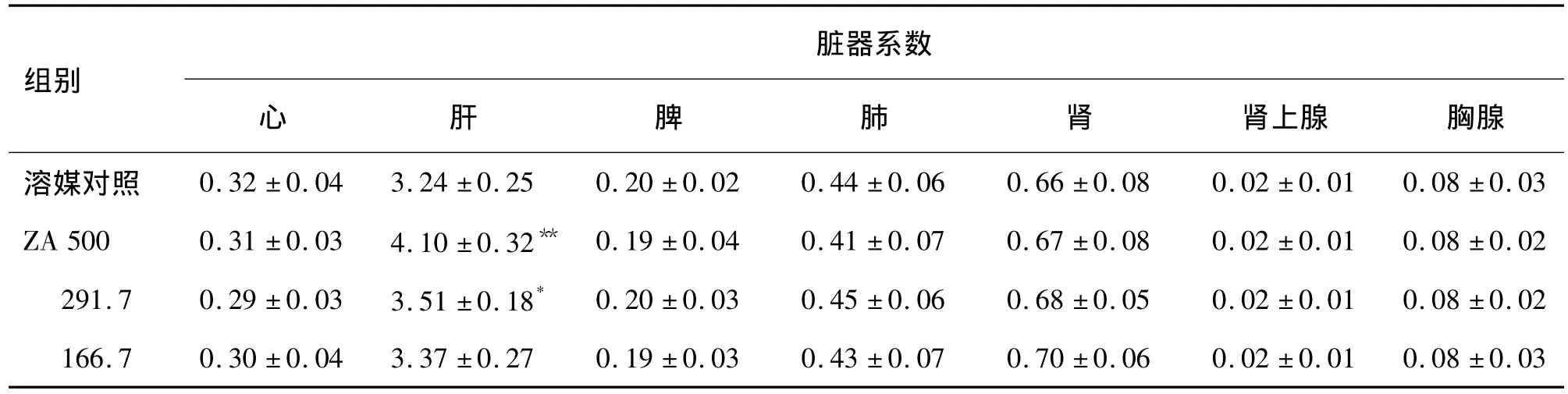
表8 AZ给药13周后对大鼠主要脏器系数的影响Tab.8 Effect of AZ ig given for 13 weeks on main organ coefficients in rats
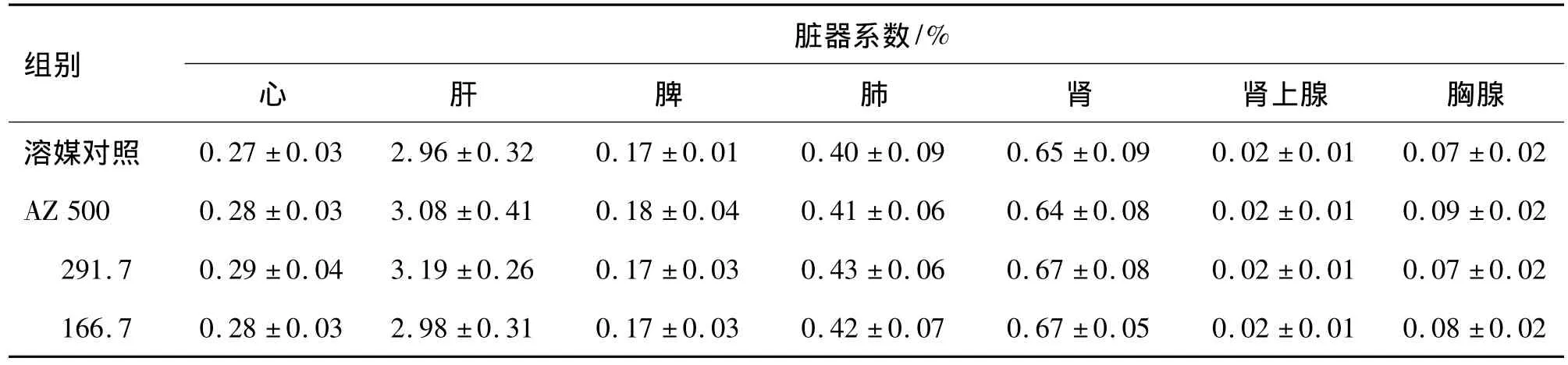
表9 AZ停药2周后对大鼠主要脏器系数的影响Tab.9 Effect of AZ on organ coefficients in rats 2 weeks after AZ administration
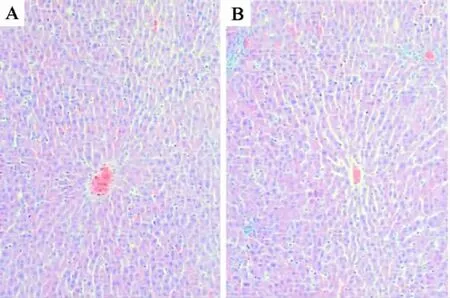
图1 AZ给药13周后对大鼠肝组织形态的影响(×100).动物分组给药见表3.A:正常对照组;B:AZ 500 mg·kg-1组.Fig.1 Effects of AZ for 13 weeks on hepatic histopathology of rats(×100)
3 讨论
通过急性毒性试验测出AZ的小鼠ig给药途径LD50为2053 mg·kg-1,根据化学物质急性毒性分级标准,该化合物为低毒级别,其LD50约为临床拟定日剂量(8.3 mg·kg-1)的250 倍,显示该化合物毒性较小且安全范围较大。根据《化学药物急性毒性试验技术指导原则》的要求,化学药物急性毒性试验的给药途径至少包括临床拟用途径和一种至少能使原型药物较完全进入循环的途径。由于AZ水溶性较小,作静脉注射制剂可行性不大,所以实验除采用经口给药途径外使用腹腔注射给药途径。由于AZ难溶于水,微溶于乙醇,考虑到使用CMC-Na作为助悬剂,以水为分散介质可使溶媒对急性毒性的影响更小,所以采用CMC-Na水溶液把供试品配成混悬液。另外实验中增加了CMC-Na生理盐水溶液的溶媒对照组,结果显示该溶媒对小鼠并无明显毒性影响。
AZ的长期毒性实验结果显示,连续给药AZ 13周及停药2 周后,AZ 500,291.7 和166.7 mg·kg-1组大鼠均未见严重毒性反应。大鼠ig给予AZ 166.7 mg·kg-1(临床拟定剂量20倍量)时,各项指标与溶媒对照组相比均无显著性差异。AZ 500和291.7 mg·kg-1给药13周后显示有血清转氨酶和及肝脏器系数升高现象,AZ 291.7 mg·kg-1组异常指标基本在正常范围内,病理组织学检查显示仅高剂量组个别大鼠出现肝组织汇管区炎细胞浸润,推断AZ 500 mg·kg-1对大鼠肝脏功能应有损害作用,AZ 291.7 和166.7 mg·kg-1的肝毒性并不明显。AZ 500 mg·kg-1组血清尿素氮水平虽有所升高,但基本在正常范围内[5],同时血清肌酐未见明显升高,肾脏脏器系数和肾脏组织病理学检查也未见与给药有关的异常,考虑到血清尿素氮的改变受多种因素影响,因此认为AZ 500 mg·kg-1对肾功能的影响较小。停药后肝肾损伤可逆,未见药物延迟性毒性反应。除对肝肾功能的影响外,AZ各剂量组大鼠均未见其他与给药相关的明显病变和毒性反应。而药效研究实验中大鼠给药剂量分别为333.3,166.7 和83.3 mg·kg-1(为临床拟用剂量的40倍、20倍和10倍[6]),因此推断AZ设定此临床拟用剂量应该有较好的安全性。
本实验结果显示,AZ 500 和 291.7 mg·kg-1组T-CHO与溶媒对照组相比均显著降低,说明AZ 500 mg·kg-1能显著降低正常大鼠血清 T-CHO,AZ 166.7 mg·kg-1时对血清 T-CHO 影响不显著。本结果还显示AZ对APTT无显著影响。其原因是因为AZ为阿魏酸结构修饰物,主要是通过抑制血小板聚集发挥抗血栓作用[6],而APTT测定的原理是以部分凝血活酶代替血小板因子Ⅲ,观察乏血小板血浆凝固所需的时间,由此推断AZ对APTT的影响不显著应属于正常。AZ在毒性剂量下对正常动物各项血脂指标及凝血功能指标的影响有待进一步的实验研究。
[1] 许 军,彭 红.阿魏酸酯及其制备方法和应用[P].CN03109056,7,2003.4.3.
[2] 徐淑云,卞如濂.药理实验方法学[M].第2版,北京:人民卫生出版社,2002:1202.
[3] 《化学药物急性毒性试验技术指导原则》课题研究组.化学药物急性毒性试验技术指导原则[S].北京:中国医药科技出版社,2005.
[4] 卫生部药政局.新药(西药)临床前研究指导原则汇编[S].1993:198-201.
[5] 孙敬方.动物实验方法学[M].北京:人民卫生出版社,2001:87.
[6] 欧仕益,包惠燕,蓝志东.阿魏酸及其衍生物的药理作用研究进展[J].中药材,2001,24(3):220-221.

