二甲双胍对胰岛素抵抗肥胖儿童的影响
杰克
引言
自20世纪70年代以来,儿童肥胖大幅上升;年龄在6~11岁的儿童中有19.6%达到肥胖(BMI≥同一年龄和性别组的第95百分位数)。儿童体内过多的脂肪,和胰岛素抵抗以及血糖代谢紊乱相关,并且它还可以作为预测将来成年后代谢综合征的风向标。胰岛素抵抗需要特别关注,因为它和儿童时期的代谢异常以及2型糖尿病的进展独立相关。
行为方式强化干预,可以降低略微肥胖儿童的体脂,但对于严重肥胖的个体几乎没有效果,因此需要发展其他有效的办法来处理这个问题。控制良好的儿童减肥药物相关的临床试验很少。目前,美国FDA批准的、用于治疗年龄<12岁的儿童肥胖的药物还没有。
最近,二甲双胍有助于儿童体重控制的潜力作用,受到了广泛关注。二甲双胍是FDA批准的、用于治疗年龄≥10岁儿童的2型糖尿病;它抑制肝脏葡萄糖产生,并且在高血药浓度情况下,可以改善外周胰岛素的敏感性。无论糖尿病还是非糖尿病成人,二甲双胍可以使体重稳定或小幅降低。一系列涉及肥胖儿童和规模相对较小的随机试验,以及一项为期48周的多中心试验,都表明,二甲双胍可使BMI/体重小幅下降,6个月平均大约可降低 1.4kg/m2(3kg),1 年 可 降 低 1.1kg/m2。 一些小规模的试验也表明,在多囊卵巢综合征或青春期阴毛早现患儿,二甲双胍可以改善胰岛素抵抗和雄激素过多症。但是,对于年龄6~12岁的严重肥胖儿童,没有随机对照试验评估二甲双胍对体重和体脂的影响。涉及这一年龄组的研究很重要,因为,已有研究表明,肥胖在儿童时期治疗,可能会更易解决。
我们针对年龄6~12岁的肥胖儿童研究了二甲双胍的影响,因为这一年龄组的儿童的胰岛素抵抗程度很显著,被认为特别危险。我们认为,二甲双胍可以降低儿童的体重、BMI和脂肪含量;提高胰岛素敏感性;改善代谢综合征各组分。
研究设计与方法
研究样本
纳入标准包括:肥胖儿童,年龄6~12岁,BMI≥第95位百分位数(根据美国疾病控制和预防中心2000年生长曲线图);青春期前的或青春期早期;曾有空腹高胰岛素血症(定义为,空腹胰岛素≥15μU/mL)。排除标准包括:空腹血糖异常,有糖尿病,被诊断有肾病、心脏病、内分泌疾病、肺病以及肝脏疾病,基线时肌酐>1mg/dL,谷丙转氨酶(ALT)或谷草转氨酶(AST)超过实验室正常范围上限的1.5倍。这项研究得到了儿童以及父母的同意,签署了书面同意书。这项研究由数据和安全监督委员会监督。
设计概述
我们进行的是单中心试验,时间从2000年9月~2008年8月。首先,纳入的受试者进入为期6个月的随机安慰剂组对照双盲试验阶段,然后两组受试者都进行开放标签的二甲双胍治疗6个月。
随机阶段和开放标签阶段
我们以1:1的比例,把受试者随机分配到二甲双胍组或安慰剂组,就餐服用,每天两次。研究者给受试者进行了编号,使用的是符合美国药典的二甲双胍胶囊(250mg/胶囊)。
一旦完成基线评估,受试者的药物剂量根据预期算法逐步增加(3周为一疗程),起始剂量为500 mg/每天两次,逐步增加至最大剂量为1000 mg/每天两次。我们使用了成人最大剂量为儿童最大剂量,因为,被纳入的严重肥胖受试者(表1)的预期算法类似于成年人。我们对于耐受困难的受试者,每次减少250 mg,为期1周,然后再尝试增加剂量到目标值。如果250 mg/天都不能耐受,药物中断。每日给予多种维生素咀嚼片(含有6μg维生素B12)。随机阶段结束后,2组受试者逐步增加二甲双胍剂量至规定的最大剂量2000mg/天,再加上多种维生素咀嚼片/天,为期6个月。
在这两个研究阶段,每个受试者和家长/监护人,每月进行一次由营养师指导管理的减重和改变生活方式教育,以督促降低膳食热量,增加体育运动。受过培训的受试者需完成饮食日记,并由营养师审查。当个性化定制的膳食摄入达到或超过500 kcal/天,要求减少脂肪和热量摄取。运动要求每天进行30分钟的有氧运动,并尽可能使用计步器。
初步评估
符合纳入标准的受试者需评估的项目包括:①体重;②身高;③腹围、臀围和三头肌皮褶厚度;④血压(坐姿,至少休息5分钟后测量);⑤手部X线光片(以确定骨龄);⑥全身双能X线骨密度仪(DEXA)和空气置换法(ADP)测定的肌肉脂肪含量;⑦以L2-L3和L4-15为中心的MRI测定的腹腔内和腹部皮下脂肪组织。⑧基线时和随后的研究中进行2小时高糖(200mg/dL)钳夹试验,以评估胰岛素敏感性和第一时相的胰岛素分泌(取前15分钟胰岛素分泌的平均值)。葡萄糖代谢率(M)定义为,调整经尿葡萄糖损失的量和葡萄糖自身容量后的外源性葡萄糖输注率。⑨胰岛素敏感性(SIclamp)还可以通过葡萄糖代谢率和稳态时的胰岛素水平(I)的比值(M/I)来计算。
基线时和后续的研究中,在受试者空腹状态测量ALT、AST、总胆固醇、HDL-C、LDL-C和甘油三酯水平。采集空腹血浆样本,以检测葡萄糖水平(使用了罗氏诊断产品)。C-反应蛋白通过高灵敏度仪器(灵敏度为0.020mg/L)进行了测量。维生素B12和胰岛素水平采用了西门子医疗诊断仪器进行了测定。空腹血浆样本用来计算HOMA-IR指数,公式为:HOMA-IR指数=胰岛 素(μU/mL)× [血 糖(mmol/L)/22.5]。达到至少3个以下组分就可以诊断为儿童代谢综合征,包括:①腰围、血压和甘油三酯≥同一年龄和性别组的第90个百分位数;②HDL-C≤同一年龄和性别组的第10个百分位数;③空腹血糖≥100mg/dL。
检查内容
该研究预先确定的主要研究终点是BMI的Z分数,在为期6个月的随机治疗阶段结束时可以确定。次要研究终点是BMI、体重和脂肪含量的变化,也是在随机治疗阶段结束时确定。第三个指定终点是皮褶厚度、体围、内脏脂肪组织、胰岛素抵抗和代谢综合征各组分的变化。
受试者接受访问,每月一次,返回未使用的药物,同时接受新的药物,我们利用每月返回的胶囊来评估受试者的依从性。每次访问需测量:BMI,血压,肝功,循环乳酸,血清维生素B12。6个月后,受试者被重新评估,然后进入为期6个月的开放标签的二甲双胍治疗阶段,期间也是每月访问一次。
统计学分析
把握度或统计效能(在统计学中,将实际上有差异而试验能得出阳性结果的可能性称为把握度或检验效能)是根据肥胖儿童(存在高胰岛素血症、年龄6~11岁)6个月的BMI变化的数据资料确定的,经过计算我们得出该试验的把握度为80%。该研究的主要数据分析使用的是Windows环境下的SPSS软件,版本14.0。另外,对为期6个月的随机双盲对照研究的2组受试者进行了疗效分析。利用O'Brien-Fleming方法,确定P值<0.04515被认为在研究结束时有统计学意义。我们采用多重填补方法模型对缺失数据进行多次填补,评估了意向性治疗样本(所有的被随机分配的受试者)的治疗疗效。BMI 的Z分数变化(或每个次要终点变量的变化)是因变量;二甲双胍治疗是自变量;年龄、性别、种族/族裔是协变量。
为了评估结果的敏感性,我们进行了三项额外的分析:①假设所有退出研究的受试者的体重增加最多(≥2.27kg);②那些接受二甲双胍治疗的受试者的体重没有增加,而那些接受安慰剂的受试者的体重增加最多;③那些接受安慰剂的受试者的体重没有增加,而那些接受二甲双胍治疗的受试者的体重增加最多。
结果
所有受试者(N=100)被随机分配到两个研究组(图1)。受试者和退出者没有显著的人口差异。受试者存在显著的胰岛素抵抗迹象;很多有2型糖尿病家族史。当受试者被分为青春期前和青春期,2组在种族、既往史或实验室数据没有显著差异(均P> 0.46),其中包括胰岛素抵抗的程度(HOMA-IR:二甲双胍组+青春期前4.3±2.0,二甲双胍组+青春期4.6±2.3;安慰剂组+青春期前4.5±4.1,安慰剂组+青春期5.0±2.9)。
受试者的85%完成了为期6个月的随机对照试验(二甲双胍组为85%;安慰剂组为85%,P=0.98)。共有85人进入了为期6个月的二甲双胍开放标签试验,其中67%的受试者最终完成了该研究阶段(图1)。参与研究的受试者和退出研究的人员相比,社会人口特征和基线时测量的或实验室检查的数据没有显著差异性(所有的P>0.65)。
体重和身体组成的变化
在安慰剂对照随机试验阶段(图2),二甲双胍组和安慰剂组儿童BMI的Z分数都显著降低(P<0.01);但是,相比安慰剂组,二甲双胍组儿童BMI的Z分数的降低幅度多0.07(95th CI -0.12~ -0.01,P=0.02),BMI的降低幅度多 1.09kg/m2(CI -1.87 ~ -0.31,P=0.006),体重的降低幅度多3.38kg(CI -5.2~-1.57,P<0.001),总体脂的量的降低幅度也更为显著(P<0.05)。有3名二甲双胍组(安慰剂组1名也没有)儿童在治疗6个月后,减重效果显著,BMI达到了同一年龄性别组的第97个百分位数以下(P=0.25)。另外,相比安慰剂组,二甲双胍组儿童的体围、皮褶厚度也显著降低,但两组的腹内脂肪含量没有显著差异性。
在开放标签二甲双胍治疗试验阶段,各组前后2个不同的试验阶段相比,前安慰剂组儿童BMI的Z分数降低显著;而前二甲双胍组儿童BMI的Z分数没有显著变化(图2);BMI绝对值增加了,这一点和预计的一样(因为儿童开始进入发育阶段)。和基线时相比,12个月后的儿童BMI 的Z分数显著降低,幅度为0.091(CI -0.183~-0.001,P=0.05)。

图1 试验流程

图2 BMI的变化
额外的分析发现,在随机对照试验阶段,和非西班牙裔或西班牙裔白人儿童(0.108±0.017)相比,非西班牙裔黑人儿童BMI的Z分数(0.035±0.021) 的 降 低 幅 度 少 0.073(CI 0.020~0.127,P=0.008),但是治疗组组内的种族差异性并不显著(P=0.064)。和基线时相比,治疗后儿童的体脂达标对严重胰岛素抵抗状况或进入青春期并没有显著影响,即使调整种族因素后也是如此(所有P≥0.20)。
胰岛素抵抗和代谢的变化
和安慰剂组相比,二甲双胍组儿童的空腹血清胰岛素水平(P=0.02)、血糖水平(P=0.02)和HOMA-IR指数(P=0.006)获得的改善更多。然而,无论是胰岛素分泌的第一时相(P=0.34),还是胰岛素敏感性(P=0.52),2组儿童比较结果显示都没有显著差异性。其他实验室通常观察到的可以显著降低体重的因素,在本研究中的2组儿童,没有显示显著差异性。2组比较,二甲双胍组儿童代谢综合征的患病率也没有显示有显著改善(P=0.71)。
不良事件
没有报告出现严重或危及生命的不良事件。没有受试者的AST或ALT的浓度异常或发生酸中毒。所有为期12个月试验涉及的受试者的血清维生素B12在正常范围内(220~960 pg/mL),只是,在随机试验阶段,安慰剂组儿童血清维生素B12水平(173± 67pg/mL)增加,二甲双胍组儿童血清维生素B12水平(-57±58 pg/mL)降低(P<0.001)。未发现存在二甲双胍相关的血红蛋白浓度差异性(P= 0.53)。
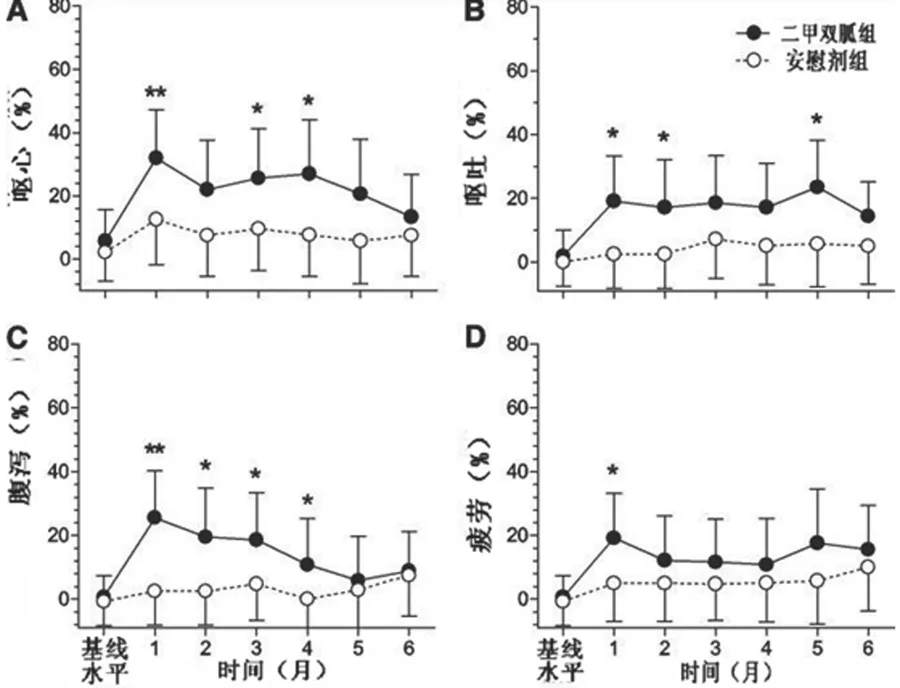
图3 安慰剂对照试验阶段所报告的副作用
二甲双胍组儿童的胃肠不适发生率显著增加。和安慰剂组相比,二甲双胍组儿童的副作用事件更多;包括水泻或稀便(二甲双胍组41.5%,CI 30.1%~55.9%;安慰剂组17%,CI 7.6%~30.8%,P=0.01),呕吐(二甲双胍组41.5%,CI 29.1%~55.9%;安慰剂组21.3%,CI 10.7%~32.7%,P=0.05),疲劳(二甲双胍组37.7%,CI 24.8%~52.1%;安慰剂组14.9%,CI 6.2%~28.3%,P=0.02)。另外,二甲双胍组儿童对于平常感兴趣的活动会失去兴趣,但这些副作用适应一段时间后可以消失。二甲双胍相关的副作用事件在前1个月发生最多,之后逐渐下降,因此,在随机对照试验或开放标签试验结束时,2组的不良事件的平均发生率并没有显著差异(图3)。
在随机安慰剂组试验阶段结束时,二甲双胍组中有17.0%的儿童的二甲双胍剂量(500~1,500 mg/天)没有达到最高(2000mg/天),而安慰剂组中只有2.1%(P=0.03);但是,只有一名受试者因二甲双胍不耐受而退出试验。和不能耐受二甲双胍的儿童相比(10.3 ± 1.4岁),那些没有给予二甲双胍充分剂量的儿童的年龄比较小(8.8±1.9岁,P=0.01),但在BMI或脂肪含量上2组没有显著差异性,在对药物的依从性方面2组也没有显著差异性。
讨论
儿童期开始肥胖,预示着以后的生活中易患CVD相关因素。在肥胖儿童,预防肥胖相关的并发症(包括2型糖尿病),是一个主要的医疗目标。以证据为基础的研究表明,在肥胖和肥胖相关的并发症儿童,服用二甲双胍有益;成人数据显示,二甲双胍可延缓2型糖尿病的发生,我们检验了这样的一个假设,即,在存在胰岛素抵抗、6~12岁的肥胖儿童,二甲双胍可以改善葡萄糖代谢异常、降低体重和体脂。
二甲双胍可以适度改善儿童BMI的Z分数,并且,大多数可以保持为期1年的治疗。尽管有一些研究(不是所有的)结果显示,二甲双胍减少腹腔内的脂肪并不显著,但是和安慰剂相比,二甲双胍可以减少体脂。这可能是因为,二甲双胍的主要作用,即,抑制肝脏糖异生;二甲双胍改善空腹胰岛素和血糖水平,而HOMA-IR指数(测量胰岛素敏感性的方法),似乎主要是反映的是肝脏对胰岛素的敏感性,但是二甲双胍并不能大大改善全身(主要是肌肉)胰岛素的敏感性。有研究显示,在以色列军队新兵,空腹血糖水平>86mg/dL的年轻人,随后的6年期间的糖尿病风险持续增加。
该研究受试者的基线血糖水平平均为92mg/dL,6个月后,二甲双胍组儿童的血糖水平平均值略有下降,而安慰剂组儿童额外增加了3.5 mg/dL。本研究的结果显示,二甲双胍使受试者保持空腹血糖水平在一个较低的水平,这表明,在高危儿童,二甲双胍可能有预防或延缓2型糖尿病发生的作用。
在胰岛素抵抗相关的代谢异常的其他方面,二甲双胍治疗并没有导致显著的变化。观察到的体重变化有限,也许还合并有越来越严重的全身性胰岛素抵抗(通常发生在进入青春期的儿童),这可以说明,以前针对青少年在代谢方面的研究,未能发现二甲双胍引起显著改善的原因所在。
约有17%的受试者不能够耐受二甲双胍的副作用,特别是年龄较小的青少年患者。尽管努力达到充分剂量,但因不能耐受2,000mg/天,可能限制了本可观察到的疗效。在一定程度上,剂量的可变性,使确定二甲双胍的功效更困难。我们的数据表明,目标为2,000 mg/天,并不是所有二甲双胍治疗的儿童所能达到的。其他研究显示受试者对低剂量的耐受性良好,但是,青少年使用二甲双胍缓释剂2,000mg/天治疗,也有类似的副作用。除了恶心、便溏,我们也观察到疲劳症状,和先前公布的二甲双胍组儿童一样。最后,还有血清维生素B12水平相对降低,尽管同时还服用多种维生素片。维生素B12缺乏是不太可能被二甲双胍组儿童报道的,因为,膳食摄入B12长期不足,才能被临床发现,但是,有报道称,在经最长时间、最高剂量二甲双胍治疗后获得最好效果的成人,血清维生素B12水平降低14%~30%。
这项研究的局限性在于,只涉及到100名儿童;因此,就一些肥胖相关的合并症而言,确定安慰剂组和二甲双胍组之间的差异性的效力不足。安慰剂对照试验阶段的时间只有6个月,最长的治疗时间也只是1年;因此,这项研究并没有探讨二甲双胍的远期疗效,而这个因素对于治疗慢性疾病(如,肥胖)是必需的。这项研究结果的普遍性也有所限制,事实上,仅涉及到了严重胰岛素抵抗的肥胖儿童;目前还不清楚,二甲双胍对于较少胰岛素抵抗和没有那么肥胖的儿童的疗效。Wilson等人发现,不存在胰岛素抵抗的青少年有着非常相似的结果。
最后,由于减肥干预旨在为以后可能会运用到临床实践做示范作用,营养师每月仅访问一次,二甲双胍引起体重下降的幅度,可能发生在强化行为干预方案阶段(本文没有提及)。
总之,在存在胰岛素抵抗、年龄在6~12岁的肥胖儿童,二甲双胍可是适度降低体重和肥胖,以及改善葡萄糖代谢异常情况。虽然体重下降的幅度比较小,二甲双胍可以做这样一个“承诺”,即,在2型糖尿病高危儿童,它可以预防或延缓糖耐量减低的出现。

