乙酰基二茂铁缩甘氨酸Schiff碱金属配合物的合成及抑菌活性研究
尹大伟, 王 青, 刘玉婷
(1.陕西科技大学化学与化工学院, 陕西 西安 710021; 2.商丘医学高等专科学校, 河南 商丘 476100)
0 引 言
Schiff碱是羰基化合物与氨基缩合形成的具有碳氮双键的一类化合物.早在1864年Schiff Hugo首次报道了伯胺与醛、酮类活泼羰基化合物的缩合反应,生成了含亚胺基(Azomthine group)(-RC=N-)的一类化合物,后人称之为Schiff碱,从此拉开了人们研究Schiff碱的帷幕.Schiff碱合成相对容易,能够灵活地选择各种胺类及带有羰基的不同醛和酮进行反应,改变连接的取代基,并改变给予体原子本性及位置,可开拓出许多从链状到环合、从单齿到多齿、性能不同、结构多变的配体及金属配合物[1].有大量的文献报道,Schiff碱可与过渡金属离子、部分主族金属与稀土元素形成配合物,该类配合物具有很强的生理活性,可作为抗菌、抗癌、、抗肿瘤、抗结核等的药物;该类配合物还具有较高的催化活性,对氧负离子有很好的抑制作用[2],可广泛应用于医学治疗、合成、生物调节剂、热敏或压敏材料中的染料、聚合物改性、分析试剂、螯合剂等领域.本文合成了6种新型的含二茂铁基的甘氨酸Schiff碱过渡金属配合物(如图1所示),并对其抑菌活性进行了初步探索.
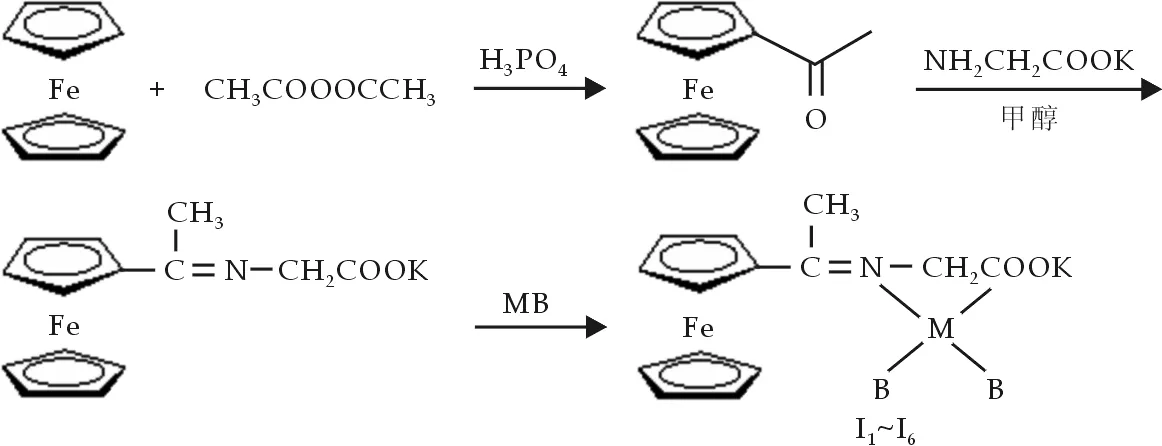
图1 含二茂铁基的甘氨酸Schiff碱过渡金属配合物的合成反应式
(MB1:醋酸铜;MB2:醋酸锌;MB3:氯化铜;MB4:氯化钴;MB5:氯化锌;MB6:硝酸铁)
1 实验部分
1.1 仪器与试剂
红外光谱采用德国Bruker公司VECTOR22型傅立叶变换红外光谱仪测定,KBr压片;元素分析采用德国Elemeraor公司Vario EL Ⅲ型元素分析仪测定;电导率采用上海精密仪器科学有限公司DDS-307型电导率仪测定;热重分析采用美国TA公司SDTQ 600V 80Build 95 热分析仪测定,在氮气气氛下测量,温度范围为25~800 ℃,升温速率10.0 ℃/min;熔点采用北京泰克仪器有限公司X-4数字显示显微熔点测定仪,温度计未经校正.
所用试剂均为分析纯,乙酰基二茂铁按文献[3]合成,m.p.: 84~85 ℃(文献[3]值: 85±1 ℃ );乙酰基二茂铁缩甘氨酸Schiff碱按文献[4]合成,m.p.: 271~272 ℃(文献[4]值:272 ℃ ).
1.2 过渡金属配合物I1~I6的合成
将1 mmol乙酰基二茂铁缩甘氨酸Schiff碱溶于10 mL无水甲醇中,搅拌下滴加含有1 mmol无机盐(MB1~MB6)的无水甲醇溶液,在氮气保护下回流反应5 h,反应完毕后冷却,抽滤,无水乙醇,乙醚洗涤,真空干燥.
I1为墨绿色土黄色粉末状固体,产率:59.1%,m.p:283~286 ℃;
I2为浅土黄色粉末状固体,产率:51.4%, m.p:291 ℃变黄,未见溶化;
I3为浅蓝色粉末状具有荧光的固体,产率:53.3%,m.p:350 ℃,未见熔化;
I4为玫红色粉末状固体,产率:60.2%,m.p:303 ℃,变成泡状;
I5为浅土色粉末状固体,产率:49.5%,m.p:282~283 ℃;
I6为褐色粉末状固体,产率: 65.4%,m.p:350 ℃,未见熔化.
1.3 抑菌活性测试
采用滤纸片法对目标化合物进行抑菌活性测试.
将用无水乙醇溶解的目标化合物的药物原液平铺于含菌的平皿上,放入培养箱中培养,在28 ℃下培养48 h后观察,测量抑菌圈直径(抑菌环为琼脂培养基上透明的圆环,未生长细菌部分),同时进行空白对照.出现抑菌圈直径大,说明该化合物抑菌活性强.实验菌株为金黄色葡萄糖菌、大肠杆菌、放线菌、酵母菌.
2 结果与讨论
2.1 化合物表征
2.1. 1 配体及配合物的元素分析及性质

表1 配体和配合物的元素分析数据(括号内为计算值)
配体配合物元素分析数据列于表1.
从表中可以看出,元素分析的测定值与理论值基本吻合.配体在空气中不太稳定,配体易溶于氯仿、DMF、DMSO、甲醇、乙醇,难溶于乙醚、异丙醇.配合物均是过渡金属盐与相应的Schiff碱1∶1反应的产物.配合物在空气中较稳定.
2.1.2 配体及配合物的摩尔电导
配体及配合物元素的摩尔电导数据列于表2.

表2 配体和配合物的摩尔电导数据
在室温下浓度为1.0×10-3mol·L-1的水溶液(配体在乙醇中)中测定摩尔电导,结果表明:除硝酸铁配合物外,其他配合物均为非电解质(与小于42.5 s·cm-2·mol-1的范围相一致[5]),说明Cl-、Ac-在内界,硝酸铁配合物为1∶1 型电解质,2个硝酸根在内界,1个硝酸根在外界.
2.1.3 红外光谱分析
配体及配合物的红外光谱数据列于表3.

表3 配体及配合物的主要红外光谱数据(cm-1)
将乙酰基二茂铁与配体的红外光谱图比较,可以看出它们的IR光谱发生了较大的变化,在1 665 cm-1处的C=O伸缩振动吸收峰已经消失,在1 612 cm-1处出现了新的吸收峰,这说明C=O键已经转变为C=N键.比较配合物与相应的Schiff碱的红外光谱可以发现:配体中1 612 cm-1处的C=N伸缩振动吸收峰vC=N在生成配合物后发生了位移,表明配体中的亚胺基团上的N原子也参与了配位.另外,与羧酸根,在配合物中的vas(COO-)、vs(COO-)与配体相比较,波数均发生了变化,说明羧酸根参与了配位.从羧酸对称和反对称频率之差且Δv(vas-vs)>200 cm-1,可推知在这些化合物中羧酸根以单齿配位[6].硝酸铁配合物在1 497、1 384、1 287、1 041、8 32 cm-1附近出现了NO3-吸收峰,其中1 384、832 cm-1附近的振动峰,表明配合物中存在自由的NO3-,而1 497、1 287、1 041 cm-1振动峰的出现,表明配合物中存在配位的NO3-且1 497 cm-1和1 287 cm-1相差约210 cm-1,说明配合物内界有以双齿形式配位的NO3-存在[7,8].配合中有水分子存在,这与元素分析和热重分析结果相吻合.
2.1.4 配合物的热重分析[9].
采用SDT型热分析系统,在氮气气氛中进行,以Al2O3为参比物,升温速度为10 ℃/min,在室温至800 ℃区间内对配合物进行了热重分析.部分配合物的热重分析数据列于表4.

表4 配合物的热分析数据
从表4可以看出所有配合物中组成水都为结晶水.从失重比率可以看到,这些配合物热分解最终产物均为铁和金属的混合物.利用差热分析对配合物的热稳定性进行了研究,得出热稳定性次序为:Zn配合物>Cu配合物>Co配合物 ≈Fe配合物(Zn配合物的最终分解温度大于800 ℃,Cu配合物约为620 ℃,Co配合物约为600 ℃).

表5 配体及其过渡金属配合物的抑菌活性/抑菌圈直径:mm
注“…”表示未发现抑菌圈.
2.2 目标化合物的活性
配体及其过渡金属配合物的抑菌活性(抑菌圈直径)结果见表5.
配合物对金黄色葡萄球菌、大肠杆菌均有不同程度的抑制作用;对放线菌、酵母菌无抑制作用,而对革兰氏阳性菌类金黄色葡萄球菌的抑制作用较显著;与配体相比,配合物的抑菌活性显著的提高,这可能是因为配合物比配体更容易穿透细菌细胞膜,提高了膜内药物浓度,改变了细胞膜的电性质,从而干扰了细菌细胞膜的正常功能,抑制了细菌的生长[10].配合物对测试菌种的抑制作用有一定的选择性,其作用机理还不十分清楚,尚需要进一步深入研究.
3 结束语
本文以乙酰基二茂铁缩甘氨酸Schiff碱配体与过渡金属铜、钴、锌、铁等的盐反应,合成了6种新型含二茂铁基的Schiff碱过渡金属配合物,并通过表征了确定化合物的结构.对目标产物进行的生物活性的实验结果表明配合物与配体相比,配合物的抑菌活性显著的提高.
参考文献
[1] 郑匀飞,陈文纳,李德昌,等. Schiff碱及其配合物的应用研究进展[J]. 化工技术与开发, 2004,33(4):26-29.
[2] 李建章,秦圣英,李仲辉,等. 冠醚化单和双Schiff碱的合成及其钴配合物的氧加合性能[J]. 合成化学,1998,6(2):137-148.
[3] 刘玉婷. 有机合成化学实验[M]. 长春: 吉林大学出版社,2006:117-119.
[4] 孙为银. 配位化学[M]. 北京:化学工业出版社,2004:31-35.
[5] Geary WJ. Use of conductivity measnremeuts in organic solvents for characterization of coorolination compounds[J]. Coord Chem Rev., 1971,(7):81.
[6] Nakamoto K. Infrared and Ram an Spectra of Inorganic and Coord Ination Compounds[M]. 4th Ed, NewYork: Wiley £Sons, 1986.
[7] 中本一雄著,黄德如译. 无机和配位化学物的红外和拉曼光谱[M]. 北京:化学工业出版社,1986: 208-237.
[8] 刘宝殿,徐永祥. 混合二烃基二氯化锡与水杨醛缩苯胺类Schiff 碱配合物的合成和表征[J]. 高等化学学报,1994, 15(9): 1 322-1 326.
[9] 沈 兴. 差热、热重分析与非等温固相反应动力学[M]. 北京:冶金工业出版社,1995:22-96.
[10] 赵雁武,周振中,王宪伟. 3,4-二羟基苯甲醛缩氨基硫脲锌(Ⅱ)配合物合成、表征与抑菌活性[J]. 武警工程学院学报,2003,19(2):13-14.

