喉咽清口服液中蜕皮甾酮测定法的改进
何选林, 王群英
(湖南省永州市药品检验所,湖南永州425100)
喉咽清口服液主要由土牛膝、马兰草、车前草、天名精等中药组成,辅料为蔗糖、防腐剂,具有清热解毒、利咽止痛的作用[1]。土牛膝中含有黄酮苷、氨基酸、有机酸、酚类、挥发油及生物碱等成分[2],《中国药典》2010版一部该品种采用高效液相色谱法测定喉咽清口服液中蜕皮甾酮,该方法提取时杂质太多,影响蜕皮甾酮的分离,导致测定的含量偏低,本实验修改了提取的溶剂,该法简单、快速、结果直观。并通过生产厂家提供的6批样品进行了比较。结果表明改进法准确有效。
1 仪器与试药
Waters高效液相色谱系统1525泵,2996紫外检测器(美国),Empowers工作站。蜕皮甾酮对照品(中国药品生物制品检定所,批号11638-200402),喉咽清口服液样品(规格每支10 mL,为某公司生产的6批产品080605、080607、080608、080704、080706、080801);乙腈为色谱纯、重蒸馏水。
2 方法与结果
2.1 色谱条件 色谱柱为Hypersil-ODS C18(250 mm×4.6 mm,5 μm),以乙腈-水(20 ∶80)为流动相;检测波长为 248 nm;柱温 室温,进样量 20 μL。在此条件下[3]67,[4-9],色谱图见图1,蜕皮甾酮的保留时间为7.8 min,理论塔板数按蜕皮甾酮计算为6 800。

图1 高效液相色谱图
2.2 对照品溶液制备 精密称取蜕皮甾酮对照品30 mg,置50 mL的量瓶中,加乙醇适量,振摇使蜕皮甾酮溶解,并稀释至刻度,摇匀,作为对照品溶液贮备液。
2.3 供试品溶液的制备 取本品25 mL,置具塞锥形瓶中,加正丁醇25 mL,超声30 min,放冷后,滤过,用乙醇10 mL分数次洗涤容器及残渣,合并滤液和洗液蒸干,残渣加乙醇溶解并转移至25 mL量瓶中,加乙醇稀释至刻度,作为供试品溶液。
2.4 阴性对照溶液的制备 精密称取处方中除土牛膝的细粉(约相当于蜕皮甾酮3 mg),置具塞锥形瓶中,加正丁醇25 mL,超声30 min,放冷后,滤过,用乙醇10 mL分数次洗涤容器及残渣,合并滤液和洗液蒸干,残渣加乙醇溶解并转移至25 mL量瓶中,加乙醇稀释至刻度,作为阴性对照溶液。
2.5 线性关系考察 精密量取对照品溶液贮备液1、2、3、5、10 mL溶液分别置50 mL量瓶中,加流动相稀释至刻度,注入液相色谱仪,记录色谱图,以质量浓度为横坐标(X),峰面积为纵坐标(Y),求得回归方程:Y=7 680.2+674 256.4X,r=0.999 96,结果表明,当进样量为 20 μL 时,蜕皮甾酮在12~120 μg/mL质量浓度范围内,呈良好的线性关系。
2.6 精密度考察 取2.2项下质量浓度为60 μg/mL的对照品溶液,依法测定,记录连续5次的峰面积,RSD为0.98%。
2.7 重复性试验 取同份样品按2.11项测定蜕皮甾酮5次,含蜕皮甾酮质量浓度为62.4 μg/mL,RSD为0.66%;结果表明重复性好。
2.8 稳定性试验 取同份样品分别在0、4、8、12、16 h测定蜕皮甾酮,质量浓度为59 μg/mL,RSD为0.61%;结果表明稳定性好。
2.9 阴性对照试验 取对照品溶液、供试品溶液、阴性对照溶液按本实验条件进样为20 μL,色谱图见图1,在本实验条件下阴性对照无干扰。
2.10 回收率试验 精密称取已测定的同一批样品9份,分别精密加入对照品适量,按2.3项制备样品,依法测定回收率,结果见表1。

表1 样品的回收率测定结果
2.11 样品测定 取本品25 mL,置具塞锥形瓶中,加正丁醇25 mL,超声30 min,放冷后,滤过,用乙醇10 mL分数次洗涤容器及残渣,合并滤液和洗液蒸干,残渣加乙醇溶解并转移至25 mL量瓶中,加乙醇稀释至刻度,作为供试品溶液。分别吸取供试品溶液与对照品溶液各20 μL,注入高效液相色谱仪,记录色谱图见图1B,按外标法以峰面积计算质量浓度与法定方法质量浓度[3]1159比较结果见表2。
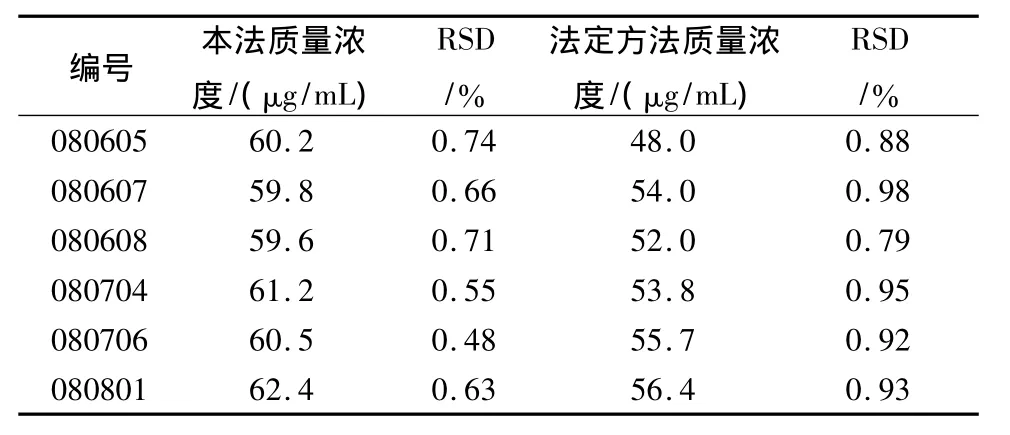
表2 样品测定结果(n=3)
3 讨论
3.1 色谱条件的选择 本实验选用了较为常用的C18柱和以乙腈-水(20∶80)为流动相;检测波长为248 nm,得到良好的分离效果,且配置简单。
3.2 检测波长 经紫外扫描蜕皮甾酮在247.6 nm处有最大吸收故选择在248 nm测定。
3.3 溶剂的选择 本测定,先采用法定方法只用乙醇稀释,测定分离不太好,后采用甲醇、50%甲醇、50%乙醇及本法采用正丁醇提取,乙醇溶解。经试验,本实验配制的溶液在16 h内进样并无任何变化且分离好。
3.4 检测浓度 根据线性范围的计算,本实验选择了60 μg/mL,在此质量浓度条件下定量测定。
[1]国家食品药品监督管理局.WS3-036(Z-009)-2005(Z)咽清口服液质量标准[S].2005.
[2]张丹雁.广东土牛膝化学成分的初步研究[J].中国民族民间医药杂志,1999,(4):232-234.
[3]国家药典委员会.中华人民共和国药典:2010年版一部[S].北京:中国医药科技出版社,2010.
[4]刘志刚,邓伟杰,孙维峰,等.HPLC测定泄浊除痹方中薯蓣皂苷元、蜕皮甾酮含量[J].中成药,2010,32(2):243-246.
[5]张翠英,梁生旺,张广强.不同产地牛膝中蜕皮甾酮的含量测定[J]. 中国药学杂志,2001,36(10):699-700.
[6]宋闫军,尚聪敏.牛膝及三妙丸中脱皮甾酮的薄层扫描测定[J].河南中医药学刊,2000,15(6):9-10.
[7]张 英,韦 异,粟 晖,等.超声提取反相高效液相色谱法测定牛膝中蜕皮甾酮[J].光谱实验室,2002,19(5):668-671.
[8]李文莉,汪文涛,雷玉萍,等.RP-HPLC测定脉络宁注射液中蜕皮甾酮的含量[J].华西药学杂志,2001,(16):382-383.
[9]刘 姣,周亚球,彭超怀.怀牛膝蜕皮甾酮的含量测定[J].安徽中医学院学报,2005,24(3):43-44.

