光催化降解甲基橙过程的评价方法研究
李伟,侯楚楚,毛子文,朱霞月,张一平
(浙江外国语学院理工学院,浙江杭州310012)
1 引言
染料厂和印染厂排放废水具有成分复杂、色度高、排放量大、毒性大、可生化性差的特点,其中有的还含苯环、胺基、偶氮基团等致癌物质,一直是废水处理中的一个难题.近年来,利用TiO2在染料的光催化降解方面的研究日益增多,并取得了一定的成果[1-8].
然而,已有的研究大多仅以分光光度法测定脱色率为指标来评价光催化反应的活性[9-11],单纯从颜色是否变化来判断是否发生了降解反应.在染料光催化降解中,脱色是初始步骤,染料脱色的完成并不意味整个化合物的完全降解,可能只是染料结构中发色基团的破坏,剩下的仍旧是有机污染物.所以单凭色差来判断是否降解是不科学的.
在染料废水治理和水质监测过程中,更重要的是要说明染料发生的是深度氧化的矿化反应而不仅仅是脱色反应.在染料降解过程中,化学需氧量,即COD(Chemical Oxygen Demand),这个指标值的变化反映了染料被深度氧化的程度.目前COD值的测定大都采用重铬酸钾回流法.这种方法具有测定结果准确、重现性好等优点.也有兼以COD测定结果证明染料发生的是矿化反应的[12-14],但很少在整个过程对比和综合考察脱色率和COD降解率.
本实验以300W汞灯为光源,纳米TiO2为光催化剂,以偶氮染料甲基橙(MO)为目标降解物,在TiO2/UV体系中进行光催化氧化降解,以分光光度法测定染料废水脱色率,以重铬酸钾回流法测定其COD降解率,通过溶液pH值、染料初始浓度和TiO2投加量等因素的变化,综合考察染料脱色率与COD降解率这两个指标,以期更全面准确地判断光催化反应的效率.
2 实验部分
2.1 实验试剂与仪器
试剂:二氧化钛TiO2(德国Degussa P25,其中,BET表面积50±15m2/g;原生粒径21nm;压实密度130g/L;锐钛型与金红石型之比约为80∶20);硫酸亚铁、硫酸亚铁铵、硫酸银、邻菲啰啉、浓硫酸、重铬酸钾、甲基橙,均为分析纯.
仪器:XPA-2型搅拌式光催化反应器;UV-2550型紫外可见分光光度计.
2.2 实验方法
反应在XPA-2型光催化反应器中进行.每次实验向反应器中加入染料甲基橙溶液1000mL及光催化剂TiO2,分别在不同的溶液pH值、染料初始浓度和TiO2投加量下进行光催化降解实验.先将体系在磁力搅拌下暗态吸附1h,以保证反应体系达到吸附/脱附平衡后,打开光源进行光催化反应,并以此时溶液浓度作为反应初始浓度,定时取样,测其脱色率和COD降解率.
2.3 分析方法
2.3.1 脱色率的测定
样品以2000r/min速度离心分离20min,取上层清液,在甲基橙的最大吸收波长464.20nm处,利用UV-2550型紫外可见分光光度计测定反应前后的吸光度,按照以下的公式计算脱色率DCOLOR:DCOLOR%=(A0-A)/A0×100%,式中A0、A分别为反应前后甲基橙溶液吸光度值.
2.3.2 COD降解率的测定
按照标准重铬酸钾法(GB11914-89)进行COD的测定.取适量的甲基橙水样,准确加入10.0mL浓度为0.0250mol/L的重酸钾标准溶液,慢慢加入30mL的硫酸-硫酸银溶液,在电热套上加热回流2h,稍冷后用水冲洗冷凝器壁,加水90mL,等冷却到室温后加1~2滴亚铁灵指示剂,用0.01mol/L的硫酸亚铁铵标准溶液滴定到刚变成红褐色为止,记录消耗的硫酸亚铁铵的标准溶液的用量,同时做空白实验.
计算COD的公式如下:COD(mg/L)=(V0-Vt)×C×8000/V,式中C为硫酸亚铁铵标准溶液的浓度,Vt为水样消耗的硫酸亚铁铵的体积数,V0为空白消耗的硫酸亚铁铵的体积数,V为水样的体积.
COD的降解率DCOD依下式计算:DCOD%=(COD0-COD)/COD0×100%,式中COD0、COD为反应前后计算所得的化学需氧量值.
3 结果与讨论
3.1 光催化反应原理
当用能量等于或大于半导体禁带宽度(3.2eV)的光照射半导体TiO2时,作为光的吸收剂,TiO2产生光生电子-空穴对(e--h+),可诱发其表面吸附的羟基或水氧化生成羟基自由基(·OH).产生的羟基自由基具有很高的氧化电位及很强的得电子能力,能够迅速氧化废水里的有机物,即使难氧化的物质也均能被氧化[15].
3.2 甲基橙的紫外可见光谱图及其标准曲线
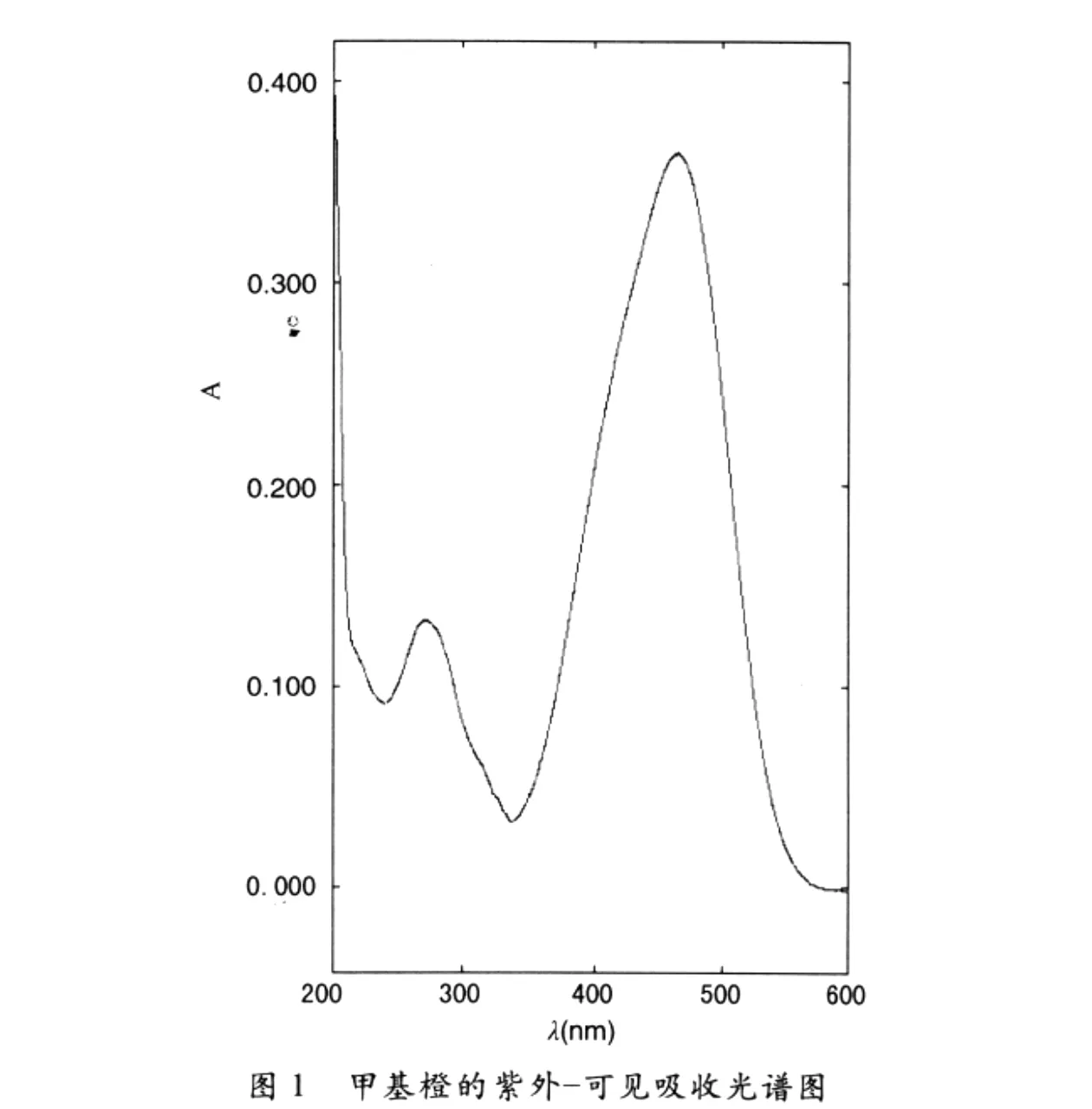
图1是一次典型反应过程中的甲基橙紫外-可见吸收光谱图.可以看到,在200~600nm范围内,甲基橙在464.20nm和273.00nm处出现两个最大吸收峰,分别对应为偶氮结构和苯系物的吸收峰.偶氮键为甲基橙的发色团,因此,我们选择464.20nm为测定波长,在此波长下测定吸光度A,根据朗伯—比尔定律,计算出甲基橙的浓度C.
以464.20nm为测定波长,测定不同浓度的甲基橙标准溶液在此波长下的吸光度A,以吸光度值A为纵坐标,甲基橙标准溶液浓度C为横坐标,作标准曲线图2.从图2可看出,甲基橙溶液浓度C与吸光度值A在测定范围内成线性关系,线性拟合得到标准曲线方程:A=0.0815C+0.0059,线性相关系数R=0.9985.

3.3 自身降解反应中两种分析方法的研究
自身降解反应在无光催化剂、无光源照射条件下进行.
以30mg/L甲基橙溶液进行自身降解反应.表1是在不同反应时间T后甲基橙自身降解反应的脱色率(DCOLOR)和COD降解率(DCOD)数据.
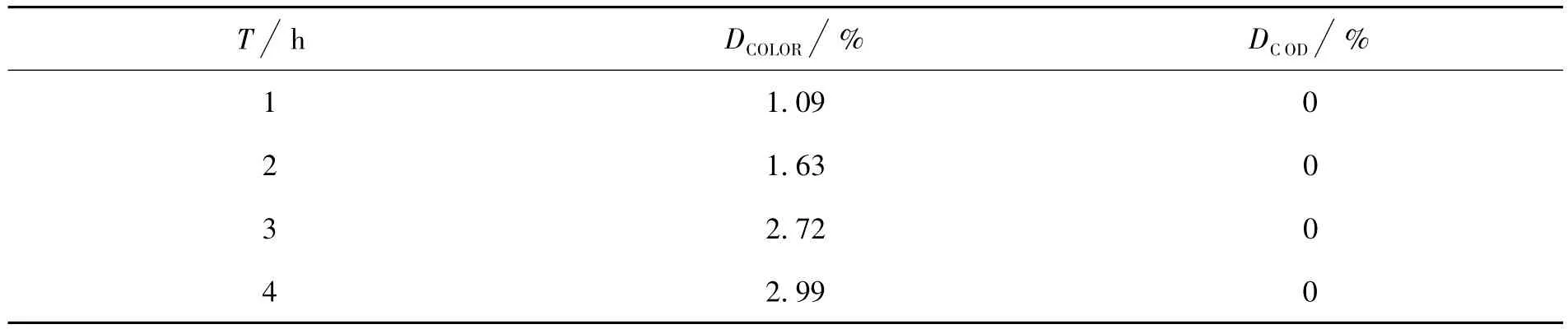
表1 甲基橙自身降解反应的脱色率(DCOLOR)和COD降解率(DCOD)
从上表可以清楚地看到,在无催化剂,无光源情况下,4h后甲基橙的自身降解反应脱色率只有2.99%,而COD降解率为0.说明甲基橙的自身降解可以忽略.
从上表还可以看出,在同一反应时间脱色率的数值高于COD降解率.这是因为在染料光催化降解中,脱色是初始步骤,染料脱色的完成仅表征染料结构中发色基团的破坏,但整个化合物并不一定完全降解,所以脱色比COD降解更容易发生.
3.4 pH值的影响反应中两种分析方法的研究
甲基橙的初始浓度为10mg/L,TiO2为0.5g/L,pH值不同的条件下,先暗态吸附1h,然后进行光催化反应,定时取样,按上述分析方法处理所得溶液.图3、4分别是不同pH值下,在不同反应时间T,甲基橙溶液的脱色率(DCOLOR)和COD降解率(DCOD).
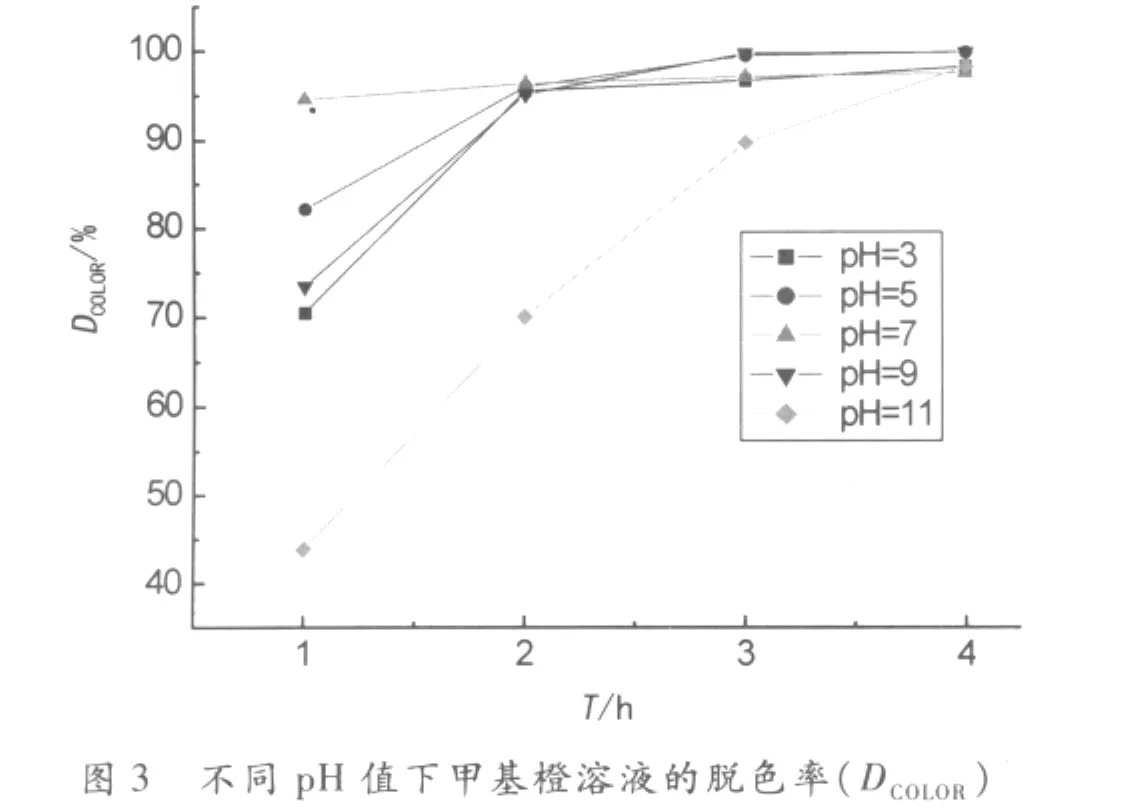
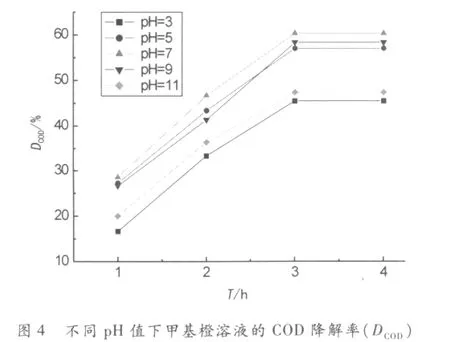
由图3、4可以看出,甲基橙溶液初始pH值对脱色率和COD降解率均影响很大.首先,随着pH值增大,两者均开始是升高,pH=7时最高,然后明显下降,光催化氧化反应的较高速率出现在了中性pH值区.pH值对光降解过程的影响非常复杂,关键在于溶液的pH值直接影响了催化剂表面所带电荷的性质[16-18].pH值较低时,TiO2表面带有正电荷,不利于光生空穴(h+)向催化剂表面迁移,与表面吸附的一些电子供体H2O、OH-等反应产生的羟基自由基(·OH)较少,这样甲基橙的降解反应速率就会降低.pH值较高时,TiO2表面带有负电荷,不利于光生电子(e-)向催化剂表面迁移,与表面吸附的O2反应受到抑制,导致了电子(e-)与空穴(h+)的复合,也使羟基自由基(·OH)的产生减少,从而也不利于甲基橙的降解.综合考虑上述影响因素,pH值过高或过低都不利于甲基橙的光催化降解.
其次,在同一反应时间,仍旧是脱色率的数据高于COD降解率.尤其在反应4h后,无论何种pH值条件下,甲基橙的脱色率均达到98%以上,远高于COD降解率.这更进一步说明脱色反应比深度的COD降解容易发生.如果仅以染料的脱色来评价其降解情况,得到的有机物降解信息并不真实,还必须测定染料的COD以供判断.
3.5 甲基橙初始浓度的影响反应中两种分析方法的研究
甲基橙在自身pH值下,TiO2为1g/L,初始浓度不同的条件下,先暗态吸附应1h,然后进行光催化反应,定时取样,按上述实验方法处理所得溶液.图5、6分别是不同初始浓度下,在不同反应时间T,甲基橙溶液的脱色率(DCOLOR)和COD降解率(DCOD).
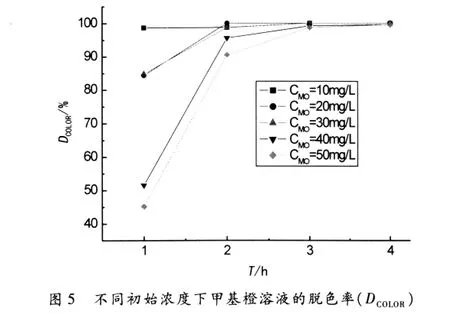
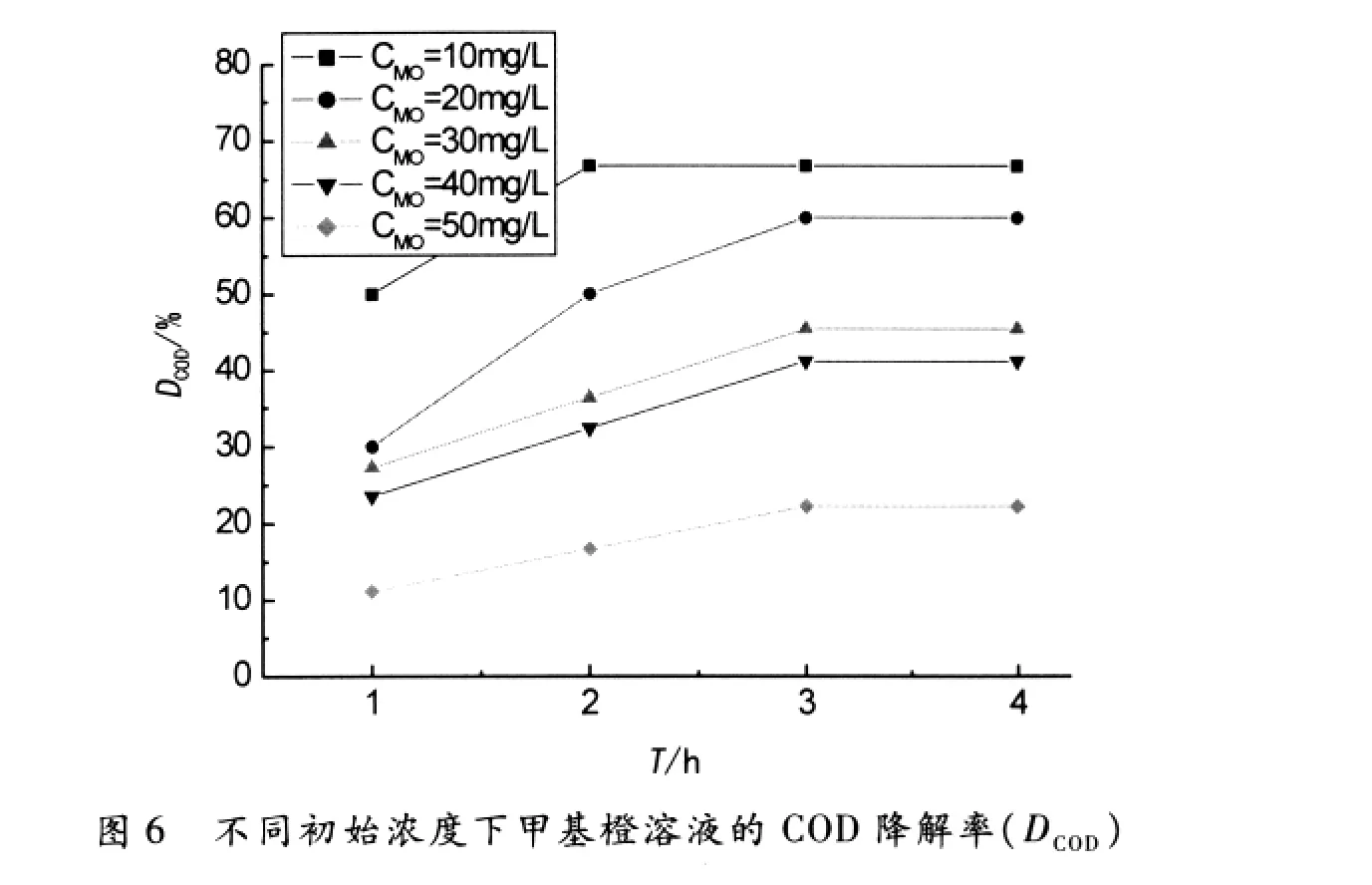
从图5、6可以看出,无论从脱色率分析,还是从COD降解率分析,低的初始甲基橙浓度有利于光降解.这可能是因为,随着初始浓度的增大,被吸附在催化剂表面的甲基橙也不断增加,导致催化剂产生的活性自由基减少;而且初始浓度越高,光穿透溶液的能力越弱,被溶液吸收的光子能量越多,TiO2对光的利用率就越低,从而导致光催化降解效率下降.这也是为什么目前高浓度染料废水难以处理的原因之一.
同时,在同一反应时间,仍旧是脱色率的数据高于COD降解率.尤其在反应4h后,无论在何种初始甲基橙浓度条件下,甲基橙的脱色率均达到98%以上,远高于COD降解率.这再一次说明了脱色反应比深度的COD降解容易发生.
3.6 TiO2投加量的影响反应中两种分析方法的研究
甲基橙初始浓度为30mg/L,在自身的pH值下,催化剂TiO2的投加量不同的条件下,先暗态吸附1h,然后进行光催化反应,定时取样,按上述实验方法处理所得溶液.图7、8分别是TiO2不同投加量下,在不同反应时间T,甲基橙溶液的脱色率(DCOLOR)和COD降解率(DCOD).
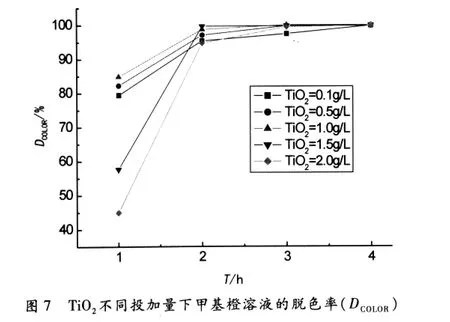
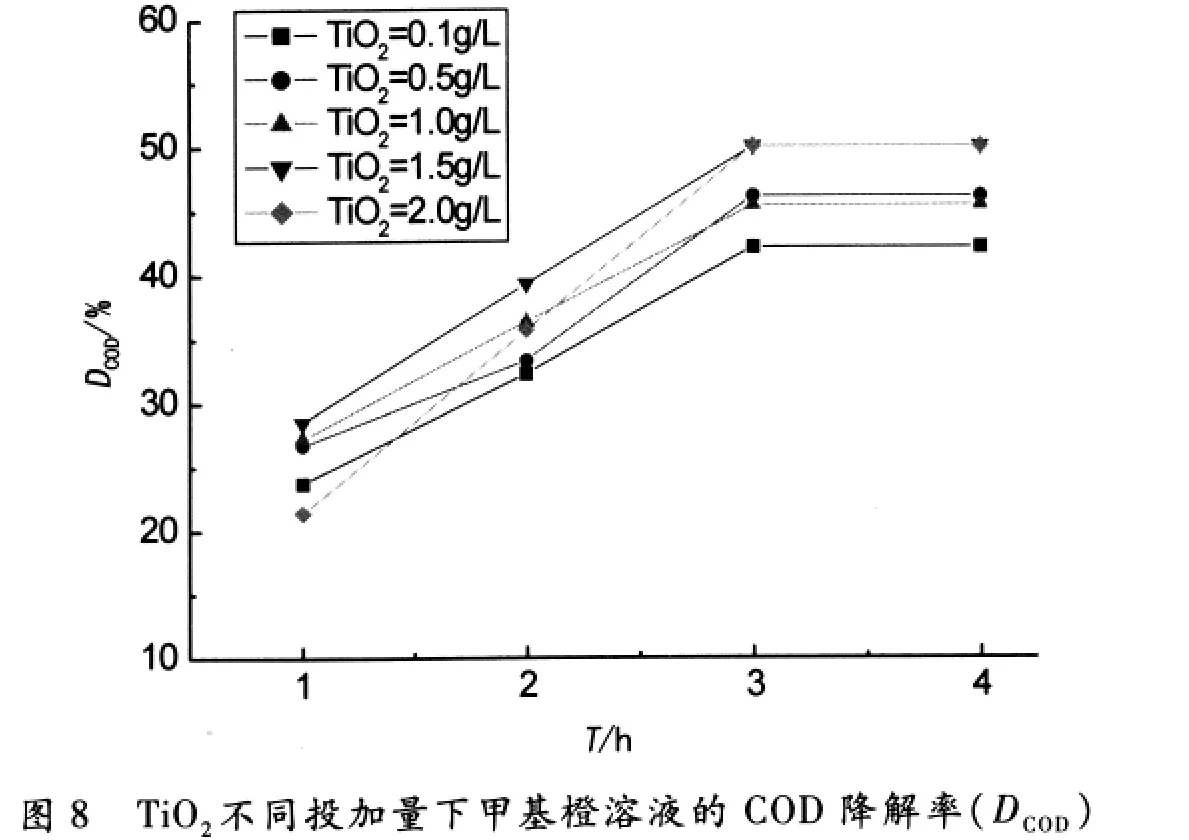
从图7、8可以看出,对于甲基橙降解,TiO2投加量为1.0~1.5g/L时比较适宜.光催化剂用量较少时,光源产生的光子不能被完全转化为化学能,光子能量没有得到充分利用;适当增加催化剂用量,能产生更多的活性物种,提高光催化降解的效率;但催化剂用量增加到一定程度,过多的粒子会产生光散射,使有效光强度减弱,从而影响光的吸收.因此TiO2投加量需在适宜的范围内.
同时,在同一反应时间,仍旧是脱色率的数据高于COD降解率.尤其在反应4h后,无论在何种TiO2投加量条件下,甲基橙的脱色率均达到98%以上,远高于COD降解率.这更进一步说明了脱色反应比深度的COD降解容易发生.
4 结论
染料的降解一般分为两步:染料的脱色和中间产物的降解矿化.在染料的降解研究中,一般都是以染料的脱色来评价其降解情况.而TiO2作为光催化剂的主要优点之一,就是可以将有机污染物彻底矿化为CO2、H2O等无机小分子,实现对环境的有效净化.所以染料的光催化降解还需考察TiO2光催化剂对染料的矿化能力.在本研究中,我们以测定甲基橙溶液的COD来评价光催化剂的矿化能力.
实验结果表明,在染料甲基橙的光催化降解反应中,色度的变化比COD的变化明显.这主要是因为,脱色是降解的初始步骤,染料脱色的完成表征染料结构中发色基团的破坏,但并不意味整个化合物的彻底降解,所以脱色要比COD降解更容易发生.在光催化降解染料的研究工作中,将脱色率、COD降解率等指标的变化综合考虑,将有助于我们更全面准确地判断光催化反应的效率.
[1] Fujishima A,Rao T N,Tryk D A.Titanium dioxide photocatalysis[J].Journal of Photochemistry and Photobiology,C:Photochemistry Reviews,2000(1):1-21.
[2] Wang Y Z.Solar photocatalytic degradation of eight commercial dyes in TiO2suspension[J].Water Research,2000,34(3):990-994.
[3] Fujishima A,Zhang X,Tryk D A.TiO2photocatalysis and related surface phenomena[J].Surface Science Reports,2008,63:515-582.
[4] Sakkas V A,Islam M A,Stalikas C,et al.Photocatalytic degradation using design of experiments:A review and example of the Congo red degradation[J].Journal of Hazardous Materials,2010,175(1-3):33-44.
[5] 唐玉朝,胡春,王怡中.TiO2光催化反应机理及动力学研究进展[J].化学进展,2002,14(3):192-199.
[6] 王学刚,刘金辉.TiO2可见光降解水中污染物的研究进展[J].环境科技,2008,21(6):49-52.
[7] 齐普荣,王光辉.光降解偶氮染料的研究进展[J].染料与染色,2007,44(2):1-4.
[8] 普春燕,任爱玲,赵文霞.提高纳米TiO2光催化活性的研究进展[J].河北工业科技,2009,26(1):65-68.
[9] 传秀云,卢先春,卢先初.负载TiO2的硅藻土对亚甲基蓝的光降解性能研究[J].无机材料学报,2008,23(4):657-661.
[10] 王晓兵,寇玉鹏,梁慧君,等.纳米TiO2光催化降解活性染料研究[J].河南师范大学学报:自然科学版,2008,36(2):70-74.
[11] 邱克辉,邹璇,张佩聪,等.纳米TiO2光催化降解亚甲基蓝[J].矿物岩石,2007,27(4):13-16.
[12] 李静谊,斯琴高娃,刘丽娜.TiO2/膨润土光催化降解有机污染物[J].物理化学学报,2007,23(1):16-20.
[13] 李静谊,刘丽娜,斯琴高娃,等.紫外和可见光照射下金属离子对TiO2/沸石光降解罗丹明B的催化性能影响[J].内蒙古师范大学学报:自然科学汉文版,2008,37(2):219-223.
[14] 路彦景,李向清,穆劲.CuO-NiO助催化剂对TiO2(P25)光催化活性的影响[J].无机化学学报,2009,25(7):1149-1152.
[15] 刘守新,刘鸿.光催化及光电催化基础与应用[M].北京:化学工业出版社,2005:51-52.
[16] Qaradawi S A,Salman R.Photocatalytic degradation of methyl orange as a model compound[J].Journal of Photochemistry and Photobiology A:Chemistry,2002,148(1-3):161-168.
[17] Sivalingam G,Nagaveni K,Hegde M S,et al.Photocatalytic degradation of various dyes by combustion synthesized nano anatase TiO2[J].Appl Catal B:Environ,2003,45(1):23-38.
[18] 方世杰,徐明霞,黄卫友,等.纳米TiO2光催化降解甲基橙[J].硅酸盐学报,2001,29(5):439-442.

