钴掺杂二氧化钛光催化剂制备及光催化活性*
,
(内蒙古科技大学化学与化学工程学院,内蒙古包头 014010)
TiO2的带隙能适中,对污染物的吸附能力强,光催化活性高,具有无毒、稳定、廉价的优点和自洁、除臭、灭菌等功能,因而成为环境污染治理领域的研究热点[1-4]。但是TiO2自身的能隙较宽(3.0~3.2 eV),光谱响应范围较窄,对光的利用率较低(2%~3%),限制了其应用范围。为了提高TiO2的量子效率,可适当增加其表面缺陷以捕获电子使光生电子和空穴分离,降低二者复合的几率,提高其对光能的利用率[5-6]。掺杂是常用的一种改性方法,而掺杂剂的存在形态及含量对光催化剂表面光生电子和空穴的复合影响显著,进而影响其光催化活性。过渡金属离子的适当掺杂能够提高TiO2光催化剂的活性[7-8]。笔者采用溶胶-凝胶法制备了TiO2及钴掺杂的TiO2复合纳米粒子,采用XRD、TEM、UV-Vis等手段对Co/TiO2纳米粒子结构进行表征。并以甲基橙的降解为依据,考察了钴含量、焙烧温度、催化剂的用量等因素对催化降解效率的影响。
1 实验部分
1.1 试剂
钛酸四丁酯、无水乙醇 、冰醋酸、 硝酸钴、甲基橙,均为分析纯;实验用水为二次蒸馏水。
1.2 Co/TiO2 光催化剂的制备
将10 mL钛酸丁酯于剧烈搅拌下滴加到26 mL无水乙醇中,得到浅黄色透明溶液A。将20 mL 无水乙醇、1.05 mL盐酸和1.0 mL 硝酸钴的水溶液混合得溶液B,再把溶液B于剧烈搅拌下滴入溶液A中,持续搅拌至溶液黏度足够大时停止。将所得溶胶用扎有小孔的薄膜封住瓶口,常温常压下放置直到成透明片状干凝胶,研磨成粉末,然后在设定温度的马弗炉中焙烧2 h,即得到所需的粉末样品,其中Co的掺杂量为0~1.2%(物质的量分数,下同)。
1.3 Co/TiO2 光催化剂的表征
采用D/Max-3c X 射线粉末衍射仪对样品进行物相分析,测试条件:Cu 靶Kα衍射,Ni 滤波,电压40 kV,电流40 mA,扫描范围为20~60°,扫描速度为2°/min。紫外漫反射(DRS)用UV-2101型紫外可见分光光度仪测定,BaSO4作参比。
1.4 催化剂活性评价
将一定量的催化剂分散到25 mL质量浓度为12.0 mg/L的甲基橙溶液中,用300 W高压汞灯照射,汞灯与反应溶液之间的距离为15 cm,反应开始后每隔一定时间取样,离心分离除去催化剂颗粒,用U-2000型紫外-可见分光光度计(λmax=464 nm)测定反应溶液的吸光度。根据光照前后溶液吸光度变化, 计算甲基橙的降解率, 并以此来评价催化剂的光催化活性,计算公式为:η=[ (A0-At)/A0]×100 %(η为甲基橙降解率,%;A0为光照前甲基橙溶液的吸光度;At为光照后甲基橙溶液的吸光度)。
2 结果讨论
2.1 Co/TiO2光催化剂的XRD分析
图1是不同Co掺杂量的Co/TiO2样品在600 ℃的XRD谱图。由图1可见,Co/TiO2样品具有良好的结晶度,并且样品都出现了25.3、37.9、47.9、54.1、54.8、62.8°等典型的四方晶系锐钛矿型结构的TiO2特征衍射峰,没有发现其他晶型TiO2的特征衍射峰,随着Co掺杂量的增加(101)峰强度降低,半峰宽变大,说明催化剂的结晶度降低,这是纳米粒子的普遍特征。因为纳米粒子的粒径越小,与原子或分子相差也越小,同时构成微晶的原子数较少,以致不能再近似看成具有无限多晶面的理想晶体,这样无序的晶间结构及晶体中缺陷使点阵间距变化,导致X射线衍射峰变宽。以上结果表明,峰的宽窄与晶粒尺寸有关,粒子越小峰越宽[9]。从图1中看不到明显的钴的特征峰,这可能是:1)钴氧化物可能为非晶态,但由于其含量较少,未能观察到;2)钴元素完全进入TiO2的结构中,均匀地分散在TiO2晶格中,与之形成了固溶体,导致在纳米复合微粒中检测不到钴元素形成晶体结构的XRD 特征峰[10-11]。另外,Co掺杂TiO2粉体中刚出现金红石相,说明Co的掺杂能抑制TiO2晶相转变,同时还提高了相转化温度。

图1 不同Co掺杂量的Co/TiO2样品的XRD谱图
2.2 UV-Vis漫反射
图2为纯TiO2和Co/TiO2催化剂的DRS谱图。由图2可见,掺杂钴后,Co/TiO2粒子对波长大于360 nm 的光的反射率明显降低,样品发生明显的不同程度红移,随着Co掺杂量的增加红移量有所减少,这是因为掺杂离子浓度的增加,能够抑制晶粒的生长,使晶粒细化、能隙变宽所致。从图2还可看出样品对光的吸收能力提高,可吸收波长范围更宽的光,从而提高其光催化活性,这与催化剂的活性评价结果一致。上述结果表明,催化剂的吸光能力与光催化活性之间存在很好的对应关系,催化剂吸光能力越强,光催化活性越高。这是由于在光催化反应中,紫外光作为光源为激发电子产生电子-空穴对提供能量,吸光能力越强,其对光的利用率越高,激发电子产生的电子-空穴对数目越多,相当于增加了光催化氧化还原的活性位,提高了催化剂的活性。

图2 TiO2和Co/TiO2样品的DRS谱图
2.3 光催化活性评价结果
2.3.1 Co掺杂量对甲基橙脱色率的影响
Co掺杂量分别为0.5%、0.7%、1%、1.2% 的TiO2光照一定时间后,降解率变化曲线见图3。从图3可以看出,钴掺杂催化剂的可见光催化性能均高于未掺杂的TiO2。当Co掺杂量为1%时Co/TiO2催化剂的光催化活性最高。这是因为掺杂少量的钴离子会在TiO2晶格中引入捕获阱,使光生电子和空穴得到有效的分离。同时,由于掺杂导致其吸收带边红移,禁带宽度减小,提高了对可见光的利用率,从而提高了光催化活性。由于金属离子既可以捕获电子,又可以捕获空穴,当掺杂量较高时会导致金属离子成为电子和空穴的复合中心,从而降低了催化活性,而且掺杂量过大会使空穴和电子向表面的迁移中遇到更多的捕获,从而降低了量子效率。

图3 Co掺杂量对光催化性能的影响
2.3.2焙烧温度对甲基橙光催化的影响
图4 为x(Co)=1%的Co/TiO2催化剂经不同温度焙烧后对甲基橙的光催化降解曲线。由图4可见,焙烧温度对光催化活性有很大影响。较高的焙烧温度有利于Co/TiO2催化剂的固相反应并形成完整的晶体结构,从而提高其光催化活性。但如果煅烧温度太高,会引起金红石型TiO2大量生成,就会导致催化剂活性降低。因此,实验选择最佳煅烧温度为600 ℃,高于或低于此温度都会引起光催化活性下降。这是由于600 ℃时,样品中同时存在锐钛矿型TiO2和少量金红石型TiO2,这种混晶效应有效地促进了锐钛矿型晶体中光生电子(e-) 和空穴电荷(h+) 的分离,从而提高TiO2的光催化活性[14]。
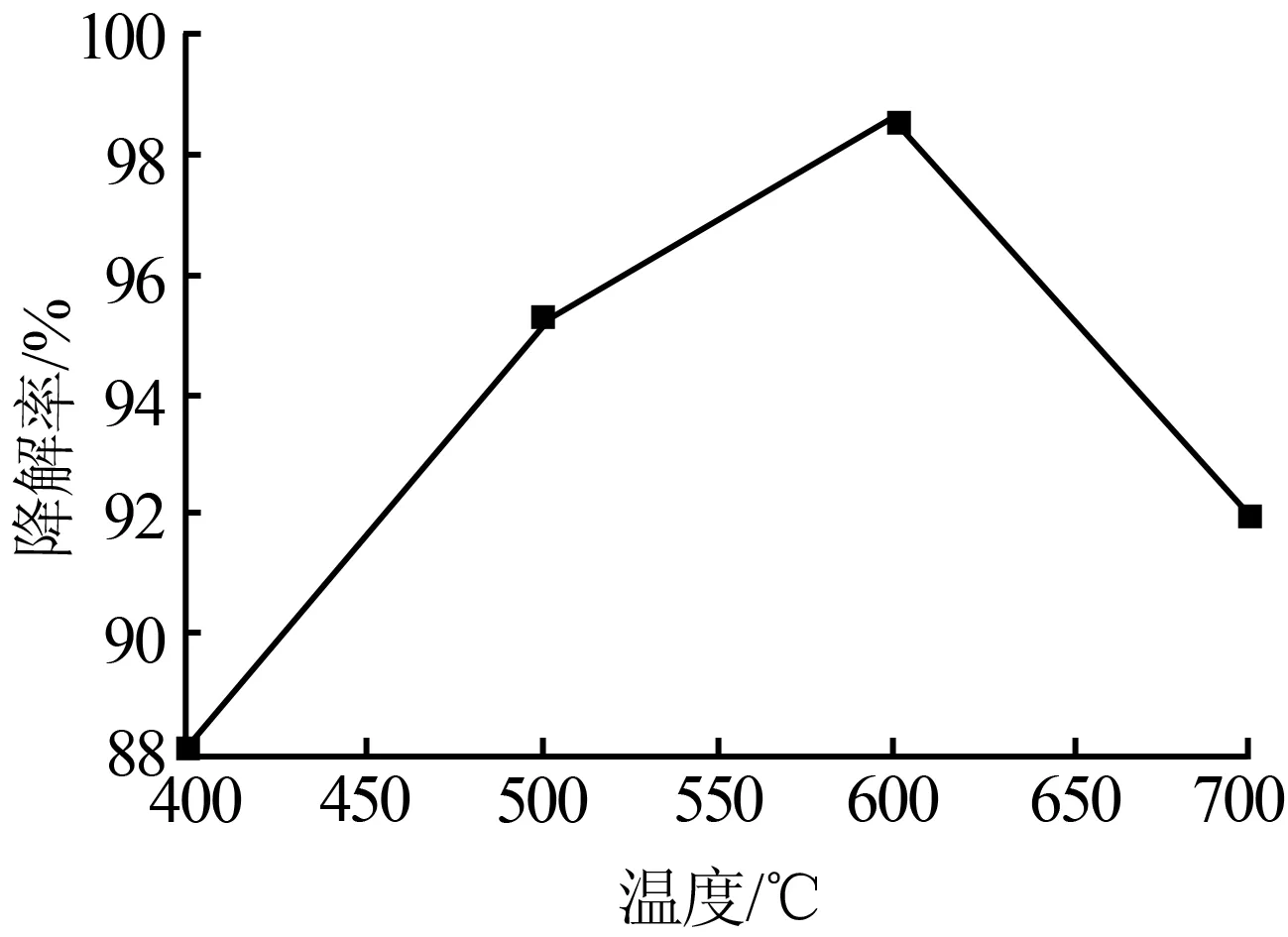
图4 不同温度下Co/TiO2 催化剂对甲基橙的降解率
3 结论
采用溶胶-凝胶法制备了TiO2和Co/TiO2粉末, 低温焙烧时,钴以非晶态化合物存在或与TiO2形成固溶体。焙烧温度对Co/TiO2粉末的微观和宏观性质影响较大,随着焙烧温度的升高,TiO2的结构由锐钛矿型逐步向金红石型转变,Co/TiO2粉末的光催化活性先升高再降低。另外,钴的掺杂对TiO2的各方面性能也有较大影响,掺杂钴以后光谱吸收发生了明显的红移, Co/TiO2光催化剂的可见光响应波长拓宽,掺杂Co以后TiO2粉末的光催化活性均有提高。以降解甲基橙为探针反应,获得最佳催化性能的催化剂中Co与Ti的物质的量比为0.010[即x(Co)=1%],最佳焙烧温度为600 ℃。

[2] Burda C,Lou Y B, Chen X B,et al.Enhanced nitrogen doping in TiO2nanoparticles[J].Nano Lett.,2003,3(8):1049-1051.
[3] Hosseini S N,Borghei S M, Vossoughi M.,et al.Immobilization of TiO2on perlite granules for photocatalytic degradation of phenol[J].Appl.Catal.,B:Environ.,2007, 74(1/2):53-74.

[5] 钟超阳,潘海波,郭龙发,等.四磺基酞菁锌敏化TiO2的原位自组装合成及可见光光催化[J].光谱学与光谱分析,2007,27(11):2329-2332.

[7] Ghorai T K,Biswasa S K,Pramanik P.Photooxidation of different organic dyes (RB, MO,TB,and BG) using Fe(Ⅲ)-doped TiO2nanophotocatalyst prepared by novel chemical method[J].Applied Surface Science,2008,254(22):7498-7504.
[8] Chen R F,Zhang C X,Deng J,et al.Preparation and photocatalytic activity of Cu2+-doped TiO2/SiO2[J]. Materials,2009,16(2):220-225.
[9] 辛柏福,井立强,付宏刚,等.掺杂Cu的TiO2纳米粒子的制备、表征及其光催化活性[J].高等学校化学学报,2004,25(6):1076-1080.
[10] 苏碧桃, 张彰, 郑坚.Fe3+掺杂的TiO2纳米复合粒子的合成及表征[J].化学学报,2002, 60(11):1936-1940.
[11] 谌攀, 曹江林, 冷文华,等.掺钴氧化钛电极的制备、表征及其光电性能[J].化学物理学报,2003,16(4):307-311.
[12] 钱斯文, 王智宇, 王民权.La3+掺杂对纳米TiO2微观结构及光催化性能的影响[J].材料科学与工程,2003,21(1) :48-52.

