干热提高蛋清粉凝胶性过程中美拉德反应的研究
王玉堃 杨严俊
(江南大学食品学院,江苏 无锡 214122)
干热提高蛋清粉凝胶性过程中美拉德反应的研究
王玉堃 杨严俊
(江南大学食品学院,江苏 无锡 214122)
葡萄糖与卵白蛋白在不同的干热条件下进行反应(温度:55,65℃;相对湿度:51.4%、65%、78.9%),研究不同的反应条件下卵白蛋白-葡萄糖(OVA-Glu)反应体系的褐变程度、游离氨基、溶解度及蛋白聚合物变化趋势。OVA-Glu体系在不同的温度与湿度条件下反应4d,对反应后的样品研究发现:样品褐变程度随着时间呈线性升高;温度和湿度对游离氨基数量的影响都非常明显,其总体的变化趋势随时间呈指数关系曲线下降;OVA-Glu反应体系在干热过程中蛋白溶解度明显下降。OVA单体蛋白聚合成二聚体是在反应1d内出现的,随时间延长其数量明显增多,二聚体主要是通过二硫键连接的,温度对提高聚合物的数量起明显的促进作用。
卵白蛋白;美拉德反应;干热条件
蛋清粉以其良好的凝胶性广泛应用于食品加工领域,比如火腿、腊肠、鱼糜制品等生产中的黏结剂;面类的增强剂;食品的防脱水剂[1]。因此,对蛋清粉凝胶性的研究一直是蛋品加工领域的研究热点。Hegg等[2]最早提出了干热法可以显著提高蛋清粉的功能性质。在近些年的研究中,许多文献指出干热过程中引入美拉德反应可以进一步提高蛋清粉的凝胶性与起泡性。Naotoshi Matsudomi等[3-4]在蛋清粉中加入硫酸化葡聚糖(dextran sulfate,DS)进行干热,研究蛋白质-糖复合体系功能性质的变化;同时也研究了半乳甘露聚糖对蛋清粉的改性效果,结果发现:通过美拉德反应对蛋清粉的改性,蛋白的凝胶性、持水性、透明性都有明显提高。但是由美拉德反应的高级阶段产生的蛋白褐变与溶解度降低严重制约着美拉德反应在蛋清粉改性方面的应用。针对这个问题,许多人也做过多方面研究。Kato等[5]研究了还原糖结构上的细微差别会导致褐变程度上的显著差异,同时指出葡萄糖分子中的C-4羟基末端在美拉德反应高级阶段中起着至关重要的作用。Yuanxia Sun[6]等人通过不同结构的还原性单糖对卵白蛋白进行改性,研究不同单糖的分子结构对美拉德高级阶段的影响,并测定卵白蛋白在改性过程中褐变、溶解度及凝胶强度变化。关于还原糖分子结构对卵白蛋白凝胶性的改性效果已经做了很多研究,但是很少有文献报道美拉德反应条件对卵白蛋白凝胶性的影响。本试验通过改变美拉德反应过程中的温度、湿度和时间这几个因素的变化来研究美拉德反应条件对卵白蛋白改性的影响。
1 材料与方法
1.1 材料与仪器
卵白蛋白(OVA):自制,新鲜蛋清经过脱黏工艺[7]去除蛋清中的黏蛋白,脱黏蛋清通过Q-Sepharose FF离子交换层析色谱分离纯化[8],纯度通过12%的SDS-PAGE鉴定;
葡萄糖:国药集团化学试剂有限公司;
Follin-酚试剂盒、三硝基苯磺酸(TNBS):Sigma公司;
层析仪:AKTApurifer,瑞典GE healthcare公司;
高速冷冻离心机:Avanti J-26xp,美国 beckmancoulter公司;
落地式冻干机:BL,美国Labconco公司;
可见分光光度计:UNICO 2000,上海尤尼克仪器有限公司;
紫外可见分光光度计:岛津UV-2450,日本岛津公司。
1.2 试验方法
1.2.1 糖基化卵白蛋白样品制备 在卵白蛋白中加入9%的葡萄糖(按蛋白的干重计),溶于20mM磷酸盐缓冲溶液中(pH 8.0),配制5%的蛋白-葡萄糖混合溶液,溶液混合均匀后冷冻干燥。冻干后的样品平均分成6组,分别在55℃ 和65℃两个温度条件下,以相对湿度51.4%、65%、78.9% 的条件下干热1~4d,以未加葡萄糖的蛋白样品为空白,3个相对湿度分别通过饱和NaBr、饱和KI、饱和KCl来控制。收集到的样品分别用去离子水溶解,透析脱糖,然后再次冻干,冻干后的样品即为糖基化的卵白蛋白(OVAGlu),每份样品等分为3份,分别作为3份平行试验,测定结果取平均值。
1.2.2 蛋白褐变程度的测定 将样品溶解于10mM磷酸盐缓冲溶液(pH 8.0)中,配制成1mg/mL蛋白溶液。用可见分光光度计在420nm下测定其吸光度,利用此吸光度表征其褐变程度。
1.2.3 蛋白溶解度的测定 糖基化蛋白用去离子水配制2mg/mL的溶液,充分溶解后在4℃下以19 900g×15min的条件下冷冻离心。取上清液用Follin-酚法测定蛋白浓度[9],以牛血清白蛋白做标准曲线,用糖基化蛋白与未改性蛋白浓度的百分比来表征蛋白样品的溶解度。
1.2.4 卵白蛋白侧链上游离氨基的测定 通过TNBS法测定不同干热条件下糖基化卵白蛋白游离氨基的变化[10]。1mL的蛋白溶液(0.8mg/mL)中加入1mL 4%的 NaHCO3溶液和1mL 0.1%的TNBS溶液,充分混合后在40℃下保温2h。然后依次加入1mL 10%的SDS溶液,0.5mL 1M的HCl溶液,再用0.01M的HCl溶液稀释1倍,在340nm下读出紫外吸光值,用糖基化蛋白与未改性蛋白吸光值的百分比来表征蛋白样品游离氨基的含量。
1.2.5 凝胶电泳 将蛋白在浓度为12%的聚丙烯酰胺(SDS-PAGE)分离胶中进行非还原电泳层析,然后用考马斯亮蓝染色[11]。在蛋白样品中加入巯基乙醇(2-ME)进行还原电泳层析。
2 结果与讨论
2.1 糖基化卵白蛋白的褐变
2.1.1 蛋白褐变的变化趋势 美拉德反应高级阶段产生的类黑精是引起褐变的主要物质[5],通过对OVA-Glu反应体系褐变程度进行测定,可以对美拉德反应的高级阶段进行初步判断[12]。由图1可知,65℃的干热条件下,褐变随着反应时间而迅速提高,但由于干热第4天后,65℃样品溶解度损失较为严重,对褐变的测定造成较为严重的干扰,所以第4天65℃下样品的褐变值未在图1中列出。在55℃条件下,OVA-Glu体系褐变进行的较为缓慢,这是因为在美拉德反应中较高的温度提供了充足的自由能使酰基化葡萄糖分子内部的化学键发生断裂与重组,经过Amadori分子重排的过程最终生成1-氨基-1-脱氧-2-酮糖,在吸收一定的自由能之后在C-3和C-4之间发生断裂,含有OVA酰基的部分随即进入美拉德反应高级阶段最终生成类黑精,产生褐变[13]。由此可见:在OVA-Glu反应体系中温度是蛋白发生褐变较为关键的因素。从图1中还可以看出:随着相对湿度的提高,OVA-Glu褐变程度也发生一定程度的提高,这是因为美拉德反应一些重要中间产物的形成及转化需要在适当的水分活度条件下完成,因此,较高相对湿度对美拉德反应高级阶段的进行起促进作用。
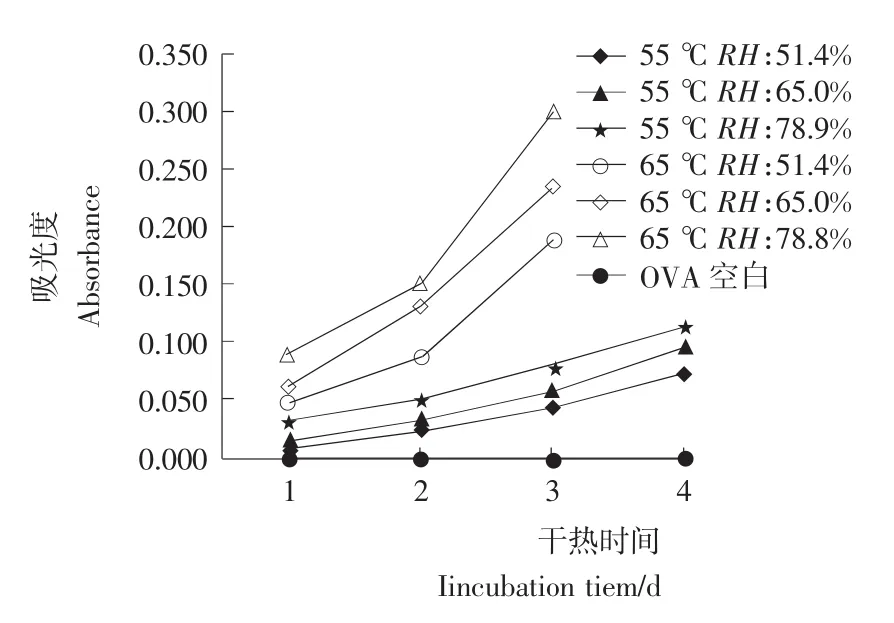
图1 褐变趋势图Figure 1 Brown color development of ovalbumin
2.1.2 蛋白褐变过程中分子结构的变化 Kato等[14]在研究美拉德反应产生褐变过程中提出了Amadori分子重排产物的协同断裂机制,具体变化过程如图2所示。

图2 美拉德初期反应重要中间产物的变化过程Figure 2 Intermediate changes during the primary maillard rection
由图2可以看出:天然的葡萄糖分子与卵白蛋白在干热的条件下,葡萄糖的醛基末端与卵白蛋白游离氨基发生脱水缩合完成了美拉德反应的第一步。酰基化后的OVA-Glu经历了Amadori重排形成了具有典型结构的顺式六元环N-取代1-氨基-1脱氧-2-酮糖中间体。这种结构通过葡萄糖分子上的3-OH、5-OH、C2-酰基和4-OH之间的氢键来稳固(如图2中的c结构),这种结构并不稳定,提高反应体系温度可以有效诱导氢键断裂,顺式六元环状结构被破坏,C3和C4发生断裂产生e和v的分子结构,其中v部分进入美拉德反应高级阶段形成类黑精最终产生褐变,这也可以说明65℃下OVA-Glu体系发生显著褐变现象的原因。
2.2 游离氨基变化趋势及反应条件对其影响
图3为游离氨基变化趋势。由图3可知,在温度为55℃、相对湿度为51.4%的时候,OVA游离氨基变化趋势明显区别于其他干热条件下OVA游离氨基的变化趋势。OVA在温度为55℃、相对湿度为51.4%的干热条件下反应第1天,游离氨基数量在90%以上。在相同温度(55℃)下,反应体系的相对湿度上升到65%,干热1d后游离氨基就已经下降到70%左右;如果在相同的相对湿度下 (RH:51.4%),将反应体系的温度上升为65℃,干热1d后游离氨基即下降到了60%以下。说明温度和湿度对游离氨基的变化都有较大的影响。但是随着干热时间的延长,大多数OVA-Glu反应体系中游离氨基占总氨基的40%左右,只有在温度为55℃、相对湿度为51.4%的干热条件下OVAGlu反应体系游离氨基占总氨基的60%左右。说明低温和低湿对OVA蛋白链的氨基末端酰基化具有一定的抑制作用。
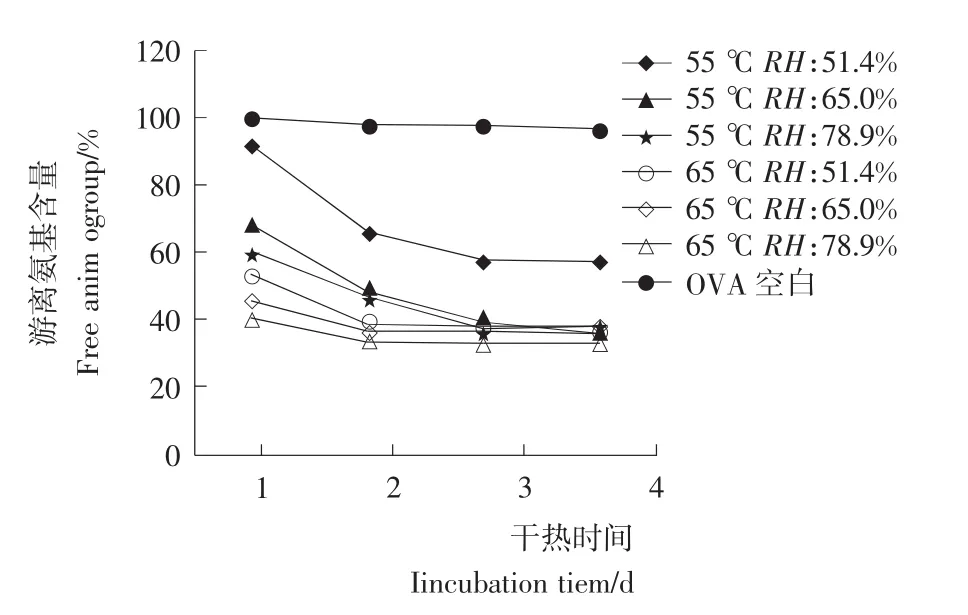
图3 游离氨基变化图Figure 3 Decrease in free amino groups of ovalbumin during incubation
从图3中看出(除去“55℃RH:51.4%”曲线),游离氨基的数量在干热第2天的时候减少至50%以下,在之后的干热过程中下降趋势趋于平缓。这说明美拉德反应的初级阶段(即-NH2末端与-C=O结合至Amadori分子重排产物的生成)在干热反应初期很快完成。卵白蛋白分子中的20个游离氨基与还原糖的醛基末端这种非线性结合趋势可能是由于卵白蛋白分子天然构象或反应过程中轻微的构象变化造成的[15]。从图1中可以看出:OVA褐变是随着干热时间的延长而线性上升的,根据Hodge理论,美拉德反应初级阶段是不发生褐变的[16]。由此可以推断在OVA-Glu反应体系中,美拉德初级和高级反应并不是同步进行的,初级阶段的反应速率是以指数曲线下降,而高级阶段的反应速率是以直线形式保持基本恒定的。
2.3 溶解度变化趋势及反应条件的影响
一般来说,溶解度的变化在一定程度上可以表征蛋白的变性程度。蛋白受热以后,内部的疏水基团暴露于蛋白分子表面,从而导致其溶解度下降[17]。图4显示:未加入葡萄糖的卵白蛋白溶解度下降的趋势极为微弱,因为卵白蛋白的变性温度为84℃[18],远远高于干热处理的设定温度,所以可以推测蛋白分子变性并不是导致溶解度下降的主要原因。在图5(a)的SDS-PAGE中可以看出,加入葡萄糖以后,蛋白在干热过程中容易发生聚合。如图5(a)所示:在温度为65℃、相对湿度为78.9%的干热条件下,分子量小于116.0kDa蛋白单体或低聚物几乎已经不存在,这一现象与Plancken等[19]报道较为吻合,他在文献中指出脱糖蛋清粉样品中的水分含量在4.9%以上时,干热后单体蛋白容易聚合成较大颗粒的聚合物,从而变得难于溶解。这样就可以推断在OVA-Glu体系中大多数糖基化卵白蛋白很可能聚合成为不溶性多聚物。
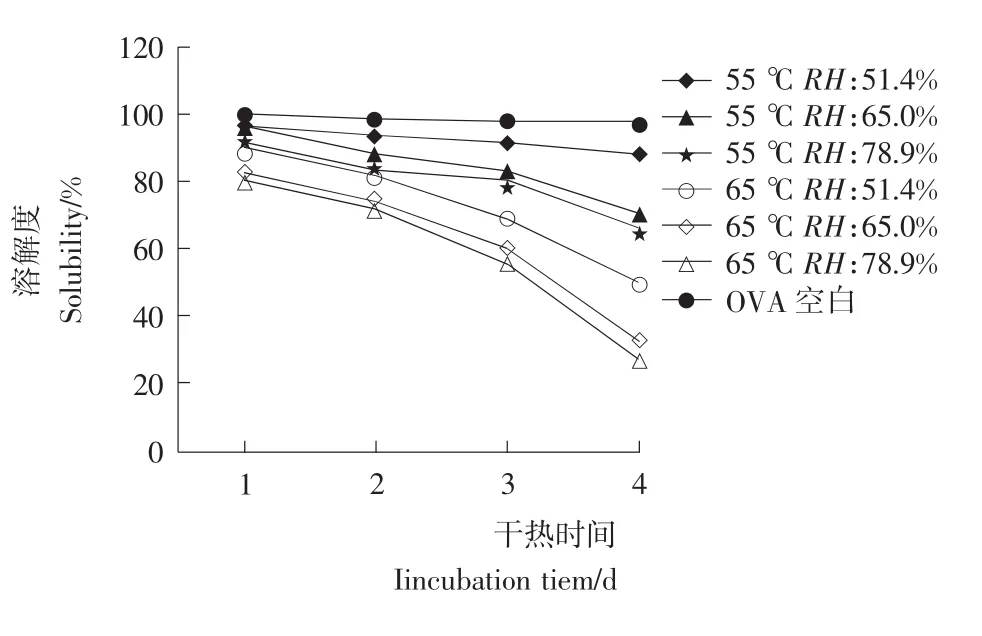
图4 溶解度变化图Figure 4 Solubility of glycated OVA
糖基化蛋白溶解度随着干热时间的延长逐渐降低,在干热2d后,不同湿度条件下的蛋白溶解度都有较为明显的下降。在相对湿度为78.9%的条件下尤为明显,在干热4d后,溶解度下降至原来的40%以下,这可能是水分使蛋白的变性速度和程度加剧,水合凝结导致溶解度下降[19]。
2.4 蛋白聚合变化的趋势及反应条件对该趋势的影响
变性非还原电泳(SDS-PAGE)可用来检测由美拉德反应引起的蛋白聚合情况。可以看出,在1~4d的干热过程中,卵白单体蛋白条带随时间逐渐变浅,这说明卵白单体蛋白的数量在干热过程中逐渐减少,同时也可以发现单体蛋白的条带有轻微的上升。通过两个假设可以解释这种现象:每个卵白蛋白分子链上有20个游离氨基,根据图2所示的游离氨基的数据可以粗略计算出每个蛋白至少连接了10个葡萄糖分子,其相对分子量至少提高了1.8kDa的分子量;卵白蛋白侧链的NH+4被葡萄糖醛基末端酰基化从而导致游离氨基所带的正电荷被屏蔽,使蛋白条带有向高分子方向移动的趋势。
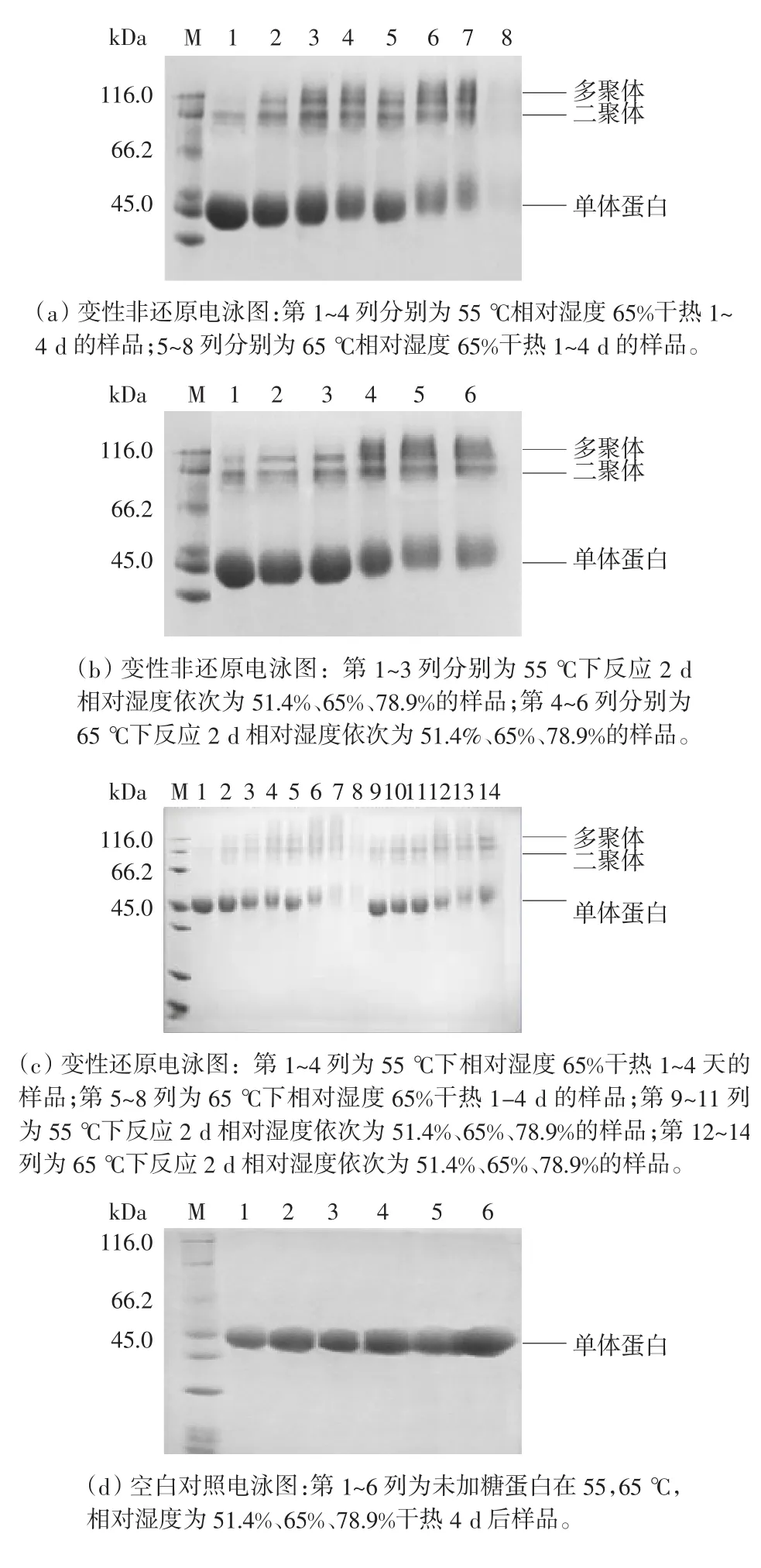
图5 蛋白电泳图Figure 5 Electrophoretic profiles of protein
图5(a)中可以看到,55℃的干热条件下,第1天开始出现卵白蛋白二聚体(分子量大约在88~92kDa之间),干热第2天在分子量约为120kDa处开始出现条带,而且随时间的延长该条带的颜色明显加深,根据条带位置推测其可能是卵白蛋白的三聚体(因为卵白蛋白分子量约为44.5kDa[17])。在图5(b)中对比55℃和65℃两组样品发现:65℃ 条件下聚合物的数量明显比55℃时聚合物的数量多,而单体蛋白在65℃条件下数量明显减少。并且随着反应条件中相对湿度的提高,聚合物的数量也会小幅的提高。这说明在较高温度和湿度的条件下卵白蛋白更容易发生聚合。在图5(c)中看出,样品在巯基乙醇的处理之后,二聚体的条带几乎消失。但是在干热反应的后阶段仍然出现存在少量的二聚体,这说明蛋白交联形成二聚体主要通过二硫键连接,同时也存在少量非共价键连接。每个卵白蛋白分子含有4个巯基,但都包埋于分子内部。从图5(d)中看到,未加入葡萄糖的卵白蛋白样品在干热4d后未出现明显的二聚体条带,这说明反应体系中的葡萄糖分子诱导卵白蛋白分子构象发生变化,使其包埋于内部的游离巯基暴露于表面,从而使分子间的巯基发生相互作用形成二硫键[20]。Mireille Weijers等[21]研究了卵白蛋白聚合物的形态与最终形成的凝胶之间的关系。结果发现卵白蛋白聚合物如果呈线性结构的话,其溶解度良好,加热后会形成透明的、高凝胶强度且有良好持水性的凝胶;相反,卵白蛋白聚合物如果呈团状结构的话,其溶液几乎不可溶,最终难以形成凝胶结构。根据此结论并结合电泳图可初步判断较高的温度和湿度并不利于卵白蛋白形成凝胶。
3 结论
在蛋白褐变过程中温度起主导作用,这是因为在Amadori分子重排产生的顺式六元环N-取代1-氨基-1脱氧-2-酮糖中间体分子共价键与氢键的断裂与重组需要足够的自由能来补给,从而顺利进入美拉德反应的高级阶段。游离氨基数量随干热时间按指数曲线方式下降,干热温度和相对湿度对游离氨基数量的影响都非常明显,在温度及相对湿度较低的条件下(温度55℃;相对湿度51.4%)游离氨基的数量呈较高状态,但在温度大于55℃、相对湿度大于51.4%条件下,干热2d后游离氨基数量下降到50%以下。因此,美拉德反应的初级阶段的反应速率是以指数曲线下降的,而高级阶段的反应速率是以直线形式保持基本恒定的。
未加入葡萄糖的卵白蛋白样品干热后,溶解度几乎没有任何损失,而加入葡萄糖以后,蛋白溶解度明显下降。温度对溶解度损失影响较为明显,这可能是葡萄糖诱导蛋白分子构象发生改变使内部疏水基团暴露于表面或者是葡萄糖诱导单体蛋白聚合成不溶性多聚体而导致的溶解度下降。在葡萄糖存在的条件下,卵白蛋白分子发生一定程度的聚合,OVA单体蛋白聚合成二聚体是在反应1d内出现的,并随时间的延长二聚体数量明显增多,蛋白单体分子之间是通过二硫键形成的二聚体,在聚合过程中温度对聚合物的数量起明显的促进作用。
1 Mine Y.Recent advances in the understanding of egg white protein functionally[J].Trends in Food Science and Technology,1995,6(7):225~231.
2 Hegg P O,Martens H,L9fqvist B.Effects of pH and neutral salts on the formation and quality of thermal aggregates of ovalbumin.A study on thermal aggregation and denaturation[J].J.Sci.Food Agric.,1979,30(10):981~993.
3 Naotoshi Matsudomi,Kaori Nakano,Akiko Soma,et al.Improvement of gel properties of dried egg white by modification with galactomannan through the maillard reaction[J].Journal of Agricultural and Food Chemistry,2002,50(14):4 113~4 118.
4 Naotoshi Matsudomi,Kazuichi Tomonobu,Eiko Moriyoshi,et al.Characteristics of heat-reduced transparent gels from egg white by the addition of dextran sulfate[J].Journal of Agricultural and Food Chemistry,1997,45(3):546~550.
5 Kato Y,Matsuda T,Kato N,et al.Browning and protein polymerization induced by amino-carbonyl reaction of ovalbumin with glucose and lactose[J].J.Agric.Food Chem.,1988,36(4):806~809.
6 Yuanxia Sun,Shigeru Hayakawa,Ken Izumori.Modification of ovalbumin with a rare ketohexose through the maillard reaction:Effect on protein structure and gel properties[J].J.Agric.Food Chem.,2004,52(5):1 293~1 299.
7 Guérin-Dubiard C,Pasco A M,Hietanen B A,et al.Hen egg white fractionation by ion-exchange chromatography[J].Journal of Chromatography A,2005,1 090(1-2):58~67.
8 Thomas Croguennec,Francise Nau,Stéphane Pezennec,et al.Simple rapid procedure for preparation of large quantities of ovalbumin[J].J.Agric.Food Chem.,2000,48(10):4 883~4 889.
9 Lowry O H,Rosebrough N J,Farr A L,et al.Protein measurement with the folin phenol reagent[J].J.Biol.Chem.,1951,193(265):265~275.
10 Haynes R,Osuga D T,Feeney R E.Modification of amino groups in inhibitors of proteolytic enzymes[J].Biochemistry,1967,6(2):541~547.
11 Laemmli U K.Cleavage of structural proteins during the assembly of the head bacteriophage T4[J].Nature,1970,227(259):680~685.
12 Marcus A,Glomb,Vincent M,et al.Reactive intermediates of the maillard reaction[J].The Journal of Biological Chemistry,1995,270(17):10 017~10 026.
13 Yasuko Kato,Tsukasa Matsuda,Natsuki Kato,et al.Browning and protein polymerization induced by amino-carbonyl reaction of ovalbumin with glucose and lactose[J].J.Agric.Food Chem.,1988,36(4):806~809.
14 Yasuko Kato,Tsukasa Matsuda,Natsuki Kato,et al.Browning and insolubilization of ovalbumin by the maillard reaction with some aldohexoses[J].J.Agric.Food Chem.,1986,34(2):351~355.
15 Yasuko Kato,Tsukasa Matsuda,Natsuki Kato,et al.Maillard reaction of disaccharides with protein:Suppressive effect of nonreducing end pyranoside groups on browning and protein polymerization[J].J.Agric.Food Chem.,1989,37(4):1 077~1 081.
16 Hodge J E.Dehydrated foods,chemistry of browning reactions in model systems[J].J.Agric.Food Chem.,1953,1(15):928~943.
17 Ana Cláudia Carraro Alleoni.Albumen protein and functional properties of gelation and foaming[J].Sci.Agric.,2006,63(3):291~298.
18 Powrie W D,Nakai S.Characteristics of edible and fluids of animal origin:Eggs[M].New York:Marcel Dekker,Inc,1985:829~855.
19 Plancken I V,Loey A V,Hendrickx M.Effect of moisture content during dry-heating on selected physicochemical and functional properties of dried egg white[J].J.Agric.Food Chem.,2007,55(1):127~135.
20 Schmidt R H,Cornell J,Illingworth B.Multiple regression and response surface analysis of the effects of calcium chloride and cysteine on heat-induced whey protein gelation[J].Journal of Agriculture and Food Chemistry,1979,27(3):529~532.
21 M ireille Weijers,Kerensa Broersen,O Peter A,et al.Net charge affects morphology and visual properties of ovalbumin aggregates[J].Biomacromolecules,2008,9(11):3 165~3 172.
Study of maillard reaction of dry-heating process for improving gel properties of hen ovalbumin
WANG Yu-kunYANG Yan-jun
(Institute of Food Biochemistry,Southern Yangtze University,Wuxi,Jiangsu,214122,China)
The maillard reaction of ovalbumin (OVA)and gluose(Glu)in several dry-heating conditions (temperature:55 ℃ and 65℃,relative humidity:51.4%,65.0%,78.9%)was investigated by several properties such as extent of browning,loss of free amino groups,solubility and aggregation process.OVA-Glu was incubated in preset conditions for 4d.The extent of browning was linearly increasing with incubation time.Both temperature and relative humidity strongly induced the loss of free amino groups.The number of free amino groups was decrease exponentially with increasing incubation time.Significant loss of solubility was observed during the OVA-Glu incubation.Dimers of OVA molecules appeared within 1dof incubation,and the number of them increased with the increasing incubation time.The main linkage of two OVA monomers which formed a dimer was found to be disulfide bond.And temperature played an important role during the aggregation process.
ovalbumin;maillard reaction;dry-heating condition
10.3969 /j.issn.1003-5788.2010.05.012
王玉堃(1985-),男,江南大学在读研究生。E-mail:bingsu2006@163.com
杨严俊
2010-06-01

