羰基化合物与二卤海因的α-卤代反应
陈梓湛, 管细霞, 郑祖彪, 邹新琢
(华东师范大学 化学系,上海 200062)
羰基化合物与二卤海因的α-卤代反应
陈梓湛, 管细霞, 郑祖彪, 邹新琢
(华东师范大学 化学系,上海 200062)
报道了脂肪(环)酮与1,3-二溴-5,5-二甲基海因(DBDMH)在甲醇中、室温下进行的α-溴代反应,并在此基础上,进一步报道了以脂肪(环)酮、β-酮酯和丙二酸酯为底物,使用1,3-二氯-5,5-二甲基海因(DCDMH)和对甲苯磺酸在乙腈中、室温下进行的α-氯代反应.其中β-酮酯和丙二酸酯以87%~96%的高收率得到α-单氯代反应产物.
α-氯代; α-溴代; 脂肪酮; β-酮酯; 丙二酸酯; 1,3-二氯-5,5-二甲基海因; 1,3-二溴-5,5-二甲基海因
0 引 言
各种脂肪酮、β-酮酯和1,3-丙二酸酯等羰基化合物的α-卤代化合物是医药和农药等精细有机合成化学品的重要中间体[1-3].氯气,SOCl2,SO2Cl2,HCl和液溴等是最常用的廉价卤代试剂,但由于该类试剂的毒性、对设备的腐蚀性、生产和运输上的安全性问题及产生大量酸性废气等原因,其使用日益受到限制.因此,近年来,各种羰基化合物的绿色卤代试剂及其卤代方法,特别是可工业推广的方法研究受到了重视.如N-氯代丁二酰亚胺(NCS)[4,5]、N-溴代丁二酰亚胺(NBS)[6]、MgCl2和 CuCl2等.1,3-二氯-5,5-二甲基海因(DCDMH)和1,3-二溴-5,5-二甲基海因(DBDMH)是一类廉价的新型消毒杀菌剂和漂白剂,已被广泛应用于工业和生活用水的消毒和杀菌.胡艾希等人将其用作卤代试剂[7].本课题组也提出了一类使用DCDMH和DBDMH作为绿色卤代试剂,在温和条件下高收率制备高纯度α-单卤代或者α,α-二卤代苯乙酮的方法[8-10].为了拓展其应用范围,希望能最终将其作为绿色的卤代方法推广到工业生产中,本文对该反应作了进一步的调查和研究,报道了利用DCDMH和DBDMH作为卤代试剂对各种脂肪酮、β-酮酯等羰基化合物的α-氯(溴)代反应(见图1).
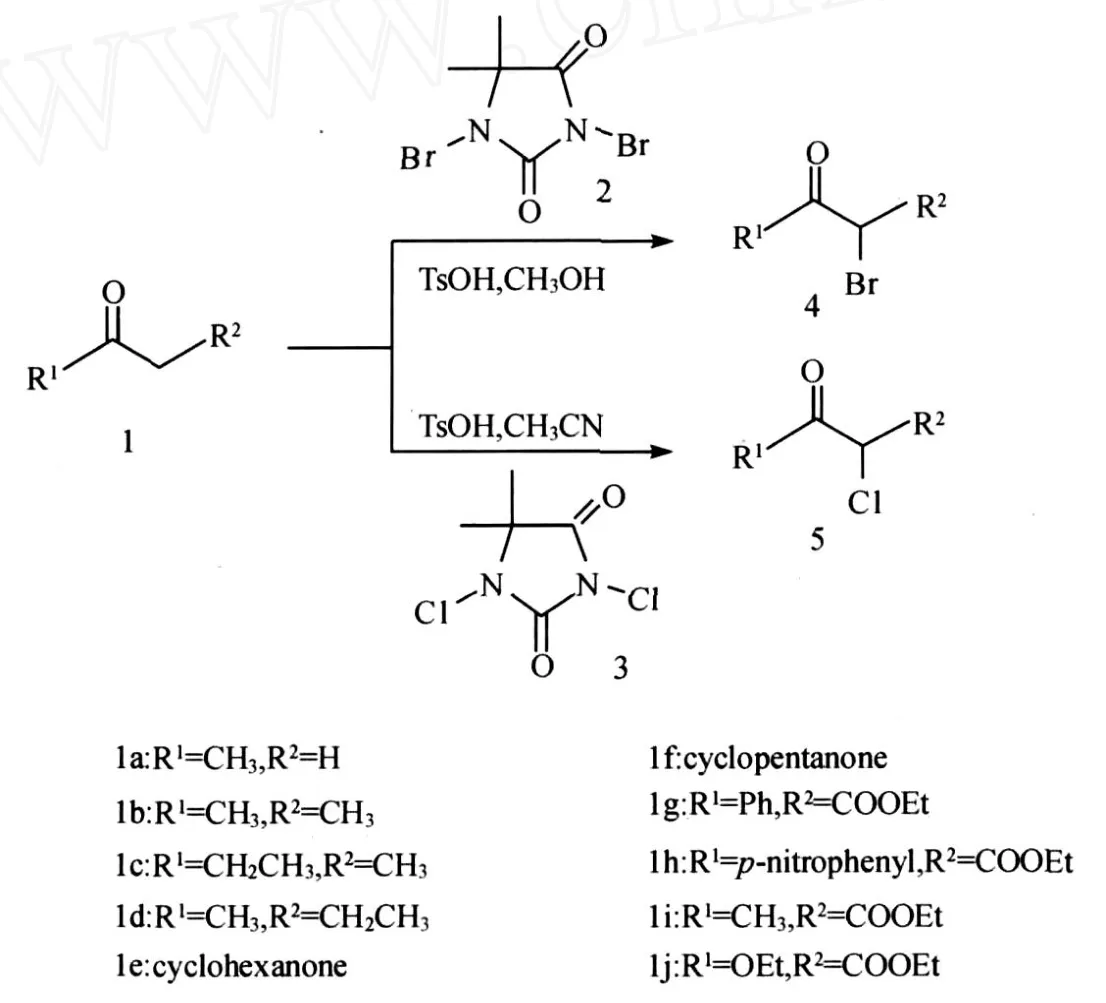
图1 二卤海因与羰基化合物的α-卤代反应Fig.1 α-Halogenationofcarbonylcompoundswith1,3-dihalo-5,5-dimethylhydantoin
1 实验部分
本文中1HNMR由varianINOVA-500型核磁共振仪测定,内标为 TMS;GC为浙江福立分析仪器公司的GC-9750,30m的AC-5毛细管柱,程序升温.一般试剂为市售品,按常规方法进行蒸馏和无水处理.
1.1 典型实验例1
在装有磁力搅拌子,回流冷凝管和恒压滴液漏斗的三颈瓶中加入1.7g(20mmol)3-戊酮(1c)和1.7g(10mmol)对甲苯磺酸,溶于10mL甲醇中,室温下搅拌,滴加含3.1g(11mmol)1,3-二溴-5,5-二甲基海因的甲醇饱和溶液.8h后停止反应,旋转蒸发仪减压蒸除甲醇,残余物加30mL二氯甲烷溶解,再用40mL水分两次洗,有机相用无水硫酸镁干燥,旋除溶剂,得粗产物.粗产物经减压蒸馏,得无色液体 2-溴-3-戊酮(4c)2.7g,收率82%.1HNMR(CDCl3,500MHz)δ:1.11(t,3H,CH3),1.74(d,3H,CH3),2.60,2.86(2dq,1Heach,CH2),4.41(q,1H,CHBr).
其它溴代反应同上操作,其产物数据如下所示.
溴代丙酮(4a) 无色液体,收率70%,1HNMR(500MHz,CDCl3)δ:2.38(s,3H,CH3),3.90(s,2H,CH2Br).
丁酮(1b)的反应产物 无色液体,收率74%,1HNMR(500MHz,CDCl3)1-溴丁酮δ:1.12(t,J=7Hz,3H,CH3),2.69(q,J=7Hz,2H,CH2),3.90(s,2H,CH2Br);3-溴丁酮 (4b)δ:1.55(d,J=7Hz,3H,CH3),2.26(s,3H,CH3CO),4.18(q,J=7Hz,1H,CHBr).
2-戊酮(1d)的反应产物 无色液体,收率82%,1HNMR(500MHz,CDCl3)1-溴-2-戊酮δ:0.95(t,3H,CH3),1.65(m,2H,CH2),2.63(t,2H,CH2),3.88(s,2H,CH2Br);3-溴-2-戊酮 (4d)δ:1.01~1.04(m,3H,CH3),1.85~1.88(m,1H,CH2CH3),1.97~2.01(m,1H,CH2CH3),2.30(s,3H,CH3CO),4.00(t,1H,CHBr).
2-溴代环己酮(4e) 无色液体,收率72%,1HNMR(500MHz,CDCl3)δ:1.85~1.88(m,2H,CH2),1.90~1.94(m,2H,CH2),1.97~2.10(m,2H,CH2CHCl),2.36~2.39(m,2H,CH2CO),4.20~4.23(m,1H,CHBr).
2-溴代环戊酮(4f) 无色液体,收率52%,1HNMR(500MHz,CDCl3)δ:2.08~2.14(m,2H,CH2),2.30~2.39(m,2H,CH2),2.42~2.54(m,2H,CH2),4.00(t,1H,CHBr).
1.2 典型实验例2
在装有磁力搅拌子,回流冷凝管和恒压滴液漏斗的三颈瓶中加入4.8g(20mmol)4′-硝基苯甲酰乙酸乙酯(1h)和1.7g(10mmol)对甲苯磺酸,溶于10mL乙腈中,室温下搅拌,滴加2.2g(11mmol)1,3-二氯-5,5-二甲基海因的乙腈饱和溶液.8h后停止反应,旋转蒸发仪减压蒸除乙腈,残余物加30mL二氯甲烷溶解,再用40mL水分两次洗,有机相用无水硫酸镁干燥,旋除溶剂得无色液体的2-(4′-硝基苯甲酰基)-2-氯乙酸乙酯(5h)5.0g,收率93%.mp:130 ℃.1HNMR(500MHz,CDCl3)δ:1.35(t,J=7Hz,3H,CH3),4.33(q,J=7Hz,2H,CH2),5.83(s,1H,CHCl),7.88(d,J=9Hz,2H,ArH),8.27(d,J=9Hz,2H,ArH).IR(neat):3470,3082,2971,1742,1700,1590,1580,1530,1451,1321,1315,1301,1260,1190,1023,968,886,768,734,666cm-1.MS(m/z):273,271,152,151,124,77,51,47.
其它氯代反应同上操作,其产物数据如下所示.
丙酮(1a)的反应产物 无色液体,1HNMR(500MHz,CDCl3)氯代丙酮 (5a)δ:2.31(s,3H,CH3),4.09(s,2H,CH2);1,3-二氯丙酮 (13%)δ:4.51(s,4H,CH2).
丁酮(1b)的反应产物 无色液体,1HNMR(500MHz,CDCl3)1-氯丁酮δ:1.08(t,J=7Hz,3H,CH3),2.59(q,J=7Hz,2H,CH2),4.05(s,2H,CH2CO);3-氯丁酮(5b)δ:1.57(d,J=7Hz,3H,CH3),2.30(s,3H,CH3CO),4.29(q,J=7Hz,1H,CHCl);1,3-二氯丁酮δ:1.63(d,J=7Hz,3H,CH3),4.42(q,J=6Hz,1H,CHCl),4.63(d,J=7Hz,2H,CH2Cl).
3-戊酮(1c)的反应产物 无色液体,1HNMR(500MHz,CDCl3)2-氯-3-戊酮 (5c)δ:1.08(t,J=8Hz,3H,CH3),1.58(d,3H,CH3CHCl),2.58~2.66(m,1H,CH2CO),2.72~2.80(m,1H,CH2CO),4.30~4.35(q,J=7Hz,1H,CHCl);2,4-二氯-3-戊酮δ:1.62(d,J=7Hz,6H,CH3),4.89(q,J=7Hz,2H,CHCl).
2-戊酮(1d)的反应产物 无色液体,1HNMR(500MHz,CDCl3)1-氯-2-戊酮δ:0.95(t,J=5Hz,3H,CH3),1.64~1.68(m,2H,CH2CH3),2.57(t,J=7Hz,2H,CH2CO),4.07(s,2H,CH2Cl);3-氯-2-戊酮 (5d)δ:1.02~1.05(m,3H,CH3),1.86~1.89(m,1H,CH2CH3),1.98~2.02(m,1H,CH2CH3),2.32(s,3H,CH3CO),4.13(t,J=6Hz,1H,CHCl);1,3-二氯-2-戊酮δ:1.02~1.05(m,3H,CH3),1.64~1.68(m,1H,CH2CH3),1.86~1.89(m,1H,CH2CH3),4.41~4.45(m,3H,CHCl,CH2Cl).
环己酮(1e)的反应产物 无色液体,1HNMR(500MHz,CDCl3)2-氯环己酮 (5e)δ:1.86~1.89(m,2H,CH2),1.91~1.95(m,2H,CH2),1.98~2.11(m,2H,CH2CHCl),2.37~2.40(m,2H,CH2CO),4.37~4.40(m,1H,CHCl);2,6-二氯环己酮δ:1.72~1.75(m,2H,CH2),1.97~2.04(m,2H,CH2),2.06~2.11(m,2H,CH2),2.33~2.36(m,2H,CH2),4.52~4.56(m,1H,CHCl),4.83~4.85(m,1H,CHCl).
环戊酮(1f)的反应产物 无色液体,1HNMR(500MHz,CDCl3)2-氯环戊酮 (5f)δ:2.09~2.15(m,2H,CH2),2.31~2.40(m,2H,CH2),2.43~2.55(m,2H,CH2),4.12(t,J=7Hz,1H,CHCl);2,5-二氯环戊酮δ:1.94~1.99(m,2H,CH2),2.17~2.22(m,2H,CH2),4.26(t,J=6Hz,1H,CHCl),4.26(t,J=6Hz,1H,CHCl),4.30(t,J=6Hz,1H,CHCl).
2-苯甲酰基-2-氯乙酸乙酯(5g) 无色液体,收率95%,1HNMR(500MHz,CDCl3)δ:1.18(t,J=7Hz,3H,CH3),4.30(q,J=7Hz,2H,CH2),5.56(s,1H,CHCl),7.43(t,J=7Hz,2H,ArH),7.57(t,J=7Hz,1H,ArH),7.91(d,J=7Hz,2H,ArH).IR(neat):3468,3068,2986,1764,1694,1598,1580,1467,1451,1370,1305,1264,1184,1023,1000,948,876,822,760,732,686cm-1.MS(m/z):228,226,125,106,105,77,51.
2-乙酰基-2-氯乙酸乙酯(5i) 无色液体,收率96%,1HNMR(500MHz,CDCl3)δ:1.31(t,J=7Hz,3H,CH3),2.38(s,3H,CH3CO),4.30(q,J=7Hz,2H,COOCH2),4.75(s,1H,CHCl).IR(neat):3450,2986,2942,2910,2878,1771,1743,1657,1620,1464,1437,1363,1302,1266,1100,1071,1036,884,850,778cm-1.MS(m/z):166,164,136,124,122,119,118,96,94,76,69,43.
2-乙氧羰基-2-氯乙酸乙酯(5j) 无色液体,收率87%,1HNMR(500MHz,CDCl3)δ:1.33(t,J=7Hz,6H,CH3),4.31(q,J=7Hz,4H,CH2),4.85(s,1H,CHCl).IR(neat):3580,3010,2922,2900,1790,1770,1720,1640,1600,1427,1360,1302,1266,1065,1026,874,820,772cm-1.MS(m/z):196,194,160,152,132,129,113,90,76,62,48.
2 结果与讨论
首先,尝试将本课题组高国锐等已报道的DBDMH-对甲苯磺酸-甲醇反应体系进一步应用到脂肪(环)酮的α-溴代反应中[9],反应在室温下进行8h,经蒸馏纯化得到产物.丙酮、丁酮和3-戊酮等脂肪酮类化合物的一溴代产物产率在52%~82%(见表1).以丙酮(1a),3-戊酮(1c),环己酮(1e)和环戊酮(1f)为底物时,产物经 GC和1HNMR检测,为单一的一溴代物.而以丁酮(1b)和2-戊酮(1d)为底物时,所得产物为1-溴丁酮与3-溴丁酮的混合物,两者比例为3.3∶1.以2-戊酮为底物时,所得产物为1-溴-2-戊酮与3-溴-2-戊酮的混合物,两者比例为2∶1.溴代反应的粗产物中,发现了少量的二溴代物,导致一溴代产物的收率有所下降.丙酮和丁酮的收率偏低,可能是由于这两种底物沸点较低,在反应过程中挥发所致.环己酮(1e)与环戊酮(1f)的收率也偏低,在粗产物的分析中,发现缩酮及半缩酮等副产物,这可能是导致收率降低的重要原因.在3-戊酮(1c)的反应中,若对甲苯磺酸更换成等摩尔量的乙酸或丙二酸等有机弱酸,其他条件相同,则几乎没有检测到产物;当对甲苯磺酸的用量从10mmol减少为5mmol,有48%的3-戊酮(1c)未转化;将二溴海因的用量减少为8mmol,对甲苯磺酸用量仍为10mmol,也有30%的3-戊酮(1c)未转化.
脂肪(环)酮在DCDMH-对甲苯磺酸-甲醇反应体系的α-氯代反应也被进一步进行了考察,其结果和溴代反应类似.除了得到预期的α-氯代反应产物之外,反应也得到了甲醇和脂肪(环)酮羰基的缩合和半缩合副产物.此外,考虑到DCDMH在甲醇中的溶解度较小,反应需要较多的溶剂.为了选择合适的反应溶剂,二氯海因25℃时在乙腈、二氯甲烷、甲醇和水中的溶解度分别被测定为10g/100g,6.7g/100g,3.5g/100g和<1g/100g溶剂.其中二氯海因在乙腈中的溶解度为最大.综合上述因素,DCDMH-对甲苯磺酸-乙腈被选择作为α-氯代反应体系.
考虑到脂肪(环)酮的反应活性比芳香酮高,可能存在多氯代和位置选择性的问题.3-戊酮(1c)被作为底物进行反应条件的优化实验.其结果表明,当3-戊酮∶DCDMH∶对甲苯磺酸的摩尔比等于1∶0.55∶0.5;反应温度为25℃;反应时间为8h时,可以避免生成偏二氯代产物的生成;催化剂的用量从10mmol减少为5mmol,经GC分析,有58%的3-戊酮(1c)未被转化;将二溴海因的用量减少为8mmol时,有36%的3-戊酮(1c)未转化.
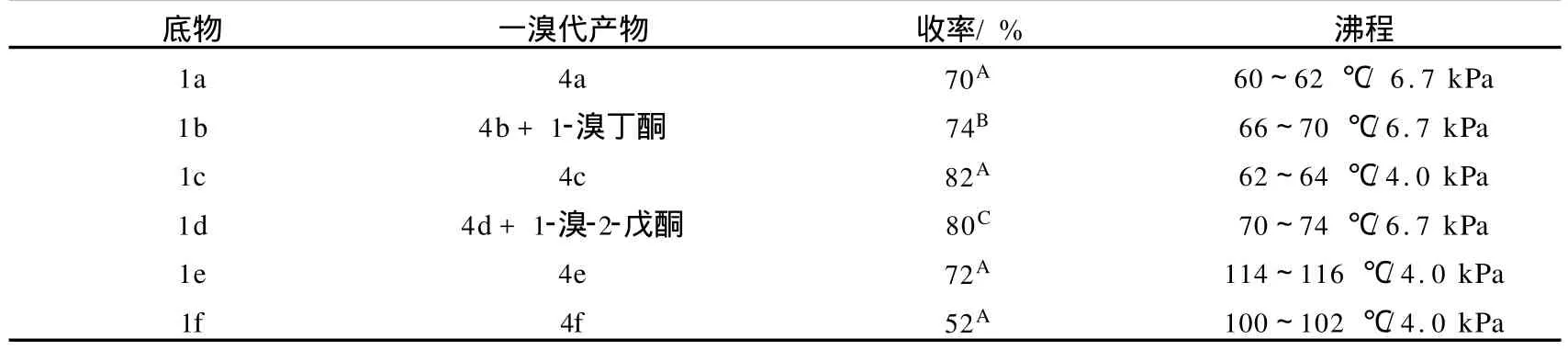
表1 脂肪(环)酮类化合物与二溴海因在甲醇中溴代反应的结果 The result s ofα-bromination of aliphatic ketones with DBDMH in methanol
进一步选择了一些具有代表性的脂肪酮、脂环酮、β-酮酯以及丙二酸酯类化合物按上述条件进行了α-氯代反应,其结果如表2所示.结果表明,DCDMH与脂肪(环)酮反应,可以顺利得到α-氯代产物.溶剂乙腈的使用避免了缩酮化等副反应.GC和1HNMR分析表明,脂肪酮和脂环酮的情况,产物为一氯代物与二氯代物的混合物;通过其比例,折算出收率,一氯代物产率在56%~82%之间.在反应产物中未发现原料酮的存在,同上述溴代反应的情况相类似,丙酮和丁酮的收率也偏低.由于脂肪(环)酮的活泼性,在此反应条件下,主要产物为一氯代产物;在同一α位发生氯代反应产生的偏二氯代产物未明显发现;但发生在两个α位的双氯代产物难以避免.当底物为丁酮(1b)或2-戊酮(1d)时,在溴代反应中,1-溴代物生成的比例更高;而在氯代反应中,3-氯代物生成的比例更高.这可能与溴原子体积较大有关,体积较大的溴原子相对于体积较小的氯原子更倾向于进攻底物中位阻较小的1-位,从而生成更多的1-位卤代物.这一现象也发生在使用单质溴卤化不对称酮的反应中,并已被应用于药物合成中[11].脂环酮的情况,在此反应条件下,明显提高了氯代反应得率,其主要产物为一氯代产物.β-酮酯的反应可以高收率(>93%)得到α-单氯代产物.反应似乎与β-位的取代基无关,无论是苯基(1g)、有强吸电子基的对硝基苯基(1h),还是供电子性的甲基(1i),反应都能顺利进行.有趣的是:DCDMH与1,3-二烷氧羰基化合物的丙二酸二乙酯也可以发生α-氯代反应,产率达87%,但乙酸乙酯的α-氯代反应完全未发生.表明丙二酸酯的α-氯代反应可能是由二个烷氧羰基的累积效应所致.

表2 羰基化合物和DCDMH的α-氯代反应的结果 The result s ofα-chlorination of carbonyl compounds with DCDMH in acetonit rile
3 结 论
各类脂肪(环)酮和β-酮酯等羰基化合物于室温条件下,在二卤海因-对甲苯磺酸催化-甲醇(乙腈)反应体系中能容易地发生α-位卤代反应.使用乙腈作为溶剂可避免了缩酮化等副反应,β-酮酯和丙二酸酯的反应可以高收率地选择性得到α-单氯代产物.与传统的卤代试剂(如氯气等)相比,二卤海因具有高效、低毒、对设备无腐蚀、不污染环境以及副产物的5,5-二甲基海因可以回收再利用等优点,符合绿色化学发展的趋势;而且原料价格便宜,可以代替价格昂贵的NBS或NCS试剂.因此该方法有较好的工业应用前景.
[1] WANG C , TUNGE J . Selenocatalyticα-halogenation [J ] . Chem Commun , 2004 , 23 : 2694-2695.
[2] TANEMURA K, SUZU KI T , NISHIDA Y, et al . A mild and efficient procedure for bromination of ketones usingN-bromosuccinimide catalysed by ammonium acetate [J ] . Chem Commun , 2004 (4) : 470-471.
[3] CHIAPPE C , L EANDRI E , TEBANO M. [ Hmim][NO3]—an efficient solvent and promoter in t he oxidative aromaticchlorination [J ] . Green Chem , 2006 (8) : 742-745.
[4] MELL EGAARD-WAETZIG S R , WANG C , TUNGE J . Selenium-catalyzed oxidative halogenation [J ] . Tet rahedron2006 , 62 (30) : 7191-7198.
[5] MARIGO M , BACHMANN S , HALLAND N , et al . Highly enantioselective direct organocatalyticα-chlorinationof ketones [J ] . Angew Chem Int Ed , 2004 , 43 (41) : 5507-5510.
[6] PRAVST I , ZUPAN M , STAVBER S. Solvent-f ree bromination of 1 ,3-diketones andβ-keto esters wit h NBS[J ] . Green Chem , 2006 (8) : 1001-1005.
[7] 胡艾希,史文革,王先锋,等.氯化铜对芳基烷基酮的选择性氯化反应[J].应用化学,2004,21(2):174-177.
HU A X , SHI W G, WANG X F , et al . Chlorination of arylalkyl ketone wit h cupric ( Ⅱ) chloride in alcohol [J ]Applied Chem , 2004 , 21 (2) : 174-177.
[8] XU ZJ , ZHANGD Y, ZOU X Z. α-Chlorination of acetophenones using 1 ,3-dichloro-5 ,5-dimet hyl-hydantoin[J ] .Synt h Commun , 2006 , 36 (2) : 255-258.
[9] 高国锐,管细霞,邹新琢.一种使用1,3-二溴-5,5-二甲基海因对于苯乙酮类化合物α-溴代的新方法[J].有机化学,2007,27(1):109-111.
GAO G R , GUAN X X , ZOU X Z. A novel met hod forα-bromination of acetophenones using 1 ,3-dibromo-5 ,5-dimet hylhydantoin[J ] . Chinese J Org Chem , 27 (1) : 109-111.
[10] CHEN Z Z , ZHOU B , CAI H H , et al . Simple and efficient met hods for selective preparation ofα-mono orα,α-dichloro ketones andβ-ketoesters by using DCDMH [J ] . Green Chem , 2009 (11) : 275-278.
[11] CARON S , DU GGER R W, RU GGERI S G, et al . Large-scale oxidations in t he pharmaceutical indust ry [J ] .Chem Rev , 2006 , 106 (7) : 2943-2989.
α-Halogenation of carbonyl compounds with1 ,3-dihalo-5 ,5-dimethylhydantoin
CHENZi-zhan, GUANXi-xia, ZHENGZu-biao, ZOUXin-zhuo
(Department of Chemist ry , East China N ormal Universit y , S hanghai 200062 , China)
α-Bromination of aliphatic ketones using 1 ,3-dibromo-5 ,5-dimethylhydantoin (DBDMH) in methanol at room temperature was described. α-Chlorination of aliphatic ketones ,β-keto-esters and malonic ester using 1 ,3-dichloro-5 ,5-dimethylhydantoin (DCDMH) and p-toluenesulfonic acid in acetonit rile at 25 ℃was also reported. β-Keto-esters and dimethyl malonate give α-monochloroproduct s in high yields (87 %~96 %) .
α-chlorination ; α-bromination ; aliphatic ketones ; β-keto-esters and malonic ester; 1 ,3-dichloro-5 ,5- dimethylhydantoin ; 1 ,3-dibromo-5 ,5- dimethylhydantoin
O621.3
A
1000-5641(2010)04-0125-06
2009-09
上海市科委重点项目(073919106)
陈梓湛,男,博士研究生,研究方向为精细有机合成.E-mail:52070606026@ecnu.cn.
邹新琢,男,博士,教授,研究方向为精细有机合成.E-mail:xzzou@chem.ecnu.edu.cn.

