饱和NaCl溶液浸泡下混凝土试块中有机阻锈剂对钢筋腐蚀行为的影响
郑雷刚 杨怀玉
(中国科学院金属研究所,金属腐蚀与防护国家重点实验室,沈阳 110016)
饱和NaCl溶液浸泡下混凝土试块中有机阻锈剂对钢筋腐蚀行为的影响
郑雷刚 杨怀玉*
(中国科学院金属研究所,金属腐蚀与防护国家重点实验室,沈阳 110016)
利用电化学阻抗谱(EIS)、半电池腐蚀电位(Ecorr)和宏观电池腐蚀电流密度(Icorr)测量技术,在饱和NaCl溶液浸泡的硬化混凝土试块中,研究了4种醇胺基阻锈剂对钢筋电极腐蚀电化学行为的影响和长期阻锈性能.在浸泡初始的100 d内,与空白样相比,添加阻锈剂后钢筋电极腐蚀电位升高,阻抗膜值增大,腐蚀电流密度值降低,表明电极表面处于钝态,阻锈剂表现出良好的阻锈性能.随浸泡时间延长,电极腐蚀电位和阻抗膜值下降,腐蚀电流密度增大.浸泡后期,除添加醇胺基CI-4样外,电极电位和腐蚀电流密度与空白样相比无明显差别,表明电极由钝态转变为活性腐蚀状态.但添加CI-4样品,钢筋电极始终保持在钝化状态,阻锈性能最好.基于阻锈剂与Cl-间的竞争吸附,分析探讨了可能的阻锈机理.
阻锈剂;钢筋防护;Cl-诱导的局部腐蚀;电化学技术
混凝土中钢筋的腐蚀是混凝土结构性能退化或破坏的主要原因之一[1-4].通常情况下,混凝土的高碱性环境(pH 12.5-13.5)可使钢筋表面保持钝化状态.但当外界Cl-侵入后(如沿海建筑,跨海大桥及使用除冰盐的公路等场合)将导致钢筋/混凝土界面钝性环境破坏,钢筋表面失钝,并进一步诱发腐蚀,使混凝土结构性能下降甚至失效[2].因此,混凝土中钢筋的防腐已成为亟待解决的技术问题.
有许多措施可用来减缓或阻止钢筋的腐蚀,其中在混凝土浇筑时添加阻锈剂,以其防腐效果好、成本低廉和操作简便等特点,在国内外已受到普遍关注和广泛应用[5].亚硝酸盐是最早被研究的无机混凝土阻锈剂,能显著降低钢筋的活性及腐蚀速率,并已广泛应用于大量钢筋混凝土结构的耐久性保护.但因其为典型的氧化型阻锈剂,在保护钢筋的同时,亚硝酸盐自身不断被消耗,其长期阻锈效果难以保证,用量不足时还可能促进钢筋的腐蚀.另外,亚硝酸盐是有毒物质,在一些欧洲国家,如瑞士和德国已被禁止使用[6].单氟磷酸盐是另一种能够有效降低混凝土中钢筋腐蚀速率的无机阻锈剂,但会降低混凝土的力学性能[7],其应用也受到限制.近年来,有机阻锈剂因其毒性低,环境友好而受到人们的广泛关注,如醇胺类、醛类、炔醇类以及分子中含N、P和S杂环化合物等[8-11].有机阻锈剂可在钢筋表面形成致密吸附膜,从而阻止腐蚀产物及与腐蚀反应的相关物质在钢筋/混凝土界面的自由扩散,达到抑制腐蚀的效果[12].
醇胺基化合物因其无毒、成本低等优点,在国外已受到广泛关注[7-8,10,13-14].然而,文献调研表明,有关该类阻锈剂在实际混凝土体系中的阻锈性能,尤其是长期阻锈效果的研究,仍存在不同的观点,也缺少足够的腐蚀电化学信息去揭示其相关的阻锈机理[8,10-13].本文利用电化学交流阻抗、半电池腐蚀电位及宏观电池腐蚀电流密度测定技术,在饱和NaCl溶液浸泡的硬化混凝土试块中,对4种醇胺基阻锈剂(分别记作CI-1、CI-2、CI-3和CI-4,其主要成份分子结构示于图1)的阻锈性能进行了长期检测.以研究该类化合物在混凝土体系中对钢筋腐蚀电化学行为的影响以及长期阻锈性能,探讨可能的阻锈机理.
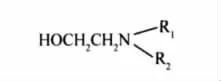
图1 阻锈剂主要成份的分子结构Fig.1 Molecular structure of the main component of corrosion inhibitorR1=R2=CH3for CI-1;R1=R2=H for CI-2;R1=H,R2=C2H4OH for CI-3;R1=R2=C2H4OH for CI-4
1 实验方法
实验用水泥为PS 32.5矿渣硅酸盐水泥,细骨料为河砂,使用前用筛子(筛孔约1.5 mm)过筛.钢筋电极由建筑用普通钢筋加工成Φ7 mm×35 mm的圆柱形,表面依次用SiC砂纸逐级打磨到1000#,一端焊接铜导线,除5.88 cm2的工作面外,其余部分用环氧树脂密封.使用前表面依次用蒸馏水清洗,丙酮除油,冷风吹干后,置于干燥器中备用.辅助电极采用Φ 6 mm×55 mm石墨棒.混凝土试块为40 mm×100 mm×140 mm的长方体,其结构如图2所示.试块制备物料配比(质量比)为蒸馏水∶水泥∶河沙为1∶2∶4,水与水泥用量比为0.5.因各阻锈剂中有效成分的含量不同,为便于比较,阻锈剂添加量均以水泥质量计,分别加入2.0%和4.0%(质量分数),以保证有效成分的一致.试块制备过程参照GB 8076-1997进行,在标准条件下成型,24 h后脱模,在(25±1)℃,相对湿度(RH)≥95%的标准养护箱中养护28 d.
将养护后的混凝土试块侧面浸入饱和NaCl溶液中,每隔一定时间测量一次体系的电极腐蚀电位、宏观电池电流密度和电化学阻抗.阻抗的测量在Parstat 2273(Princeton Applied Research,USA)电化学系统上进行,激励信号为±20 mV正弦波,测量频率范围为100 kHz-10 mHz,所有阻抗测定均在自腐蚀电位下进行.用Fluke 8845A(Fluke Corporation, USA)型数字万用表,依据ASTM-C876标准测定钢筋电极的腐蚀电位,ASTM-G109标准测量钢筋电极的宏观电池电流密度.所有电位均相对于饱和KCl甘汞电极(SCE).所用试剂均为分析纯.
2 结果与讨论
2.1 半电池腐蚀电位和宏观电池腐蚀电流密度测量结果
图3和图4分别为添加不同阻锈剂及空白混凝土试块中钢筋半电池腐蚀电位、宏观电池腐蚀电流密度随浸泡时间的变化结果.通常Ecorr和Icorr可作为判断钢筋腐蚀状况的重要依据.根据Ecorr的高低可将钢筋的腐蚀分为:(a)当Ecorr>-250 mV(vs SCE)时,钢筋具有较低的腐蚀倾向,(b)当Ecorr<-250 mV时,钢筋具有高腐蚀倾向[15].
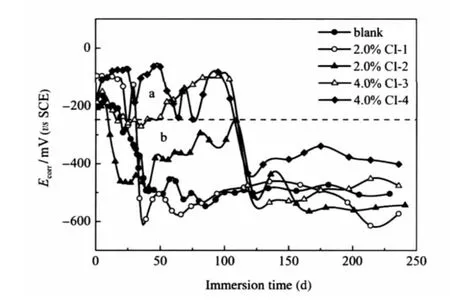
图3 混凝土试块中钢筋电极腐蚀电位随饱和NaCl溶液浸泡时间的变化Fig.3 Variation of the corrosion potential for steel rebar inside mortar specimens immersed in saturated NaCl solution with the immersion timea)region of low corrosion probability,b)region of high corrosion probability;2.0%and 4.0%are mass fractions.
由图3可以看出,在浸泡初期(约10 d),所有混凝土试块中钢筋的电极电位均高于-200 mV,表明钢筋表面在混凝土高碱性环境下处于钝化状态,钢筋处于低腐蚀倾向区.但随浸泡时间的延长,空白、添加CI-1和CI-2的混凝土试块中钢筋的Ecorr快速下降,在接近50 d时已低于-400 mV,而后趋于稳定,表明随着Cl-的渗透,钢筋表面逐渐失去钝化性能而处于活性腐蚀状态,进入高腐蚀倾向区.而添加其它阻锈剂的混凝土试块在浸泡的前100 d内,钢筋电极Ecorr基本保持在-200 mV,表明钢筋表面钝化性能完好,阻锈剂的加入有效维持了钢筋的钝态;但在100 d后,添加CI-3和CI-4试块的钢筋电位开始下降,钢筋电极由钝态转变为活化状态,而后电位趋于稳定,并进入高腐蚀倾向区.电位的这种变化,与外界Cl-的渗透到达钢筋表面后聚集,从而引起钢筋表面发生局部腐蚀密切相关.
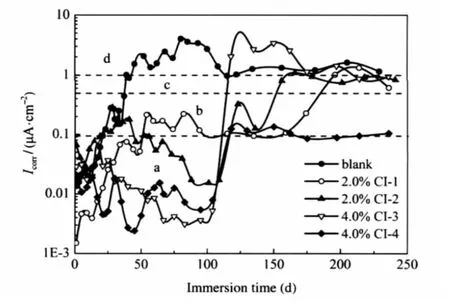
图4 混凝土试块中钢筋电极腐蚀电流密度随饱和NaCl溶液浸泡时间的变化Fig.4 Variation of the macrocell corrosion current density for steel rebar inside mortar specimens immersed in saturated NaCl solution with the immersion timea)passive state,b)low corrosion rate,c)moderate corrosion rate, d)high corrosion rate
钢的局部腐蚀(如点蚀)通常是由表面宏观电池腐蚀(macrocell corrosion)引起的,与微观电池腐蚀(microcell corrosion)相比较,其区别在于宏观电池腐蚀的阴极区和阳极区位置相对固定,而微观电池腐蚀的阴极区和阳极区位置则随时间的变化而随机改变,当电极表面面积相对较小的阳极区被面积相对较大的阴极区所包围时,钢铁就会遭受局部腐蚀[16].碱性混凝土体系中(pH值约12.5),钢筋表面通常处于钝态,然而,在盐水浸泡条件下,水和侵蚀性Cl-可通过混凝土孔隙渗透到其内部并到达钢筋表面,由于混凝土体系的非均匀性,不同部位的渗透、富集程度差别很大.在优先渗透到达部位,Cl-的富集可使钢筋表面钝化膜离子电导增大,保护性降低,钢筋表面将首先发生阳极溶解,生成的铁离子与Cl-形成可溶性化合物(如FeCl2等),而氯化物的水解反过来又促使钢筋表面局部pH值降低,Cl-重新回到阳极区进一步参与腐蚀反应,对局部阳极溶解产生自催化效应,从而导致局部钝性环境破坏,钝化膜受损,发生局部腐蚀.因此,通过测定宏观电池腐蚀电流密度可直观地反映钢筋的腐蚀状况[17-18].根据宏观电池电流密度的大小,可将钢筋腐蚀分为:(a)当Icorr<0.1 μA·cm-2,钢筋处于钝化状态;(b)当Icorr处于0.1-0.5 μA·cm-2内,钢筋存在较低至中等程度的腐蚀;(c)当Icorr在0.5-1.0 μA·cm-2内,钢筋发生中等至较高程度的腐蚀;(d)当Icorr>1.0 μA·cm-2时,钢筋处于高的腐蚀状态(分别标注于图4)[19].由图4可以看出,在浸泡的初期(约25 d),空白试块中钢筋电极电流密度上升很快,在接近50 d时已高于1.0 μA· cm-2,而后随浸泡时间的延长逐步趋于稳定,但其数值始终高于1.0 μA·cm-2.表明钢筋电极表面,在Cl-的侵蚀作用下逐步由钝化状态转变为活性腐蚀状态,约浸泡50 d后进入高腐蚀速率区.而添加阻锈剂的试样,在浸泡的前100 d,钢筋的宏观电池电流密度均小于0.5 μA·cm-2,其中添加CI-3和CI-4时的电流密度始终小于0.1 μA·cm-2,表明此时钢筋电极表面仍处于钝化状态.浸泡100 d后,添加阻锈剂试样的Icorr虽不同程度地增大,但在整个实验周期内,其电流密度大多低于空白试样.尤其是添加CI-4阻锈剂的试样,既使在浸泡236 d时,其Icorr值仍保持在0.1 μA·cm-2左右,远小于空白试样的Icorr.这表明阻锈剂的加入明显抑制了Cl-对钢筋的侵蚀作用,延缓了钢筋开始锈蚀的时间.吸附在钢筋表面的阻锈剂分子可通过阻止Cl-在钝化膜上的吸附而延长局部腐蚀的诱发时间,阻锈剂与Cl-在钢筋表面的吸附是竞争性的[20-21].
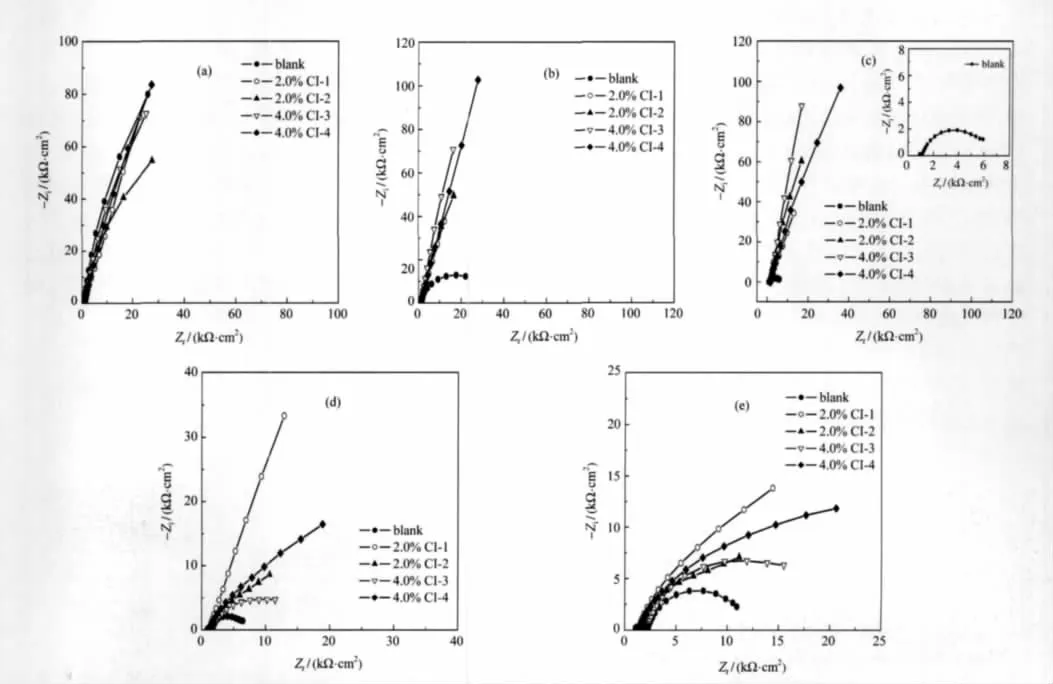
图5 在饱和NaCl溶液中不同浸泡时间下混凝土试块中钢筋电极的阻抗行为Fig.5 Nyquist diagrams for steel rebar electrode inside the mortar specimens immersed in saturated NaCl solution at different time(a)1 d;(b)50 d;(c)100 d;(d)170 d;(e)236 d
另外,由图3和图4结果对比可以发现,Ecorr和Icorr随浸泡时间的变化规律并不完全一致,即电极电位的下降并不一定意味着钢筋腐蚀速率的加快.这是因为钢筋的电极电位不仅受电极表面阴、阳极反应平衡电位的影响,同时还受电极表面电化学活性物种种类、浓度等因素影响,电极电位的变化有时不能完全反映腐蚀速率的变化[5,22].对于处于活性腐蚀状态下的钢筋电极,较低的电极电位值可能是电极表面出现氧浓差极化的结果.因为在钢筋发生腐蚀后,始终处在饱和盐水浸泡下的钢筋电极,周围孔溶液中的溶解氧不断被消耗,而氧的传输又因混凝土层的存在受到阻碍,当氧的传递速度低于阴极还原反应速率时,钢筋电极表面将发生负电荷的积聚,从而造成钢筋电极电位的下降[23].
2.2 交流阻抗结果
图5为添加不同阻锈剂时钢筋电极的阻抗行为随浸泡时间的演化结果.由图5(a)可以看出,在浸泡初始阶段,钢筋电极的阻抗行为均表现出钝化金属所具有的特征,即在阻抗复平面上存在一个半径很大的容抗弧.表明钢筋仍处于钝化状态,电极表面主要受电荷传递过程控制.此时,由于电极表面电荷传递电阻值很大,而界面电容值较小,体系时间常数较大,特征频率低,因此很难测得较为完整的容抗弧.而随着浸泡时间的延长,阻抗行为却发生很大变化.在浸泡50 d后(图5(b)),空白试样电极阻抗中容抗弧半径显著减小,阻抗模值大大降低,表明在Cl-的侵蚀作用下,钢筋表面钝化膜遭到破坏,出现局部腐蚀.电极表面法拉第传递电阻的减小,使腐蚀更易进行[24].而添加阻锈剂混凝土试块的阻抗行为,在100多天的浸泡过程中却变化不大(见图5(a-c)),阻抗值和浸泡初期比较接近,且始终高于空白值.这表明阻锈剂对钢筋的腐蚀具有较好的抑制效果,钢筋开始锈蚀的时间延长.在浸泡100 d后(见图5(d,e)),空白试块的阻抗基本趋于稳定,而添加阻锈剂电极的阻抗虽有所降低,但始终高于空白试块电极的阻抗值.即使在浸泡236 d时,添加阻锈剂时的阻抗值仍大于空白试块,表明阻锈剂具有良好的缓蚀效果.这主要得益于阻锈剂中含有电负性较大的O、N原子极性基团和烷基非极性基团,极性基团吸附于金属表面,从而改变了双电层结构,提高了金属离子化活化能;而非极性基团远离金属表面作定向排布形成疏水层,对参与腐蚀反应相关物种在钢筋界面的扩散起到屏障作用,进而抑制腐蚀的发生[12].
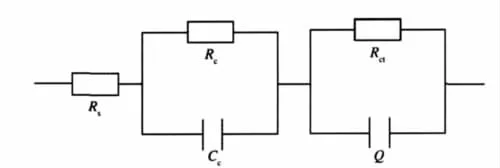
图6 阻抗拟合等效电路图Fig.6 Equivalent circuit model used to fit the EIS experimental dataRsis the resistance of NaCl solution;Rcand Ccare the resistance and capacitance of concrete layer,respectively;Rctis charge transfer resistance;and Q represents constant phase element associated to double layer capacitance(Cdl)on the electrode surface.
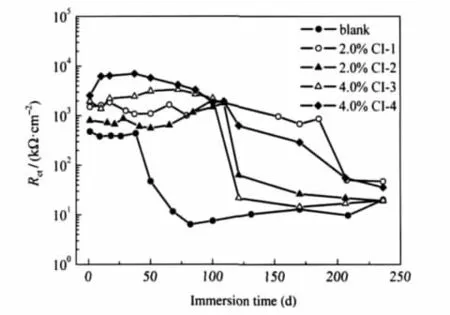
图7 混凝土试块中钢筋电极表面传递电阻随饱和NaCl溶液浸泡时间的变化Fig.7 Evolution of Rctof steel rebar inside the concrete specimens immersed in saturated NaCl solution with variation of immersion time
根据上述分析,钢筋电极的阻抗行为可通过图6所示的等效电路进行拟合.其中,Rs代表溶液电阻,Rc和Cc分别代表混凝土层的电阻和电容,Rct为电极表面腐蚀反应法拉第传递电阻,与电极表面钝化膜内铁的氧化-还原过程相关,Q为钢筋界面双电层的常相位角元件.高频端时间常数与混凝土层的存在直接相关,而中、低频部分容抗弧与钢筋/混凝土界面的双电层相对应[25-26].图7和图8分别为Rct和Cdl随浸泡时间的变化结果.可以看出,在浸泡50 d时,空白试块中电极的Rct值迅速减小并趋于稳定, Cdl大幅增大;而对于添加阻锈剂的混凝土试块,其Rct和Cdl值在浸泡110 d后才发生明显变化,这些结果很好地反映出钢筋表面由钝态向活化腐蚀的转变规律.
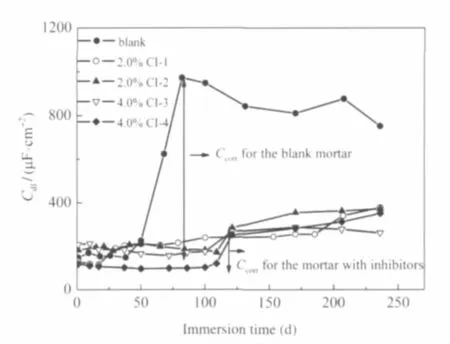
图8 混凝土试块中钢筋电极界面电容随饱和NaCl溶液浸泡时间的变化Fig.8 Evolution of Cdlof steel rebar electrode in the concrete specimens immersed in saturated NaCl solution with variation of immersion time

图9 饱和NaCl溶液浸泡236 d后添加不同阻锈剂混凝土试块中钢筋电极的表面形貌Fig.9 Surface morphologies of steel rebar electrodes inside the concrete specimens after immersion 236 d in saturated NaCl solution with different corrosion inhibitors(a)blank;(b)4.0%CI-3;(c)2.0%CI-1;(d)4.0%CI-4
钢筋周围混凝土孔隙液的化学组成、特性是影响钢筋表面状态的主要因素,其中pH值和Cl-最为重要.外部Cl-通过混凝土毛细孔或微裂纹向钢筋表面迁移,当积聚到一定临界浓度时,将使得钢筋表面失去钝性而诱发局部腐蚀[27-29].研究条件下,由于钢筋界面与浸泡液中Cl-浓度梯度大,侵蚀性Cl-可向钢筋/混凝土界面迅速扩散和渗透,当扩散和渗透达到平衡时,钢筋/混凝土界面Cl-浓度最大,足以促进钢筋表面的去钝化,进而诱发钢筋局部腐蚀的发生,促进腐蚀的进一步发展.这一过程可从空白试样Rct的急剧下降和Cdl迅速升高得到证实.Rct的下降和Cdl升高是钢筋表面局部腐蚀发生的直接结果,这与文献报道结果[29-31]相类似.但对添加阻锈剂的混凝土试块,Rct下降和Cdl值增大却明显滞后.这表明阻锈剂所形成的吸附膜可有效阻止Cl-对钢筋表面的侵蚀,从而减缓钢筋的腐蚀,延迟了钢筋开始锈蚀时间,提高了钢筋对侵蚀性Cl-的容忍度.这与电极腐蚀电位和腐蚀电流检测结果相一致.
2.3 表面形貌观察
图9为添加不同阻锈剂,饱和盐水浸泡236 d后钢筋电极的表面形貌光学照片.可以看出,在空白试样中(图9a),钢筋电极表面已出现严重局部腐蚀(点蚀),粗糙度明显增加.因在空气中放置,表面腐蚀产物已被氧化为棕红色.分别添加CI-3和CI-1阻锈剂的样品(图9(b,c)),经236 d浸泡后,电极表面的局部腐蚀清晰可见,但其锈蚀程度明显弱于空白试样.而添加4.0%CI-4的试样(图9d),电极表面较为均匀,未见明显的局部腐蚀出现.这些结果与电化学测量相一致.
3 结 论
(1)长期电化学研究结果表明,空白混凝土试块在饱和NaCl溶液中浸泡25 d后,钢筋电极表面在Cl-侵蚀下即失去钝性,进而出现局部腐蚀.而添加4种阻锈剂的混凝土试块,在浸泡100 d内,钢筋仍处于钝态,表明阻锈剂可有效减缓Cl-对钢筋的侵蚀作用,延缓钢筋开始锈蚀的时间.
(2)所研究的4种醇胺基阻锈剂均可延长钢筋起始锈蚀时间1倍以上,其中CI-4阻锈剂效果最好.
(3)所得结果为该类阻锈剂的工程应用提供了技术依据和实验支持.
1 Mehta,P.K.;Burrows,R.W.Concr.Int.,2001,23(3):57
2 Soylev,T.A.;Richardson,M.G.Constr.Build.Mater.,2008,22: 609
3 Reou,J.S.;Ann,K.Y.Mater.Chem.Phys.,2008,109:526
4 Ghods,P.;Isgor,O.B.;Mcrae,G.;Miller,T.Cem.Concr.Comp., 2009,31:2
5 Monticelli,C.;Frignani,A.;Trabanelli,G.Cem.Concr.Res., 2000,30:635
6 Jamil,H.E.;Monternor,M.F.;Boulif,R.Electrochim.Acta,2003, 48:3509
7 Söylev,T.A.;McNally,C.;Richardson,M.G.Cem.Concr.Comp., 2007,29:357
8 Mechmech,L.B.;Dhouibi,L.;Ouezdou,M.B.;Triki,E.;Zucchi, F.Cem.Concr.Comp.,2008,30:167
9 Wombacher,F.;Maeder,U.;Marazzani,B.Cem.Concr.Comp., 2004,26:209
10 Ormellese,M.;Lazzari,L.;Goidanich,S.;Fumagalli,G.;Brenna, A.Corrosion Sci.,2009,51:2959
11 Wang,S.X.;Lin,W.W.;Zhang,J.Q.;Fang,Z.K.Journal of Chinese Society for Corrosion and Protection,2000,20:15 [王胜先,林薇薇,张鉴清,方振逵.中国腐蚀与防护学报,2000, 20:15]
12 Elsener,B.;Zurich,E.Corrosion of reinforcement in concrete: mechanisms,monitoring,inhibitors and rehabilitation techniques. 1st ed.Cambridge England:Woodhead Publishing Limited,2007: 170-184
13 Ormellese,M.;Berra,M.;Bolzoni,F.;Pastore,T.Cem.Concr. Res.,2006,36:536
14 Trepanier,S.M.;Hope,B.B.;Hansson,C.M.Cem.Concr.Res., 2001,31:713
15 Fajardo,G.;Valdez,P.;Pacheco,J.Constr.Build.Mater.,2009, 23:768
16 Revie,R.W.Uhlig′s corrosion handbook.2nd ed.Trans.Yang, W.Beijing:Chemical Industry Press,2005:412-415 [Revie,R. W.尤利格腐蚀手册.杨 武译.北京:化学工业出版社,2005: 412-415]
17 Raupach,M.;Schieβl,P.NDT&E International,2001,23:435
18 Saraswathy,V.;Song,H.W.Build.Enviro.,2007,42(1):464
19 Andrade,C.;Alonso,C.Constr.Build.Mater.,1996,10(5):315
20 Aramaki,K.;Tomihara,M.;Furuya,S.;Yamaguchi,M.;Nishihara, H.Corrosion Sci.,1994,36:1133
21 Aramaki,K.;Mizoguchi,M.;Nishihara,H.J.Electrochem.Soc., 1991,138:394
22 Glass,G.K.;Reddy,B.;Buenfeld,N.R.Corrosion Sci.,2000,42 (11):2013
23 Flis,J.;Pickering,H.W.;Osseo-Asare,K.Electrochim.Acta, 1998,43:1921
24 Hu,R.G.;Du,R.G.;Lin,C.J.Electrochemistry,2003,9(2):189 [胡融刚,杜荣归,林昌健.电化学,2003,9(2):189]
25 Sagüés,A.A.;Kranc,S.C.;Moreno,E.I.Corrosion Sci.,1995,37 (7):1097
26 Qiao,G.F.;Ou,J.P.Electrochim.Acta,2007,52:8008
27 Glass,G.K.;Hassanein,A.M.;Buenfeld,N.R.Corrosion,1998, 54(11):887
28 Etteyeb,N.;Dhouibi,L.;Takenouti,H.;Alonso,M.C.;Triki,E. Electrochim.Acta,2007,52:7506
29 Mansfeld,F.Electrochim.Acta,1990,35:1533
30 Valek,L.;Martinez,S.;Mikulic,D.;Brnardic,I.Corrosion Sci., 2008,50:2705
31 Birbilis,N.;Nairn,K.M.;Forsyth,M.Electrochim.Acta,2004, 49:4331
Influence of Organic Inhibitors on the Corrosion Behavior of Steel Rebar inside Mortar Specimens Immersed in Saturated NaCl Solution
ZHENG Lei-Gang YANG Huai-Yu*
(State key Laboratory for Corrosion and Protection,Institute of Metal Research,Chinese Academy of Sciences, Shenyang 110016,P.R.China)
The long-term effects of four kinds of amine-alcohol based inhibitors on the corrosion behavior of steel rebar inside mortar specimens immersed in saturated NaCl solution were studied by electrochemical impendence spectroscopy(EIS),half cell corrosion potential(Ecorr),and macrocell corrosion current density(Icorr)measurements.We found that the Ecorrand the impedance modulus were higher than those in the control specimen after inhibitor addition. Additionally,Icorrdecreased over the initial 100 d of immersion revealing that the steel rebar electrodes are kept in passive state and the inhibitors showed good inhibition effects.With an increase in the immersion time,Ecorrand the impedance modulus for all the inhibited mortar specimens decreased while Icorrincreased.After immersion for 125 d there were no obvious differences between Ecorrand Icorrfor the inhibited systems by comparison to those in the blank sample,except for the specimen containing CI-4.This suggests that the surface of the electrode changes from passive state to active state.The best inhibition was obtained in the presence of the CI-4 inhibitor.We briefly discuss the inhibition mechanism based on the competitive adsorption of the inhibitor molecules with Cl-on the steel rebar surface.
Corrosion inhibitor; Protection of steel rebar; Local corrosion induced by Cl-; Electrochemical technique
O646;TG174
Received:March 29,2010;Revised:May 21,2010;Published on Web:July 8,2010.
*Corresponding author.Email:hyyang@imr.ac.cn;Tel:+86-24-23915899.
The project was supported by the National Key Technology R&D Program,China(2007BAB27B03).
国家科技支撑计划(2007BAB27B03)资助项目
ⒸEditorial office of Acta Physico-Chimica Sinica

