ACo2O4/HZSM-5催化剂上N2O的直接分解
王 虹 王军利 李翠清 宋永吉 迟姚玲 王 焘
(1北京石油化工学院化学工程学院,北京 102617; 2湖南长岭石化科技开发有限公司,湖南长岭 414000)
ACo2O4/HZSM-5催化剂上N2O的直接分解
王 虹1,*王军利2李翠清1,*宋永吉1迟姚玲1王 焘1
(1北京石油化工学院化学工程学院,北京 102617;2湖南长岭石化科技开发有限公司,湖南长岭 414000)
分别采用柠檬酸络合燃烧法和低温络合浸渍法制备尖晶石型复合金属氧化物催化剂ACo2O4(A=Mg,Ni, Zn)和分子筛负载尖晶石型复合金属氧化物催化剂ACo2O4/HZSM-5(A=Mg,Fe,Ni,Cu,Zn,Zr,La).采用X射线衍射(XRD)、氨程序升温脱附(NH3-TPD)、扫描电子显微镜(SEM)和X射线能谱(EDS)等手段对催化剂进行表征,并在固定床微型反应器中评价其催化分解N2O活性.实验结果表明,A位离子种类影响ACo2O4/HZSM-5催化剂活性,以Ni、Fe、Zr或La为A位离子时,催化剂的活性较好,N2O分解温度低.ACo2O4/HZSM-5催化剂的活性高于ACo2O4尖晶石型复合氧化物,一方面是ACo2O4在分子筛HZSM-5载体上高度分散,使其以超细颗粒形态存在,另一方面ACo2O4/HZSM-5催化剂具有适宜的酸性,可提高催化剂的活性.
N2O;尖晶石;分解;HZSM-5
N2O是己二酸生产过程中的重要副产物,每生产1 kg己二酸就排放出0.25 kg的N2O[1].N2O具有很强的温室效应,全球增暖潜能(GWP)是CO2的 310倍[2],在《京都议定书》中,N2O是列于CO2和CH4之后的第三大温室气体,是已知温室气体在大气中存留时间最长的气体,其大气寿命约为120年.
二十世纪70年代,科学工作者开始对N2O催化分解行为进行研究,用于N2O催化分解的催化剂主要有贵金属催化剂[3-5]、稀土氧化物及相关氧化物[6-8]、复合金属氧化物[9-14]、沸石分子筛催化剂[15-17]和水滑石热分解产物催化剂[18-21]等.尖晶石复合氧化物和沸石分子筛催化剂具有较好的N2O分解性能.本文采用低温络合浸渍法将尖晶石复合氧化物负载在分子筛载体上,研究其对N2O的分解催化性能.
1 实验部分
1.1 催化剂制备
实验用化学试剂均为分析纯,由北京益利精细化学品有限公司生产.分子筛HZSM-5由齐鲁石化催化剂厂生产.
采用柠檬酸络合燃烧法制备尖晶石型复合金属氧化物催化剂ACo2O4(A=Mg,Ni,Zn).按化学计量比称取相应金属硝酸盐和络合剂柠檬酸,溶于适量的去离子水中,在不断搅拌下加热混合溶液使其自燃,并伴有爆炸分解,得到类似海绵状、多孔、蓬松的物质,即催化剂前驱体.将催化剂前驱体置于马弗炉中,于800℃焙烧6 h,进行固相反应,得到尖晶石型复合氧化物催化剂.
采用低温络合浸渍法制备分子筛负载尖晶石型复合金属氧化物催化剂ACo2O4/HZSM-5(A=Mg,Fe, Ni,Cu,Zn,Zr,La).按化学计量比称取柠檬酸和相应的金属硝酸盐并溶于去离子水中得到混合溶液,然后将分子筛载体HZSM-5加入到溶液中得到非均相混合溶液.在不断搅拌下加热(温度低于70℃)非均相混合溶液,蒸干水分得到催化剂前驱体,然后将前驱体置于马弗炉中于800℃焙烧6 h进行固相反应,得到ACo2O4/HZSM-5催化剂.以分子筛HZSM-5为基准,ACo2O4的负载量为10%(质量分数,下同).
1.2 催化剂表征
采用日本岛津公司XRD-7000型X射线衍射仪测定催化剂的晶相结构.实验条件为Cu Kα靶,电压40 kV,电流30 mA,扫描步长0.02°,扫描速率4 (°)·min-1,扫描范围为25°-70°.
采用日本日立公司生产的S-4800扫描电子显微镜/X射线能谱仪观察催化剂局部表面特征(颗粒形貌及粒度大小),对催化剂微区成分进行定性和半定量分析.
氨程序升温脱附(NH3-TPD)测试在美国麦克公司生产的CHEMISORB-2750型脉冲化学吸附仪上进行.催化剂为40-60目颗粒,用量为100 mg.样品首先在500℃用He气处理60 min,气体流量为30 mL·min-1,然后冷却至100℃,切入10%NH3/He气体,恒温吸附1 h后,用30 mL·min-1的He气吹扫除去物理吸附的NH3,待基线稳定后,以10℃·min-1的速率升温至800℃,进行脱附,记录NH3脱附曲线.
1.3 催化剂活性评价
采用北京昆仑永泰科技有限公司制造的常压固定床微型反应器评价催化剂分解N2O活性.采用内径为8 mm的石英管反应器,称取20-40目催化剂颗粒0.4 g填充于反应器的恒温段,程序升温速率为4℃·min-1.反应气体组成为N2O,6500 μL·L-1;O2, 0.88%(体积分数);平衡气为N2,气体流量为80 mL· min-1.反应尾气采用SP-3420气相色谱在线检测,使用北京中科慧杰分析科技有限公司生产的Paropak Q色谱柱和热导检测器(TCD)检测反应尾气中剩余的N2O.采用N2O转化率为10%和95%对应的反应温度T10和T95评价催化剂活性,反应温度越低催化剂活性越好.
2 结果分析讨论
2.1 催化剂表征结果
图1是催化剂样品的XRD谱图.与XRD谱库中的标准谱图对比表明,在ACo2O4样品的XRD谱图上分别出现了归属ZnCo2O4(JCPDS 23-1390)、NiCo2O4(JCPDS 73-1702)和 MgCo2O4(JCPDS 81-0671)的尖晶石相结构的特征衍射峰,同时也发现归属CoO(JCPDS78-0431)、NiO(JCPDS 78-0643)和MgO4(JCPDS 27-0759)的特征衍射峰,表明制备的金属复合氧化物主要物相为尖晶石相,但也有杂相生成.
在10%ACo2O4/HZSM-5(A=Mg,Ni,Zn)催化剂样品的XRD谱图上,除HZSM-5的特征衍射峰外,也出现归属尖晶石相的特征衍射峰,表明金属氧化物在载体上以尖晶石结构存在,形成了分子筛负载尖晶石型复合金属氧化物催化剂.

图2是ACo2O4和ACo2O4/HZSM-5催化剂的SEM照片,从图2(A-C)可以看出,A位离子不同, ACo2O4样品的颗粒大小及形貌存在差别.MgCo2O4样品颗粒细小、均匀,颗粒间存在粘结现象,但与其他两个样品相比,颗粒的堆积相对较松散,有助于催化反应的进行;NiCo2O4样品颗粒较大,且不均匀,颗粒间存在严重的粘结现象,不利于催化反应进行; ZnCo2O4样品颗粒大小及堆积情况介于两者之间.图2(D-F)是ACo2O4/HZSM-5样品的SEM照片,与HZSM-5载体的SEM照片(图2G)对比可以看出, ACo2O4分散于HZSM-5载体表面,且颗粒细小、蓬松.A位离子不同,ACo2O4在载体上的分布形态存在很大差异.A位离子为Mg或Ni时,即MgCo2O4或NiCo2O4在载体上分布较均匀,且晶粒为超细颗粒;A位离子为Zn时,即ZnCo2O4在载体表面上虽然也以超细颗粒存在,但颗粒聚集现象严重,导致活性组分与反应物的有效接触面积减小,不利于催化反应进行.值得强调的是,与ACo2O4样品相比, HZSM-5表面负载的ACo2O4晶粒尺寸远远小于ACo2O4样品的晶粒,属于超细颗粒.超细颗粒具有高比表面积、高表面原子比例、高表面能等特性,从而可以显著提高催化剂的活性,这一点在催化剂活性评价中已得到证实.
图3和表1是催化剂微区的能谱分析结果.通过对载体表面负载活性组分的微区进行能谱分析,检测到钴和镁或锌元素,说明载体表面的附着物为钴镁或钴锌的氧化物,半定量结果显示(见表1)钴与镁或锌的摩尔比分别为1.97和1.95,与尖晶石结构中A位和B位金属的理论比值相近,再一次证明该物质具有尖晶石结构,与XRD表征结果一致.
图4是催化剂样品的NH3-TPD曲线,在低温和高温处有两个NH3脱附峰,分别对应催化剂的弱酸位和强酸位.与HZSM-5样品比较发现,HZSM-5负载尖晶石型复合氧化物后,样品的弱酸位和强酸位发生移动,弱酸位脱附峰向低温方向移动(CuCo2O4/ HZSM-5样品除外),强酸位脱附峰均向高温方向移动,从催化剂样品的NH3-TPD曲线的峰面积来看,弱酸量和强酸量均不同程度减少,见表2,说明活性组分和载体之间存在某种相互作用,活性组分起到了调变催化剂酸性中心的作用,导致催化剂酸性及酸量的变化.
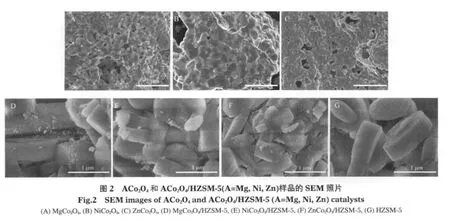


表1ACo2O4/HZSM-5(A=Mg,Zn)催化剂的活性组分组成Table 1 Amount of active components of ACo2O4/HZSM-5(A=Mg,Zn)catalysts
催化剂的NH3-TPD表征结果显示,活性组分组成,即尖晶石型复合金属氧化物中A位离子种类,影响催化剂的酸强度及酸量.与HZSM-5载体相比, A位离子为Cu,即CuCo2O4/HZSM-5催化剂的弱酸性和弱酸量无明显改变,而强酸强度增强,强酸峰位为513℃,但强酸量减少,为0.37 mmol·g-1,弱酸量与强酸量比值为2.92;A位离子为Mg、Fe或Ni,即MgCo2O4/HZSM-5、FeCo2O4/HZSM-5和NiCo2O4/ HZSM-5催化剂,弱酸量和强酸量均减少(见表2),其比值为1.96、2.16和2.26,但FeCo2O4/HZSM-5和NiCo2O4/HZSM-5催化剂的强酸强度强,其峰位分别为549和541℃,而MgCo2O4/HZSM-5催化剂的强酸强度弱,峰位为481℃.由此可见,A位离子种类既影响催化剂的酸性,也影响催化剂的酸量,从而影响催化剂的活性.

2.2 催化剂活性评价结果
2.2.1 ACo2O4与ACo2O4/HZSM-5催化活性对比
图5是ACo2O4或ACo2O4/HZSM-5催化剂上N2O分解温度与转化率的关系曲线.由图5看到,尖晶石型复合氧化物ACo2O4具有催化分解N2O性能, A位离子不同,催化剂活性存在差异,从SEM表征结果来看,ACo2O4样品的催化活性与样品颗粒尺寸及分散状态有关.其中MgCo2O4复合氧化物颗粒细小、均匀,催化分解N2O性能较好,N2O分解温度低, T95为546℃;而NiCo2O4复合氧化物颗粒较大、不均匀,且颗粒间接触非常紧密,催化分解N2O性能差,N2O分解温度高,反应温度达到650℃时,N2O只分解88%.
由图5还看到,将ACo2O4复合氧化物负载在HZSM-5载体上,催化剂性能得到明显改善,N2O分解温度大幅度降低,NiCo2O4/HZSM-5与NiCo2O4相比,T10降低42℃,为347℃,T95降低幅度大于170℃,为472℃;MgCo2O4/HZSM-5和ZnCo2O4/HZSM-5样品与MgCo2O4和ZnCo2O4样品相比,T10分别降低54和47℃,为373和370℃,T95分别降低41和84℃,为505和508℃.HZSM-5担载ACo2O4催化剂具有高N2O分解活性的可能原因有两点:(1)分子筛HZSM-5具有大比表面积和规则孔道,活性组分以超细颗粒分散在载体表面,增加活性组分与反应物的有效接触面积,超细颗粒高表面能促进活性组分与反应物接触与作用;(2)利用了HZSM-5载体的酸性,担载在分子筛载体上的活性组分ACo2O4,既提供了活性位,又与载体相互作用,改变了载体本身的酸性,为催化反应提供了适宜的酸性(见图4),促进催化反应进行.
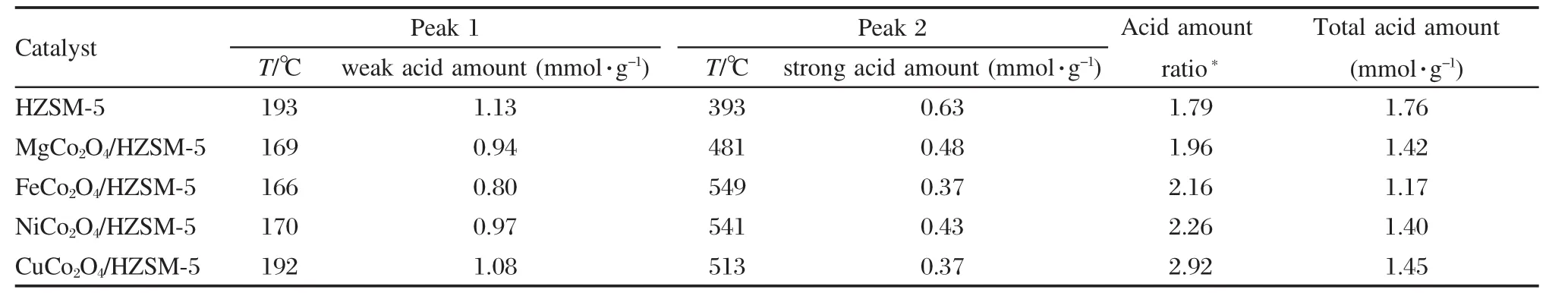
表2 ACo2O4/HZSM-5催化剂的酸强度及酸量分布Table 2 Acid strength and acid distribution of ACo2O4/HZSM-5 catalysts

2.2.2 A位离子对ACo2O4/HZSM-5催化剂活性的影响

图6给出了ACo2O4/HZSM-5催化剂上N2O分解温度与转化率的关系,A位离子不同,催化剂的活性亦不同.由图6看出,催化剂活性大致可以分为三组:A位离子为Ni、Fe、Zr、La时,催化剂的活性较好,分解温度也较低,在整个反应过程中,表现出良好的催化活性,T10为343-353℃,T95为464-473℃,其中以Fe或La为A位离子,催化剂活性好;以Zn或Mg为A位离子时,催化剂活性较差,N2O分解温度升高,T10为370-373℃,T95为505-508℃;以Cu为A位离子,催化剂活性最差,N2O分解温度高,T10为424℃,T95为575℃.A位离子不同,导致ACo2O4在载体表面的分散状况不同,催化剂酸性不同,最终影响到催化剂活性.
由NH3-TPD表征结果(见图4)看到,CuCo2O4/ HZSM-5催化剂的弱酸和强酸均较强,峰温分别为192和513℃,弱酸量与强酸量比值高,为2.92,该催化剂活性差;MgCo2O4/HZSM-5、FeCo2O4/HZSM-5和NiCo2O4/HZSM-5催化剂的弱酸性和弱酸量相近,但FeCo2O4/HZSM-5和NiCo2O4/HZSM-5催化剂的强酸强度强,峰温为549和541℃,弱酸量与强酸量比值较低,在2.2左右,其催化活性好,N2O分解温度低;而MgCo2O4/HZSM-5催化剂强酸性较弱,峰温为481℃,弱酸量与强酸量比值为1.96,其催化活性较差.由此可以推断催化剂的强酸性和弱酸量和强酸量所占比例对催化剂活性影响较大,弱酸性能也在一定程度上影响催化剂活性.
3 结 论
通过对ACo2O4和ACo2O4/HZSM-5催化剂催化分解N2O性能研究得到以下结论:
(1)将尖晶石型复合氧化物负载在分子筛HZSM-5上,与尖晶石型复合金属氧化物相比,催化剂活性得到改善,N2O分解温度大幅度降低,A位离子种类影响催化剂活性.
(2)负载在分子筛HZSM-5载体上的ACo2O4为超细颗粒,活性组分与反应物有效接触面积增加.与HZSM-5样品相比,HZSM-5负载ACo2O4尖晶石型复合金属氧化物后,催化剂的酸性发生变化,A位离子种类影响催化剂的酸性和酸量,影响催化剂活性,其中强酸性能在N2O催化分解反应中起重要作用.
1 Lu,C.H.Hebei Chem.Eng.Ind.,2009,32(9):20 [鲁长海.河北化工,2009,32(9):20]
2 Xu,X.L.;Xu X.F.;Zhang,G.T.;Niu,X.J.J.Fuel Chem.Tech., 2009,37(5):595 [徐晓玲,徐秀峰,张国涛,牛宪军.燃料化学学报,2009,37(5):595]
3 Yoshida,H.;Tsuruta,T.;Yazawa,Y.;Hattori,T.Appl.Catal.AGen.,2007,325(1):50
4 Boissel,V.;Tahir,S.;Koh,C.A.Appl.Catal.B-Environ.,2006, 64(3-4):234
5 Suarez,S.;Saiz,C.;Yates,M.;Martin,J.A.;Avila,P.;Blanco,J. Appl.Catal.B-Environ.,2005,55(1):57
6 Vasilis,G.K.;George,E.M.;Iacovos,A.V.;Kostas,S.T.Appl. Catal.B-Environ.,2009,89(3-4):627
7 Dandekar,A.;Vannice,M.A.Appl.Catal.B-Environ.,1999,22 (3):179
8 Guo,L.;Wu,B.;Zhuang,Y.H.;Li,Q.S.;Zhu,H.S.Acta Sci. Circ.,1998,18(5):458 [郭 林,吴 波,庄亚辉,李前树,朱鹤孙.环境科学学报,1998,18(5):458]
9 Cheng,H.K.;Huang,Y.Q.;Wang,A.Q.;Li,L.;Wang,X.D.; Zhang,T.Appl.Catal.B-Environ.,2009,89(3-4):391
10 Dacquin,J.P.;Lancelot,C.;Dujardin,C.;Da-Costa,P.;Djega-Mariadassou,G.;Beaunier,P.;Kaliaguine,S.;Vaudreuil,S.;Royer, S.;Granger,P.Appl.Catal.B-Environ.,2009,91(3-4):596
11 Asano,K.;Ohnish,C.;Iwamoto,S.;Shioya,Y.;Inoue,M.Appl. Catal.B-Environ.,2008,78(3-4):242
12 Xue,L.;Zhang,C.B.;He,H.;Teraoka,Y.Appl.Catal.BEnviron.,2007,75(3-4):167
13 Stelmachowski,P.;Maniak,G.;Kotarba,A.;Sojka,Z.Catal. Commun.,2009,10(7):1062
14 Xue,L.;Zhang,C.B.;He,H.Chin.J.Rare Earth Society,2006, 24(Special Issue):10 [薛 莉,张长斌,贺 泓.中国稀土学报, 2006,24(专辑):10]
15 Abu-Zied,B.M.;Schwieger,W.Appl.Catal.B-Environ.,2009, 85(3-4):120
16 Campa,M.C.;Indovina.V.;Pietrogiacomi,D.Appl.Catal.BEnviron.,2009,91(1-2):347
17 Labhsetwar,N.;Dhakad,M.;Biniwale,R.;Mitsuhashi,T.;Haneda, H.;Reddy,P.S.S.;Bakardjieva,S.;Subrt,J.;Kumar,S.;Kumar, V.;Saiprasad,P.;Rayalu,S.Catal.Today,2009,141(1-2):205
18 Obalova,L.;Jiratova,K.;Kovanda,F.;Pacultova,K.;Lacny,Z.; Mikulova,Z.Appl.Catal.B-Environ.,2005,60(3-4):289
19 Obalova,L.;Fia,V.Appl.Catal.B-Environ.,2007,70(1-4):353
20 Obalova,L.;Pacultova,K.;Balabanova,J.;Jiratova,K.;Bastl,Z.; Valaskova,M.;Lacny,Z.;Kovanda,F.Catal.Today,2007,119 (1-4):233
21 Yu,J.J.;Zhu,L.;Zhou,B.;Shao,L.N.;Zhang,Y.T.;He,X.W. Acta Phys.-Chim.Sin.,2009,25(2):353 [於俊杰,朱 玲,周波,邵立南,张玉婷,何绪文.物理化学学报,2009,25(2):353]
Decomposition of N2O on ACo2O4/HZSM-5 Catalysts
WANG Hong1,*WANG Jun-Li2LI Cui-Qing1,*SONG Yong-Ji1CHI Yao-Ling1WANG Tao1
(1Department of Chemical Engineering,Beijing Institute of Petrochemical Technology,Beijing 102617,P.R.China;2Hunan Changling Petrochemical Scientific and Technical Developing Company Limited,Changling 414000,Hunan Province,P.R.China)
ACo2O4(A=Mg,Ni,Zn)and ACo2O4/HZSM-5(A=Mg,Fe,Ni,Cu,Zn,Zr,La)catalysts were synthesized by the citric acid-ligated combustion method and by low-temperature complex impregnation,respectively.The catalysts were characterized by X-ray diffraction(XRD),ammonia temperature-programmed desorption(NH3-TPD), scanning electron microscopy(SEM),and energy dispersive X-ray microanalysis(EDS).The performance of the catalysts was evaluated with micro fixed bed reactor.The results showed that the catalytic activity was affected by the A-site ion,and when the A-site ion was Ni,Fe,Zr,or La,the catalysts had better catalytic activity and the temperature of N2O decomposition was lower.Compared with ACo2O4,the ACo2O4/HZSM-5 catalyst had better catalytic activity. ACo2O4was present as ultrafine particles on the HZSM-5 zeolite and the ACo2O4/HZSM-5 catalyst had good acidity. All these factors are useful in improving the performance of these catalysts.
N2O;Spinel;Decompose;HZSM-5
O643
Received:April 13,2010;Revised:May 24,2010;Published on Web:July 20,2010.
*Corresponding authors.LI Cui-Qing,Email:licuiqing@bipt.edu.cn;Tel:+86-10-81292038.WANG Hong,Email:wanghong@bipt.edu.cn;
Tel:+86-10-81292131.
The project was supported by the Science and Technology Development of Bejing Education Committee,China(KM200910017002)and Academic Human Resources Development in Institutions of Higher Learning Under the Jurisdiction of Beijing Municipality,China(PHR200907129).
北京市教委科技计划(KM200910017002)和北京市属高等学校人才强教计划(PHR200907129)资助项目
ⒸEditorial office of Acta Physico-Chimica Sinica

