动态浊度法定量检测茵栀黄注射液中细菌内毒素
江苏省盐城市药品检验所(224002)王梅娟
茵栀黄注射液为茵陈提取物、栀子提取物、金银花提取物及黄芩苷经加工制成的灭菌水溶液,具有清热、解毒、利湿、退黄的功能,临床应用于用于肝胆湿热,面目萎黄,胸胁胀痛,恶心呕吐,小便黄赤。急性、迁延性、慢性肝炎。临床用药广泛,又常用于静脉滴注,现标准为进行热原检查,且为中药制剂,对它进行热原控制有实际意义,因细菌内毒素限值检查具有较大的干扰性,故选用动态浊度法测定其细菌内毒素可消除其干扰,结果准确可靠,且对茵栀黄注射液进行添加内毒素回收试验及热原检查的对比试验,以此建立分析方法,现报告如下:
1 材料与仪器
茵栀黄注射液(批号20080903、20081107、20090109、20090206,江苏省长江药业有限公司);TAL 试剂(批号20080208,λ=0.03EU·ml-1,规格0.5ml·Amp-1,湛江海洋生物制品检定厂);细菌内毒素国家标准品(批号2008-3,70EU·Amp-1,中国药品生物制品检定所);细菌内毒素检查用水(批号20080208,规格10ml·Amp-1,湛江海洋生物制品检定厂);BET-32C 细菌内毒素测定仪(天津大学无线电厂)。
2 方法与结果
2.1 细菌内毒素限值的确定[1]公式为:L=K·M-1,K为规定的给药途径,即每人每公斤体重每小时最大可接受的内毒素剂量,注射剂为5 EU·kg-1;M为1h每公斤体重的最大给药剂量为10ml·kg-1,计算得样品的内毒素限值L为0.5EU·ml-1。
2.2 标准曲线制备及可靠性[1]细菌内毒素检查用水将内毒素国家标准品进行10及2倍稀释,最终细菌内毒素浓度分别为0.5、0.25、0.125、0.0625、0.0313 EU·ml-1稀释系列;各取0.1ml分别加到预先加有0.1ml TAL试剂反应管内,混合均匀,立即插入BET-32C细菌内毒素测定仪内进行自动检测,其中每一浓度重复3管。结果见附表1。回归方程:lgT=3.029-0.3304lgC,其中,相关系数r=-0.9987;最低浓度λ1=0.0313 EU·ml-1,空白对照管在检测时间外,故标准曲线成立。
2.3 干扰试验
2.3.1 样品稀释倍数计算[1]公式为:MVD=L·C·λ1-1。L为茵栀黄注射液内毒素限值;C为1ml·ml-1;λ1为标准曲线的最低内毒素浓度0.0313 EU·ml-1;计算得茵栀黄注射液最大有效稀释倍数MVD为16倍。
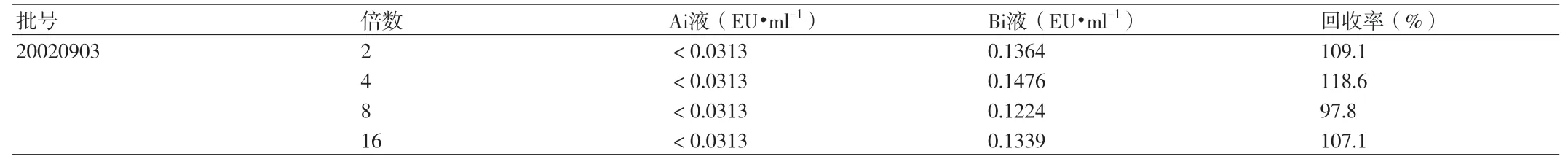
2.3.2 样品溶液配制及干扰试验 将复方丹参注射液用内毒素检查用水依次稀释为2、4、8、16倍溶液,记为Ai液;同时另取4管,进行同样倍数稀释,但在稀释液中添加浓度为M(4λ1)的细菌内毒素标准溶液;作为样品添加内毒素阳性对照管,记为Bi液;分别取上述各液0.1ml,加入预先加有0.1ml TAL试剂的反应管内,混匀立即插入BET-32C细菌内毒素测定仪内进行检测,其中每一个浓度重复3管,计算回收率。回收率(%)=(Bi液内毒素值-Ai液内毒素值)×M-1×100%。结果见附表2。标准曲线:lgT=3.029-0.3304lgC,r=-0.9987。样品的添加内毒素平均回收率均在50%~200%范围内,符合中国药典2000年版规定,表明样品的4个浓度溶液对鲎试剂无干扰影响。
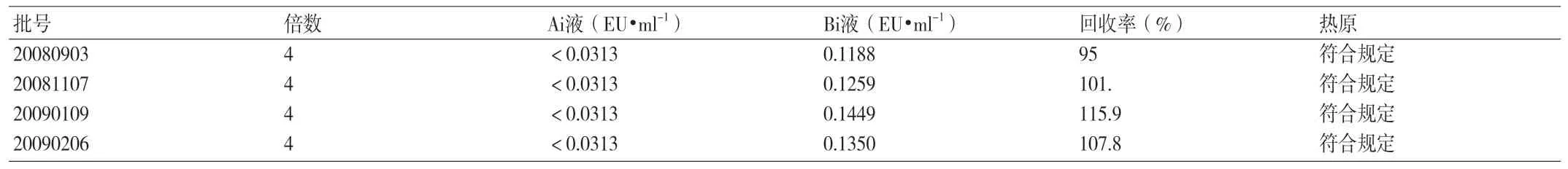
2.4 样品溶液正式试验 分别取4批茵栀黄注射液,用细菌内毒素检查用水制成4倍稀释液,记为Ai液;同时另取4管进行4倍稀释,并在稀释液中添加浓度为M(4λ1)的细菌内毒素标准溶液,记为Bi液;分别取上述各液0.1ml,加入0.1ml TAL试剂的反应管进行检测,其中每一个浓度重复3管,计算回收率。结果见附表3。标准曲线:lgT=2.928-0.3027lgC,r=-0.9988,4批复方丹参注射液的回收率均在50%~200%范围内,表明茵栀黄注射液在本实验条件下对TAL试剂无干扰影响,因此日常检验选用4倍即可。同时进行4批供试品的家兔热原检查对比试验,结果一致,均为阳性。

附表1 标准曲线的可靠性(n=3)
附表2 茵栀黄注射液的干扰试验(n=3)
附表3 茵栀黄注射液正式干扰试验(n=3)
3 讨论
3.1 从茵栀黄注射液的干扰试验结果发现:茵栀黄注射液用细菌内毒素动态浊度法检测,由于内毒素回收率在50%~200%范围内,表明不存在干扰因素影响,且4批茵栀黄注射液的内毒素含量均在规定限度0.5EU·ml-1以下。
3.2 用传统的家兔法检测细菌内毒素,由于操作复杂,影响因素多,对试验结果影响很大。利用动态浊度法进行细菌内毒素定量检测,具有操作简便、结果准确、检测灵敏度高等优点,尤其避免了由于家兔差异及人为主观判断所出现的假阳性或假阴性结果。经过对比试验,样品的细菌内毒素定量检测结果与家兔热原检测结果一致,说明使用细菌内毒素动态浊度法测定复方丹参注射液的细菌内毒素是可行的,可用细菌内毒素定量检查法代替家兔热原检查法。

