不同酸体系中杨梅红色素加工稳定性的研究
夏 红,朱庆珍,丁俊鹏
(苏州农业职业技术学院,江苏 苏州 215008)
不同酸体系中杨梅红色素加工稳定性的研究
夏 红,朱庆珍,丁俊鹏
(苏州农业职业技术学院,江苏 苏州 215008)
以1、0.1、0.01mol/L的盐酸、柠檬酸、酒石酸和抗坏血酸为溶剂从杨梅果实中提取红色素,过滤后将溶液进行70℃水浴加热5h、超声处理1h,处理后的溶液再置于自然光照下3d,以吸光度变化率为指标观察杨梅红色素在不同酸中对加热、超声、光照的稳定性。结果表明:杨梅红色素在不同浓度的盐酸、柠檬酸、酒石酸和抗坏血酸溶液中经过加热、超声处理和光照后吸光度均有不同程度的下降,表现出不稳定性。但其不稳定性的表现程度随酸的种类和浓度的不同而有所不同,变化情况较复杂。比较而言,在抗坏血酸溶液中色素对加热、超声和光照处理最不稳定。盐酸溶液中色素对加热处理相对较稳定,其中在1mol/L的盐酸溶液中加热后的吸光度变化最小;本实验条件下,色素在盐酸、柠檬酸、酒石酸溶液中对超声处理相对较稳定,其中在0.01mol/L柠檬酸溶液中色素经超声处理后吸光度的变化最小;光照处理时,在0.1mol/L的盐酸溶液中色素的吸光度变化率最小。
酸体系;杨梅红色素;稳定性
色、香、味是食品感官品质的重要考察因素,因此食品加工中常采用添加剂来提高食品的感官品质。色素是常用的食品添加剂,在饮料、糕点等食品生产中应用广泛。随着人们生活水平和生活质量的不断提高,天然食用色素由于其安全、营养而较合成色素日益受到青睐[1]。天然食用色素的资源开发、性质及提取工艺的研究也受到科研工作者的关注[2-11],这些研究为食用天然色素的应用提供了理论基础。植物色素是天然食用色素的主要来源,从化学结构而言,可以分为多酚色素、多烯色素等。多酚色素为水溶性色素,主要分布在植物的花、果实中。这些色素在酸性体系中较稳定,但其稳定性受许多因素的影响[12-18],在其应用于食品加工时,许多加工手段也会对其色泽稳定性等产生影响,从而可能影响其使用效果。在天然色素的研究中,红色素引起较多研究者的注意,其中许多研究者杨梅红色素的性质、提取工艺作了较多的研究。严和平等[19]、马银海等[20]对杨梅红色素的提取工艺进行了研究,都用酸浸泡萃取色素得到提取液后进行提取纯化,叶日英等[21]对杨梅色素的理化性质进行了分析,这些性质都表现出植物多酚色素的共性;林璇[22]对杨梅红色素的提取、纯化及其理化性质进行了研究,采用不同的杨梅品种,提取其红色素,经纯化后进行光谱实验,推测花色苷主要成分为矢车菊花色苷,少量为芍药花色苷和天竺葵花色苷,都表明杨梅红色素为多酚类色素。由于多酚类色素具有一定的不稳定性,与应用条件有很大的关系。本实验以杨梅红色素为研究对象,观察其在不同酸系中受加热、超声、光照等食品加工手段的影响而发生的变化,为其应用提供参考。
1 材料与方法
1.1 材料
杨梅购自苏州东山,大叶细蒂种。鲜杨梅购买后速冻保存供实验用,使用时解冻。
1.2 试剂
盐酸(分析纯) 常州市武卫试剂有限公司;柠檬酸(分析纯) 上海试剂一厂;酒石酸(分析纯) 上海化学试剂采购供应站;抗坏血酸(分析纯) 上海申翔化学试剂有限公司;实验采用蒸馏水。
1.3 仪器与设备
TU-1810型紫外-可见分光光度计 北京普析通用仪器有限公司;722S可见分光光度计 上海精密科学仪器有限公司;KQ-100DB型数控超声波清洗器 昆山市超声仪器有限公司。
1.4 方法
配制1、0.1、0.01mol/L的酸溶液,按杨梅质量与酸液体积比1:4浸提45min后过滤,滤液即为不同酸系中的色素溶液。
上述色素溶液分别进行加热处理和超声处理。将滤液置于超声波清洗器中超声处理1h后,比较超声前后溶液吸光度的变化;加热处理时将其置于70℃水浴中保持5h,比较加热前后溶液吸光度的变化,考察热对不同酸体系中杨梅红色素稳定性的影响。加热后的溶液继续静置于自然光照下,3d后再测定其吸光度,观察变化。上述实验经重复实验2次,每次重复实验时每种酸浓度设平行实验。
1.5 吸光度测定
经检测,不同酸系中的杨梅红色素溶液在可见光范围内于波长510~518nm处有最大吸收,同种酸浓度大时最大吸收波长略有红移。为了操作方便,同时考虑到不影响实验结果比较,所有溶液均以512nm作为测定波长。吸光度变化率按下式计算。平均变化率为两次重复实验平均变化率的平均值。
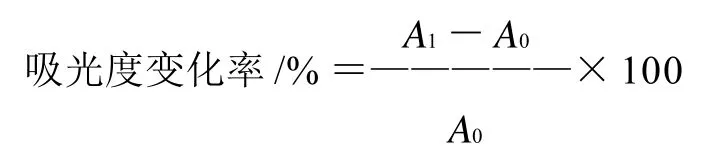
式中:A0为处理前溶液的吸光度;A1为处理后溶液的吸光度。
2 结果与分析
2.1 不同酸溶液对杨梅红色素加热稳定性的影响
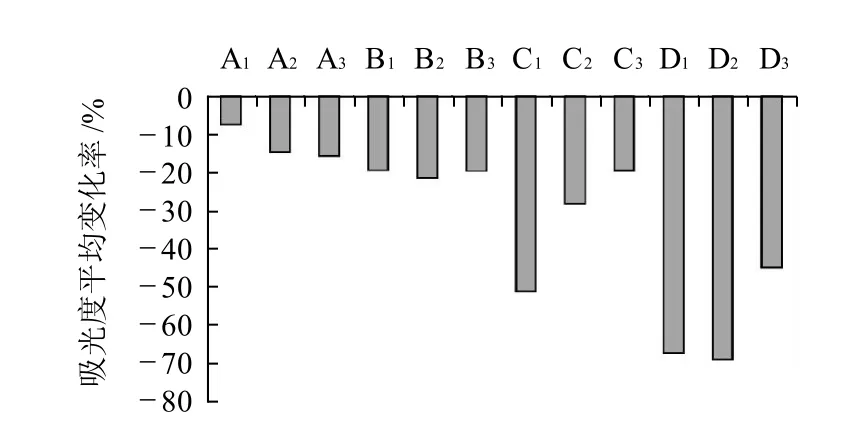
图 1 不同酸溶液中杨梅红色素加热后吸光度的平均变化率Fig.1 Average absorbance change of red pigment from Myrica rubra in different acid systems after heating treatment
由图1可以看出,酸溶液中加热后,杨梅红色素溶液的吸光度均下降,表现出对加热的不稳定性。以吸光度的平均变化率考察,相对而言,抗坏血酸溶液中加热后色素吸光度的变化最大,其次为酒石酸溶液中,再次为柠檬酸溶液中,盐酸溶液中色素吸光度的变化最小。结果说明,杨梅红色素在酸溶液中加热表现出不稳定性,不同酸中这种不稳定性还存在差异。这可能与酸的性质有关,抗坏血酸是对热不稳定的弱酸,且有还原性,而盐酸为强酸。上述性质都可能会影响杨梅红色素的加热稳定性。以同浓度的不同酸考察,基本也呈现出上述变化规律。在浓度较小的不同酸溶液中,色素对加热的不稳定性差异较小,而随着酸溶液浓度的增加,不同酸中色素对加热的不稳定性的差异增大。总体而言,杨梅红色素酸溶液对加热的稳定性依次为盐酸>柠檬酸>酒石酸>抗坏血酸。
虽然加热使不同浓度盐酸溶液中色素的吸光度都下降,但其变化率不尽相同。重复实验的结果表明,0.01mol/L盐酸溶液中吸光度变化最大,其次为0.1mol/L盐酸,但两者的变化率较接近,而1mol/L盐酸溶液中色素加热后的吸光度变化最小,这从一个方面表明,在本实验范围内,盐酸溶液的浓度越高,杨梅红色素对加热的稳定性相对越高。不同浓度柠檬酸中色素加热后的吸光度变化率趋势在两次重复实验中有差异。但同一重复实验中,色素溶液吸光度的变化率都比较接近。总体而言杨梅红色素在酒石酸溶液中对加热的稳定性较差,加热后吸光度下降平均可达32.92%。而且在1mol/L浓度的溶液中加热后吸光度的变化最大,随酒石酸浓度的减小,加热后色素溶液吸光度的变化率减小。结果反映出杨梅色素在酒石酸溶液中对热的稳定性随酸浓度的增大而减弱。杨梅红色素在抗坏血酸溶液中对热极不稳定,加热后吸光度平均下降率为60.18%。在0.01mol/L的抗坏血酸溶液中相对变化率较小;在0.1mol/L溶液中变化率最大,1mol/L溶液中的变化率与0.1mol/L溶液中的变化率相差不大。
2.2 不同酸溶液对杨梅红色素超声稳定性的影响

表 1 不同酸溶液中杨梅红色素溶液超声处理后吸光度的变化Table 1 Absorbance change of red pigment from Myrica rubra in different acid systems after ultrasonic treatment
表1表明,杨梅红色素在盐酸、柠檬酸和酒石酸溶液中经超声处理后,吸光度基本呈下降趋势,但变化率较小,相对比较稳定。但在抗坏血酸溶液中吸光度下降的变化率很大。色素在盐酸溶液中超声处理时,吸光度的变化趋势随酸浓度的变化而有所不同。低浓度盐酸溶液中变化较大。色素在柠檬酸和酒石酸溶液中超声处理时,吸光度变化率随酸溶液浓度的增大而增大,即在低浓度酸中相对稳定。同样在抗坏血酸溶液中,低浓度时色素进行超声处理时,其吸光度的变化相对较小,从一个方面反映出相对稳定性,而在中等浓度(0.1mol/L)的抗坏血酸溶液中吸光度变化率最大,相对最不稳定。
2.3 不同酸溶液对杨梅红色素光照稳定性的影响

图2 杨梅红色素在不同酸溶液中经3d光照后吸光度的平均变化率Fig.2 Average absorbance change of red pigment from Myrica rubra in different acid systems after light treatment
从图2可以看出,杨梅红色素在抗坏血酸溶液中对光照极不稳定,3d光照后溶液的吸光度下降平均达85.49%。在酒石酸和盐酸溶液中相对较稳定,吸光度平均下降20%左右。在柠檬酸溶液中光照稳定性居中。
同种酸溶液中,酸浓度对色素的光照稳定性也有影响。在盐酸溶液中,色素在0.1mol/L的酸溶液中最稳定,在1mol/L的酸溶液中最不稳定,即盐酸浓度最大的溶液中,色素的光照稳定性最差,而且与较低浓度酸溶液中的稳定性差异较大;在柠檬酸和酒石酸溶液中,色素对光照的稳定性都随酸浓度的降低而增强,而且在高浓度的酸溶液中色素的稳定性与较低浓度酸溶液中稳定性的差异较大。在不同浓度的抗坏血酸溶液中,色素的不稳定性虽有差异但差异不大。
3 结 论
通过不同浓度的酸为溶剂直接浸提杨梅红色素,将色素溶液进行加热、超声、光照处理,以吸光度变化观察色素在不同酸溶液中的稳定性。结果表明,在进行处理后,色素溶液的吸光度均发生变化,而且以吸光度减小为主,表现出色素本身的不稳定性。同时酸的种类和浓度对杨梅红色素的加热、超声、光照稳定性都产生影响。色素在抗坏血酸溶液中对所有处理都表现出极不稳定性。加热处理时,在1mol/L的盐酸溶液中相对稳定;超声处理时,在盐酸、柠檬酸、酒石酸溶液中都较稳定,而在0.01mol/L柠檬酸溶液中变化最小。光照处理时,在0.1mol/L的盐酸溶液中变化最小。
[1] 胡珍珠. 家庭食疗手册[M]. 天津: 天津科学技术出版社, 1983: 116.
[2] 高居易, 余仲平. 福建古田红曲色素的研究[J]. 福建师范大学学报:自然科学版, 1995, 11(1): 91-94.
[3] 高居易, 郑怀舟. 新法提取竹叶绿色色素及其毒性和稳定性的研究[J]. 竹子研究汇刊, 2000, 19(4): 58-62.
[4] 刘振华, 丁卓平, 董洛文. 辣椒中红色素的提取工艺研究[J]. 食品科学, 2006, 27(12): 291-295.
[5] 曹军胜, 曹娟云, 刘长海. 桑葚红色素的提取及其稳定性[J]. 食品工业, 2002(3): 20-21.
[6] 王琳, 岳田利. 桑葚红色素研究进展[J]. 食品科技, 2004(6): 58-61.
[7] 焦中高, 刘杰超, 王思新, 等. 黑莓红色素的提取及其稳定性的初步研究[J]. 食品科学, 2005, 26(3):154-157.
[8] 马银海, 彭永芳, 庞敏, 等. 杨梅红色素的提取研究[J].食品科学, 2004,25(7): 112-113.
[9] 孙 健, 蒋跃明, 彭宏祥, 等. 红毛丹果皮色素的提取及其稳定性的研究[J]. 食品科学, 2009, 30(11): 71-75.
[10] 赵慧芳, 李维林, 王小敏, 等. 黑莓果实色素纯化及干燥工艺研究[J].食品科学, 2009, 30(12): 35-39.
[11] 高居易, 檀东飞, 陈伟生. 杨梅水溶性红色素的提取和性质研究[J].天然产物研究与开发, 2001, 13(2): 59-62.
[12] 阿布来提·阿布都热西提. 甜石榴皮和酸石榴皮中天然黄色素的提取及其稳定性比较分析[J]. 食品科学, 2009, 30(15): 130-132.
[13] 吕丽爽, 孙美玲. 何首乌色素稳定性研究[J]. 食品科学, 2009, 30(15):67-70.
[14] 魏明英, 江建军. 红阳猕猴桃色素理化性质及其稳定性研究[J]. 食品科学, 2009, 30(3): 100-103.
[15] 迪丽努尔·马里克, 米丽班·霍加, 古丽娜尔·帕提古丽. 野蔷薇果皮色素的提取和稳定性研究[J]. 食品科学, 2008, 29(3): 116-118.
[
16] 田成. 蛇莓果实色素的稳定性研究[J]. 食品科学, 2008, 29(4): 124-127.[
17] 白晓杰, 张光霞. 食用天色杨梅色素的性质及应用研究[J]. 廊坊师范学院学报, 2002, 18(4): 68-69.
[18] 陈健初, 叶兴乾, 席与芳. 抗坏血酸对杨梅花色苷色素稳定性的影响[J]. 浙江大学学报: 农业与生命科学版, 2005, 31(3): 298-300.
[19] 严和平, 张举成, 徐宏刚. 杨梅红色素的提取工艺研究[J]. 食品工业科技, 2009(6): 306-308.
[20] 马银海, 彭永芳, 庞敏, 等. 杨梅红色素的提取研究[J]. 食品科学,2004, 25(7): 112-113.
[21] 叶日英, 张俊. 杨梅色素的理化性质分析[J]. 农牧产品开发, 2000(1):11-12.
[22] 林璇. 杨梅红色素的提取、纯化及其理化性质[J]. 漳州师范学院学报: 自然科学版, 2002, 15(3): 98-101.
Processing Stability of Red Pigment from Myrica rubra in Different Acidic Systems
XIA Hong,ZHU Qing-zhen,DING Jun-peng
(Suzhou Polytechnic Institute of Agriculture, Suzhou 215008, China)
Red pigment was extracted from fruits of Myrica rubra using 1, 0.1 mol/L and 0.01 mol/L hydrochloric acid, citric acid, tartaric acid and ascorbic acid. Different pigment solutions were obtained by filtration. Pigment solutions were subjected to heating treatment at 70 ℃ for 5 hours and ultrasonic treatment for 1 hour. The treated pigment solutions were placed in the natural light for 3 days. The absorbance change of pigment solutions was determined to evaluate the stability of pigment. Results showed that red pigment was not stable in acidic systems. The pigment was very unstable to heating, ultrasonic and light treatments in ascorbic acid system. However, the pigment exhibited relative stability to heating treatment in hydrochloric acid system with the minimum absorbance change in 1 mol/L hydrochloric acid. Moreover, the pigment also exhibited the relative stability to ultrasonic treatment in hydrochloric acid, citric acid and tartaric acid. Meanwhile, the minimum absorbance change of pigment after ultrasonic treatment was observed in 0.01 mol/L citric acid. Furthermore, the minimum absorbance change of pigment after natural light treatment was revealed in 0.1 mol/L hydrochloric acid.
acid systems;red pigment;Myrica rubra;stability
TS264.4
A
1002-6630(2010)09-0059-03
2009-09-20
2008年江苏省大学生实践创新训练项目((2008-237)
夏红(1965—),女,教授,硕士,研究方向为食品化学与农产品贮藏加工。E-mail:xhfood@163.com

