HPLC-ELSD测定胡芦巴降糖缓释片中薯蓣皂苷元的含量
李季文,景明,刘效栓,李喜香
(1.甘肃省中医院,甘肃 兰州 730050;2.甘肃中医学院,甘肃 兰州 730000)
HPLC-ELSD测定胡芦巴降糖缓释片中薯蓣皂苷元的含量
李季文1*,景明1,刘效栓2,李喜香2
(1.甘肃省中医院,甘肃 兰州 730050;2.甘肃中医学院,甘肃 兰州 730000)
目的:建立HPLC-ELSD测定胡芦巴降糖缓释片含量的方法。方法:高效液相色谱法测定含量,色谱柱:岛津VP-ODS(4.6 mm×150 mm,5μm),流动相:甲醇-水(84∶16),检测波长:203 nm,流量:1.0 mL·min-1,柱温:40℃,漂移管温度:85℃,气流体积流量:2.5 L·min-1。结果:该方法下薯蓣皂苷元标准曲线为Y=812 991.42X+1 252 792.92,r=0.999 6(n=5),线性范围为0.842~8.42μg,平均回收率为98.53%(n=6)。结论:该方法准确可靠、重现性好,可用于胡芦巴降糖缓释片中著蓣皂苷元的含量测定。
胡芦巴降糖缓释片;薯蓣皂苷元;高效液相色谱
胡芦巴Trigonella foenum-graecumL.为豆科植物胡芦巴的干燥成熟种子。现代药理研究表明,胡芦巴具有抗糖尿病、降胆固醇作用[1]。胡芦巴降糖缓释片是以中药材胡芦巴的乙醇提取物与一定缓释材料制成的口服缓释降糖药,用于治疗高血糖和高血脂。胡芦巴中含有丰富的甾体皂苷类成分,其中薯蓣皂苷元(diosgenin)和雅莫皂苷元(yamogenin)的含量在0.6%~1%[2-5],因此本实验采用高效液相色谱法,以测定薯蓣皂苷元的含量来控制胡芦巴降糖缓释片的含量。
1 仪器与试药
1.1 仪器
岛津LC-20AB型高效液相色谱仪,SIL-20AC自动进样器,CTO-20AC柱温箱,CBM-20A控制器,DGU-20A3脱气机、LC solution色谱工作站(日本岛津),SEDEX75蒸发光散射检测器(迪马公司),D-800L型智能药物溶出仪(天津大学无线电厂),BS110电子天平(北京塞多利斯仪器有限公司),R-200旋转蒸发仪(瑞士布奇),KT-350W超声波清洗器(江苏昆山超声技术有限责任公司),HH-601恒温水浴锅(金坛市恒丰仪器厂)。
1.2 试药
胡芦巴降糖缓释片(自制,批号20080901,20080902,20081003),薯蓣皂苷元对照品(中国药品生物制品检定所,批号110648-200708),甲醇(山东省禹王实业有限公司,批号20070317)、三氯甲烷(烟台市双双化工有限公司,批号20070612)、盐酸(山东省禹王实业有限公司,批号20070218)为色谱纯,水为蒸馏水,其他试剂均为分析纯。
2 含量测定
2.1 色谱条件
色谱柱:岛津VP-ODS(4.6 mm×150 mm,5μm),流动相:甲醇-水(84∶16),检测波长:203 nm,流量:1.0 mL·min-1,柱温:40℃,漂移管温度:85℃,气流体积流量:2.5 L·min-1。塔板数以薯蓣皂苷元计,不低于2 000。
2.2 对照品溶液的制备
精密称取薯蓣皂苷元对照品5.46 mg,置10 mL量瓶中,加甲醇使溶解并稀释至刻度,摇匀,即得(每1 mL含薯蓣皂苷元0.546 mg)。
2.3 供试品溶液的制备
取本品25片,研细,精密称取5 g,置量瓶中,加甲醇25 mL,超声30 min,用甲醇稀释至刻度,摇匀,滤过。滤渣用甲醇20 mL洗涤,合并甲醇液,回收甲醇蒸干,残渣加3 moL·L-1盐酸溶液20 mL(10,5,5 mL)溶解,依次转移至锥形瓶中,水浴中加热水解30 min。取出,放冷,加入三氯甲烷30 mL,加热回流15 min,用三氯甲烷30 mL同法处理1次,滤过,再用三氯甲烷30 mL洗涤容器及残渣,合并三氯甲烷液,回收三氯甲烷至干,残渣加甲醇溶解并转移至25 mL量瓶中,加甲醇至刻度,摇匀,即得。
2.4 线性关系考察
精密称取薯蓣皂苷元对照品,置于10 mL量瓶中,用甲醇溶解并稀释至刻度,即为对照品储备液(4.21 mg·mL-1)。精密吸取此储备液5 mL,置25 mL量瓶中,用甲醇稀释至刻度,摇匀,即得对照品溶液。精密吸取1,2,4,6,8,10μL,注入液相色谱仪,记录峰面积,以对照品进样量(μg)为横坐标,峰面积积分值为纵坐标,绘制标准曲线并进行线性回归,得回归方程Y=812 991.42X+1 252 792.92,r=0.999 6,结果薯蓣皂苷元在0.842~8.42μg与其色谱峰面积呈良好线性关系。
2.5 精密度试验
精密吸取薯蓣皂苷元对照品溶液10μL,注入液相色谱仪,连续进样6次,测得薯蓣皂苷元峰面积积分值的RSD=1.12%(n=6)。
2.6 稳定性试验
精密吸取同一供试品溶液10μL,分别在0,2,4,8,12 h注入液相色谱仪中,测定薯蓣皂苷元峰面积,积分值的RSD=1.47%。结果表明,样品溶液在12h内稳定。
2.7 重复性试验
取同一批胡芦巴缓释片粉末6份,平行制备供试品溶液,各取10μL进样测定,薯蓣皂苷元的平均含量为0.47 mg·g-1,RSD=1.95%(n=6),结果表明本方法的重复性较好。
2.8 加样回收率试验
取已知含量的胡芦巴缓释片粉末(过四号筛),精密称取6份,分别精密加入薯蓣皂苷元对照品溶液(4.21 mg·mL-1)0.3 mL,以本法测定含量并计算加样回收率,结果见表1。
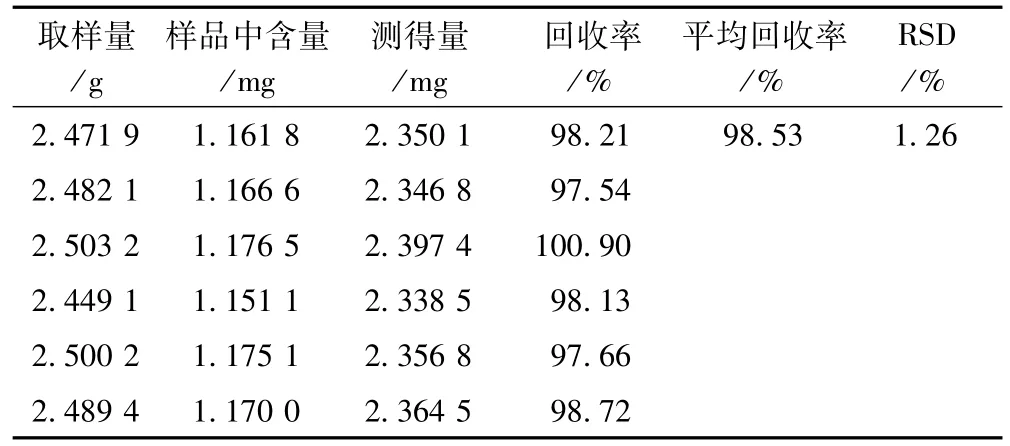
表1 薯蓣皂苷元加样回收率
2.9 样品含量测定
取20080901,20080902,20081003 3批样品,研细,按2.3项下方法制备,精密吸取10μL,注入高效液相色谱仪,进行测定,每批样品平行测定2次,薯蓣皂苷元含量测定结果依次为0.47,0.51,0.43 mg·g-1,HPLC图见图1。

图1 对照品及供试品HPLC图
3 讨论
以薯蓣皂苷元含量为评价指标,采用高效液相色谱法建立胡芦巴降糖缓释片的含量测定方法,通过本实验对3批样品的测定结果进行比较,结果良好。采用高效液相色谱法,方法学考察表明该方法重现性好,结果准确可靠,可用于胡芦巴降糖缓释片中著蓣皂苷元的含量测定。
[1]李宗友.胡芦巴的抗糖尿病和降胆固醇作用[J].国外医学·中医中药分册,1999,21(4):9.
[2]Yoshikawa M.Medicinal foodstuffs IV.fenugreek seed(1):Structures of trigoneo sides Ia,Ib,IIa,IIb,IIIa and IIIb,new furostano saponins from the seeds of IndianTrigonella foenumgraecumL[J].Chem Pharm Bull,1997,45(1):81-87.
[3]Yoshikawa M.Medicinal foodstuffs V III.fenugreek seed(2):Structures of six new furostanol saponins trigoneosides IVa,Va,Vb,VI,VIIb and VIIIb from the seeds of IndianTrigonella foenum-graecumL.[J].Heterocycles,1998,47(1):397-405.
[4]Murakami T,Kishi A,Matsuda H,et al.Medicinal foodstuffs.XVII.fenugreek seed(3):Structures of new furostanol-type steroid saponins,trigoneosides Xa,Xb,XIb,XIIa,XIIb and XIIIa from the seeds of Egy-ptianTrigonella foenum-graecumL.[J].Chem Pharm Bull,2000,48(7):994-1000.
[5]ShangM Y,Cai SQ,Kadda S,etal.Structure identification of trigoneoside VIII[J].Acta Pharm Sin,2001,36(11):836-839.
Determination of Diosgenin in Fenugreek Hypoglycemic Sustained-Release Tablets by HPLC-ELSD
Li Jiwen1,Jing Ming1,Liu XiaoShuan2,Li Xixiang2
(1.Gansu Province hospital of Traditional Chinesemedicine,Lanzhou Gansu730050,China;2.Gansu college of Traditional Chinese Medicine,Lanzhou Gansu730000,China)
Objective:To establish a HPLC-ELSD method of content determination of hypoglycemic sustained release tablets of fenugreek.Methods:HPLC-ELSD was employed a VP-ODS(4.6 mm×150 mm,5μm)column,methanol-water(84∶16)was used as mobile phase,detection wavelength was203 nm,flow rate was1.0mL·min-1,column temperature was40℃,and with drift tube temperature of85℃,air volume flow was2.5 L·min-1.Results:The method involves a diosgenin standard curveY=812 991.42X+1 252 792.92,r=0.9996(n=5),the linear range of 0.842~8.42μg,and recovery rate of 98.53%(n=6).Conclusion:This method is accurate,reliable and reproducible,which can bewaed to determine Diosgenin in Hypoglycemic sustained-release tablets It canmeet the quality standards requirements.
Hypoglycemic sustained-release tablets;Diosgenin;HPLC
*李季文,E-mail:ljwlzh888@163.com
2010-05-22)

