心钠素表达细胞移植降低高血压大鼠的血压和增加其尿量
李涛,梁红雁,路金芝,陈伟京,卢圣栋
中国医学科学院基础医学研究所 北京协和医学院基础学院 医学分子生物学国家重点实验室,北京 100005
医学与免疫生物技术
心钠素表达细胞移植降低高血压大鼠的血压和增加其尿量
李涛,梁红雁,路金芝,陈伟京,卢圣栋
中国医学科学院基础医学研究所 北京协和医学院基础学院 医学分子生物学国家重点实验室,北京 100005
为探讨心钠素基因转移治疗高血压和慢性心肾功能衰竭等慢性疾病的潜力,首先利用逆转录病毒载体获得可表达和分泌人心钠素的遗传工程细胞,然后将这种细胞植于自发性高血压大鼠SHR的皮下。结果发现,人心钠素遗传工程细胞的移植可使动物血浆中的心钠素浓度在移植后第 7天时明显升高。在整个实验期间,虽然实验组动物的血压会随个体发育而逐渐升高,但在实验开始后的42 d内却始终明显低于空载体组,其中第14天血压的差异高达33 mm Hg。在实验开始后的第14天和第21天,实验组动物的尿量也明显增加。以上结果说明,人心钠素遗传工程细胞的皮下移植可明显抑制SHR大鼠血压的上升趋势和改善其泌尿功能,提示该方法具有治疗高血压和慢性心肾功能衰竭等慢性疾病的潜力。
心钠素,基因治疗,逆转录病毒载体,高血压,自发性高血压大鼠
Abstract:To investigate the potential of gene therapy for the treatment of chronic diseases such as hypertension, chronic heart failure, and chronic renal failure, we established the neonatal rat fibroblast line engineered to secrete the mutant human atrial natriuretic peptide (mhANP), and then transplanted the cell line into young spontaneously hypertensive rats (SHR) subcutaneously.We found that a single transplantation of the cell line caused an obvious rise in the concentration of mhANP in serum 7 d after transplantation ((135 ± 8)vs(106 ± 7) pg/mL,P< 0.01). The animals’ blood pressure in test group was always remarkably lower than that of empty vector group within 42 d after transplantation, even though the blood pressure in all groups was constantly increasing in the process of ontogeny ((175 ± 10) mm Hgvs(189 ± 12) mm Hg,P< 0.05). A maximal blood pressure reduction of 33 mm Hg((157 ± 9) mm Hgvs(124 ± 112) mm Hg,P< 0.01) was observed 14 d post cell transplantation. There was a marked increase in urine volume in test group from second week after treatment beginning ((5.9 ± 0.7) mL/6 hvs(4.3 ± 0.8) mL/6 h,P< 0.01) and the effect lasted 14 d ((6.1 ± 1.1) mL/6 hvs(4.0 ± 0.8) mL/6 h,P< 0.01), however the statistical difference in concentration of K+and Na+in serum and urine was not observed. The results suggested that subcutaneous implantation of fibroblasts-expressing mhANPsignificantly reduced blood pressure in young SHR during the period of ontogeny and efficiently improved their renal function and the somatic gene transfer of mhANP may have potential value in the treatment of human chronic diseases such as hypertension,chronic heart failure, and chronic renal failure.
Keywords:atrial natriuretic factor, gene therapy, retroviral vector, hypertension, spontaneously hypertensive rat
虽然治疗药物或手段已有不少,但由于疗效的限制,目前全世界的高血压患者人数仍然超过 10亿,高血压病则仍然是脑卒中、冠心病和心肾功能衰竭等严重疾病的主要诱因[1]。心钠素 (Atrial natriuretic peptide,ANP,或 Atrial natriuretic factor,ANF) 是一种由28个氨基酸构成的多肽激素,主要由心房肌细胞合成和分泌。以ANP基因为标靶的转基因动物试验[2]、基因敲除试验[3]以及以ANP受体基因为标靶的基因敲除试验[4]证明,ANP与心血管系统功能之间的关系密切。体内外活性试验则证明,ANP具有利尿利钠、舒张血管、降低血压、抑制肾素-血管紧张素系统和改善心肾功能等广泛的生物学活性[5-6],因此,ANP的基因工程产品Carperitide已于1995年在日本批准用于治疗急性心衰,与其类似的重组脑钠素 (Brain natriuretic peptide,BNP)Nesiritide于2001年在美国批准用于治疗急性心衰,源于肾脏的Ularitide也已经在美国和欧洲开展治疗急性心衰的临床试验[5-6]。不过作为多肽激素的ANP等也存在着半衰期短因而需要长时间静脉滴注才能有效发挥治疗作用的不足,这使其无法满足高血压和慢性心肾功能衰竭等慢性疾病治疗的需要。为充分发挥ANP的应用潜力,引入了ex vivo基因治疗策略[7],即借助于逆转录病毒载体首先将突变型人心钠素基因 (mhANP) 导入自发性高血压大鼠(Spontaneously hypertensive rat,SHR) 新生鼠的皮肤成纤维细胞,以获得可表达和分泌突变型人心钠素多肽 mhANP的遗传工程细胞,然后将该细胞移植到幼龄SHR大鼠的皮下,以期通过为动物持续提供稳定的 mhANP来源的方法来实现治疗慢性疾病的目的。结果表明,该方法可显著抑制动物血压的上升趋势和增强其肾脏的泌尿功能,在高血压和慢性心肾功能衰竭等慢性疾病的治疗方面具有潜在的应用价值。
1 材料和方法
1.1 材料
DMEM 培养基、G418和 Lipofectamin购自Gibco-BRL公司。BCA (bicinchoninic acid) 试剂盒是美国 PIERCE公司产品。PCR引物 P1(5′-GGAT CCATGAGCTCCTTCTCC-3′) 和 P2(5′-CTCGAGTC AGTACCGGAAGCT-3′) 由赛百盛公司合成。逆转录病毒包装细胞系PA317、NIH3T3细胞由中国医学科学院基础所刘德培教授惠赠。心钠素放免试剂盒购自北京北方免疫试剂所。小牛血清购自中国医学科学院学血液病研究所。RBP-1型大鼠血压测定仪购自中日友好医院。自发性高血压大鼠购自中国医学科学院阜外医院。
携带有 mhANP cDNA的逆转录病毒表达重组体pLHY24由本实验室构建。构建时所用逆转录病毒载体是Clontech公司的pLNCX质粒 (http://www.clontech.com),其中含有为质粒扩增提供选择压力的抗性基因Ampr,为逆转录病毒感染后提供选择压力的抗性基因Neor,供逆转录病毒整合进宿主细胞基因组的主要元件 5′LTR和 3′LTR,控制外源基因表达的人巨细胞病毒启动子 CMVp,以及供外源基因插入的多克隆位点 (MCS)。本研究中的pLHY24就是把mhANP cDNA 插入其CMVp和3′LTR之间的MCS而获得的。
1.2 方法
1.2.1基因组中整合有mhANP cDNA的移植细胞的获得及mhANP表达水平的检测
携带目的基因 mhANP cDNA的逆转录病毒表达重组体pLHY24的包装、SHR新生鼠皮肤成纤维细胞的原代培养物的建立、逆转录病毒对该培养物的感染以及目标多肽 mhANP表达水平的放免法检测等参照文献[8]的方法进行。
1.2.2移植细胞基因组中整合的目的基因mhANP cDNA的检测
采用 PCR扩增的方法来检测目的基因 mhANP cDNA在移植细胞基因组中的整合情况,分别以被空载体pLNCX逆转录病毒颗粒感染的SHR新生鼠皮肤成纤维细胞和被表达重组体 pLHY24逆转录病毒颗粒感染的SHR新生鼠皮肤成纤维细胞的基因组DNA为模板,以mhANPcDNA特异的核苷酸序列为引物 (5′-端引物 P1: 5′-GGATCCATGAGCTCCTT CTCC-3′和 3′-端引物 P2: 5′-CTCGAGTCAGTACCG GAAGCT-3′),进行PCR扩增,并对扩增产物进行分子量鉴定。进行该检测时,以携带有目的基因mhANP cDNA的表达重组体质粒pLHY24为阳性对照,以构建pLHY24时所用空载体质粒pLNCX为阴性对照。
1.2.3鼠尾胶原的制备[9]
将冻存于−20℃的成年大鼠尾剪成 2 cm 的小段,于70%的乙醇浸泡30 min,用镊子抽取尾腱,尽可能将尾腱剪碎,用0.02 mol/L的冰醋酸400 mL于4℃浸泡48 h,于4℃、5000 r/min离心1.5 h,将上清液移于另一管中,于同样条件下离心2 h,收集上清液,以 6∶1 (V/V) 的比例加入 0.1 mol/L的NaOH以中和冰醋酸,室温下5000 r/min离心10 min,弃上清液,用新配制的0.02 mol/L的冰醋酸再溶解胶原蛋白,10 b高压灭菌10 min,−20℃保存备用。胶原蛋白的浓度根据 BCA试剂盒使用说明书提供的方法测定。
1.2.4细胞移植物的制备
所用遗传工程细胞有两种,一种为基因组中整合了空载体pLNCX的SHR新生鼠皮肤成纤维细胞,其无法表达和分泌 mhANP多肽,另一种为基因组中整合有目的基因mhANP cDNA表达系统的SHR新生鼠的皮肤成纤维细胞,其能够表达和分泌mhANP多肽。
首先将上述两种遗传工程细胞分别悬浮于 5×D-MEM (即浓度为正常使用的 D-MEM 培养液的 5倍) 中,使细胞密度为3×106个/mL,然后按大鼠尾胶原 (2 mg/mL)∶5× D-MEM∶小牛血清∶细胞悬液=3∶1∶0.5∶0.5 (V/V) 的比例混合各组分,使移植物中细胞的密度为3×105个/mL。
1.2.5体内细胞移植试验
将购回并饲养7 d后的雄性SHR大鼠随机分成两组 (各10只/组),用腹腔注射戊巴比妥钠 (45 mg/kg)的方法麻醉,按5 mL移植物/只的剂量将移植物缓慢注入动物背部两侧4个点的皮下。
1.2.6血压、体重和尿量等生理指标的测定[10]
每周定期称量动物体重,用鼠尾夹法测大鼠尾动脉收缩压,用代谢笼法收集尿液并测量其体积和其中的钾、钠等电解质浓度,自眼眶取血、分离血浆并测定其中mhANP多肽的浓度。
1.2.7统计学处理
2 结果
2.1 目的基因mhANPcDNA在移植细胞基因组中的整合和表达情况
对PCR扩增产物进行的分子量鉴定结果见图1,其中只有以携带有目的基因mhANP cDNA的表达重组体质粒pLHY24为模板的阳性对照组 (泳道2) 和以被表达重组体 pLHY24逆转录病毒颗粒感染的SHR新生鼠皮肤成纤维细胞的基因组DNA为模板的试验组 (泳道 5),其 PCR产物中才含有特定分子量的扩增片段,而在以空载体质粒pLNCX (泳道1) 或被空载体病毒颗粒感染的细胞基因组 DNA为模板(泳道4) 时,则没有任何扩增产物存在。这提示目的基因mhANPcDNA整合进了移植细胞的基因组。对移植细胞的培养液上清进行放免法检测时所获结果与此一致,即只有基因组中整合了目的基因mhANPcDNA的移植细胞才能有效表达 mhANP多肽,106个细胞在.24 h内的表达水平为 (13.37 ± 2.36) ng。
2.2 mhANP表达细胞移植对SHR大鼠血浆ANP浓度的影响
针对ANP进行的放免法检测结果见表1。可以看出,与空载体组动物血浆中的ANP浓度相比,在细胞移植7 d后,实验组动物血浆中的ANP浓度显著高于空载体组 (P<0.01)。虽然这种差异的显著性从第14天起就消失了,但实验组动物血浆中的ANP浓度在未来几周里却始终保持在一个相对较高的水平。该结果表明,由移植到动物皮下的 mhANP表达细胞表达和分泌的 mhANP多肽可顺利进入动物的血循环。
2.3 mhANP表达细胞移植对 SHR大鼠血压的影响
与动物血浆中ANP浓度的情况一致,虽然实验组动物的血压也会随个体发育而不断升高,但其血压值在细胞移植后的49 d内却始终显著低于空载体组 (表2),其中又以第14天时的差距最大,达33 mm Hg (P<0.01)。该结果表明,由mhANP表达细胞表达和分泌的 mhANP多肽不但能顺利进入动物的血循环,而且还能正常发挥其降血压的生物学活性。该结果提示,尽管人与大鼠的ANP之间存在着一定的种属差异,然而这种差异尚不足以影响人ANP功能的发挥。

图 1 PCR检测突变型人心钠素 cDNA在遗传工程细胞基因组中的整合情况Fig.1 Integration of mhANP cDNA in the genome of the cell line genetically engineered to express and secrete mhANP. 1: the PCR template was retroviral empty vector pLNCX; 2: the PCR template was retroviral vector pLHY24 carrying mhANP cDNA;3: DNA marker; 4: the PCR template extracted from the infant rat skin fibroblast line infected with retroviral empty vector pLNCX;5: the PCR template was extracted from the infant rat skin fibroblast line infected with retroviral vector pLHY24 carrying mhANP cDNA.
2.4 mhANP表达细胞移植对 SHR大鼠尿量的影响
对动物尿量的监测结果见表 3。可以看出,与血浆中的ANP浓度和血压的情况一致,在实验开始后的第7天和第14天,实验组动物的尿量都显著高于空载体组 (P<0.01)。该结果表明,由mhANP表达细胞表达和分泌的 mhANP多肽还能正常发挥其利尿活性,并且再次提示,人与大鼠ANP之间的种属差异尚不足以阻止人ANP功能的发挥。
2.5 mhANP表达细胞移植对 SHR大鼠体重的影响
对动物体重的监测结果见表 4。可以看出,在整个实验期间,实验组和空载体组动物的体重均不断增长,并且在两者间的差异也无显著性。这说明mhANP表达细胞的移植不会影响幼龄SHR大鼠体重的正常增长。
2.6 mhANP表达细胞移植对SHR尿中Na+、K+离子浓度的影响
对动物尿液中 Na+、K+离子浓度的监测结果见表5和表6。可以看出,在整个实验期间,mhANP表达细胞的移植对幼龄SHR尿中Na+、K+离子浓度无显著影响。
表1 mhANP表达细胞移植对SHR大鼠血浆ANP浓度的影响 (nmol/L,±s)Table 1 Effect of transplantation of the cell line genetically engineered to express and secrete mhANP on the ANP concentration in serum
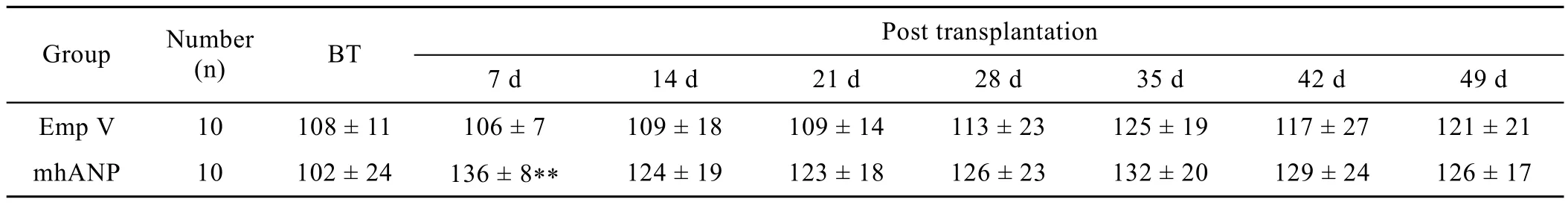
表1 mhANP表达细胞移植对SHR大鼠血浆ANP浓度的影响 (nmol/L,±s)Table 1 Effect of transplantation of the cell line genetically engineered to express and secrete mhANP on the ANP concentration in serum
Emp V: empty vector; BT: before transplantation. ∗∗P< 0.01vsempty vector.
Post transplantation Group Number(n) BT 7 d 14 d 21 d 28 d 35 d 42 d 49 d Emp V 10 108 ± 11 106 ± 7 109 ± 18 109 ± 14 113 ± 23 125 ± 19 117 ± 27 121 ± 21 mhANP 10 102 ± 24 136 ± 8∗∗ 124 ± 19 123 ± 18 126 ± 23 132 ± 20 129 ± 24 126 ± 17
表2 mhANP表达细胞移植对SHR大鼠血压的影响 (mm Hg,±s)Table 2 Effect of transplantation of the cell line genetically engineered to express and secrete mhANP on blood pressure

表2 mhANP表达细胞移植对SHR大鼠血压的影响 (mm Hg,±s)Table 2 Effect of transplantation of the cell line genetically engineered to express and secrete mhANP on blood pressure
Emp V: empty vector; BT: before transplantation. ∗P< 0.05; ∗∗P< 0.01vsempty vector.
Post transplantation Group Number(n) BT 7 d 14 d 21 d 28 d 35 d 42 d 49 d Emp V 10 147 ± 6 145 ± 8 157 ± 9 169 ± 6 166 ± 7 181 ± 8 183 ± 10 189 ± 12 mhANP 10 148 ± 8 131 ± 9 ∗∗ 124 ±12∗∗ 152 ± 9∗∗ 154 ± 8∗∗ 163 ± 9∗∗ 170 ± 8∗∗ 175±10∗
表3 mhAnP表达细胞移植对SHR大鼠尿量的影响 (mL/6 h,±s)Table 3 Effect of transplantation of the cell line genetically engineered to express and secrete mhANP on urine volume

表3 mhAnP表达细胞移植对SHR大鼠尿量的影响 (mL/6 h,±s)Table 3 Effect of transplantation of the cell line genetically engineered to express and secrete mhANP on urine volume
Emp V: empty vector; BT: before transplantation. ∗∗P< 0.01vsempty vector.
?
表4 mhNAP表达细胞移植对SHR大鼠体重的影响 (g,±s)Table 4 Effect of transplantation of the cell line genetically engineered to express and secrete mhANP on urine volume

表4 mhNAP表达细胞移植对SHR大鼠体重的影响 (g,±s)Table 4 Effect of transplantation of the cell line genetically engineered to express and secrete mhANP on urine volume
Emp V: empty vector; BT: before transplantation.
Post transplantation Group Number(n)BT 7 d 14 d 21 d 28 d 35 d 42 d 49 d Emp V 10 92 ± 15 117 ± 14 138 ± 12 164 ± 28 170 ± 32 194 ± 35 205 ± 37 219 ± 43 mhANP 10 90 ± 16 114 ± 16 134 ± 18 154 ± 30 169 ± 35 178 ± 39 189 ± 34 206 ± 35
表5 mhANP表达细胞移植对SHR大鼠尿Na+浓度的影响 (mmol/L,±s)Table 5 Effect of transplantation of the cell line genetically engineered to express and secrete mhANP on urine Na+
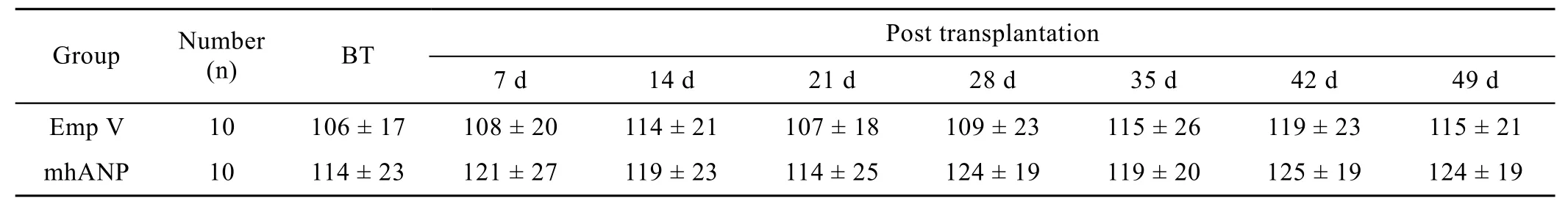
表5 mhANP表达细胞移植对SHR大鼠尿Na+浓度的影响 (mmol/L,±s)Table 5 Effect of transplantation of the cell line genetically engineered to express and secrete mhANP on urine Na+
Emp V: empty vector; BT: before transplantation.
Post transplantation Group Number(n) BT 7 d 14 d 21 d 28 d 35 d 42 d 49 d Emp V 10 106 ± 17 108 ± 20 114 ± 21 107 ± 18 109 ± 23 115 ± 26 119 ± 23 115 ± 21 mhANP 10 114 ± 23 121 ± 27 119 ± 23 114 ± 25 124 ± 19 119 ± 20 125 ± 19 124 ± 19
表6 mhANP表达细胞移植对SHR大鼠尿K+浓度的影响 (mmol/L,±s)Table 6 Effect of transplantation of the cell line genetically engineered to express and secrete mhANP on urine K+

表6 mhANP表达细胞移植对SHR大鼠尿K+浓度的影响 (mmol/L,±s)Table 6 Effect of transplantation of the cell line genetically engineered to express and secrete mhANP on urine K+
Emp V: empty vector; BT: before transplantation.
Post transplantation Group Number(n) BT 7 d 14 d 21 d 28 d 35 d 42 d 49 d Emp V 10 102 ± 20 115 ± 19 122 ± 17 116 ± 20 119 ± 22 124 ± 21 122 ± 21 120 ± 18 mhANP 10 99 ± 19 108 ± 17 116 ± 18 118 ± 18 114 ± 17 118 ± 19 118 ± 23 115 ± 16
3 讨论
大量基础研究和临床实践表明,ANP多肽不但能够有效治疗急性心衰,而且还具有治疗高血压和慢性心肾功能衰竭等慢性疾病的应用潜力,但是,其半衰期短和需要长时间静脉滴注才具疗效的不足却限制了其应用潜力的充分发挥[5-6]。为弥补 ANP多肽的这一不足,更为探求治疗上述慢性心血管系统疾病的新方法,笔者将药物形式由半衰期只有2.5 min的 ANP多肽改为相对稳定的 ANP基因mhANP,并引入了ex vivo基因治疗策略,即将可稳定表达和分泌 mhANP多肽的遗传工程细胞直接导入幼龄SHR大鼠体内。结果表明,该方法可显著抑制幼龄SHR大鼠血压的上升趋势和增强其肾脏的泌尿功能。
第一,人mhANP表达细胞移植于SHR大鼠皮下可有效发挥ANP多肽生理作用的基础。虽然人与大鼠的ANP之间存在着种属差异,但这种差异尚不足以阻止 ANP功能的发挥,Fürst等的工作早已证明了这一点[11],因此,本实验将人 mhANP表达细胞移植于SHR大鼠皮下可显著抑制血压的上升趋势和增强泌尿功能,关键首先在于mhANPcDNA在SHR新生鼠皮肤成纤维细胞基因组中的整合、表达和分泌,更在于 mhANP表达细胞移植后其表达产物可顺利地进入血液循环,后者表现为实验组动物血浆心钠素浓度在细胞移植 7 d后明显升高,并且在整个实验过程中 (49 d) 都处于相对较高的水平。
第二,mhANP表达细胞移植的有效性。与空载体组动物的血压相比,虽然实验组动物的血压同样会随个体发育而不断升高,但实验组动物的血压在整个实验过程中 (49 d) 都处于明显的低水平状态。而从肾功能方面来看,mhANP表达细胞移植则可显著增强动物的泌尿功能。显然,泌尿功能的改善对于动物血压上升幅度的缩小和血压状况恶化进程的推迟是有利的。
mhANP表达细胞移植一次的有效利尿作用时间和有效降血压作用时间分别为14 d和49 d,这是目前临床所用利尿剂和降压药难以企及的。就半衰期只有 2.5 min因而需长期静脉滴注才可有效治疗急性心衰的心钠素多肽来说,mhANP表达细胞移植的这种长效性无疑是一次质的飞跃。
总之,mhANP表达细胞移植具有相对高效和长效等特点,在高血压和慢性心肾功能衰竭等慢性疾病的治疗方面具有应用潜力,值得进一步研究。
REFERENCES
[1] Israili ZH, Hernández-Hernández R, Valasco M. The future of antihypertensive treatment.Am J Ther,2007,14(2): 121−134.
[2] Steinhelper ME, Cochrane KL, Field LJ. Hypertension in transgenic mice expressing atrial natriuretic factor fusion genes.Hypertension, 1990, 16(3): 301−307.
[3] John SW, Krege JH, Oliver PM,et al.Genetic decreases in atrial natriuretic peptide and salt sensitive hypertension.Science,1995, 267(5198): 679−681.
[4] Lopez MJ, Wong SK, Kishimoto I,et al.Salt-resistant hypertension in mice lacking the guanylyl cyclase-A receptor for atrial natriuretic peptide.Nature,1995,378(6552): 65−68.
[5] Lee CY, Burnett JC Jr. Natriuretic peptides and therapeutic applications.Heart Fail Rev, 2007, 12(2): 131−142.
[6] Nomura F, Kurobe N, Mori Y,et al.Multicenter prospective investigation on efficacy and safety of carperitide as a first-line drug for acute heart failure syndrome with preserved blood pressure COMPASS:arperitide effects observed through monitoring dyspnea in acute decompensated heart failure study.Circ J, 2008,72(11): 1777−1786.
[7] Lortal B, Gross F, Peron JM,et al.Preclinical study of anex vivogene therapy protocol for hepatocarcinoma.Cancer Gene Ther, 2009, 16(4): 329−337.
[8] Li T, Liang HY, Lu G,et al.Hypotensive effect of encapsulated genetically engineered fibroblasts expressing mutant atrial natriuretic peptide in hypertensive rats.Nat Med J Chin, 2002, 82(16): 1086−1089.
李涛, 梁红雁, 卢果, 等. 皮下移植心钠素表达细胞胶囊对高血压大鼠的降血压效应. 中华医学杂志, 2002,82(16): 1086−1089.
[9] E Z. Tissue Culture and Molecullar Cellular Techology.Beijing: Beijing Press, 1995: 50−70.
鄂征. 组织培养和分子细胞学技术. 北京: 北京出版社,1995: 50−70.
[10] Chao J, Jin L, Chen LM,et al. Systemic and portal vein delivery of human kallikrein gene reduces blood pressure in hypertensive rats.Hum Gene Ther, 1996, 7(8):901−911.
[11] Fürst R, Brueckl C, Kuebler WM,et al. Atrial natriuretic peptide induces mitogen-activated protein kinase phosphatase-1 in human endothelial cells via Rac1 and NAD(P)H oxidase/Nox2-activation.Circ Res, 2005, 96(1):43−53.
Transplantation of atrial natriuretic peptide-expressing fibroblasts reduces blood pressure and increases urine volume in spontaneously hypertensive rats
Tao Li, Hongyan Liang, Jinzhi Lu, Weijing Chen, and Shengdong Lu
National Laboratory of Medical Molecular Biology,Institute of Basic Medical Sciences,Chinese Academy of Medical Sciences,School of Basic Medicine,Peking Union Medical College,Beijing100005,China
Received:December 8, 2009;Accepted:March 15, 2010
Corresponding author:Shengdong Lu. Tel: +86-10-65295905; Fax: 86-10-65124876; E-mail: lusd@pumc.edu.cn

