充电电压上限对磷酸亚铁锂电化学性能的影响
郑洪河,张晓丽,张玉玺
(河南师范大学化学与环境科学学院,河南新乡453002)
作为新型锂离子电池正极材料,橄榄石型磷酸亚铁锂具有比容量高、工作电压平稳、价格低廉、稳定性好和对环境无污染等突出的特点[1],其理论比容量达170 mAh/g,放电电位平台适中(3.4 V),充放电过程中电极的结构变化小[2-4],是一种有发展前途的锂离子电池正极材料[5]。它不仅在小功率电池中获得了应用[6],而且在高功率密度的动力电池中也有很好的前景[7],因此它是制造“低成本、安全型锂离子电池”的理想材料。
然而,目前研究者对这一新型材料的充电电压上限的控制比较混乱,文献报道一般在3.7~4.1 V不等。研究充电电压上限对材料电化学性能的影响不仅有助于选择合理的充电电压,也有助于我们深入了解这种材料的过充电行为。本文通过恒电流充、放电和交流阻抗技术,研究了充电终止电压对橄榄石型LiFePO4正极材料电化学性能的影响。
1 实验
1.1 电极的制备
本实验使用的LiFePO4是由Hydro Quebec公司提供,LiFePO4、乙炔黑导电剂和电极粘结剂PVDF(质量比为80.8∶12∶7.2)分散在NMP溶剂中,高速搅拌混合均匀后在铝箔上涂膜,120℃条件下真空干燥24 h作为研究电极。
1.2 电性能测试
在充满高纯氩气的手套箱中组装三电极模拟电池,参比和辅助电极均为光亮锂箔,隔膜为Celgard 2400聚丙烯微孔膜,电解液为l mol/L LiPF6/(EC+DEC)(体积比 1∶2)。使用美国Arbin公司生产的BT2000型电池测试系统对模拟电池进行循环伏安和恒电流充放电实验。循环伏安的扫描速率为0.1 mV/s,扫描电位范围为2~4.5 V。充放电实验的充电终止电压分别为 3.5、3.7、3.9、4.1、4.3 V 和 4.5 V,化成放电终止电压均为2.5 V,倍率性能测试的终止电压为2.1 V。电压控制精度为±0.1 mV;电池化成的充、放电电流密度为 0.05C(8 mA/g),倍率性能的电流密度分别为 0.1、0.2、0.5、1、2、5、10 C和20 C,电流控制精度为±1μ A。
电化学阻抗测试使用Sorlatron 1255电化学测试系统,测试频率范围100 kHz~10 MHz。实验前,电极于40%放电深度(DOD)条件下恒压3 h以上,以保证测试过程中电极处于准电位平衡状态。
2 结果与讨论
图1为橄榄石型LiFePO4正极材料在2 V和4.5 V间前三次循环的伏安行为,扫描速率为0.1 mV/s。由图可见,在该扫描速率下,阳极过程的峰值电位在3.65 V,当电极电位达到3.70 V时,氧化峰没有完全结束,说明材料的脱锂反应仍在进行,此时终止充电过程的话,电极活性物质将不能得到充分利用,会导致该电极材料的放电容量不高。随着电极电位的逐渐升高,脱锂峰强度迅速减弱,3.9~4.0 V时电极脱锂过程已经基本结束。再继续升高电极电位,没有出现其它反应形式,电极表现为简单的极化过程。
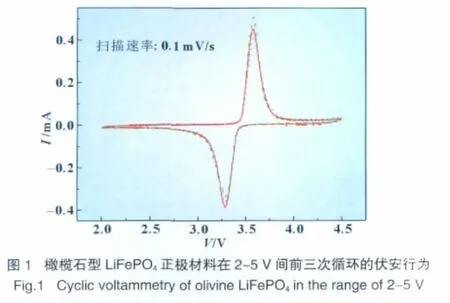
阴极过程中电极在3.5 V出现还原峰,峰值电位大约在3.4 V左右,2.5 V脱锂过程全部结束,为此,本文对LiFePO4正极材料恒电流充放电实验的放电终止电压控制在2.5 V。
为了更精确测定LiFePO4正极材料的嵌脱锂电位,我们对该电极组装的半电池在0.02C(即3.2 mA/g)的电流密度下进行首次充放电循环,由此得到电极首次循环的dQ/dV与电池电压的关系(见图2)。由图可见,在极其缓慢(准静态)的条件下进行充放电循环,LiFePO4的脱锂电位在3.45 V左右,3.48 V时脱锂反应已经全部结束,放电过程的嵌锂电位则集中在3.41 V左右,3.38 V放电过程亦全部结束,说明该材料用于锂离子电池电压平稳,过电位低。
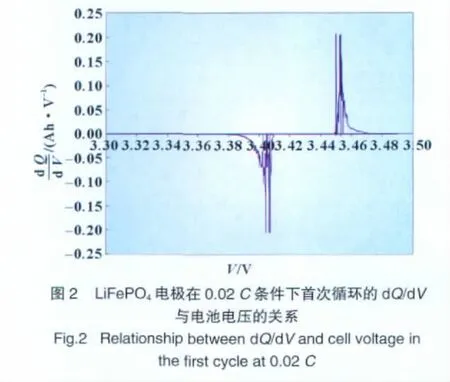
图3为橄榄石型LiFePO4电极在0.05C,不同充电电压上限时的首次恒电流充放电的实验曲线,之所以选择0.05C的电流密度是因为许多锂离子电池的充电条件是首先恒电流充电至一定电压,然后恒电压充电至电流小于0.05C结束。由图可见,电极的充电平台在3.46 V,放电平台为3.36 V,这两个平台与图2所得到的峰值电位比较接近,但与循环伏安得到的峰值电位有差别,主要是因为循环伏安实验选择的扫描速率较快,电极极化比较明显的缘故。

比较可见,在0.05C的电流密度下,充电电压上限对电池的首次充、放电容量有影响,但影响不大。充电电压上限为3.5 V时,材料的首次充电比容量为154.54 mAh/g,放电比容量为151.33 mAh/g,首次充放电的库仑效率为97.93%。充电电压上限为3.7 V时,首次充电比容量为156.8 mAh/g,放电比容量为156.79 mAh/g,首次充放电的库仑效率达到99.99%。随着充电电压上限的继续增加,电极充、放电容量也略有增长,但增长幅度很小,充放电比容量均维持在157~159 mAh/g左右。但对充电终止电压附近的充放电曲线放大后可以看出,电极充电到4.1 V后,充电曲线有平缓的趋势,说明此时发生了充电过程的副反应。副反应的形式很多,包括电解液在电极表面的氧化反应,正极材料活性物质的流失,甚至晶体结构的坍塌和转变等。一般来讲,这类副反应的出现对电极过程是不利的。从这个意义上讲,LiFePO4电极的充电电压上限不宜超过4.1 V。
图4示为橄榄石型LiFePO4电极充电至不同电压上限时的首次充电比容量和放电比容量与电压上限的关系。可见,当充电电压为3.5 V时,电极的首次充电比容量和放电比容量均有些偏低,但相差只有3 mAh/g左右,这很可能是由于电极活性物质的利用率不高。另一方面,电极过程的库仑效率也偏低,产生这种现象的原因还有待进一步考证。当充电电压上限在3.7~3.9 V时,电极的首次充电比容量和放电比容量基本上达到了其理论比容量,且电极过程的库仑效率几乎达到100%。说明在这样的充电条件下,电极过程没有明显的副反应发生,电极过程主要表现为Li的嵌脱过程。而当充电电压高于4.1 V时,电极的首次充电比容量随充电电压的升高呈现较快增长,放电比容量虽有增加,但增加很小,电极过程的库仑效率也因此逐渐降低。这主要是由于在较高电位条件下,电极过程中发生了如电解液氧化等副反应的缘故。

图5为橄榄石型LiFePO4电极充电至3.9 V化成后,0.1C的电流密度充电至3.9 V,接着在3.9 V条件下恒压充电至电流小于0.05C,然后在不同放电倍率下放电,得到该电极在2.1 V和3.9 V间充放电循环的倍率放电曲线。可见,随着放电倍率的增大,不仅电极本身的放电比容量下降,电极的放电电位平台也有明显降低,这时因为高倍率条件下电极过程阻力大的缘故。尽管如此,该电极材料在1C放电倍率下的比容量保持率达到94%,10C条件下的比容量保持率也在80%以上,说明这种材料的倍率性能是十分优异的。
LiFePO4正极材料经化成后,在各充电电压上限时的倍率性能(0.1、0.2、0.5、1、2、5、10、20C)如图 6。可以看出,充电电压上限在3.5~3.9 V之间时,电极的倍率性能变化不大,只是3.5 V时略差一些,说明此时电极的表面电阻没有因充电电压的升高而明显增长。随着充电电压上限的继续增加,电极的倍率性能开始变差,当充电电压上限达到4.3 V,特别是4.5 V时,电极从0.5C以后的倍率性能便有明显下降。这说明高充电电位条件下,电极的电阻明显增长,而电阻的增长无疑与电极过程中的副反应有关。

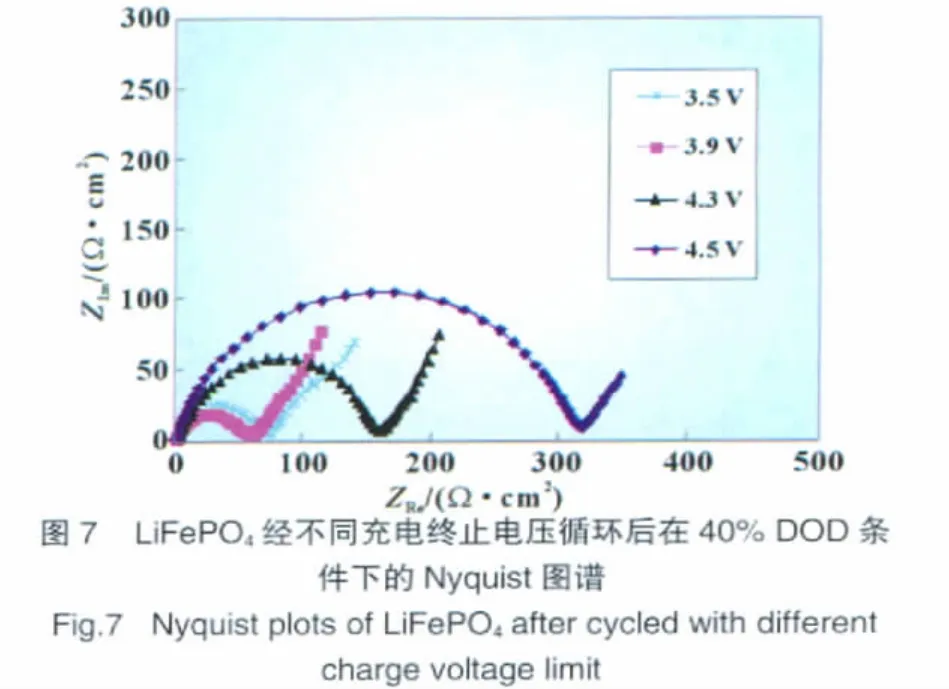
为了揭示不同充电电压条件下电极电阻的变化情况,我们对电极循环后进行了交流阻抗分析。图7示为40%DOD、30℃条件下LiFePO4经不同充电电压化成和倍率性能测试后的Nyquist图谱。可以看到,充电电压上限对电极的电阻有明显的影响,当充电电压控制在3.5~3.9 V间循环时,电极本身的电阻不大,电极电阻随充电电压上限的变化也不明显,这就解释了图6所示的在3.5~3.9 V的充电电压上限进行循环,电极倍率性能优良的原因。当充电电压超过4.3 V,甚至达到4.5 V时,电极的电阻随充电电压上限的升高明显增长,这与电极此时的倍率性能差是一致的。
3 结论
充电电压上限会影响橄榄石型正极材料磷酸亚铁锂的电化学嵌脱锂性质。比较发现,充电电压上限控制在3.5~4.5 V的范围内,对磷酸亚铁锂放电比容量的影响不大,但高电位条件下,特别是4.3 V以上易于引发电极过程的副反应,副反应会造成电极界面电阻增长,对电极的倍率性能不利。总体来看,充电电压上限控制在3.7~3.9 V之间,电极表现出较好的比容量和最佳的倍率充放电性能,这一结果对开发基于LiFe-PO4的大功率锂离子电池有指导意义。
[1]CHEN J J,WHITTINGHAM M S.Hydrothermal synthesis of lithium iron phosphate[J]Electrochem Commun,2006,8(5):855-858.
[2]OUYANG C Y,SHI S Q,WANG Z X,et al.First-principles study of Li ion diffusion in LiFePO4[J].Phys Rev B,2004,69(10):104303.1-104303.5.
[3]JIANG J,OUYANG C Y,LI H,et al.First-principles study on electronic structure of LiFePO4[J].Solid State Communications,2007,143(3):144-148.
[4]WANG Zhong-li,SU Shao-rui,YU Chun-yang,et al.Synthesises,characterizations and electrochemical properties of spherical-like Li-FePO4by hydrothermal methode[J].J Power Sources,2008,184(2):633-636.
[5]YANG S F,SONG Y N,NGALA K,et al.Performance of LiFePO4as lithium battery cathode and comparison with manganese and vanadium oxides[J].J Power Sources,2003,119-121:239-246.
[6]陈立泉.锂离子电池正极材料的研究进展[J].电池,2002,32(z1):6-8.
[7]GU Yi-jie,ZENG Cui-song,WU Hui-kang,et al.Enhanced cycling performance and high energy density of LiFePO4based lithium ion batteries[J].Materials Letters,2007,61(25):4700-4702.

