穿黄消炎胶囊的制备及质量标准研究
狄永良
(江苏省溧阳市中医院,江苏 常州 213300)
穿黄消炎胶囊由穿心莲和一枝黄花组成[1],具清热解毒之功效,用于治疗急性上呼吸道感染、急性扁桃体炎、咽喉炎等热毒壅盛证,穿心莲内酯与脱水穿心莲内酯为其主要有效成分,为进一步严格控制质量,笔者对其质量标准进行了补充研究,现报道如下。
1 仪器与试药
高效液相色谱仪(日本岛津),包括LC-10ATVP型溶剂输送泵,SPD-10AVP型紫外-可见检测器;HW-2000型色谱工作站(南京千谱软件有限公司)。脱水穿心莲内酯对照品(批号为110854-200705),穿心莲内酯对照品(批号为110797-200707),穿心莲对照药材(批号为121082-200702),一枝黄花对照药材(批号为121433-200801),均购自中国药品生物制品检定所;硅胶G和GF254(薄层色谱用,青岛海洋化工厂);甲醇为色谱纯,水为超纯水,其他试剂均为分析纯。
2 方法与结果
2.1 处方和制备
处方:穿心莲750 g,一枝黄花1 250 g,淀粉116 g,制成1 000粒。
制备:按处方量取以上2味药材,将穿心莲200 g粉碎成细粉,其余穿心莲与一枝黄花一起加水煎煮2次,第1次2h,第2次1.5 h,合并煎液,滤过,滤液浓缩成相对密度为1.14~1.16(85℃)的清膏,放冷,加乙醇成含醇量为60%,搅拌,静置48 h,滤过,滤液浓缩成相对密度为1.31~1.35(60~80℃)的稠膏,加入上述穿心莲细粉及淀粉,混匀,干燥,粉碎成细粉,混匀,装入胶囊,即得。
2.2 一般质量控制
性状:本品为胶囊剂,内容物为灰绿色的粉末,味苦。
检查:应符合2005年版《中国药典(一部)》附录ⅠD胶囊剂项下各有关规定。
2.3 薄层色谱鉴别
穿心莲:参考穿黄消炎片质量标准和2005年版《中国药典(一部)》[2]穿心莲项下鉴别方法。取本品内容物1 g,加乙醇20 mL,加热回流30 min,滤过,滤液浓缩至1 mL,即得供试品溶液。取穿心莲对照药材1 g,按供试品溶液制备方法制备,即得对照药材溶液。取脱水穿心莲内酯、穿心莲内酯对照品,加无水乙醇制成每1 mL各含1 mg的混合溶液,即得对照品溶液。取不含穿心莲的阴性样品1 g,按供试品溶液制备方法制备,即得阴性对照品溶液。照薄层色谱法试验,吸取上述4种溶液各5 μL,分别点于同一以羧甲基纤维素钠为黏合剂的硅胶GF254薄层板上,以氯仿-醋酸乙酯(4∶5)为展开剂,展开,取出,晾干,置紫外光灯(254 nm)下检视。结果供试品溶液色谱中,在与对照药材溶液色谱和对照品溶液色谱相应位置上分别显相同颜色的斑点,阴性对照品溶液无干扰(图 1 A)。
一枝黄花:取本品内容物4 g,加甲醇-水(1∶1)60 mL加热回流1 h,趁热滤过,滤液浓缩至约20 mL,加水10 mL,再加稀硫酸约0.5 mL,继续回流1 h,放冷,用醋酸乙酯振摇提取2次,每次30 mL,合并醋酸乙酯液,蒸干,残渣加甲醇1 mL使溶解,即得供试品溶液。取一枝黄花对照药材6 g,按供试品溶液制备方法制备,即得对照药材溶液。取不含一枝黄花的阴性样品4 g,按供试品溶液制备方法制备,即得阴性对照品溶液。照薄层色谱法试验,吸取上述3种溶液各10 μL,分别点于用1%氢氧化钠溶液制备的硅胶G薄层板上以甲苯-醋酸乙酯 -甲酸(5∶4∶1)为展开剂,喷以1%三氯化铝乙醇溶液,热风吹干置紫外光灯(365 nm)下检视。供试品溶液色谱中,在与对照药材溶液色谱相应位置上显相同颜色的荧光主斑点,阴性对照品溶液无干扰(图 1 B)。

图1 薄层色谱图
2.4 含量测定[3]
2.4.1 色谱条件与系统适用性试验
色谱柱:Shim-packVP-ODS柱(150mm×4.6 mm,5 μm);流动相:甲醇 -水(55 ∶45);检测波长:250 nm;流速:1.0 mL/min;灵敏度:0.02 AUFS。在上述条件下,脱水穿心莲内酯和样品中其他组分色谱峰达到基线分离,理论板数按脱水穿心莲内酯峰计算应不低于4 000。色谱图见图2。
2.4.2 溶液制备
取本品内容物适量,混匀,取约1 g,精密称定,置锥形瓶中,精密加入40%甲醇 50 mL,称定质量,浸泡 1 h,超声(功率160 W,频率40 kHz)处理30 min,放冷,再称定质量,用40%甲醇补足减失的质量,摇匀,滤过,精密量取续滤液10 mL,置中性氧化铝柱(200~300 目,5 g,内径 1.5 cm)上,用甲醇20 mL洗脱,收集洗脱液,蒸干,用甲醇溶解,转移至10 mL量瓶中,加甲醇稀释至刻度,摇匀,用微孔滤膜(0.45 μm)滤过,取续滤液,即得供试品溶液。取不含穿心莲的阴性样品,同法制备阴性对照品溶液。精密称取脱水穿心莲内酯对照品15.0 mg,置50 mL量瓶中,加甲醇溶解并稀释至刻度,摇匀,作为对照品贮备液;精密吸取该液适量,置10 mL量瓶中,加甲醇稀释至刻度,摇匀,作为对照品溶液。

图2 高效液相色谱图
2.4.3 方法学考察
干扰试验:分别吸取供试品溶液、阴性对照品溶液及对照品溶液各10 μL,注入液相色谱仪,进行测定。结果色谱图中在脱水穿心莲内酯峰位置无其他干扰出现(图2)。
标准曲线制备:分别精密吸取对照品贮备液 1,2,3,4,5 mL,置10 mL量瓶中,加甲醇稀释至刻度,摇匀,吸取10 μL,注入高效液相色谱仪测定峰面积。以对照品质量浓度(X)对峰面积积分值(Y)进行线性回归,得回归方程 Y=7 673 873.333 33 X-7 858.6,r=0.999 9(n=5)。结果表明,脱水穿心莲内酯质量浓度在0.03~0.15 g/L范围内与峰面积积分值有良好的线性关系。
精密度试验:精密吸取对照品溶液(0.12 g/L)10 μL,按上述色谱条件,连续进样6次。结果平均峰面积积分值为918 952,RSD=0.54%(n=6),表明方法精密度良好。
稳定性试验:精密吸取同一批(批号为080101)供试品溶液,按上述色谱条件,分别在 0,1,2,3,4,5,6,7,8,24 h 时进样测定。结果平均峰面积积分值为795 830,RSD=0.53%(n=10),表明供试品溶液24 h内基本稳定。
重复性试验:取同一批(批号为080101)供试品,按样品含量测定方法操作,平行制备5份,按上述色谱条件测定含量。结果脱水穿心莲内酯平均含量为1.99 mg/粒,RSD=1.3%(n=5),表明方法重复性良好。
加样回收试验:精密称取已知含量的样品(批号为080101,含量为1.99 mg/粒)适量,精密加入质量浓度为0.5 g/L的脱水穿心莲内酯对照品溶液5 mL,依法测定其含量,计算回收率。结果见表1。
2.4.4 样品含量测定
分别精密吸取供试品溶液和对照品溶液10 μL,注入液相色谱仪,测定峰面积,计算含量。结果见表2。根据10批样品的检测结果,结合穿黄消炎片标准中脱水穿心莲内酯含量测定限度规定,暂订本品每粒含穿心莲以脱水穿心莲内酯(以C20H28O4计)不得少于1.40 mg。
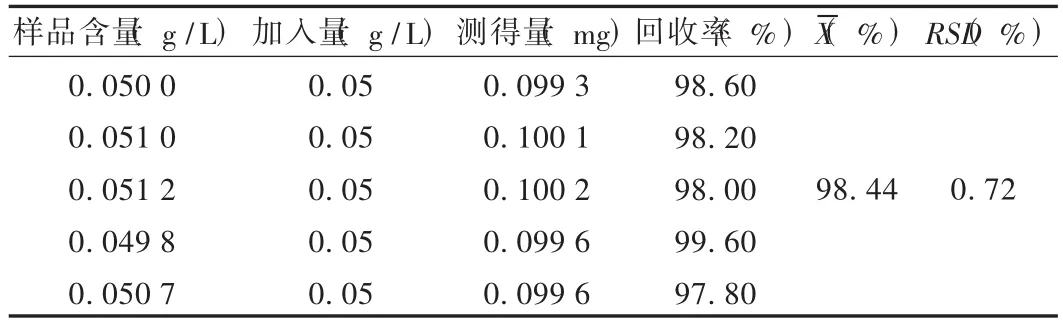
表1 脱水穿心莲内酯加样回收试验结果(n=5)

表2 样品含量测定结果(n=10)
3 讨论
对脱水穿心莲内酯对照品的甲醇溶液进行紫外扫描,发现其在250 nm波长处有强吸收,与2005年版《中国药典(一部)》中穿心莲含量测定项下脱水穿心莲内酯检测波长254 nm接近,故选择250 nm作为检测波长。
脱水穿心莲内酯易溶于甲醇、乙醇或含水甲醇、含水乙醇,故样品制备可采用一定浓度的甲醇或乙醇作为提取溶剂。原穿黄消炎片质量标准中含量测定项下样品制备采用70%乙醇浸渍过夜,因脂溶性成分和叶绿素较多,故采用正己烷振摇提取,脱去脂溶性成分和叶绿素,处理步骤较烦琐。参考2005年版《中国药典(一部)》穿心莲药材含量测定项下样品制备方法,采用40%甲醇超声提取,脂溶性成分和叶绿素提出较少,可省去正己烷振摇提取脱脂溶性成分和叶绿素步骤。对供试品溶液制备过程中超声时间(15,30,45,60 min)及柱洗脱溶剂体积(10,20,30,40 mL)分别进行考察,结果超声提取30 min、洗脱溶剂用量为20 mL时含量基本不再增加,最终确定超声时间为30 min,柱洗脱用甲醇体积为20 mL。
曾参考原穿黄消炎片质量标准项下一枝黄花的鉴别进行试验,供试品溶液色谱中,在与对照药材溶液色谱相应位置上显相同颜色的荧光斑点,阴性对照品溶液无干扰。但供试品溶液和对照药材溶液色谱清晰度均较差,经加大点样量,斑点仍不够清晰。色谱照片较难拍摄清晰。改用文中所述方法进行试验后,荧光斑点清晰易辨。
[1]中华人民共和国卫生部药典委员会.中华人民共和国药典(一部)[M].北京:人民卫生出版社,1977:1.
[2]国家药典委员会.中华人民共和国药典(一部)[M].北京:化学工业出版社,2005:189-190.
[3]WS-11053(ZD-1053)-2002,国家中成药标准汇编(中成药地方标准上升国家标准部分)内科肺系(一)分册[S].

