胱氨酸改性TiO2可见光下催化活性及催化机理
于秀娟程修文
(1黑龙江大学环境科学与工程系,哈尔滨 150080)
(2黑龙江省普通高等学校高效转化的化工过程与技术重点实验室,哈尔滨 150080)
胱氨酸改性TiO2可见光下催化活性及催化机理
于秀娟*,1,2程修文1
(1黑龙江大学环境科学与工程系,哈尔滨 150080)
(2黑龙江省普通高等学校高效转化的化工过程与技术重点实验室,哈尔滨 150080)
以胱氨酸为掺杂剂,采用溶胶-凝胶法制备了胱氨酸改性的TiO2可见光催化剂,并对其进行了TG-DTA、XRD、表面光电压光谱(SPS)及XPS表征。XRD结果表明,胱氨酸有效抑制了TiO2晶粒的生长,提高了锐钛矿向金红石相的转变温度。SPS分析结果显示,改性TiO2光催化剂可见光吸收增强,吸收带边明显红移,且胱氨酸用量为4.2%的样品光伏响应强度最大。XPS分析结果表明,胱氨酸改性TiO2样品表面的羟基含量明显增加,且O2p价带的VMB(价带最大值)值为2.3 eV,小于非改性TiO2。以罗丹明B为模型污染物,考察了胱氨酸掺杂量与焙烧温度对改性TiO2在可见光下催化性能。结果表明,胱氨酸掺杂量(相对TiO2)为4.2%、350℃焙烧的催化剂催化活性最好。波长为380~630 nm、470~800 nm的光辐射120 min后,罗丹明B的降解率分别达到 91.02%、78.44%。
光催化;TiO2;胱氨酸;罗丹明B
随着社会经济的飞速发展,环境污染控制与治理成为人类亟待解决的重大课题。TiO2因其高效、廉价、耐光和化学腐蚀而成为研究的热点,但其也存在着一些缺陷:TiO2属宽隙半导体,带隙能为3.2 eV,只能响应λ≤387.5 nm的紫外光等缺点。而紫外光仅占太阳光谱的4~6%左右[1],通过改性提高TiO2对太阳光的利用率成为了当今研究的热点。传统的TiO2光催化剂改性方法主要有:金属离子掺杂、染料光敏化和半导体复合等。虽然它们在一定程度上能提高对可见光的利用率,但也存在着光催化剂稳定性的降低、敏化剂稳定性的下降以及载流子复合中心的增多等缺陷,而非金属离子掺杂在提高TiO2光催化活性上表现出优越的条件。Asahi等[2]在nN2/nAr比为2∶3氛围中溅射TiO2靶,在N2氛围下在500℃煅烧4 h制备TiO2-xNx光催化剂薄膜。在可见光(波长低于500 nm)照射下,TiO2-xNx对亚甲基蓝的光催化活性显著提高。密度函数理论(DFT)计算表明,N掺杂纳米TiO2对可见光响应系Ti-N晶格间的半导体带隙降低所致。刘守新等[3]以TiCl4和(NH4)2SO4为原料,采用酸催化水解法合成TiO2前驱体,并在NH3/N2气氛下制得不同焙烧温度的N掺杂TiO2(TON)光催化剂。在紫外光区、可见光区以及太阳光下降解苯酚表现出较高的光催化活性。唐玉朝[4]、任凌[5]等报道了N掺杂TiO2光催化剂具有很好的可见光催化活性。王永强等[6]采用钛酸丁酯(TNB)和硫脲为原料,利用加热法制备了具有可见光催化活性的光催化剂S/TiO2。XPS结果表明:S/TiO2中S通过置换晶格中金属离子Ti4+以形成S6+阳离子。表面光电压光谱(SPS)结果表明:S/TiO2仍为n型半导体,其吸收带边红移至550 nm。模拟太阳光下降解苯甲酸的试验结果表明:S/TiO2在可见光下的催化活性是未改性TiO2的2.7倍。王玉萍等[7]采用改进的sol-gel制备S-TiO2光催化剂,对L-酸的降解表明了改性光催化剂具有良好的紫外和可见光催化活性。由于单元素掺杂容易引起电荷的不平衡,由此产生的缺陷成为电子-空穴对的湮灭中心,降低其光催化性能[8]。因此国内外很多研究者采用非金属元素共掺改性来提高TiO2光催化剂的催化活性,并取得了一定得效果。Yu等[9]以 Ti(SO4)2和 NH3·H2O为原料,采用水热法合成N、S共掺杂改性纳米TiO2光催化剂。光催化降解丙酮和甲醛的实验证明,该催化剂在保持了紫外光催化活性的同时,太阳光照射下的去除率是Degussa P25 TiO2的10倍。Xie等[10]采用硫脲为掺杂剂,利用化学法制备了具有可见光催化活性的N、S共掺杂改性的TiO2光催化剂。在可见光(λ≥420 nm)下降解亚甲基蓝的光催化效率是Degussa P25 TiO2的 3 倍。Wei[11]、Rengifo-Herrera[12]等也报道了以硫脲为掺杂剂制备的N、S共掺杂TiO2光催化剂具有良好的可见光催化效果。但其也存在诸多缺点,例如制备过程中释放出有毒有害气体、需要较高的焙烧温度等等。
本工作利用钛酸四丁酯为钛源,以相对环境友好型的胱氨酸(C6H12N2O4S2)为掺杂剂,采用溶胶-凝胶法制备了胱氨酸改性的TiO2可见光催化剂,并对其进行了TG-DTA、XRD、XPS及SPS表征。以罗丹明B为模型污染物,分别考察了可见光下胱氨酸用量与焙烧温度对罗丹明B的降解效果。
1 实验部分
1.1 光催化剂的制备
将10 mL无水乙醇滴加到溶解有一定量胱氨酸的10 mL去离子水溶液和2 mL浓硝酸的混合液中,待搅拌均匀后迅速将其转移至60 mL分液漏斗中备用,记为A液。将10 mL钛酸四丁酯滴加至40 mL无水乙醇和1.0 mL冰醋酸的混合液中开展水解,待滴加完毕后再继续搅拌30 min,制得B液。强力搅拌下,将A液以1 mL·min-1的速度控速滴加至B液,滴加完毕后继续搅拌60 min。室温静置陈化6 h,再于80℃烘箱下干燥36 h后研磨,装入水平石英管式反应器中,接着以3℃·min-1升温至350℃焙烧4 h制得了胱氨酸改性的TiO2纳米粒子。重复以上过程,只是在10 mL去离子水中不添加胱氨酸,其余步骤相同,同样制得未掺杂改性的TiO2纳米粒子。
1.2 光催化剂表征
采用美国Perkin Elmer的TGA-7和DTA-1700型热分析仪对所制样品进行TG-DTA分析。载气(N2)流速为100 mL·min-1,以Al2O3作参比。采用D/maxⅢB型X-射线衍射仪(Rigaku,Japan)对样品进行物相分析,测试条件为:Cu Kα 射线(λ=0.154 18 nm),石墨单色器,管电压40 kV,电流30 mA,取样点/步长为 0.02°,扫描速度 12°·min-1。XPS 测试在 PHI-5700 型上进行,X 射线源采用 Al Kα(hⅤ=1486.6 eV)射线,以仪器污染碳C1s(Binding Energy=284.62 eV)作能量校正。SPS测试在自组装的表面光电压光谱仪上进行[13-16]。
1.3 催化剂活性测试
以罗丹明B(RhB)溶液的光催化降解来评估样品的光催化活性,降解的中间产物没有被检测。采用350W氙灯作光源,光源距反应器15 cm,用截止波长为470~800 nm的滤光片滤去紫外光和红外光部分,以获得可见光。将20 mL浓度10 mg·L-1的罗丹明B模型污染物与20 mg催化剂样品混合后避光振荡30 min,待吸附-脱附平衡后,开启氙灯光源,待5 min后光源稳定开始计时,每隔20 min取样,迅速离心后以0.22 μm微孔滤膜过滤,取上清液用北京谱析通用仪器有限公司的T6紫外-可见分光光度计通过在553 nm处的特征吸收值来检测罗丹明B的浓度,降解率可通过(C0-Ct)/C0来计算,其中C0和Ct分别为原始的和t时间的罗丹明B水溶液浓度。
2 结果与讨论
2.1 胱氨酸用量的影响
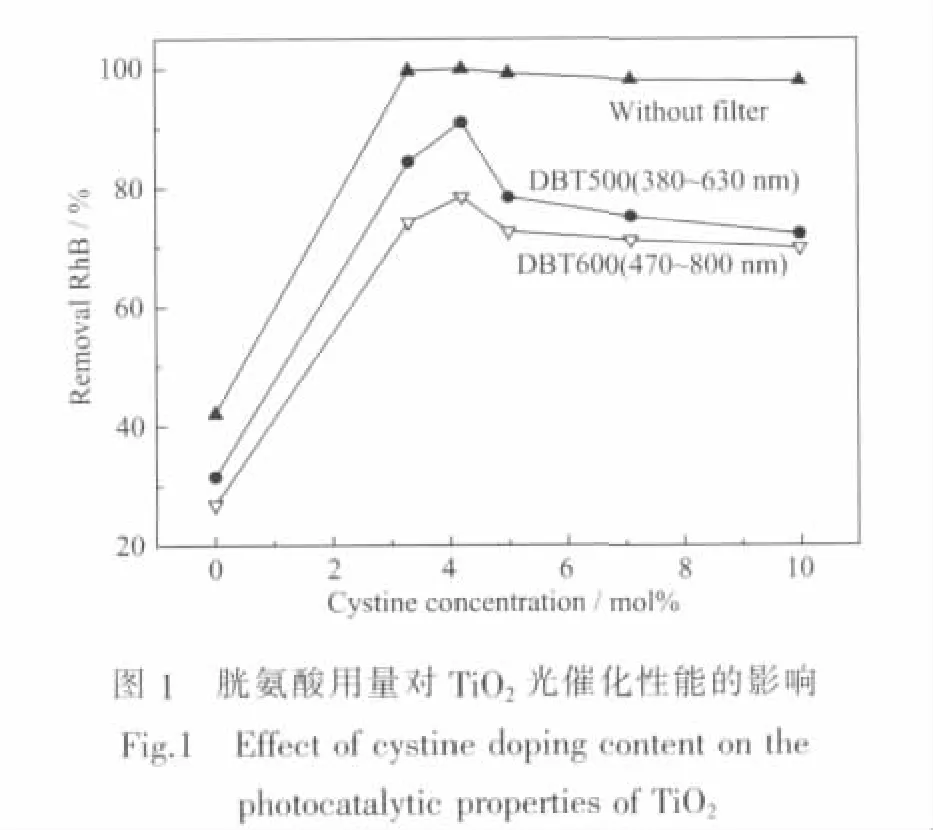
图1为不同胱氨酸改性TiO2光催化剂对对罗丹明B的降解效果。由图1可知,胱氨酸比例存在一个最佳量,当胱氨酸与钛酸四丁酯的物质的量比为 4.2%时,350℃焙烧的改性TiO2光催化活性最佳。在波长为470~800 nm光照射下,经过120 min光作用后,其对罗丹明B的降解率高达78.44%;辐照波长为380~630 nm,对罗丹明B的降解率高达91.02%;采用350 W氙灯作为光源时,对罗丹明B的降解率高达100%。
2.2 焙烧温度的影响
图2为胱氨酸比例为4.2%时,不同焙烧温度下改性TiO2对罗丹明B的降解效果。结果表明,350℃焙烧样品降解效果最佳。在波 长为380~630 nm和470~800 nm光作用下,经过120 min光照后对罗丹明B的降解效果分别达91.02%和78.44%。
图3为原料中胱氨酸物质的量的比是4.2%时改性TiO2光催化剂的TG-DTA曲线。DTA图中,在0~200℃范围内的热效应源于凝胶粉中吸附的水分和有机溶剂(乙醇、乙酸等)的挥发以及掺杂剂胱氨酸的分解脱附引起的,同时TG上有明显的失重现象。随着温度的升高,DTA图中300℃左右有一小的放热峰,对应于乙醇、乙酸等有机物的受热分解、TiO2由无定形向锐钛矿的相变[17]以及胱氨酸掺杂反应的进行。400~600℃范围内,TG上有明显失重现象,并且DTA上伴随着出现了轻微的放热峰和吸热峰,对应着残留有机官能团的氧化和少量羟基的解析。750℃左右的放热峰代表TiO2由锐钛矿型向金红石型的转变。因此,该催化剂焙烧温度应该大于300℃,但又不能过高,否则会导致粒子的团聚乃至羟基的解析以及晶型的转变。
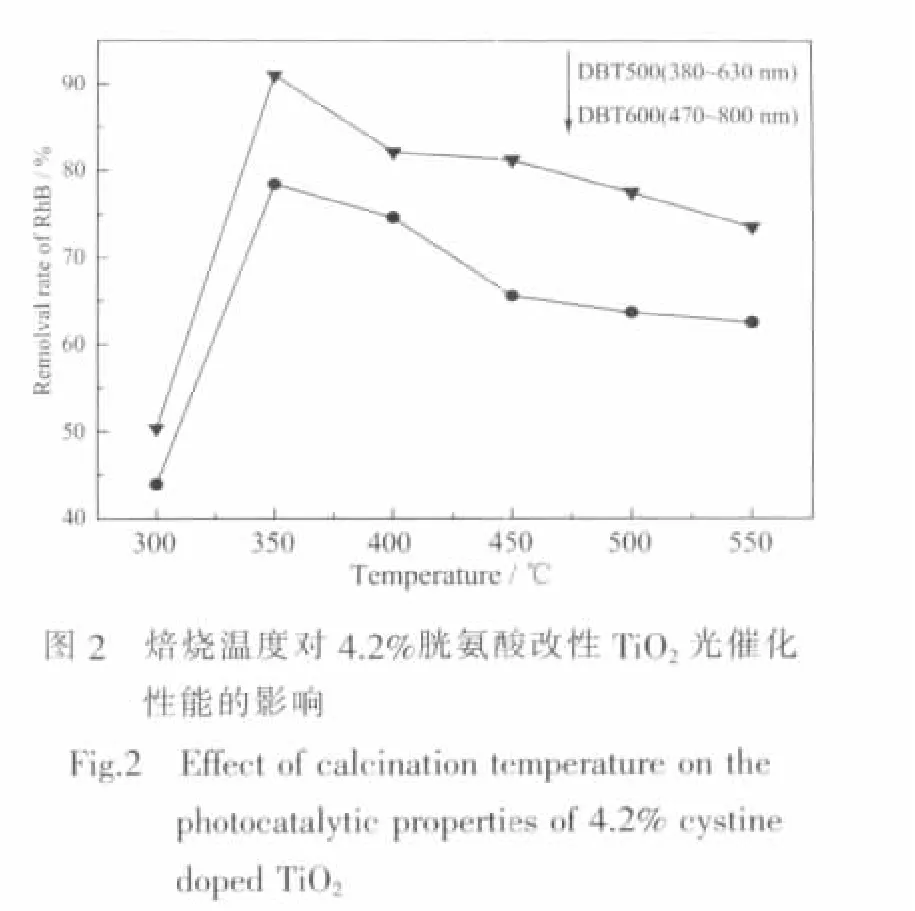
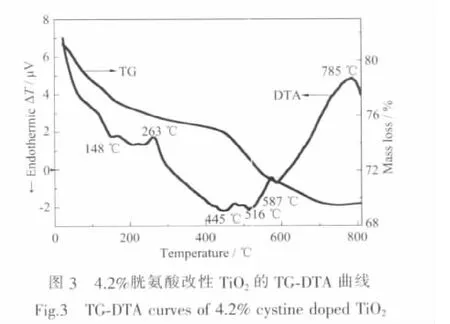
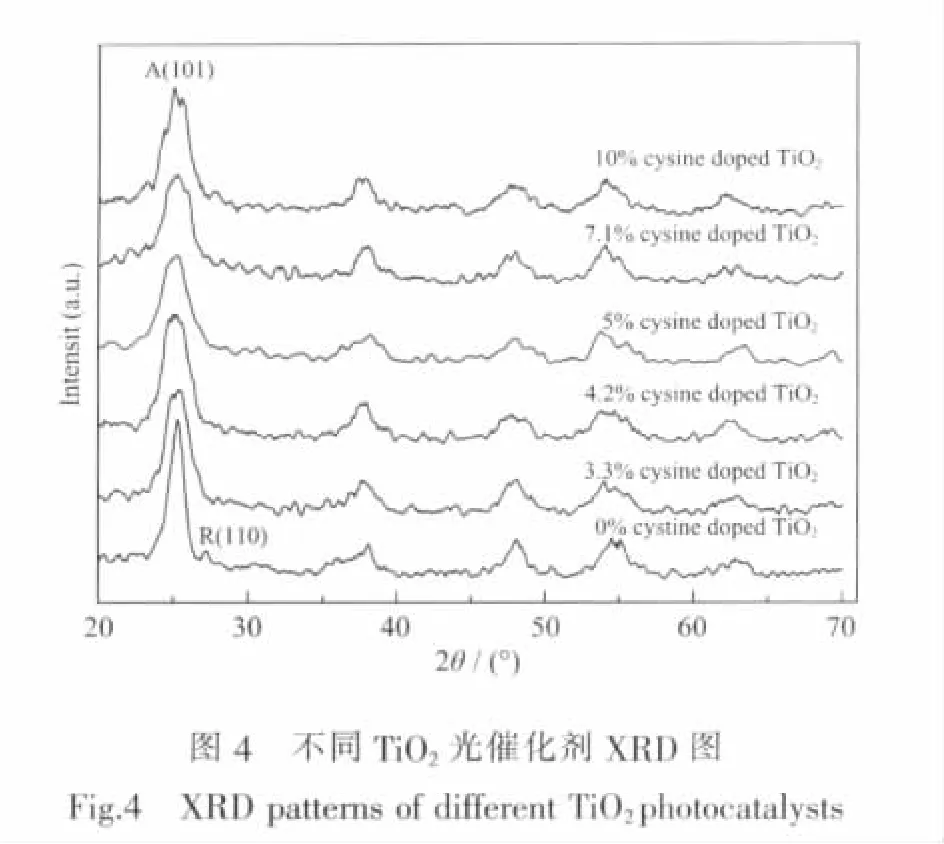
图4为350℃焙烧条件下不同胱氨酸掺杂量的改性TiO2光催化剂XRD图。从图4中可以看出,胱氨酸掺杂改性TiO2的XRD图与非改性TiO2相比有明显的变化。在 TiO2的 XRD 图中,2θ=25.28°(101面)处的衍射峰是锐钛矿的特征衍射峰,而在2θ=27.4°(110面)处的衍射峰是金红石相的特征峰[18-19]。图4中非改性TiO2为锐钛矿(A)和金红石(R)两种晶型的混晶结构,且衍射峰比较尖锐,而改性TiO2光催化剂的晶型为单一的锐钛矿型(A),且衍射峰的强度有所降低,峰形宽化。说明掺杂的胱氨酸有效的抑制了TiO2锐钛矿相向金红石相的转变,同时阻碍了晶粒的团聚。
同时胱氨酸改性TiO2的XRD图中未出现因胱氨酸掺杂引起的新衍射峰,也未出现TiO2衍射峰的移动现象,说明胱氨酸未改变TiO2的晶相结构。利用XRD特征衍射峰峰强,利用Scherrer公式可以求得晶粒尺寸D。经计算,纯TiO2纳米粒子的微晶尺寸为5.2 nm。而胱氨酸改性后的TiO2纳米粒子微晶尺寸按胱氨酸掺杂量的增加依次分别为3.4、3.3、3.1、3.1和3.1 nm。说明改性后的TiO2纳米粒子具有更小的粒径,更大的比表面积,应该具有更好的光催化活性。
2.3 胱氨酸改性TiO2催化机理分析
2.3.1 XPS分析
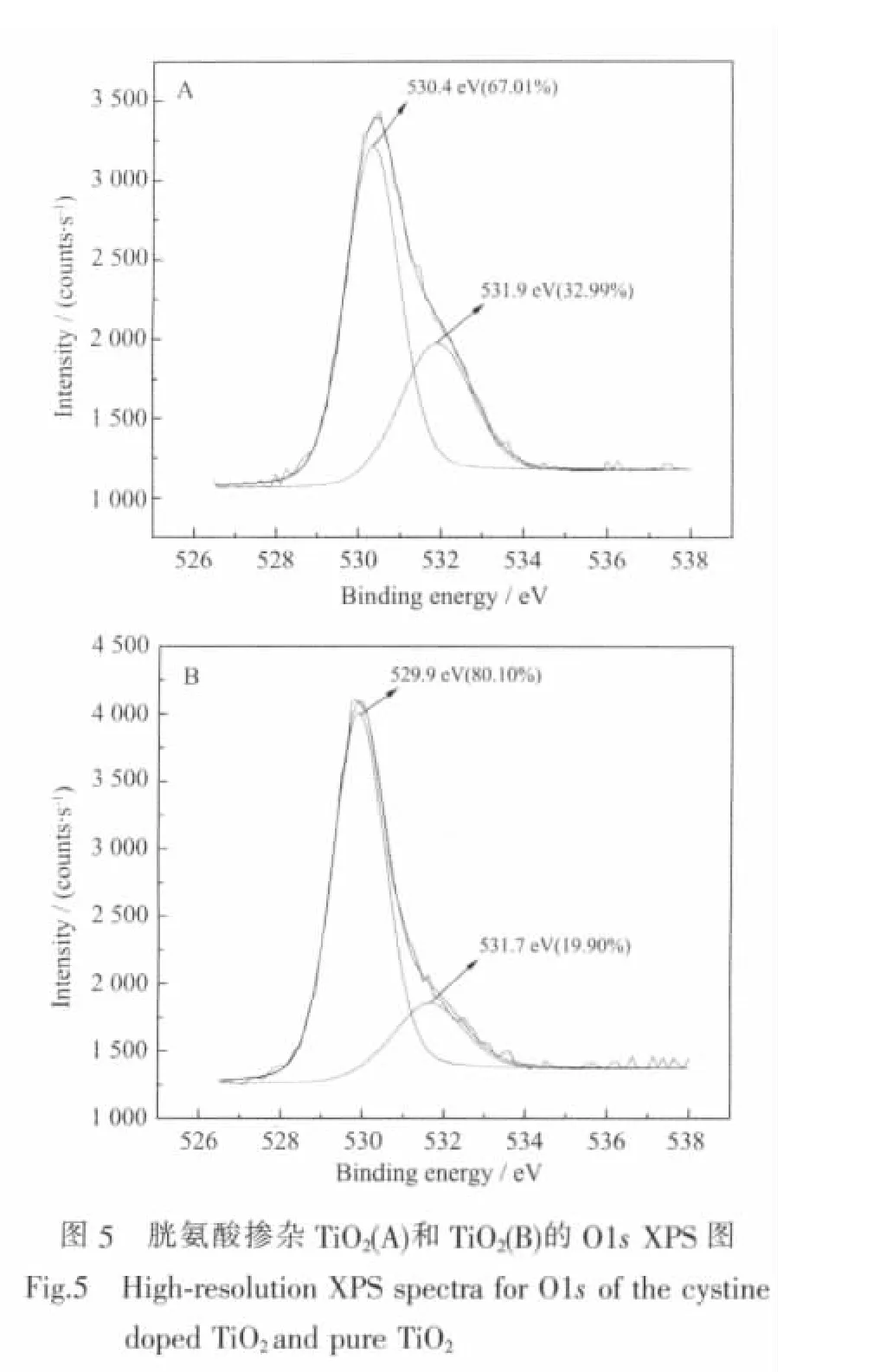
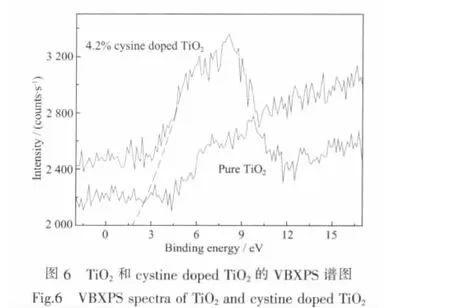
图5为4.2%胱氨酸改性TiO2(A)和纯TiO2(B)光催化剂的O1s精细扫描图。从图5可知,该光催化剂中至少存在两种氧,即晶格氧 (Ti-O)和晶格氧(-OH)。胱氨酸改性TiO2光催化的羟基氧含量为32.99%,明显高于纯TiO2光催化剂中的19.90%,羟基氧的存在对光催化活性是有益的[20],这也是胱氨酸改性后提高TiO2光催化活性的主要原因之一。为进一步研究胱氨酸改性TiO2光催化剂的电子结构,分别对4.2%胱氨酸改性TiO2和非改性TiO2光催化剂进行了VBXPS(Valence Bond X-ray Photoelectron Spectroscopy)测试,结果如图6所示。与TiO2相比,胱氨酸改性TiO2能量响应区域更低,表面更加丰富。采用线性外推法可得,胱氨酸改性TiO2光催化剂的O2p价带的VBM(Valance Bond Maximum)值为2.3 eV,比TiO2(3.2 eV)更小。这也说明改性TiO2光催化剂的价带更窄,光生电子-空穴对的分离效率更高,光催化活性更高。
2.3.2 SPS 分析
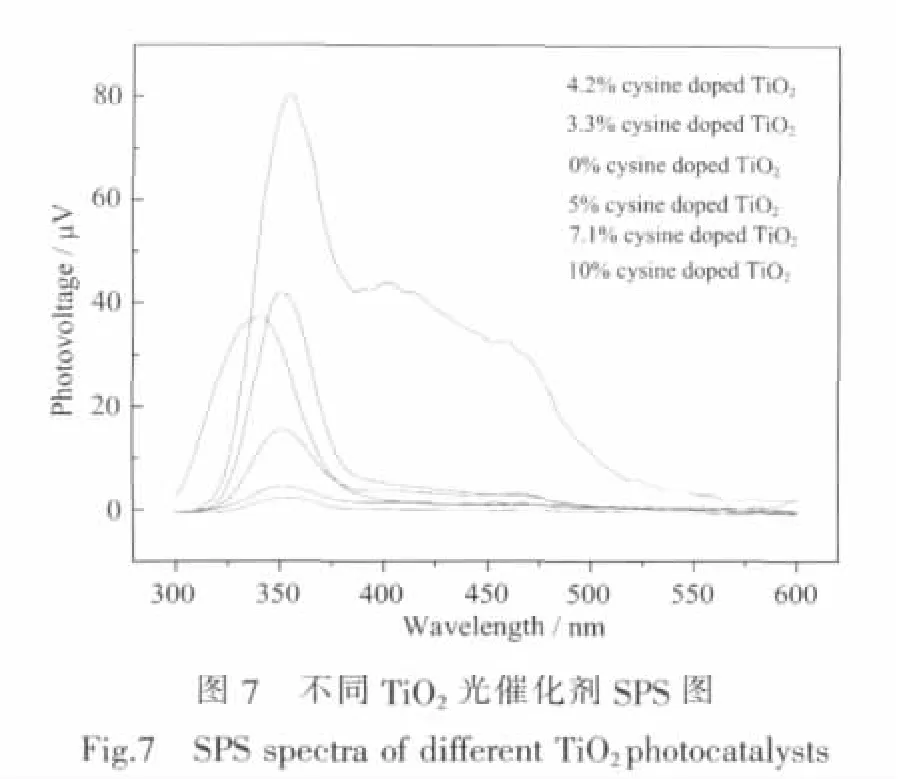
图7为不同TiO2光催化剂的SPS曲线。由图7可见,相对于非改性TiO2的最大响应波长为339 nm(O2p→Ti3d),经过胱氨酸改性的 TiO2,其吸收峰表现出明显的红移现象。并且由图可知,随着胱氨酸添加量的增加,相应改性TiO2光催化剂的SPS响应信号逐渐增强。当胱氨酸用量为4.2%时,其光伏响应信号达到最大值。此时,纳米TiO2颗粒间电荷输运势垒更小,光生电子-空穴对的分离效率更高[21],光催化能力更强,而且其可见光响应范围一直延长至570 nm。相对于非改性TiO2的300~400 nm而言,可见光响应信号的增强也进一步说明经过胱氨酸改性后的TiO2在可见光下具有良好的光催化活性。当增加原料中胱氨酸含量时,SPS信号强度依次减小,光生-电子空穴对的分离效率降低,光催化活性降低。
3 结 论
以钛酸四丁酯为前躯体,胱氨酸为改性材料,采用溶胶-凝胶法制备了胱氨酸改性的TiO2光催化剂。胱氨酸的添加,提高了催化剂表面羟基的含量,得到的改性TiO2晶粒尺寸小,控制一定焙烧温度,可以制备出全部由锐钛矿相构成的催化剂。该催化剂价带窄,O2p价带的VMB值为2.3 eV,小于非改性TiO2;可见光吸收增强,吸收带边明显红移,原料中胱氨酸物质的量比为4.2%的样品对可见光的响应强度最大,光生电子-空穴对的分离效率最高。在可见光下,胱氨酸改性TiO2对罗丹明B的光催化氧化效率高,胱氨酸含量为4.2%的改性TiO2催化活性最好,反应120 min,波长为380~630 nm、470~800 nm的光辐射120 min后,罗丹明B的降解率分别达到 91.02%、78.44%。
[1]JIAN Pan-Ming(菅盘铭),XIA Ya-Mu(夏亚穆),LI De-Hong(李德宏),et al.Chin.J.Catal.(Cuihua Xuebao),2001,22(2):161-164
[2]Asahi R,Morikawa T,Ohwaki T,et al.Science,2001,293(13):269-271
[3]LIU Shou-Xin(刘守新),CHEN Xiao-Yun(陈孝云),LI Xiao-Hui(李 晓 辉).Chinese J.Inorg.Chem.(Wuji Huaxue Xuebao),2008,24(2):253-259
[4]TANG Yu-Chao(唐玉朝),HUANG Xian-Huai(黄显怀),YU Han-Qing(俞 汉 青),et al.Chinese J.Inorg.Chem.(Wuji Huaxue Xuebao),2005,21(11):1747-1751
[5]REN Ling(任 凌),YANG Fa-Da(杨发达),ZHANG Yuan-Ming(张渊明),et al.Chinese J.Inorg.Chem.(Wuji Huaxue Xuebao),2008,24(4):541-546
[6]WANG Yong-Qiang(王永强),YU Xiu-Juan(于秀娟),YANG Hong-Fen(杨 红 芬),et al.Chinese J.Inorg.Chem.(Wuji Huaxue Xuebao),2006,22(4):771-774
[7]WANG Yu-Ping(王玉萍),CAO Jin-Li(曹金丽),PENG Pan-Ying(彭 盘 英).Chinese.J.Inorg.Chem.(Wuji Huaxue Xuebao),2009,25(11):2010-2015
[8]XING Peng-Fei(邢朋飞),WANG Jin-Shu(王金淑),JIN Jian-Xin(金建新),et al.Nanoscience&Nanotechnology,2007,4:29-33
[9]Yu J G,Zhou M H,Cheng B,et al.J.Mol.Catal.A:Chem.,2006,246:176-184
[10]Xie Y,Zhao X J.J.Mol.Catal.A:Chem.,2008,285:142-149
[11]Wei Y F,Ni L S,Cui P J.Hazard.Mater.,2008,156:135-140
[12]Rengifo-Herrera J A,Pierzchaa K,Sienkiewicz A,et al.Appl.Catal.B,2009,88:398-406
[13]Jing L Q,Xu Z L,Shang J,et al.Sol.Energy Mater.Sol.Cells,2003,79:133-151
[14]Lin Y H,Wang D J,Zhao Q D,et al.J.Phys.Chem.B,2004,108:3202-3207
[15]Xin B F,Jing L Q,Ren Z Y,et al.J.Phys.Chem.B,2005,109:2805-2809
[16]QIN Xu(秦 旭),JING Li-Qiang(井立强),XUE Lian-Peng(薛 连 鹏),et al.Chinese J.Inorg.Chem.(Wuji Huaxue Xuebao),2008,24(7):1108-1112
[17]Amoresj M G,Escribano V S,Busca G.J.Mater Chem.,1995,5(8):1245-1249
[18]Jing L Q,Xin B F,Yuan F L,et al.J.Phys.Chem.B,2006,110:17860-17865
[19]Zhang Q H,Gao L,Guo J K.Appl.Catal.B,2000,26:207-215
[20]Maldotti A,Molinari A,Amadelli R.Chem.Rev.,2002,102(10):3811-3836
[21]ZHANG Xin-Tong(张昕彤),ZHUANG Jia-Qi(庄家骐),XU Jin-Jie(徐 金 杰),et al.Chem.J.Chinese Universities(Gaodeng Xuexiao Huaxue Xuebao),1999,20:1945-1947
Mechanism and Photocatalytic Activity of Cystine-Modified TiO2with Visible-Light Response
YU Xiu-Juan*,1,2CHENG Xiu-Wen1
(Department of Environmental Science and Engineering,Heilongjiang University,Harbin 150080)
(2Key Laboratory of Chemical Engineering Process&Technology for High-efficiency Conversion,College of Heilongjiang Province,Harbin 150080)
TiO2nano-particles modified by cystine were prepared through a sol-gel procedure using cystine as the doping species and characterized by TG-DTA,XRD,Surface Photo-voltage Spectroscopy (SPS)and XPS.The XRD results show that cystine added in TiO2preparation could effectively restrain the growth of crystallite and enhance the temperature of phase transformation.SPS results indicate that the light absorbance edge of cystine modified TiO2nano-particles is obviously red-shifted to visible-light and the strongest signal intensity of photovoltaic response is given by modified TiO2nano-particle with 4.2%cystine.XPS analysis implies that the content of surface hydroxyl increases significantly and VBM(Valance Bond Maximum)of O2p is 2.3 eV.The effects of calcination temperature and cystine content on the visible-light photocatalytic performance of modifed TiO2for degrading RhB were investigated.The modified TiO2calcined at 350℃with 4.2%cystine content exhibits the best photocatalytic performance.When the irradiation wavelengths are 380~630 nm and 470~800 nm,the removal rate for RhB could achieve 91.02%and 78.44%,respectively.
photocatalytic;TiO2;cystine;rhodamine B
O614.41;O613.51;O643.36
A
1001-4861(2010)12-2150-05
2010-04-12。收修改稿日期:2010-08-26。
黑龙江省高校青年学术骨干支持计划资助项目。
*通讯联系人。E-mail:hljyuxiujuan@126.com
于秀娟,女,45岁,教授;研究方向:环境催化及清洁生产。

