创伤后应激障碍大鼠海马组织 5-HT1受体 mRNA的表达
王 芳
PTSD是指受到异乎寻常的威胁或受到巨大灾难所致的心理创伤,导致出现长期持续性精神障碍[1,2],近年来成为研究和关注的焦点。5-HT受体(5-HT receptor)与焦虑、双相情感精神障碍、冲动行为、酒精依赖、精神分裂症等有关[3]。在 PTSD大鼠5-HT受体研究结果不一[4,5]。本实验通过复制PTSD模型,提取大鼠海马总 RNA,应用 RT-PCR方法检测 5-HT受体各亚型的表达,探讨 5-HT系统在PTSD发病中的作用。
1 对象和方法
1.1 动物模型的建立 150~180g的成年雄性Wistar大鼠 35只(中国医科大学实验动物中心提供),适应性喂养 7d后,将动物随机分为对照组(10只)和模型组(25只)。模型组按照 SPS(Single-Prolonged Stress)方法复制 PTSD模型[6],将大鼠连续进行以下步骤处理:禁锢 2h;强迫性游水 20min(水深40cm,水温 25℃);休息 15min后乙醚麻醉至意识丧失。各组动物无干扰饲养,常规摄食饮水,饲养温度为 18~22℃。
1.2 实验方法
1.2.1 水迷宫(Morris water mace,MWM)实验
取对照组和模型组大鼠各 5只,分别进行定位航行实验,用于测量大鼠在水迷宫中学习记忆的能力,记录各组大鼠逃避潜伏期(EL)。
1.2.2 血清皮质醇浓度监测 水迷宫实验完成后,经大鼠心脏采血 3-5ml,3000g离心 10min,收集血清。用化学发光法检测血清皮质醇浓度。
1.2.3 海马总RNA提取和 RT-PCR 将其余5只对照组大鼠和 20只模型大鼠(SPS后 1d、4d、7d、14d)麻醉后断头取脑,在冰上快速分离海马组织,按照每 100mg加入 1mlTRIZOL试剂,充分碾磨,静止5min。加入 1/5氯仿,混匀,室温静止 3min,4℃、12000g离心 15min。将水相转入新的 EP管中,加入等体积异丙醇,混匀,室温静止 10min,4℃、12000g离心 10min。弃上清,加入用 DEPC水新鲜配制的预冷 75%乙醇,振荡洗涤 RNA,4℃、7500g离心10min。弃上清,干燥 5-10min。用无 RNase水溶解RNA,用分光光度计定量后-80℃保存。取 1μgRNA,按照 Takara公司 RNA PCR Kit(AM)Ver.3.0试剂盒说明书进行逆转录和 PCR扩增。各引物序列见表1。5-HT1A PCR扩增条件:94℃ 4min;94℃ 30s;55℃ 30s;72℃ 25s;35个循环,72℃ 8min。扩增结束后取 5μl扩增产物进行 1%琼脂糖凝胶电泳,利用天能 GIS凝胶成像系统进行观察拍照并进行积分光密度分析,以目的条带与内参照 β-actin的平均吸光度的比值表示相对表达水平,进行半定量分析。
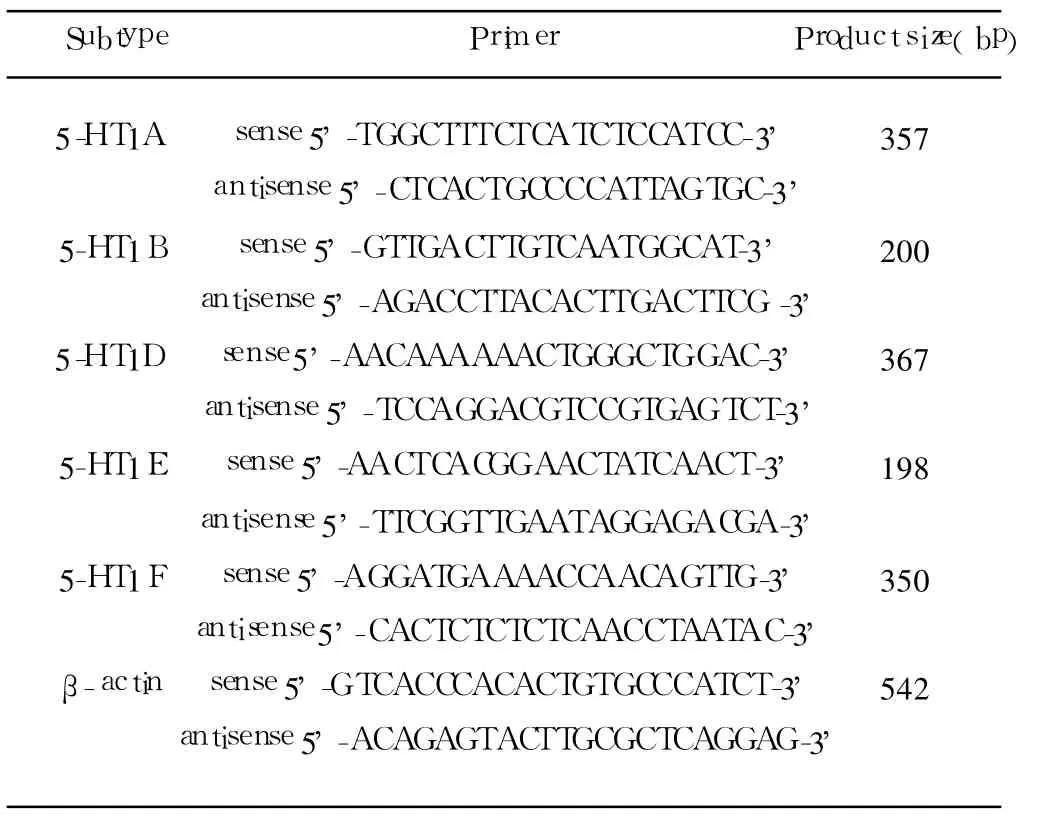
表 15-HT受体 1各亚型和β-actin PCR引物序列
1.3 统计学处理 应用 SPSS统计分析软件对数据进行统计分析,数据均以±s表示,进行方差分析和 t检验,P<0.05为差异具有统计学意义。
2 结 果
2.1 MWM实验结果 结果显示,对照组与模型组大鼠平均逃避潜伏期分别为 5.632s±1.065s、20.762s±3.236s,两组之间差异具有统计学意义(t=9.932,P<0.01)。
2.2 皮质醇浓度 对照组与模型组大鼠 16点血清皮质醇浓度分别为 1.25μg/dl±0.12μg/dl和0.58μg/dl±0.09μg/dl,差异有统计学意义 (t=7.340,P<0.01)。
2.3 海马 5-HT1A受体 mRNA表达 经凝胶成像系统分析,对照组大鼠海马 5-HT1AmRNA表达的积分光密度为 1.223±0.152,SPS1d、4d、7d和 14d分别为 0.846±0.067、0.510±0.052、1.007±0.137、1.109±0.106。见图1和图2。2.4 海马 5-HT1其他受体亚型的表达 PCR结果没见其他亚型表达。

图1 海马 5-HT1AmRNA表达的分析结果
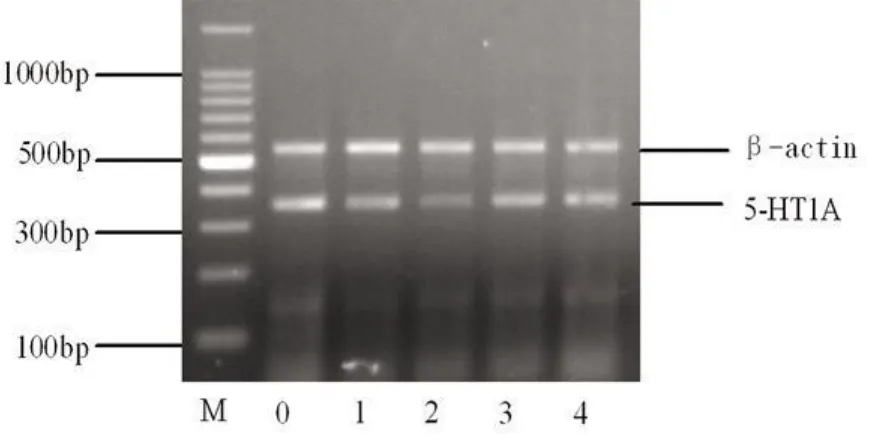
图2 海马 5-HT1A RT-PCR电泳图
3 讨 论
PTSD是指由于异常威胁性或灾难性心理创伤导致延迟出现和长期持续的精神障碍。其临床表现以再度体验创伤为特征,并伴有情绪的易激惹和回避行为,是一种创伤后心理失衡状态[7]。但 PTSD不同于一般的应激反应及其它精神疾病,PTSD患者血液中的皮质酮基础水平往往较低,存在下丘脑-垂体-肾上腺素轴(HPA轴)的紊乱[8]。以往由于缺乏理想的动物模型,使 PTSD的基础研究受到了很大限制。SPS模型作为 PTSD动物模型的确认,为深入研究应激障碍的发病机制提供了行之有效的方法[9]。本实验采用 SPS复制 PTSD模型,水迷宫实验结果表明模型组大鼠逃避潜伏期明显长于对照组大鼠,提示 SPS后大鼠记忆力减退。血清皮质醇浓度也明显低于对照组。这些都符合 PTSD的临床表现,说明模型复制成功。
海马是参与调节情感、认知、行为的重要边缘系统结构,富含突触后膜 5-HT1A受体[10]。海马 5-HT系统特别是 5-HT受体的功能改变在精神疾病发病机制和治疗中具有重要作用。5-HT1A受体和情感障碍关系最为密切[10]。研究发现在抑郁症患者海马 5-HT1A受体的结合下降,5-HT1A受体 mRNA减少[11,12]。海马是大脑的重要结构,在学习和记忆功能以及调节神经内分泌和自主神经活动中起着重要作用。有研究发现 PTSD患者右侧海马体积缩小[13]。5-HT1A受体还与神经发生有关,系统应用5-HT1A受体激动剂可引发成年大鼠齿状核锥体细胞神经发生效应。海马萎缩的一个原因可能是由于海马区 5-HT1A受体功能紊乱导致成年大鼠齿状回锥体细胞分化的显著减少,使海马萎缩。本实验结果表明,在大鼠海马 5-HT1受体中,只有 5-HT1A亚型有表达。SPS刺激后大鼠海马 5-HT1A受体 mRNA表达降低,SPS刺激后 4d达到最低,以后逐渐上升,到刺激后 14d,5-HT1A受体 mRNA的表达和对照组没有显著性差异。在 PTSD发病过程中,应激有可能通过影响 5-HT1A受体 mRNA的表达从而影响海马功能,导致一系列精神障碍。在 PTSD疾病治疗和药物开发中,也可以通过影响 5-HT1A受体作为切入点。
[1] Li S,Murakami Y,Wang M,et al.The effects of chronic valproate and diazepam in a mouse model of posttraumatic stress disorder[J].Pharmacol Biochem Behav,2006,85(2):324-331.
[2] Siegmund A,Wotjak CT.A mouse model of posttraumatic stress disorder that distinguishes between conditioned and sensitised fear[J].J Psychiatr Res,2007,41(10):848-860.
[3] Lucki L.The spectrum of behaviors influenced by serotonin[J].Biol Psychiatry,1998,44(3):151-162.
[4] Tanaka-Gomi N,Yasuda K,Nakamura M,et al.Postnatal changes in 5HT and NK1 receptors in rat trigeminal motor nucleus and surroundings[J].Int JDev Neurosci,2007,25(7):427-432.
[5] Bonne O,Bain E,Neumeister A,et al.No Change in Serotonin Type 1A Receptor Binding in Patients with Posttraumatic Stress Disorder[J].Am J Psychiatry,2005,162(2):383-385.
[6] Liberzon I,Krstov M,Young EA.Stress-restress:effects on ACTH and fast feedback[J].Psychoneuroendocrinology,1997,22(6):443-453.
[7] Wakizono T,Sawamura T,Shimizu K,et al.Stress vulnerabilities in an animal model of post-traumatic stressdisorder[J].Physiol Behav,2007,90(4):687-695.
[8] Harvey BH,Brand L,Jeeva Z,et al.Cortical/hippocampal monoamines,HPA-axis changes and aversive behavior following stress and restress in an animal model of post-traumatic stress disorder[J].Physiol Behav,2006,87(5):881-890.
[9] Gurbits TV,Shenton ME.Magnetic resonance imaging study of hippocampal volume in chronic,combat-related posttraumatic Stress disorder[J].Biopsychiatry,1996,40(11):1091-1099.
[10] Blier P,Ward NM.Is there a role for 5-HT1A agonists in the treatment of depression[J]?Biol Psychiatry,2003,53(3):193-203.
[11] Aiango V,Underwood MD,Boldrini M,et al.Serotonin 1A receptors,serotonin transporter binding and seortonin transporter mRNA expression in the brainstem of depressed suicide vietims[J].Neuorpsychopharmacology,2001,25(6):892-903.
[12] Hensler JG.Regulations of 5-HT1A receptor function in brain following agonist or antidepressant administration[J].Life Sci,2003,72(15):1665-1682.
[13] Bremner JD,Vythilingam M,Yermetten E,et al.Neural correlates of declarative for emotional valenced words in women with posttraumatic stress disorder related to early childhood sexual abuse[J].Biol Psychiatry,2003,53(10):879-889.

