标准化粉尘螨变应原脱敏疫苗中主要变应原Der f 2含量测定*
吉坤美,刘晓宇,唐 艳,詹政科,刘志刚
2.深圳大学生命科学学院,深圳 518060;
3.深圳市人民医院龙华分院,深圳 518109
标准化粉尘螨变应原脱敏疫苗中主要变应原Der f 2含量测定*
吉坤美1,刘晓宇2,唐 艳3,詹政科1,刘志刚1
目的研制粉尘螨Ⅱ组变应原Derf 2单克隆抗体(Monoclonal Antibody,McAb),并建立双单抗夹心ELISA检测方法,测定标准化粉尘螨变应原脱敏疫苗中Der f 2的含量。方法应用基因工程方法获得粉尘螨变应原Der f 2重组蛋白并通过亲和层析纯化,再免疫小鼠,利用间接ELISA筛选获得McAb杂交瘤细胞株并纯化、鉴定抗体的特异性;用一株单抗包被酶标板,同时用生物素标记另一株单抗,从而建立双单抗体夹心ELISA法;并用此法测定粉尘螨变应原脱敏疫苗中Der f 2的含量。结果成功地获得了一株单抗3B12与屋尘螨抗原具有交叉反应,另外一株单抗3G7与屋尘螨抗原没有交叉反应,并建立了双单抗夹心ELISA方法测定Der f 2的含量,其方法的检测限为0.5ng/mL,并在6.25ng/mL-300ng/mL范围内线性良好;标准化粉尘螨变应原脱敏疫苗中Der f 2的含量为100ng/10000BAU。结论成功制备了高效价抗Der f 2单抗,并建立了双抗体夹心ELISA检测方法。该方法具有很高的灵敏度,可以测定标准化粉尘螨变应原脱敏疫苗中主要变应原Der f 2含量,为临床应用奠定基础。
尘螨过敏原;Der f 2;单克隆抗体;夹心ELISA
2.深圳大学生命科学学院,深圳 518060;
3.深圳市人民医院龙华分院,深圳 518109
尘螨是世界性分布的重要变应原,室内主要分布在卧具、沙发、地面以及空调滤网等处。引发人类过敏反应的主要尘螨种类有屋尘螨(DermatophagoidesPteronyssinus,Der p)和粉尘螨(DermatophagoidesFarinae,Der f);其分泌物、排泄物及其尸体的降解物等以尘埃颗粒飞扬于空气中,过敏体质者吸入后,可诱发Ⅰ型变态反应,从而引起哮喘、过敏性鼻炎、异位性皮炎和荨麻疹等多种变态反应性疾病(又称过敏性疾病)〔1-3〕。针对这类疾病,临床上采用尘螨变应原脱敏疫苗进行治疗是目前唯一对因治疗方法〔4〕。为了保证疫苗的疗效和用药的安全性,WHO指出应该采用标准化的尘螨变应原制造脱敏疫苗〔4〕。
标准化尘螨变应原必须保证其主要致敏成分含量可以测定且批次之间一致〔4-5〕。粉尘螨中最主要的致敏成分是Ⅰ组和Ⅱ组变应原即Der f 1和Der f 2〔3〕。Der f 2前体由146个氨基酸组成,经去除信号肽加工处理后为129个氨基酸,相对分子质量(Mr)为14 000,无糖基化位点;70%~80%尘螨过敏患者血清 IgE结合Der f 2,并呈现强阳性反应〔6〕。国际上 Indoor Biotechnologies公司有针对尘螨第Ⅱ组变应原含量测定的商品化试剂盒出售,但该试剂盒不能区分粉尘螨 Derf2和屋尘螨Derp2〔7〕;目前国内尚无 Der f 2的单克隆抗体制备以及研制含量测定ELISA试剂盒的报道。本研究用重组Der f 2做抗原制备单抗并建立了双抗体夹心ELISA法,以快速检测疫苗中Der f 2含量,为实现标准化的尘螨疫苗国产化奠定了技术基础。
1 材料与方法
1.1 实验材料
1.1.1 实验动物 4w龄BALB/c小鼠(SPF级)购自中山大学医学院动物中心。
1.1.2 质粒与菌种 pET-Der f 2重组表达质粒,E.coliBL21 star(DE3)菌株由本实验室提供。
1.1.3 主要试剂和仪器HiTrap protein G,硝酸纤维素膜(Amersham Pharmacia公司),福氏佐剂(BBI公司),吐温 20、Anti-IgG-HRP 、链酶亲和素-HRP、TMB(Sigma公司),NHS-Biotin(PIERCE公司),DEME干粉培养基、胎牛血清(HyClone公司),亲和层析纯化获得的天然Der f 2标准品(英国Indoor Biotechnologies公司),标准化粉尘螨疫苗10 000 BAU/mL(美国 Allergy Laboratories药厂),美国FDA惠赠的粉尘螨疫苗标准品10 000 BAU/mL,粉尘螨和屋尘螨总蛋白由本室提供。垂直板型电泳槽(BIO-RAD),FPLC(Amersham Pharmacia公司),恒温CO2细胞培养箱(Heal force公司),洗板机(广州丰华),酶标仪(芬兰 Thermo)。
1.2 方 法
1.2.1 重组Der f 2的表达、纯化及免疫学特性按照朱健琦等报道的方法〔8〕表达与纯化Der f 2重组蛋白;经Western blot分析证实该重组蛋白能与粉尘螨过敏患者血清的特异性IgE结合,具有免疫原性〔8〕。
1.2.2 抗粉尘螨Der f 2单克隆抗体的制备
1.2.2.1 重组蛋白免疫小鼠 首次免疫以Indoor公司纯化的天然来源的Der f 2蛋白30μ g作为抗原和等量的福氏完全佐剂混合乳化后,皮下注射小鼠颈背部标准品进行免疫;加强免疫共2次,蛋白量同前,采用重组Der f 2蛋白,混入等量的福氏不完全佐剂。每次免疫间隔约3w。
1.2.2.2 细胞融合与筛选 取免疫小鼠脾细胞与小鼠骨髓瘤Sp2/0细胞在PEG作用下融合。融合后的细胞置于HAT培养基中,铺到96孔板中,在含5%CO2的培养箱中于37℃下培养。融合7~8 d后,待杂交瘤细胞生长至1/4孔大小时,取上清液进行筛选。采用有限稀释法对杂交瘤细胞培养上清液呈抗Der f 2抗体阳性的杂交瘤细胞进行克隆化。待克隆后的细胞生长至1/4孔大小时,进行再筛选、克隆,直至出现所有孔细胞上清液均呈抗体Der f 2阳性为止。
1.2.2.3 McAb小鼠腹水制备 在接种杂交瘤细胞1w前,向Balb/c小鼠腹腔注射液体石蜡。取杂交瘤细胞计数,离心后加入DMEM培养基使细胞悬浮,每只小鼠腹腔注射0.5 mL。1w后取腹水,离心取上清液,分装,-20℃下长期保存。
1.2.3 抗体的效价测定与纯化 采用常规间接ELISA法进行检测,天然Der f 2标准品蛋白作为抗原按100ng/孔4℃包被过夜,封闭液为3%BSAPBST,37℃封闭2h,以获取的腹水为一抗,同时用未免疫的BALB/c小鼠血清做平行阴性对照试验,从1∶100开始对倍梯度稀释,37℃反应1h,PBST洗3次后,加入羊抗鼠IgG-H RP作为二抗,37℃反应1h,洗3次后加底物TMB显色。测定孔O D值与阴性对照孔OD值之比大于2.1为阳性判断标准,抗体的稀释度即为抗体的效价。抗体纯化参照HiTrap protein G亲和层析说明书进行。
1.2.4 ELISA法检测抗Der f 2单克隆抗体的特异性 将天然来源的Der f 2标准品、重组Derf2蛋白、总Der f提取蛋白和总Der p提取蛋白以不同的浓度梯度包被微孔板,以抗Der f 2的单克隆抗体作为一抗,羊抗鼠IgG作为二抗,按照常规ELISA方法进行特异性检测分析;并同时进行Western blot分析。
1.2.5 McAb的标记 将纯化好的抗体的原缓冲液替换成磷酸盐缓冲溶液(PBS),然后将抗体与NHS活化的生物素(NSH-Biotin)按说明书推荐的比例混合,避光反应30min,用50kDa的超滤膜柱去除可能未参与标记的NSH-Biotin。
1.2.6 双抗体夹心ELISA法检测Der f 2含量方法的建立 微孔板每孔加纯化后的单抗 3G7 100ng,包被缓冲液为碳酸盐,采用物理吸附法包被4℃过夜。倒掉包被液,用含0.5%的吐温的 PBS洗涤液(PBST)洗一遍,每孔再加300μ L封闭液,37℃振荡反应2h,倒掉封闭液。粉尘螨抗原Der f 2标准品和基因工程重组的Der f 2分别按比例逐一稀释,每孔加 100μ L,阴性对照孔用 PBS代替。37℃振荡反应1h,完后用PBST洗3次。生物素标记的Der f 2单克隆抗体3B12按1∶1000的比例稀释,每孔 100μ L加入,37℃振荡反应 1h,之后用PBST洗3次。然后将HRP-链酶亲和素用分析缓冲液按1∶500的比例稀释,每孔加 100μ L,37℃振荡反应1h,完后用 PBST洗3次。加底物A、B液,37℃显色10min,加终止液后酶标仪读数。
1.2.7 双抗夹心ELISA法用于标准化粉尘螨疫苗中Derf2含量的检测 采ELISA法分别对美国Allergy Laboratories药厂生产的标准化粉尘螨疫苗10 000BAU/mL和美国FDA惠赠的粉尘螨疫苗标准品10 000BAU/mL中Der f 2的含量进行测定,3次求平均值,并对结果进行分析。
2 结 果
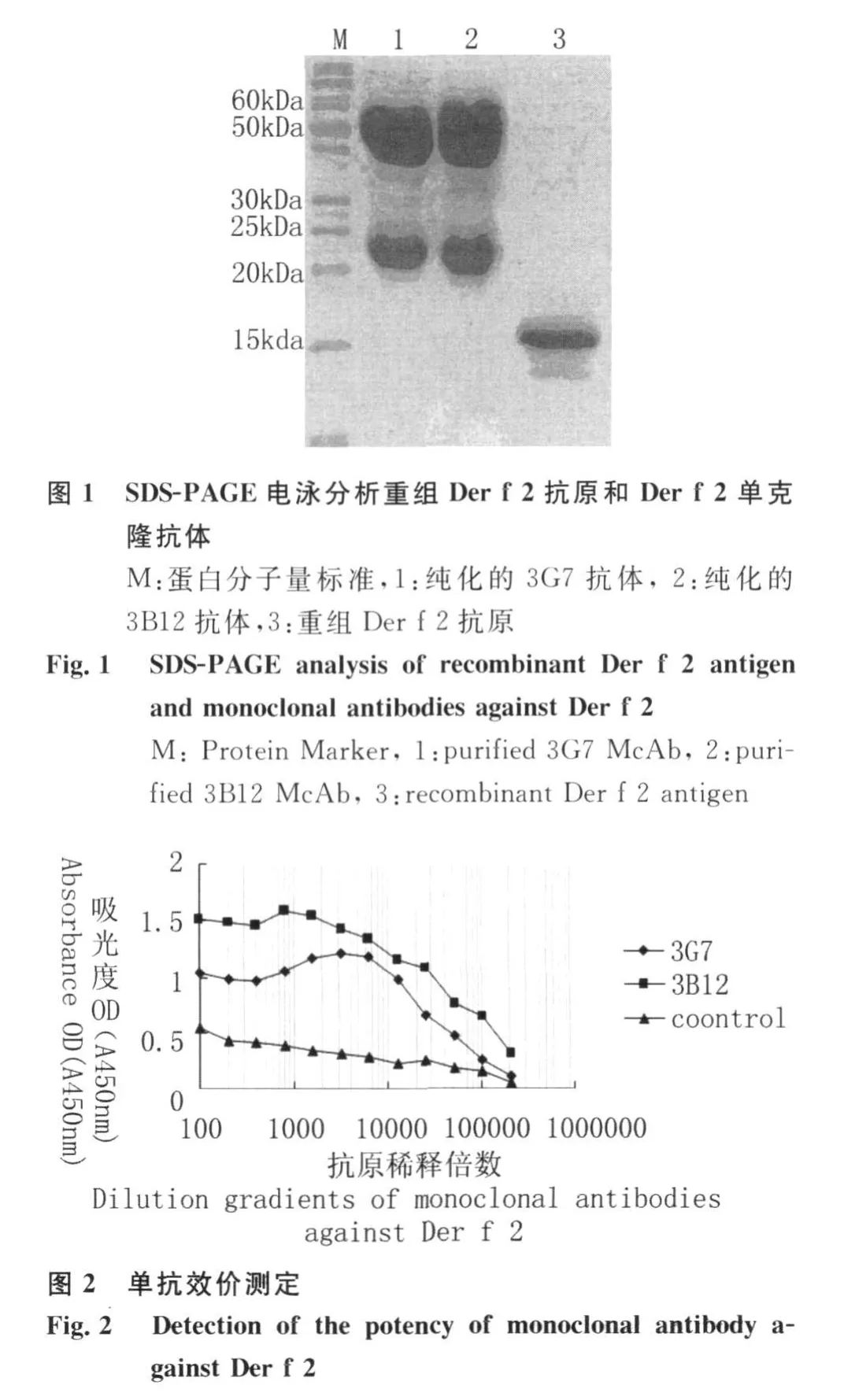
2.1 重组Der f 2的表达、纯化及免疫学特性 含重组Der f 2的阳性克隆菌株经IPTG诱导后,获高效表达。SDS-PAGE显示,在相对分子质量15kDa左右处有外源蛋白表达的条带出现,目的蛋白表达时带有6His-tag标签,表达蛋白分子量与理论预计值相符。纯化后的重组Der f 2见图1。
2.2 抗Der f 2单克隆抗体的制备与纯化 为测定疫苗中的Der f 2的含量,得到识别Der f 2不同表位的单克隆抗体,从而建立双抗体夹心的ELISA方法,我们通过一系列的克隆化,最终筛选到两株不同的抗体,分别命名为3G7和3B12,并从小鼠中得到的腹水通过亲和层析纯化后,SDS-PAGE显示,抗Der f 2单克隆 IgG抗体纯度达到95%以上,见图1。
2.3 间接ELISA检测抗体效价 间接ELISA测定鼠抗Der f 2单克隆抗体IgG效价,结果如图2,同时用未免疫的BALB/c小鼠血清做平行阴性对照试验,随着抗体稀释倍数的增加吸光值下降,以测定阳性孔OD值与阴性对照孔OD值之比大于2.1为判断标准,测得3G7单克隆抗体腹水的效价约为1∶102 400,3B12单克隆抗体的腹水效价约为1∶204 800。这说明本研究制备的抗体效价较高,可以被用来建立双抗体夹心ELISA法。
2.4 抗Der f 2单克隆抗体的特异性分析 粉尘螨与屋尘螨主要过敏原成分Ⅱ组变应原(Group II)Der f 2与Der p 2蛋白之间存在着高达80%的同源性,常常具有某些相交叉的抗原表位,所以针对它们的单克隆抗体有时难免会与两个物种来源的过敏原成分存在交叉反应〔7,9〕。为此,我们通过间接ELISA和Western blot两种方法进行了抗体特异性分析测定,结果显示(见表1和图3),单克隆抗体3B12与天然来源的Der f 2、重组蛋白Der f 2、Der f总蛋白(含有Der f 2)和Der p总蛋白(含Der p 2)均具有良好的反应活性,这说明单抗3B12与屋尘螨抗原具有交叉反应;但是另外一株单抗3G7仅与天然来源的Der f 2、重组蛋白Der f 2和Der f总蛋白(含有Der f 2)反应,不与屋尘螨总蛋白(含Der p 2)反应,说明它与屋尘螨抗原没有交叉反应。这也反映这二株抗体识别的位点有所不同。
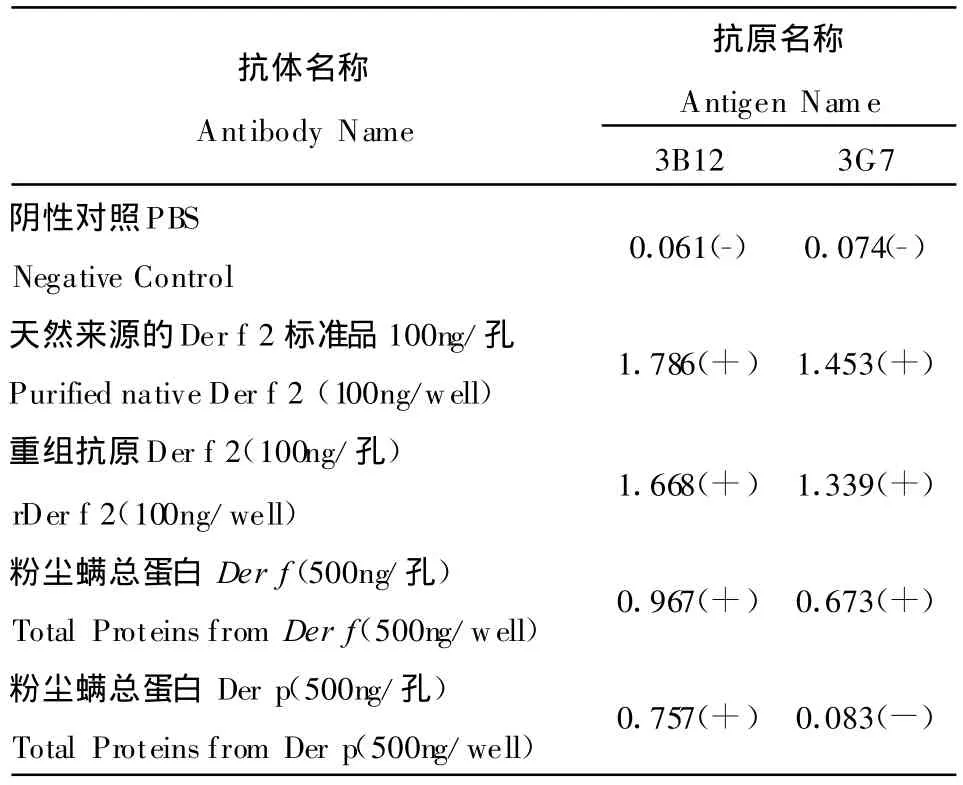
表1 间接ELISA测定单抗的特异性Table 1 Detection of specificity of monoclonal antibody against Der f 2 by indirect ELISA
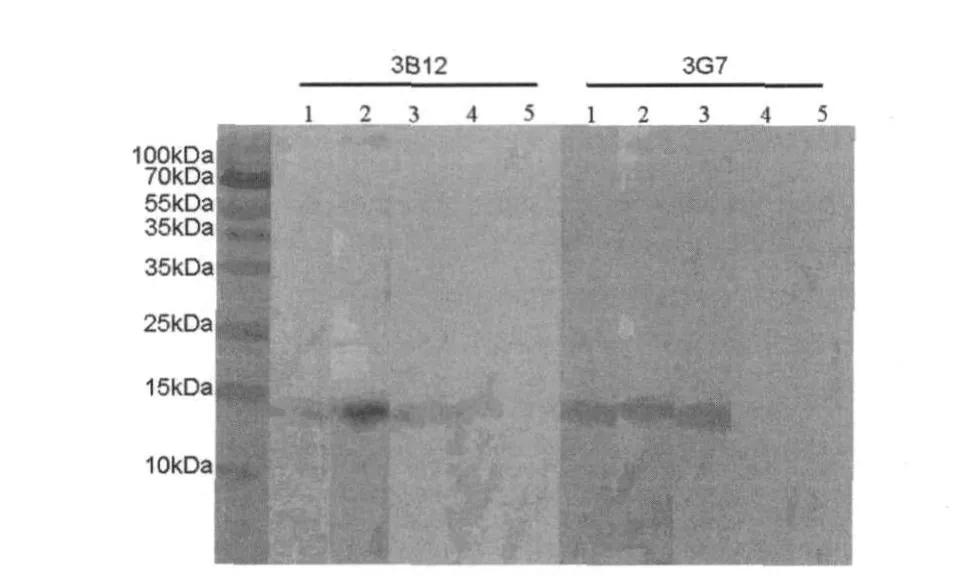
图3 抗Der f 2单克隆抗体的特异性分析1.天然来源的Der f 2;2.重组蛋白Der f 2;3.Der f总蛋白(含Der f 2);4.Der p总蛋白(含Der p 2);5、空白对照Fig.3 Detection of specificity of monoclonal antibody againstDer f 2 by Western blot 1.Native Der f 2;2.r Der f 2;3.Total proteins from Der f;4.Total proteins from Der p;5.Blank control
2.6 双抗体夹心ELISA法检测粉尘螨疫苗中Der f 2变应原含量方法曲线 利用两株不同的单抗(3G7,3B12)建立了双抗夹心的ELISA法测定Der f 2的含量。通过测定天然来源的Der f 2含量建立标准反应曲线(见图4),可见其检测限为0.5ng/mL,在6.25ng/mL-300ng/mL范围内线性良好,其R2=0.9965。
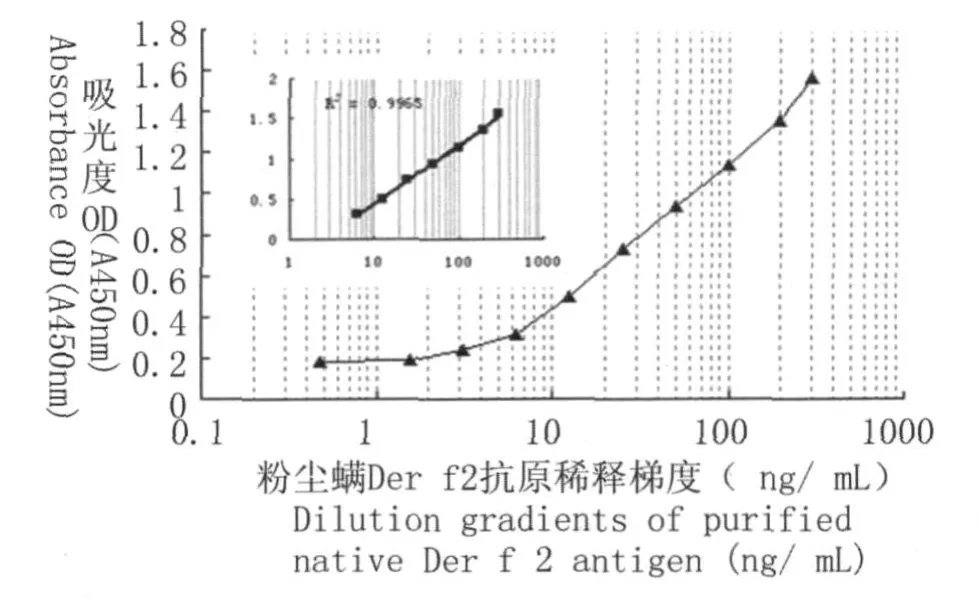
图4 双单抗夹心ELISA测定Der f 2含量的标准曲线R2:吸光度OD值与Derf2抗原浓度二者线性相关程度Fig.4 Standard curve of sandwich ELISA for determination of the concentration of native Der f 2
2.7 双抗体夹心ELISA法检测新制备粉尘螨变应原疫苗 通过上述方法在同一块ELISA板上建立标准曲线,同时测定标准化粉尘螨疫苗 10 000BAU/mL(美国Allergy Laboratories药厂)和美国FDA惠赠的粉尘螨疫苗标准品10 000BAU/mL中Der f2含量,分别重复三次取平均值,结果美国Allergy Laboratories药厂生产的标准化疫苗中的Der f 2的含量为 100ng/10 000BAU,与美国FDA惠赠的粉尘螨疫苗标准品中的Der f 2的含量为90ng/10 000BAU,二者比较接近。
3 讨 论
过敏性疾病如过敏性哮喘、过敏性鼻炎等是临床上常见病、多发病,被世界卫生组织列为二十一世纪重点防治三大疾病之一,世界各国过敏性疾病总发病率高达10%~30%〔3,6〕。尘螨作为最主要的吸入性过敏原,严重地影响过敏患者的生活质量。针对这类过敏性疾病的唯一对因治疗通过注入不同剂量的尘螨过敏原疫苗对患者进行脱敏治疗〔4〕。我国长期以来在临床上均采用粉尘螨粗浸液对过敏患者进行诊断和特异性免疫治疗,而浸液组份复杂,容易降解及受外源性物质污染,严重影响了治疗的安全性和一致性,而且存在一定的潜在危险性〔4-5〕。因此,迫切需要参照WHO的要求研制国产的标准化尘螨变应脱敏疫苗。
标准化的粉尘螨变应原必须保证其主要致敏成分Der f 1和Der f 2的含量可以测定且批次之间一致〔4,7〕。目前测定这类生化提取的、多种蛋白成分混合体系中某一组分含量的常用方法是双单抗夹心ELISA法,这种方法如果条件优化好可以获得高度特异、高度灵敏的检测效果。Jeong KY根据韩国粉尘螨物种来源的基因表达Der f 2蛋白并研制了双单抗夹心ELISA,用来测定灰尘中Der f 2的含量;但未形成商品化试剂供应〔10〕。Indoor Biotechnologies公司有针对尘螨第Ⅱ组变应原含量测定的商品化试剂盒出售,但该试剂盒不能区分粉尘螨Der f 2和屋尘螨Der p 2〔7〕。为此,要实现标准化的粉尘螨疫苗国产化必须研制基于双单抗夹心法测定Der f 2的 ELISA试剂盒。通过杂交瘤融合技术获得了二株能够稳定分泌抗Der f 2效价高的杂交瘤细胞株,并对这些单抗的生物学特性和免疫学特性进行了分析,其中一株单抗3B12与屋尘螨抗原具有交叉反应,另外单抗一株3G7与屋尘螨抗原没有交叉反应,这样构建的双单抗ELISA可以很好地区分开粉尘螨Der f 2和屋尘螨Der p 2,有利于粉尘螨疫苗研制过程中建立标准化的特异性检测其主要致敏成分Der f 2含量的方法。
采用双单抗夹心ELISA法测定提取变应原的混合体系中某一特定成分含量的方法由于不是绝对含量的测定,而只是相对含量的测定〔7,10〕。首先,选用制作标准曲线的标准品应尽可能和要测定的样品来源和性质一致。如本研究测定的对象是粉尘螨提取的混合物中Der f 2含量,为此我们选用了Indoor Biotechnologies公司从粉尘螨中生化提取并经亲和层析纯化的、具免疫学活性的天然Der f 2,这样二者性质相一致,而没有采用基因工程重组的Der f 2做标准品,因为大肠杆菌表达包涵体来源的Der f 2虽然经过变性、复性和纯化,但其免疫学性质很难和天然来源的Der f 2完全一致。其次,由于变应原生物原材料、生化提取、测定方法等存在一定的批间差异,为此采用免疫学方法测定主要变应原含量、变应原总生物活性等指标时,与国际标准品对照时会有一定的变化幅度,不可能完全一致。国家食品药品监督管理局在2003年发布的《变态反应原(变应原)制品质量控制技术指导原则》就指出,“要求所测得的抗原效价在标示效价的50%~200%之间,方法学研究应证实效价测定的标准差小于等于20%”。本研究测定结果提示美国Allergy Laboratories药厂生产的标准化疫苗与美国FDA惠赠的粉尘螨疫苗标准品中的Der f 2的含量二者比较接近,变化幅度在10%左右,符合变应原标准化的要求。
〔1〕Platts-Mills T A,Thomas WR,Aalberse RC,et al.Dust mite allergens and asthma:Report of a second international workshop〔J〕.Allergy Clin Immunol,1992,89:1046-1060.
〔2〕Busse WW,Rosenwasser LJ.Mechanisms of asthma〔J〕.J Allergy Clin Immunol,2003,111(3):799-804.
〔3〕Liu ZG,Bai Y,Ji KM,et al.Detection ofDermatophagoides f arinaein the dust of air conditioning filters〔J〕.Int A rch Allergy Immunol,2007,144(1):85-90.
〔4〕Bousquet J,Lockey R,Malling HJ.Allergen immunotherapy:therapeutic vaccines for allergic diseases.A WHO position paper〔J〕.J Allergy Clin Immunol,1998,102(4 Pt 1):558-562.
〔5〕赖乃揆,吴强.变应原的标准化〔J〕.中华微生物学和免疫学杂志,2001,21:S132-S136.
〔6〕Ichikawa S,Hatanaka H,Yuuki T,et al.Solution structure of Der f 2,the major mite allergen for atopic disease〔J〕.J Biol Chem,1998,273:356-360.
〔7〕Ovsyannikova IG,Vailes LD,Li Y,et al.M onoclonal antibodies to g roup II Dermatophagoides spp.allergens:murine immune response,epitope analy sis,and development of a two-site ELISA〔J〕.J Allergy Clin Immunol,1994,94:537-546.
〔8〕朱健琦,刘志刚,高波,等.粉尘螨Ⅱ类变应原的克隆表达、纯化及其免疫学特性〔J〕.免疫学杂志,2006,22(2):213-216.
〔9〕T homas WR,Smith WA,Hales BJ,et al.Characterization and immunobiology of house dust mite allergens〔J〕.Int Arch Allergy Immunol,2002,129:1-18.
〔10〕Jeong K Y,Jin HS,Oh SH,et al.Monoclonal antibodies to recombinant Der f 2 and development of a two-site ELISA sensitive to major Der f 2 isoallergen in Korea〔J〕.Allergy,2002,57(1):29-34.
Immunoassay for the concentration of major allergen Der f 2 in standardDermatophagoides farinaevaccine products
JI Kun-mei1,LIU Xiao-yu2,TANG Yan3,ZHAN Zheng-ke1,LIU Zhi-gang1
(1.State Key Laboratory of Respiratory Disease for Allergy,Shengzhen University,Shenzhen518060,China;
2.School of Life Sciences,ShenzhenUniversity,Shenzhen518109,China;
3.Longhua Branch,Shenzhen People's Hospital,Shenzhen518109,China)
The designed monoclonal antibodies(McAb)against rDer f 2 and sandwich ELISA were performed to detect the concentration of major allergen Der f 2 inDermatophagoides farinaevaccine products.The rDer f 2 was expressed inE.coliand purified by affinity chromatograph.Balb/c mice were immunized with rDer f 2,and the indirect ELISA was used to screen the positive clones of hybridoma cell.With a McAb coated ELISA plate and a biotin labeled McAb,sandwich ELISA was performed to assay the concentration of major allergen Der f 2 in the vaccine products.Two monoclonal antibodies against Der f 2 were made and McAb 3G7 did not react with the extract fromDermatophagoides Pteronyssinus.In sandwich ELISA,the standard curve was linear and the rDer f 2 concentrations were from 6.25 ng/mL to 300 ng/mL with a low detection limit of about 0.5 ng/mL for rDer f 2.The concentration of major allergen Der f 2 in standardDermatophagoides farinaevaccine products was about 100ng per 10000BAU.In conclusion,the two McAbs against Der f 2 were made successfully and the sandwich ELISA kit could detect the concentration of major allergen Der f 2 in the vaccine products.
dust mite allergen;Der f 2;monoclonal antibody;sandwich ELISA
R384.4
A
1002-2694(2010)07-0663-05*国家“863”专题(No.2006AA02A231)和粤港关键领域重点突破项目(No.20054982207)联合资助
刘志刚,Email:lzg@szu.edu.cn
1.呼吸疾病国家重点实验室深圳大学变态反应分室,深圳 518060;
2009-11-18;
2010-05-17

